肉桂叶非挥发性化学成分研究
2023-12-22董丽梅奚志芳林晨露吴梓怡廖煜文黄子琪赵秀娟
*董丽梅 奚志芳 林晨露 吴梓怡 廖煜文 黄子琪 赵秀娟
(广东生态工程职业学院 广东 510520)
引言
肉桂(Cinnamomum Cassia Presl)又名玉桂、菌桂、牡桂,为樟科樟属的常绿乔木,主要分布在热带及亚热带地区。肉桂在我国的栽培历史悠久,主产于广西、广东、云南、福建等省份[1]。肉桂既是我国传统的名贵中药材,也是著名的辛香食用调味料,是一种药食两用的植物。据《中国药典》等记载,肉桂具有补火助阳、活血通经、散寒止痛等功效,可用于治疗头晕头痛、虚寒呕吐、阳痿宫冷、闭经痛经等症[2]。
肉桂的食用和药用部位主要为肉桂皮,故以往对肉桂化学成分和生物活性的研究主要集中在桂皮。桂皮中主要含有酚类、二萜类、木脂素类、挥发油等成分。现代药理学研究表明,桂皮具有抗菌、抗炎、抗氧化、抗肿瘤、降血糖、降血脂、降血压、神经保护等作用[3-4]。肉桂叶作为肉桂生产过程中的副产物,资源丰富,再生能力强,可常年采集,但是由于对其化学成分与功能价值研究不足,未能充分开发利用。肉桂叶目前主要用来提取挥发油,但是提取率很低,只有0.8%~1.2%,提取后剩余大量残渣,通常被直接丢弃,导致资源浪费[5]。目前对肉桂叶化学成分的研究主要集中在挥发油,而对其非挥发性成分的研究较少。
本文以肉桂叶为研究对象,利用多种色谱分离技术对肉桂叶中的非挥发性化学成分进行系统地提取分离和结构鉴定,希望从肉桂叶中发现更多有价值的化合物,以提高肉桂叶的开发利用,实现变废为宝。
1.实验部分
(1)实验材料
肉桂叶采自广东生态工程职业学院后山园艺生态创意园,干燥后粉碎备用。
(2)主要仪器与试剂
LC-20AT高效液相色谱仪,日本SHIMADAZU公司;N1000旋转蒸发仪,日本EYELA公司;DRX-500核磁共振波谱仪,德国BRUKER公司;APCI-2000电喷雾电离质谱仪,美国Applied Biosystems公司。
实验中所用的乙酸乙酯、氯仿等分析纯化学试剂均为广州化学试剂厂生产;色谱纯甲醇、乙腈为上海安谱实验科技有限公司生产。
(3)实验方法
肉桂叶晒干(8.56kg)粉碎后用95%的乙醇浸泡提取3次(每次72h),将提取液合并,经过真空减压浓缩,得到乙醇提取物的浸膏。用蒸馏水溶解,使浸膏成为混悬液,然后用石油醚、乙酸乙酯、正丁醇分别萃取4次,用旋转蒸发仪减压浓缩后分别得到石油醚极性萃取部、乙酸乙酯极性萃取部和正丁醇极性萃取部。取乙酸乙酯极性萃取部(104.27g),采用正相硅胶柱层析法,以氯仿/甲醇(100:0~0:100)作为流动相进行梯度洗脱,根据薄层色谱(Thin Layer Chromatography)检测,合并主点相同的流分,得到E1~E9共9个组分。E3经反相中压柱层析,甲醇/水(10:90~100:0)为流动相,梯度洗脱,得到亚组分E3-1~E3-10。E3-6反复经葡聚糖凝胶柱色谱(Sephadex LH-20)分离,以甲醇作为流动相进行洗脱,得到化合物4(2.7mg)。E4经反相中压柱层析,甲醇/水(15:85~100:0)为流动相,梯度洗脱,得到亚组分E4-1~E4-8。E4-5经高效液相制备色谱分离,乙腈/水(48:52)作为流动相,流速8mL/min,得到化合物5(tR 102min,3.3mg)。E7经反相中压柱层析,以甲醇/水(30:70~100:0)作为流动相,梯度洗脱,得到亚组分E7-1~E7-8。E7-3经Sephadex LH-20色谱分离,以氯仿/甲醇(1:4)洗脱,得到化合物1(5.4mg)。E7-5反复经Sephadex LH-20色谱分离,用甲醇洗脱,得到化合物2(5.8mg)和3(6.2mg)。E8经反相中压柱层析,以甲醇/水(45:55~100:0)为流动相,梯度洗脱,得到亚组分E8-1~E8-9。E8-5反复经Sephadex LH-20色谱分离,以甲醇洗脱,得到化合物6(5.3mg)。
2.结果与分析
(1)化合物结构鉴定
化合物1:黄色粉末;ESI-MS m/z 165[M+H]+,163[M-H]-,分子式为C9H8O3;1H NMR(CD3OD,500MHz)δ:7.48(2H,d,J=8.0Hz,H-2,6),6.79(2H,d,J=8.0Hz,H-3,5),7.49(1H,d,J=16.5Hz,H-7),6.27(1H,d,J=16.5Hz,H-8);13C NMR(CD3OD,125MHz)δ:125.6(C-1),130.3(C-2,6),159.9(C-4),116.0(C-3,5),124.6(C-6),144.4(C-7),115.7(C-8),168.4(C-9)。以上数据与文献[6]中报道的波谱数据一致,因此鉴定该化合物为4-羟基肉桂酸。
化合物2:黄色粉末;ESI-MS m/z:303[M+H]+,301[M-H]-,分子式为C15H10O7;1H NMR(500MHz,CD3OD)δ:6.18(d,J=2.0Hz,1H,H-6),6.39(d,J=2.0Hz,1H,H-8),7.73(d,J=2.1Hz,1H,H-2'),6.88(d,J=8.5Hz,1H,H-5'),7.63(dd,J=8.5,2.1Hz,1H,H-6');13C NMR(125MHz,CD3OD)δ:148.0(C-2),137.2(C-3),177.3(C-4),158.2(C-5),99.2(C-6),165.6(C-7),94.4(C-8),162.5(C-9),104.5(C-10),124.2(C-1'),116.0(C-2'),146.2(C-3'),148.8(C-4'),116.2(C-5'),121.7(C-6')。上述数据与文献[7]中报道的波谱数据是一致的,因此鉴定化合物2为槲皮素。
化合物3:黄色粉末;ESI-MS m/z:309[M+Na]+,285[M-H]-,分子式为C15H10O6;1H NMR(500MHz,CD3OD)δ:6.16(d,J=2.1Hz,1H,H-6),6.37(d,J=2.1Hz,1H,H-8),8.06(d,J=8.9Hz,1H,H-2',6'),6.89(d,J=9.0Hz,1H,H-3',5');13C NMR(125MHz,CD3OD)δ:148.0(C-2),137.1(C-3),177.3(C-4),158.2(C-5),99.3(C-6),165.5(C-7),94.5(C-8),162.5(C-9),104.5(C-10),123.7(C-1'),130.6(C-2'),116.3(C-3'),160.5(C-4'),116.3(C-5'),130.6(C-6')。以上数据与文献[8]中报道的数波谱据一致,因此鉴定化合物3为山柰酚。
化合物4:无色油状;ESI-MS m/z379[M+Na]+,355[M-H]-;1H NMR(CD3OD,500MHz)δ:7.21(1H,d,J=1.9Hz,H-2),6.82(1H,d,J=8.2Hz,H-5),7.10(1H,dd,J=8.2,1.9Hz,H-6),6.41(1H,d,J=15.9Hz,H-7),7.73(1H,d,J=15.9Hz,H-8),5.58(1H,d,J=7.9Hz,H-1'),3.54-3.34(4H,m,H-2',3',4',5'),3.85(1H,dd,J=12.1,2.0Hz,H-6'),3.69(1H,dd,J=12.1,4.6Hz,H-6'),3.90(3H,s,OCH3-3);13C NMR(CD3OD,125MHz)δ:127.6(C-1),111.8(C-2),149.4(C-3),151.0(C-4),114.8(C-5),124.4(C-6),148.2(C-7),116.5(C-8),167.7(C-9),95.8(C-1'),74.1(C-2'),78.1(C-3'),71.1(C-4'),78.8(C-5'),62.4(C-6'),56.5(OCH3-3)。以上数据与文献[9]中报道的波谱数据是一致的,因此鉴定该化合物为阿魏酰基-β-D-葡萄糖苷。
化合物5:浅黄色粉末;ESI-MS m/z: 365[M+Na]+,341[M-H]-;分子式是C15H18O9;1H NMR(CD3OD,500MHz)δ:7.68(1H,d,J=15.9Hz,H-7),7.09(1H,d,J=2.0Hz,H-2),7.00(1H,dd,J=8.2,2.0Hz,H-6),6.81(1H,d,J=8.2Hz,H-5),6.33(1H,d,J=15.9Hz,H-8),5.60(1H,d,J=7.8Hz,H-1'),3.88(1H,dd,J=12.1,1.8Hz,H-6'a),3.72(1H,dd,J=12.1,4.8Hz,H-6'b),3.38-3.51(4H,m,H-2',3',4',5');13C NMR(CD3OD,125MHz)δ:167.9(C-9),150.0(C-3),148.5(C-7),147.0(C-4),127.7(C-1),123.4(C-6),116.7(C-5),115.4(C-2),114.5(C-8),95.9(C-1'),78.9(C-3'),78.2(C-5'),74.2(C-2'),71.2(C-4'),62.5(C-6').上述数据与文献[10]报道的基本一致,因此鉴定化合物5为咖啡酰基-β-D-葡萄糖苷。
化合物6:淡黄色粉末;ESI-MS m/z 247[M+Na]+,223[M-H]-,分子式是C12H16O4。1H NMR(CD3OD,500MHz)δ:6.72(2H,s,H-2,6),6.54(1H,d,J=15.8Hz,H-7),6.31(1H,dt,J=15.8,5.7Hz,H-8),4.22(2H,dd,J=5.7,1.3Hz,H-9),3.74(3H,s,OCH3),3.84(6H,s,OCH3);13C NMR(CD3OD,125MHz)δ:134.6(C-1),104.8(C-2,6),154.6(C-3,5),131.6(C-7),129.6(C-8),63.6(C-9),56.6(OCH3-3,5),61.1(OCH3-4)。上述数据与文献[11]中报道的波谱数据一致,因此鉴定该化合物为反式-3,4,5-三甲氧基肉桂醇。
3.结论
本研究采用正相硅胶柱色谱、反相C18柱色谱、葡聚糖凝胶柱色谱、半制备高效液相色谱等多种色谱分离技术从肉桂叶中分离得到6个单体化合物(图1),利用ESI-MS、1H NMR、13C NMR等波谱学技术结合理化性质鉴定化合物的结构分别为4-羟基肉桂酸(1)、槲皮素(2)、山奈酚(3)、阿魏酰基-β-D-葡萄糖苷(4)、咖啡酰基-β-D-葡萄糖苷(5)、反式-3,4,5-三甲氧基肉桂醇(6),其中化合物4、5为首次从肉桂中分离得到。
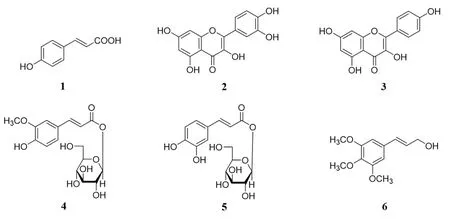
图1 化合物1~6的化学结构Fig.1 Chemical structures of compounds 1~6
文献[12]报道,4-羟基肉桂酸(1)具有抗炎、抗肿瘤、抗氧化、免疫调节、保护心血管、预防糖尿病等作用。槲皮素(2)具有抗菌、抗炎、抗氧化、抗病毒、提高免疫等作用[13]。山奈酚(3)具有抗炎、抗氧化、防癌抗癌、神经保护、治疗糖尿病、治疗骨质疏松等多种作用[14]。
本研究进一步丰富了肉桂叶的化学物质基础,对于促进肉桂叶资源的有效开发利用具有积极意义。
