赤泥合成4A分子筛及吸附去除水中Cu2+和Mn2+的机理
2023-12-19刘耀东叶翠平韩丽媛梁美生
刘耀东,叶翠平,韩丽媛,梁美生
(太原理工大学 环境科学与工程学院,山西 晋中 030600)
铜和锰是重要的战略资源,广泛用于电气工业、轻工业、机械制造业、国防工业等[1-2]。特别是在新兴的新能源汽车领域,大量使用含铜和锰的零部件,导致生产过程产生大量含Cu2+和Mn2+的废水,如不经处理直接排放会导致重金属离子污染。过量摄入的Cu2+和Mn2+会在人体内富集,导致肝硬化、代谢紊乱、慢性中毒等损伤[3-4]。因此,研究水中Cu2+和Mn2+的去除有重要意义。在化学沉淀、化学还原、电化学处理、反渗透等众多重金属去除技术中,吸附被认为是最简单、有效和环保的工艺之一[5-6]。
近年来,制备低成本吸附剂用于水中重金属离子的去除成为研究热点。4A分子筛具有规则的孔道、较大的比表面积和优异的离子交换能力,可用于重金属离子污染水体的修复,然而高昂的制备成本限制了其发展[7]。赤泥中的主要成分为氧化铝、氧化硅和氧化铁等[8],与分子筛的成分一致,可为合成分子筛提供硅源和铝源。我国是铝生产大国,赤泥是铝土矿提取氧化铝后的残渣,每生产1 t氧化铝约产生1~2 t赤泥[9]。目前,我国赤泥的堆存量已超过6×108t,且以高达每年1×108t的速度增长。以赤泥为原料合成4A分子筛无论在理论上还是经济成本上都具有可行性。但以往以赤泥为原料合成4A分子筛的过程中大量使用酸碱,在生产成本增加的同时带来酸碱废液的污染[10],且合成的4A分子筛纯度、结晶度低。
本工作通过碱熔融—水热结晶法成功合成了4A分子筛,并通过静态吸附实验及SEM-EDS、XRD、FTIR、XPS等表征手段深入探究了分子筛对Cu2+和Mn2+的吸附性能及吸附机理。
1 实验部分
1.1 材料和试剂
拜耳法赤泥,取自山西华兴铝业有限公司,主要成分(w)为:Al2O322.68%,Fe2O319.91%,SiO219.20%,Na2O 8.55%,CaO 8.51%,TiO23.38%。
五水硫酸铜(CuSO4·5H2O)、一水硫酸锰(MnSO4·H2O)、氢氧化钠(NaOH)、九水偏硅酸钠(Na2SiO3·9H2O):分析纯。
1.2 赤泥合成4A分子筛
以赤泥为原料,采用碱熔融—水热结晶法合成4A分子筛。取3 g赤泥于石墨坩埚中,与3.6 g NaOH混合均匀,置于马弗炉中以500 ℃焙烧0.5 h。碱熔融阶段将赤泥中的不溶性硅酸盐和铝酸盐转化为可溶性的硅酸钠和铝酸钠。将5 g焙烧产物投入到装有60 mL超纯水的烧杯中,超声波搅拌20 min,过滤,向滤液中添加0.92 g Na2SiO3·9H2O,调节滤液中SiO2与Al2O3的摩尔比为2.1,搅拌15 min。将混合体系置于水热反应釜中,于90 ℃水热结晶5 h,所得产物即为合成的4A分子筛。
1.3 吸附实验
用CuSO4·5H2O、MnSO4·H2O和超纯水配制溶液,模拟含Cu2+和Mn2+的废水,用0.1 mol/L盐酸和0.1 mol/L NaOH溶液调节初始pH。取50 mL一定浓度的废水于锥形瓶中,加入一定量的4A分子筛后置于水浴恒温振荡器中进行振荡吸附。每隔一段时间抽取一定体积的上清液,用0.45 μm针头式过滤器过滤,采用珀金埃尔默仪器公司PinAAcle900型原子吸收光谱仪测定滤液中Cu2+和Mn2+的浓度,计算其去除率和吸附量[11]。
1.4 表征方法
XRF:采用荷兰帕纳科公司Zetium型X射线荧光光谱仪分析赤泥的成分。
XRD:采用荷兰Malvern Panalytical公司Aeris型X射线衍射仪分析样品的晶相组成,CuKα(λ=0.154 nm)辐射源,电压40 kV,电流15 mA,扫描速率5( °)/min,扫描范围5°~70°。
SEM-EDS:采用日本电子株式会社JSMIT700HR型扫描电子显微镜对样品的表面形貌、粒径等进行分析,电压20 kV;采用英国牛津仪器科技有限公司Xplore30型能谱仪对样品的元素组成及含量进行测定。
FTIR:采用铂金埃尔默公司Sepctrum Two型傅里叶变换红外光谱仪分析样品的化学结构,分辨率0.5 cm-1,将溴化钾和4A分子筛按质量比100∶1混合压片,扫描范围400~4 000 cm-1。
XPS:采用塞默飞世尔科技公司K-Alpha型X射线光子能谱仪对样品进行元素价态分析,用XPS Peak软件进行分峰拟合。
2 结果与讨论
2.1 4A分子筛的合成结果
合成的4A分子筛的XRD谱图如图1所示。经与XRD标准卡片JCPDS 39-0222比对可知,合成的样品即为4A分子筛,且合成纯度较高,利用Jade6.0软件计算得到其结晶度为92.15%。

图1 合成的4A分子筛的XRD谱图
2.2 4A分子筛对Cu2+和Mn2+的吸附性能
2.2.1 吸附效果的影响因素
对于单一金属离子溶液,考察吸附剂投加量、初始溶液pH、吸附时间、Cu2+和Mn2+初始质量浓度以及吸附温度对水中Cu2+和Mn2+吸附效果的影响,结果如图2和图3所示。

图2 4A分子筛投加量(a)、初始溶液pH(b)和吸附时间(c)对吸附效果的影响

图3 Cu2+和Mn2+的初始浓度及温度对吸附效果的影响
由图2a可见(吸附温度为25 ℃,Cu2+和Mn2+初始质量浓度分别为200 mg/L和100 mg/L,不调节溶液pH,吸附时间12 h):当4A分子筛投加量从0.6 g/L增至1.4 g/L时,Cu2+的去除率从65.38%提高到99.94%,Mn2+的去除率从76.94%提高到99.06%;当4A分子筛投加量为1.0 g/L时,对Cu2+、Mn2+的去除率分别达到98.67%和97.34%,基本达到吸附平衡,继续增加投加量去除率变化不大。因此,后续实验中4A分子筛的投加量均选择1.0 g/L。
由图2b可见(吸附温度为25 ℃,Cu2+和Mn2+初始质量浓度分别为200 mg/L和100 mg/L,吸附时间12 h),初始溶液pH在3~5和3~8时,随着溶液pH的增加,4A分子筛对Cu2+和Mn2+的吸附能力先增加后趋于稳定。4A分子筛表面因质子化而带正电,对Cu2+和Mn2+有静电排斥作用。随着pH的增大,H+浓度呈几何级数下降,削弱了H+的竞争效应[12]。在调节溶液pH的过程中发现,含Cu2+和Mn2+溶液在pH分别超过5和8时出现沉淀,而且在使用NaOH调节Mn2+溶液pH的过程中极易导致Mn2+氧化为Mn4+而影响吸附效果。因此,后续吸附实验中不再调节溶液pH。
由图2c可见(吸附温度为25 ℃,Cu2+和Mn2+初始质量浓度分别为200 mg/L和100 mg/L):对于Cu2+和Mn2+,吸附量均随着时间的延长而增大,直至达到平衡状态;在吸附初期吸附速率较快,这是由于吸附初期固液两相之间的浓度梯度推动力大,吸附剂上的吸附位点多,随着吸附的不断进行固液两相之间浓度推动力减小,吸附位点也减少,导致吸附速率下降。4A分子筛对Cu2+和Mn2+的吸附分别在8 h和6 h时达到平衡,平衡吸附量分别为198.6 mg/g和98.5 mg/g。
由图3可见(随初始浓度增加延长吸附时间,直至吸附平衡):随着Cu2+和Mn2+初始浓度的增加,吸附量逐渐增加直至达到饱和,且在质量浓度分别低于200 mg/L和100 mg/L时,温度几乎不影响吸附能力;当质量浓度高于200 mg/L和100 mg/L后,Cu2+和Mn2+的吸附量随温度的升高而增大,说明吸附是一个吸热的过程;相同温度、相同浓度时,Cu2+的吸附量大于Mn2+;25 ℃下,4A分子筛对Cu2+和Mn2+的最大吸附量分别为210.3 mg/g和167.0 mg/g。金属(M)离子在溶液中通常以水合离子[M(H2On)]2+的形式存在,Cu2+和Mn2+的水合离子半径分别为0.419 nm和0.438 nm[13],而4A分子筛的有效孔径为0.4 nm,故Cu2+和Mn2+要进入4A分子筛的孔道中进行吸附或与分子筛骨架中的可交换阳离子进行交换,首先需要脱去水分子。脱水的难易取决于金属离子的水合能,水合能越小,金属离子越容易脱水。Cu2+和Mn2+的水合能分别为2 121 kJ/mol和1 862 kJ/mol[14]。理论上水合能小的离子更易脱水进入分子筛孔道内被吸附,但4A分子筛对Cu2+和Mn2+的吸附量并不遵循此规则,该结果可能与Cu2+和Mn2+的电负性和水合离子半径有关。Cu2+的水合半径小,Cu2+电荷中心离4A分子筛表面更近,同时Cu2+的电负性(1.90)高于Mn2+(1.55)。因此,4A分子筛表现出对Cu2+更强的亲和性。
2.2.2 吸附选择性
在吸附温度为25 ℃、Cu2+和Mn2+初始质量浓度均为200 mg/L的条件下,研究了4A分子筛在Cu2+和Mn2+二元金属离子体系中的吸附行为。吸附12 h后,测得Cu2+和Mn2+的吸附量分别为151.7 mg/g和52.1 mg/g,均较单一金属离子体系下降较大,这可能是由于两种重金属离子之间的竞争吸附所致。4A分子筛对Cu2+和Mn2+总的吸附量与单一体系下对Cu2+的吸附量数值上相近,说明4A分子筛的有效吸附位点是一定的。根据文献计算上述二元体系中金属离子在固液相的分配比(D)和选择系数(α)[15],以评价4A分子筛对Cu2+和Mn2+的吸附选择性,结果见表1。由表1可见,Cu2+和Mn2+的分配比分别为3.14和0.35,前者明显大于后者,Cu2+相对于Mn2+的选择系数高达8.97,表明4A分子筛对Cu2+具有更强的亲和性。

表1 Cu2+-Mn2+二元体系竞争吸附参数
2.2.3 循环再生性能
使用后的4A分子筛用去离子水和乙醇洗涤,以去除表面游离的Cu2+和Mn2+,并于100 ℃下干燥6 h。干燥后的4A分子筛在0.1 mol/L HNO3溶液中解吸12 h,以去除吸附的Cu2+和Mn2+,然后洗涤干燥,进行下一次吸附,5次吸附-解吸循环实验结果如图4所示(吸附温度为25 ℃,Cu2+和Mn2+初始质量浓度分别为400 mg/L和300 mg/L,Cu2+和Mn2+吸附时间分别为8 h和6 h)。经过5次循环吸附后4A分子筛对Cu2+和Mn2+的吸附能力基本保持不变。这表明,4A分子筛具有良好的循环稳定性,可重复利用,在去除废水中Cu2+和Mn2+方面具有巨大的应用潜力。

图4 4A分子筛的循环吸附性能
2.3 吸附机理分析
2.3.1 SEM-EDS分析
吸附前后4A分子筛的SEM照片和EDS分析结果分别见图5和表2。可以看出,所合成的4A分子筛为规则的立方结构,且表面光滑。吸附Cu2+后4A分子筛表面被无定形物质覆盖而变得粗糙。吸附后4A分子筛表面检测到Cu和Mn元素说明Cu2+和Mn2+被结合到4A分子筛表面上。吸附前后分子筛骨架中Si与Al的原子比基本为1,且吸附前后4A分子筛晶体形貌基本没有变化,证实其结构稳定。骨架中的Na+含量降低,Cu2+和Mn2+含量增加,证明吸附过程中存在离子交换;并且,随着吸附的进行,溶液中Cu2+或Mn2+的浓度下降而Na+浓度升高(见图6),也说明Cu2+和Mn2+的去除与其和Na+的离子交换有关。吸附Cu2+后表面覆盖的物质可能是因为4A分子筛自身的碱性以及溶液中Na+浓度的增加,促使重金属离子在分子筛表面水解为氢氧化物沉淀而附着在分子筛表面[16]。由于Mn2+水解需要的pH较高,在表面吸附-水解沉淀过程中产生的沉淀物质含量少,故吸附Mn2+后分子筛表面变化较小;而Cu2+水解需要的pH较低,故在分子筛表面水解生成的氢氧化物沉淀也较为明显。
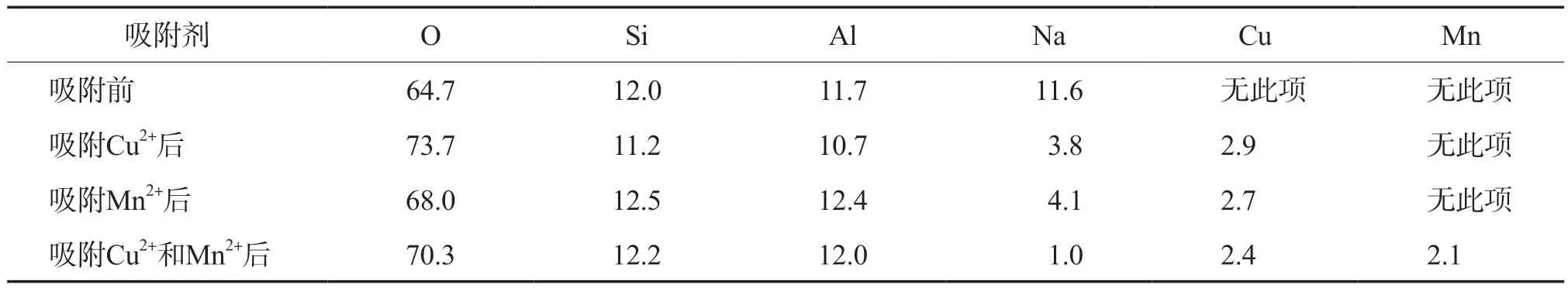
表2 吸附前后4A分子筛的EDS分析结果 x,%
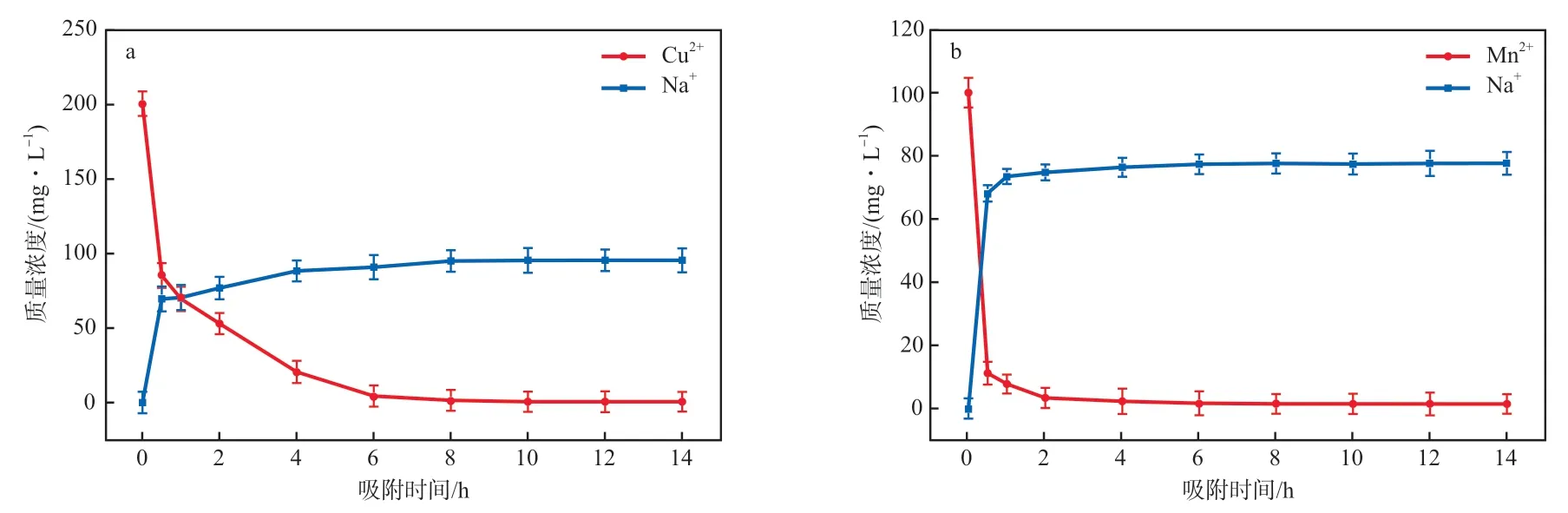
图6 Cu2+(a)和Mn2+(b)吸附过程中溶液中离子浓度的变化
2.3.2 FTIR分析
吸附前后4A分子筛的FTIR谱图如图7所示。3 440 cm-1处的吸收峰归因于4A分子筛中水分子—OH的反对称伸缩振动,1 646 cm-1处则与—OH中氢键的弯曲振动有关[17]。999 cm-1处吸收峰对应T—O—T(T为Al或Si)四面体的不对称拉伸振动特征峰[18],671 cm-1处与4A分子筛中Si—O—Na有关[19],467 cm-1处与T—O的伸缩振动有关,560 cm-1处为分子筛骨架中四元环和六元环的双环振动特征峰。4A分子筛吸附Cu2+和Mn2+后与O—H、T—O—T和T—O基团的强相互作用可能是相关波段特征峰强度和位置偏移(波数减少)的原因[20]。吸附Cu2+后的谱图变化比吸附Mn2+后明显。这是由于Si—O—Al结构中的O带负电,重金属离子的电负性越大,吸引Si—O—Al中O原子电子云能力越强,Al电负性(1.61)小于Cu(1.90),大于Mn(1.55),因此吸附Mn2+后结构基本不发生变化。进一步说明4A分子筛对Cu2+的亲和性优于Mn2+。
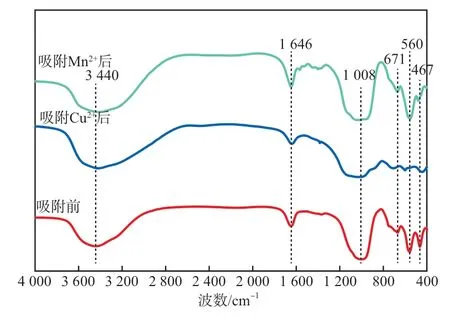
图7 吸附前后4A分子筛的FTIR谱图
2.3.3 XRD分析
吸附前后4A分子筛的XRD谱图如图8所示。吸附Cu2+后的4A分子筛的XRD谱图中出现了少量氢氧化铜的衍射峰,且4A分子筛的特征峰强度明显降低,这主要是其表面被氢氧化铜相覆盖所致,印证了SEM分析中生成氢氧化铜的推测。吸附Mn2+后4A分子筛的主要特征峰明显,只是强度有所下降。吸附Mn2+后与吸附前特征峰基本保持不变。
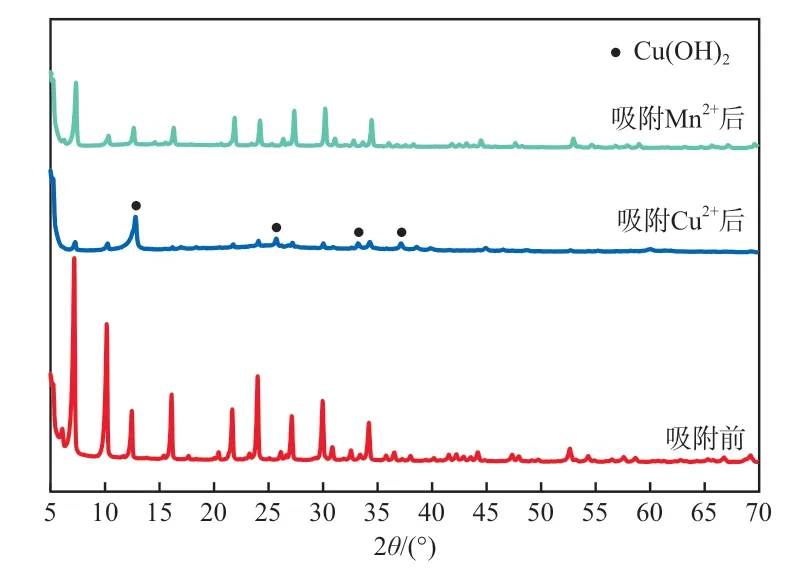
图8 吸附前后4A分子筛的XRD谱图
2.3.4 XPS分析
为了深入了解4A分子筛吸附Cu2+和Mn2+的吸附位点以及价态,对吸附前后的样品进行XPS分析,结果如图9所示。
XPS全谱中检测到Na、O、Al、Si、Cu、Mn和C,其中284.8 eV的C 1s峰为污染碳,以C 1s峰进行表面结合能修正[21]。吸附Cu2+和Mn2+后4A分子筛出现明显的Cu 2p和Mn 2p峰位,说明Cu2+和Mn2+被吸附到4A分子筛上,同时吸附后Na的峰强明显减弱,证明了吸附过程存在Na+交换机制,这与EDS结论一致。Cu 2p精细谱中出现了位于934.8 eV的Cu 2p3/2和954.7 eV的Cu 2p1/2的两个强峰,以及939~944 eV和962.4 eV的卫星峰,表明被吸附的Cu以二价的形式存在于4A分子筛表面[22],且以934.8 eV为中心的Cu 2p3/2峰被认为是Cu—O存在的证明[23-24]。Mn 2p的精细谱图由位于653.8 eV的Mn 2p1/2和642.1 eV的Mn 2p3/2,以及位于656.2 eV和645.8 eV的卫星峰构成,Mn 2p1/2和Mn 2p3/2之间11.7 eV的能量差以及卫星峰的出现表明Mn在吸附后以二价的形式存在[25]。由O 1s谱图可见:吸附前531.5 eV、530.8 eV和536.8 eV出现3个峰,分别对应Si—O、Al—O和Na KLL[26-27];吸附Cu2+和Mn2+后Na KLL峰消失,证明存在Na+交换机制;吸附Cu2+后530.9 eV处出现额外峰,这归因于Cu—O键的形成。
综上,4A分子筛对Cu2+的吸附机理为离子(Na+)交换、Cu2+在4A分子筛表面水解生成氢氧化铜沉淀以及Cu与4A分子筛骨架结构中的O结合形成化学键(Cu—O),对Mn2+的吸附机理主要为离子(Na+)交换。
3 结论
a)以赤泥为原料合成了高纯度单晶相4A分子筛,对较高浓度的Cu2+和Mn2+显示出较强的去除能力。在吸附温度为25 ℃、吸附剂投加量为1.0 g/L且不调节溶液pH的条件下,4A分子筛对Cu2+和Mn2+的最大吸附量分别为210.3 mg/g和167.0 mg/g,Cu2+和Mn2+初始质量浓度分别为200 mg/L和100 mg/L时的去除率分别可达98.67%和97.34%。该4A分子筛且具有良好的稳定性和可重复利用性,经5次循环后吸附量基本保持不变。
b)SEM-EDS、FTIR、XRD和XPS表征结果显示,4A分子筛对Cu2+的吸附机理为离子(Na+)交换、Cu2+在4A分子筛表面水解生成氢氧化铜沉淀以及Cu与4A分子筛骨架结构中的O结合形成化学键(Cu—O),对Mn2+的吸附机理主要为离子(Na+)交换。
c)4A分子筛对Cu2+的亲和性优于Mn2+,二者共存时Cu2+被优先吸附。
