儿童IgA 血管炎相关神经系统损害的临床分析
2023-12-07李芳芳李崇巍郑荣秀
李芳芳,李崇巍,郑荣秀
(1.天津医科大学总医院儿科,天津 300052;2.天津市儿童医院风湿免疫科,天津 300134)
IgA 血管炎既往称为过敏性紫癜,是儿童期最为常见的以小血管受累为主的原发性系统性血管炎。其组织病理学为IgA 介导的白细胞碎裂性血管炎,以非血小板减少性紫癜、腹痛、关节肿痛及肾脏受累等为主要临床表现,少数患者还会出现肺和神经系统损害[1]。神经系统损害发生率为2%[2]。IgA 血管炎神经系统表现多样,症状轻重不一。现将天津市儿童医院2016 年1 月至2022 年1 月收治的34例IgA 血管炎合并明确神经系统损害患儿的病例资料总结如下,为临床医师提供参考。
1 对象与方法
1.1 研究对象 收集2016 年1 月至2022 年1 月天津市儿童医院风湿免疫科收治的IgA 血管炎患儿1 879 例,其中合并神经系统损害34 例。所有患儿均具备典型紫癜样皮疹,诊断符合2010 年EULAR-PRINTO-PRES 共同修订的IgA 血管炎诊断分类标准[3]:在非血小板减少性可触及紫癜或瘀斑的基础上,有以下4 个特征之一:(1)腹痛。(2)关节炎或关节痛。(3)肾脏受累[血尿和(或)蛋白尿]。(4)组织学上以IgA 沉积为主的白细胞破坏性血管炎或增生性肾小球肾炎。34 例合并神经系统损害的IgA 血管炎患儿均有明确神经系统症状及相关阳性实验室检查。
将34 例伴随神经系统损害的IgA 血管炎患儿设为神经系统损害组,随机数字表法抽取同期非神经系统损害病例72 例设为非神经系统损害组,对两组资料进行回顾性分析并对比。
1.2 方法 所有患儿均检测腹部B 超、尿常规、尿转铁蛋白、尿微量白蛋白,测定血Ig 水平及便钙卫蛋白。神经系统损害组根据神经系统症状,分别行脑电图、头颅CT、头颅MRI、脑脊液、肌电图及神经电生理等检查。
1.3 统计学处理 采用SPSS 23.0 软件进行数据分析。计数资料以率或构成比表示,比较采用χ2检验,偏态分布的计量资料用[M(P25,P75)]表示,比较采用Mann-Whitney 秩和检验。正态分布计量资料以表示,两组间比较采用t 检验。P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料 本研究中神经系统损害发生率为1.8%(34/1 879)。神经系统损害组男19 例,女15例,男女比例为1.3∶1,年龄2~15 岁,中位数年龄为7岁;非神经系统损害组男40 例,女32 例,男女比例为1.25∶1,年龄3~15 岁,中位数年龄为7 岁,两组间差异无统计学意义。
2.2 临床表现 神经系统损害组和非神经系统损害组在消化道症状、消化道出血及皮疹出现在非典型部位方面存在统计学差异(均P<0.05),软组织肿胀及肾损害方面无统计学差异(均P>0.05),见表1。

表1 神经系统损害组与非神经系统损害组患儿一般资料、临床特征比较[M(P25,P75),n(%)]Tab 1 Comparison of general information and clinical characteristics in children between the neurological damage group and the non-neurological damage group[M(P25,P75),n(%)]
神经系统损害组中22 例出现头晕、头痛;15 例出现肌力轻度下降,其中1 例伴腱反射减弱及心率明显增快;2 例抽搐,均为多次发作,且1 例为癫痫持续状态;2 例出现晕厥;1 例出现眩晕、复视、眼球震颤;1 例出现运动障碍。
2.3 辅助检查 神经系统损害组和非神经系统损害组相关化验检查,差异无统计学意义(均P>0.05),见表2。
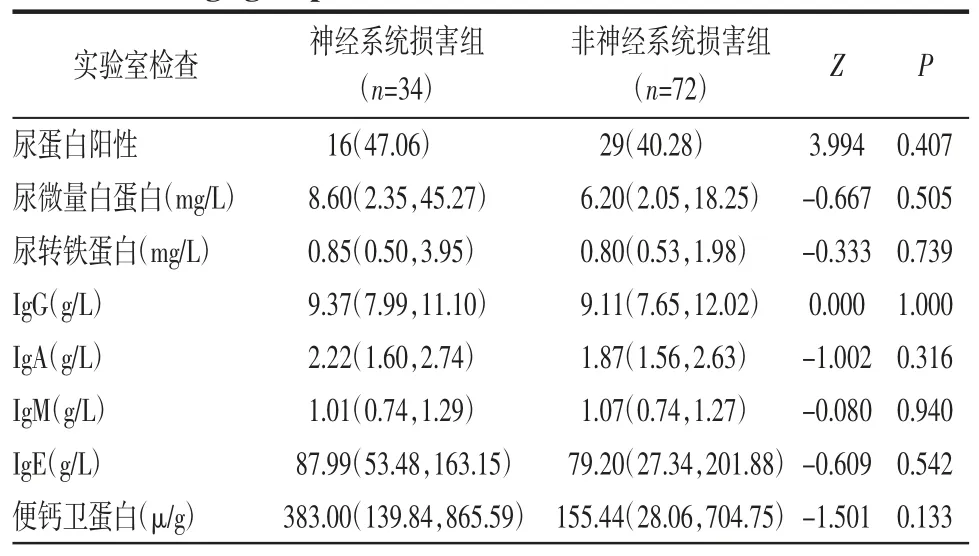
表2 神经系统损害组与非神经系统损害组实验室检查指标比较[M(P25,P75),n(%)]Tab 2 Comparison of laboratory examination indicators between the neurological damage group and the non-neurological damage group[M(P25,P75),n(%)]
此外,神经系统损害组22 例行脑电图检查,其中16 例显示清醒脑电图出现背景慢波;8 例行头部CT 检查,其中2 例显示低密度病灶;17 例行MRI检查,其中6 例提示脑实质区缺血性改变,1 例剧烈头痛者显示静脉窦血栓(该患儿抗心磷脂抗体阴性,蛋白S 活性降低),2 例抽搐者提示为大脑后部可逆性脑病综合征(PRES)(图1),1 例运动障碍患儿发现脊髓区的长T2 信号影;仅2 例患儿行腰穿脑脊液检查,未见明显异常;15 例肌力下降患儿神经电生理检查均显示周围神经损害,1 例复视患儿视觉诱发电位显示视神经通路异常。

图1 患者头MRI(PRES)结果Fig 1 Result of head MRI(PRES)in patient
2.4 治疗 神经系统损害组均接受了糖皮质激素治疗,15 例仅常规剂量激素治疗后好转,19 例均采用了强化治疗,大剂量甲强龙冲击治疗8 例,使用环磷酰胺15 例,静脉应用丙种球蛋白治疗10 例,其中7 例采用甲强龙冲击联合环磷酰胺治疗,5 例应用甲强龙冲击联合环磷酰胺及丙种球蛋白治疗。针对神经系统症状均给予对症支持治疗,抽搐者予以止痉及降颅压,血栓患儿应用肝素钙及华法林抗凝治疗,1 例表现为格林-巴利综合征的患儿予丙种球蛋白冲击治疗好转,34 例患儿均给予营养神经支持治疗。非神经系统损害组中仅3 例应用甲强龙冲击治疗,2 例应用环磷酰胺治疗,其中1 例应用了甲强龙冲击联合环磷酰胺治疗,其余68 例仅予常规剂量糖皮质激素或对症治疗后好转。
2.5 转归 两组患儿出院时病情均好转,出院后随访6 个月均未遗留后遗症。
3 讨论
IgA 血管炎是儿童期最为常见的系统性小血管炎,既往认为很少累及神经系统,本研究发现IgA血管炎相关神经系统损害发生率为1.8%,与既往报告的神经系统损害发生率(2%)[2]相符,国外文献报道发生率为0.65%~8.00%[4]。神经系统损害常发生在病情严重的IgA 血管炎患儿中,其与消化系统症状关系密切,部分文献报道亦常出现在肾损害患儿中[5-6]。本研究发现,神经系统损害容易出现在合并消化道症状尤其是出现消化道出血的IgA 血管炎患儿中,其次易发生在皮疹出现在非典型部位的IgA 血管炎患儿中,与软组织肿胀无相关性,且实验室检查并无特异性。与既往研究结果不同的是,本研究未发现神经系统损害与肾损害存在明确相关性,分析原因为IgA 血管炎肾损害发生均较急性期症状滞后,患儿前期因严重消化道症状强化治疗可能减少了肾损害的发生。
IgA 血管炎相关神经系统损害的表现多种多样,症状轻重不一,轻微的症状容易被忽略,以头晕、头痛最为常见,外周神经损伤导致肌力轻度下降出现频率较高,本研究仅统计了明确神经系统损伤的患儿,部分患儿因仅有轻微头痛或精神行为改变,未做进一步检查所以未纳入研究。IgA 血管炎可并发严重的中枢神经系统损害,表现为抽搐、视觉障碍、剧烈头疼、运动障碍和眼球震颤等。本研究发现2 例患儿出现癫痫发作,结合头颅MRI 检查考虑大脑后部可逆性脑病综合征。PRES 是一种临床放射学综合征,其特征是发生头痛、视觉功能障碍、癫痫发作和意识改变,头颅MRI 检查常表现为双侧顶枕叶皮层及皮层下多发斑片状异常信号影,通常表现为病变区域长T1 长T2 信号,FLAIR 呈高信号。IgA血管炎合并PRES 的诱因可能包括:免疫抑制剂、高血压、细胞毒药物、肾功能不全或IgA 血管炎高度活动期[7]。PRES 甚至可作为IgA 血管炎的首发症状出现[8]。本研究中2 例病例无相关诱因,考虑为疾病本身活动度高所致,IgA 沉积于脑血管,导致血-脑屏障破坏和调节功能丧失,可引发PRES[9]。静脉窦血栓形成是IgA 血管炎的罕见并发症[10],突发性头痛是其最常见的症状,也可表现为癫痫发作和失明,矢状窦是最常见的血栓形成部位,与该部位管腔壁厚不规则、血流速度缓慢有关,糖皮质激素和抗凝药物的联合治疗可有效快速缓解临床症状[11]。有研究表明,IgA 血管炎患儿和正常儿童相比,血液呈现高凝状态,推测IgA 血管炎出现血栓可能与抗磷脂抗体综合征相关[12-13]。既往文献报道IgA 血管炎外周神经系统损害发生率低,以单神经病为主,少数出现多发性神经病[4,12]。本研究中观察到周围神经系统损害发生率为44.1%,34 例患者中有14 例神经电生理检测为单发神经病变或多发单神经病变,仅1 例符合格林-巴利综合征样表现,IgA 免疫复合物可在神经纤维处沉积并造成神经损伤,诱发脱髓鞘病变引起格林-巴利综合征[12]。此外,需要关注的是维生素B12 缺乏亦可引起周围神经损伤[14],本研究中部分患儿因严重消化道症状禁食时间较长,B 族维生素摄入不足,神经电生理异常需考虑此相关因素。
IgA 血管炎并发神经系统损害的机制与IgA免疫复合物沉积在颅内血管有关,可引起脑血管炎,导致水肿、缺血、梗死、出血。脑血管炎的诊断主要依赖于临床表现结合影像学的提示,MRI 在检测早期病变方面优于CT,其最常出现枕叶和后顶叶区皮层及皮层下异常信号影[12]。本研究结果与之相符,额叶、颞叶和小脑受累少见,推测后循环的血流动力学特征可能有利于IgA 优先沉积在这些血管中[4]。脑脊液通常是正常或非炎症性的,其主要目的是排除其他病因。脑电图及神经电生理检查阳性率高,且为无创性检查,简便易行,是头痛或肌力下降的患儿首选。
关于IgA 血管炎合并神经系统损害的治疗,轻症仅予对症治疗均可好转。而存在严重中枢神经系统损害者,常与原发病活动相关,需加强原发病的治疗,糖皮质激素是首选用药,部分严重患儿可应用大剂量甲强龙冲击治疗,难治性病例可使用环磷酰胺、丙种球蛋白、霉酚酸酯、环孢素A 等作为补充治疗,血浆置换亦可作为治疗重症病例的有效措施[15]。本研究中A组的难治性病例采用联合治疗均病情好转。对于在PRES 患儿中是否应用糖皮质激素治疗尚存在争议,有学者认为大剂量糖皮质激素的应用会加重病情,推荐应用丙种球蛋白[7]。但亦有研究显示,激素在减轻血管内皮损伤和恢复血-脑屏障的通透性方面发挥有效作用[16]。本研究中两例PRES 患儿1 例应用了甲强龙冲击治疗,获得良好预后。外周神经损害多数症状较轻,1 例格林-巴利综合征患儿对于丙种球蛋白反应良好,其余轻度肌力下降患儿予营养神经对症治疗后好转。
总之,IgA 血管炎合并神经系统损害相对少见,临床以头晕、头痛和肌力轻度下降最为常见,也可出现严重神经系统损伤,如PRES、静脉窦血栓、复视、格林-巴利综合征样表现等,神经系统损害常发生在合并消化系统症状尤其是合并消化道出血的患儿中,其次易发生在皮疹出现在非典型部位的患儿中,多与疾病本身高活动度相关,治疗除予对症治疗外,常需加强原发病的治疗。
