多酶体系中谷胱甘肽HPLC 分析方法研究
2023-12-04张浩月穆玉敏秦浩杰杨梦茜刘丽荣任丽梅
张浩月,穆玉敏,秦浩杰,杨梦茜,刘丽荣,任丽梅
(1.美邦美和生物科技有限公司,河北 石家庄 050000;2.石家庄学院 化工学院,河北 石家庄 050035;3.河北省生物制药国际联合研究中心,河北 石家庄 050035;4.河北省高校微生物制药应用技术研发中心,河北 石家庄 050035;)
0 引言
人类细胞质中存在一种自然合成的三肽,由L-谷氨酸、L-半胱氨酸和甘氨酸组成的γ-L-谷氨酰-L-半胱氨酰-甘氨酸,即还原型谷胱甘肽(Glutathione,GSH),可维持细胞生物的正常功能,对正常的免疫系统功能起重要作用,并且具有解毒、抗氧化等、促生长、提高生物对不良环境影响的作用,广泛用于酒精、药物及其他各种原因导致的肝损伤治疗。
1921 年,英国生化学家发现了Hopkins 谷胱甘肽,从酵母抽提物中分离得到,并正式命名为glutathione;其后对GSH 的提取、分离及分析检测方法等方面进行了研究。生产谷胱甘肽有4 种方法,分别为溶剂萃取法、传统化学合成法、微生物发酵法和酶催化法。
在工业领域应用最广的是化学合成法和萃取法,目前酶催化法具有越来越高的研究价值。GSH工业化生产最早的方法是化学法合成法,其存在耗时长、污染大、成本高等缺点,制约了其进一步工业化的发展。近几年,体外酶催化法是生产GSH的主要研究方向。
体外酶催化法是指利用酶来催化3 种氨基酸合成GSH 的方法,生产工艺相对简单,是其最大的优势,且可有效消除反馈抑制,使GSH 有较高的产量。酶法合成GSH 的关键在于制备高性能的GSH 合成酶体系和高效率的ATP 再生体系。由于我国对谷胱甘肽钠的关注较晚,故近几年对还原型谷胱甘肽钠研究分析是人们关注的热点,测定谷胱甘肽钠的含量采用的是紫外分光光度法,但准确度不高,干扰严重;毛细管区带电泳分析法优点在于可实现快速检测,精密度及准确度较高,但对操作要求较高;药典介绍了测定谷胱甘肽片HPLC 法,C18 色谱柱(十八烷基硅烷键合硅胶填充);以磷酸盐缓冲液为流动相(称取磷酸二氢钠6.8 g,庚烷磺酸钠2.2 g,加水1 000 mL 使溶解,用磷酸调节pH 值3.0)-甲醇(96∶4),检测波长为210 nm。此方法可有效分离L-半胱氨酸、L-谷氨酸钠、甘氨酸、ATP、还原型谷胱甘肽、氧化型谷胱甘肽等,但检测时长为40 min,不利于日常分析检测。故匹配新工艺的发展,开发新的快速检测且有效的分离方法是至关重要的。
1 实验部分
1.1 仪器与试剂
高效液相色谱仪P230Ⅱ,大连依利特分析有限公司。
电子天平AUW220D,赛多利斯仪器有限公司。
pH 计Seven2 Go S2,梅特勒-托利多仪器有限公司。
还原型谷胱甘肽,阿拉丁,纯度99%。
氧化型谷胱甘肽,阿拉丁,纯度99%。
L-半胱氨酸盐酸盐一水合物,麦克林,纯度99%。
L-谷氨酸钠一水合物,麦克林,纯度99%。
甲醇为色谱纯,科密欧,99.9%。
四丁基硫酸氢胺meilunbio;纯度99%。
1.2 实验方法
1.2.1 流动相
0.05mol/L 磷酸氢二钠-0.05 mol/L 磷酸二氢钾-8 mmol/L 四丁基硫酸氢铵(pH 值为4.5)-甲醇(V/V=80∶20)
1.2.2 色谱条件
色谱柱:岛津Wonda Cract ODS-2 (4.6×250 mm,5 μm)。
流速:1.0 mL/min。
波长:214 nm。
柱温:30 ℃。
进样量:10 μL。
洗脱时间:15 min。
2 结果与讨论
2.1 流动相的选择
使用岛津Wonda Cract ODS-2 色谱柱,分别使用以下3 种洗脱体系进样检测:
(1)0.028 mol/L 磷酸二氢钾(pH 值为3.0)-甲醇(V/V=95∶5)。
(2)[0.028 mol/L 磷酸二氢钾-10 mM 庚烷磺酸钠(pH2.5)]-甲醇(V/V=96∶4)。
(3)[0.05 mol/L 磷酸氢二钠-0.05mol/L 磷酸二氢钾-8 mmol/L 四丁基硫酸氢铵(pH 值为4.5)]-甲醇(V/V=80∶20)。
当采取洗脱体系(1)时,L-半胱氨酸盐酸盐、L-谷氨酸钠、甘氨酸分离度差,三峰不能分离,混合标准溶液测试结果如图1 所示。
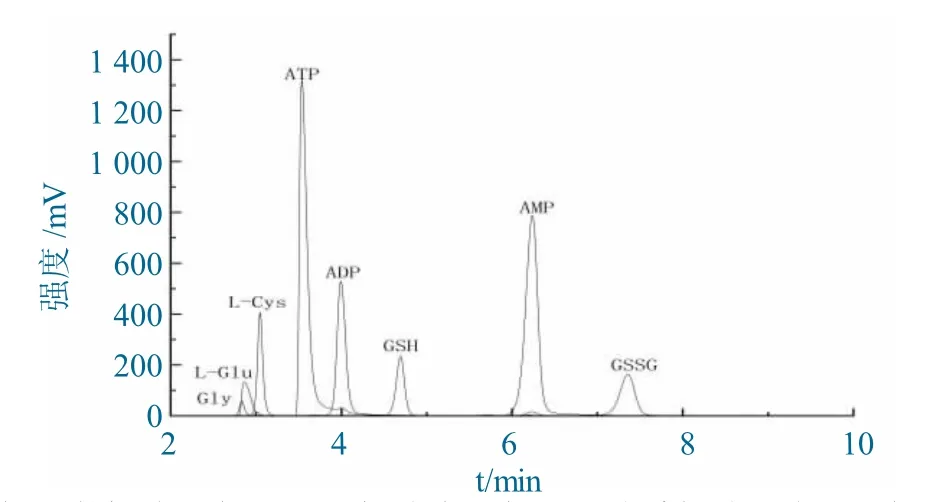
图1 混合标准溶液测试结果Fig.1 Test result of the mixed reference solution
当采取洗脱体系(2)时,ATP 钠盐的保留时间40 min,不利于实际分析应用。
混合标准溶液测试结果如图2 所示。
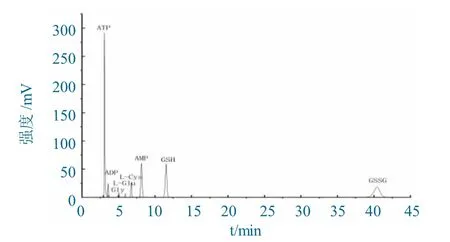
图2 混合标准溶液测试结果Fig.2 Test result of the mixed reference solution
当采取洗脱体系(3)时,ATP 出峰时间缩短约为13 min,干扰少,峰形良好,且L-半胱氨酸盐酸盐、L-谷氨酸钠、还原型谷胱甘肽、氧化型谷胱甘肽之间分离度R 分别为2.21、5.03 和2.55,均>1.5;甘氨酸与L-半胱氨酸盐酸盐之间分离度1.25,>1.0,表明各组分可较好分离,混合标准溶液测试结果如图3 所示。
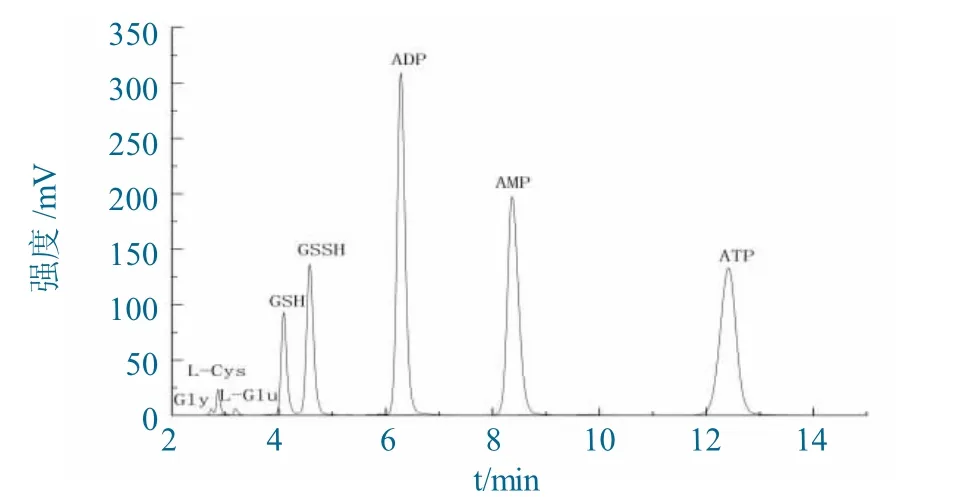
图3 混合标准溶液测试结果Fig.3 Test result of the mixed reference solution
2.2 线性关系考察
(1)准确称取还原型谷胱甘肽标准品12.5 mg,置于25 mL 容量瓶,用流动相溶解定容至刻度,摇匀得还原型谷胱甘肽标准溶液0.50 mg/kg。取上述标准溶液,用流动相分别稀释至0.01、0.05、0.10、0.25 和0.50 mg/kg,摇匀备用。
(2)准确称取氧化型谷胱甘肽标准品12.5 mg,置于25 mL 容量瓶,用流动相溶解定容至刻度,摇匀得氧化型谷胱甘肽标准溶液0.50 mg/kg。取上述标准溶液,用流动相分别稀释至0.000 2、0.000 5、0.002 0、0.005 0 和0.010 mg/kg,摇匀备用。
(3)准确称取L-半胱氨酸盐酸盐一水合标准品12.5 mg,置于25 mL 容量瓶,用流动相溶解定容至刻度,摇匀得L-半胱氨酸盐酸盐标准溶液0.50 mg/kg。取上述对标准溶液,用流动相分别稀释至0.000 5、0.001 0、0.002 5、0.005 0 和0.010 mg/kg,摇匀备用。
(4)准确称取L-谷氨酸钠一水合物标准品50.0 mg,置于25 mL 容量瓶,用流动相定溶解容至刻度,摇匀得L-谷氨酸钠标准溶液2 mg/mL。取上述标准溶液,用流动相分别稀释至0.025、0.050、0.20、0.50 和1.0 mg/kg,摇匀备用。
(5)准确称取甘氨酸标准品50.0 mg,置于25 mL 容量瓶,用流动相定溶解容至刻度,摇匀得甘氨酸标准溶液2 mg/mL。取上述标准溶液,用流动相分别稀释至0.025、0.050、0.10、0.20 和0.50 mg/kg,摇匀备用。
分别取上述各组分摇匀备用的稀释液于0.45 μm 水系滤膜过滤后,进行HPLC 检测,以峰面积(Y)为纵坐标,进样浓度(X,μg/mL)为横坐标,绘制5 组标准曲线。
线性关系测试结果见表1。
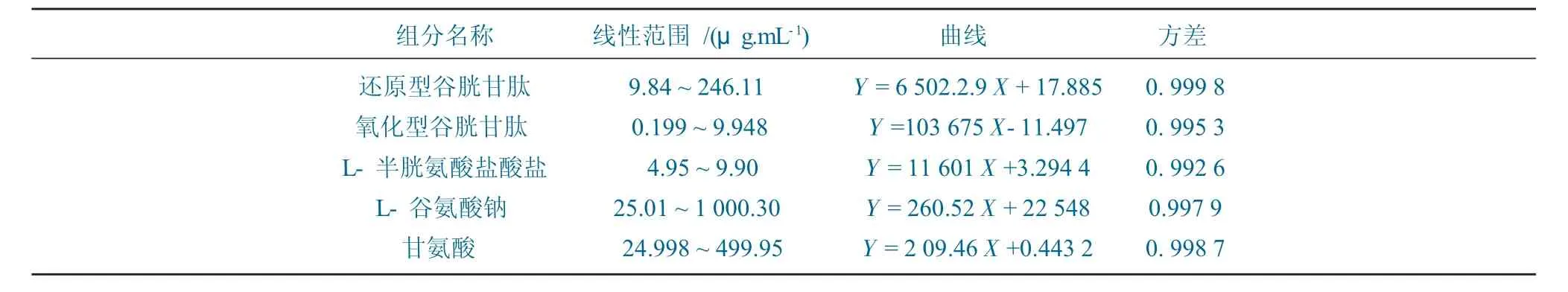
表1 线性关系测试结果Table 1 Result of linear relationship test
由表1 可以看出,GSH 在(0.01~ 0.5)mg/L内线性关系良好。方法检出限为0.2 ng,方法定量限为0.6 ng。
2.3 精密度和回收率试验
在“1.2”项色谱条件下,取不同浓度标准溶液连续进样6 次,观察各组分峰面积的RSD 及各标准品回收率。各组分峰面积的RSD 均<2.0%(n=6),表明仪器精密度良好;不同加标浓度测得样品的回收率在94.6%~110.0%,表明该方法的准确度良好。精密度和准确度结果见表2。
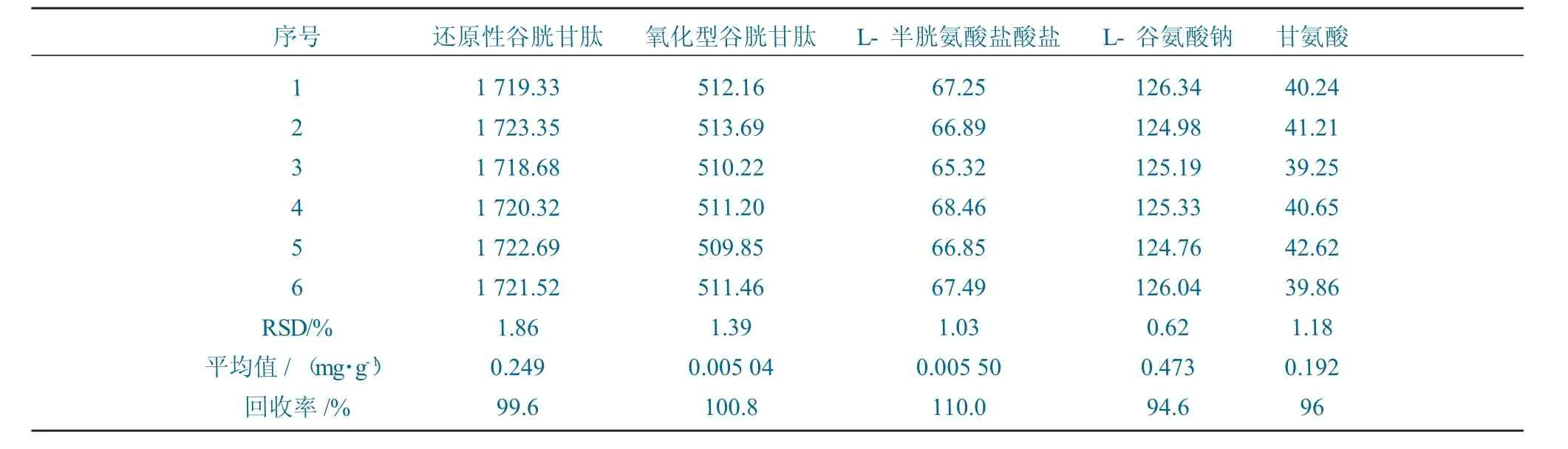
表2 精密度和准确度结果Table 2 Result of the precision and spiked recoveries
2.4 样品含量测定
反应液中还原型谷胱甘肽含量测定,1 h 反应结果如图4 所示。

图4 1 h 反应结果Fig.4 Reaction result of 1 h
反应液中还原型谷胱甘肽含量测定,2 h 反应结果如图5 所示。

图5 2 h 反应结果Fig.5 Reaction result of 2 h
反应液中还原型谷胱甘肽含量测定,3 h 反应结果如图6 所示。

图6 3 h 反应结果Fig.6 Reaction result of 3 h
反应液中还原型谷胱甘肽含量测定,4 h 反应结果如图7 所示。
2.5 反应转化率计算
(1)L-半胱氨酸盐酸盐转化生成还原型谷胱甘肽的反应转化率计算式如下:
(2)依据不同取样时间L-半胱氨酸盐酸盐转化为还原型谷胱甘肽的转化率结果,绘制对应还原型谷胱甘肽转化率曲线,表明该反应较为迅速,2 h 时转化率可以达到85%,考虑后续实验需求,在反应2 h 时即可终止反应。样本转化率见表3。
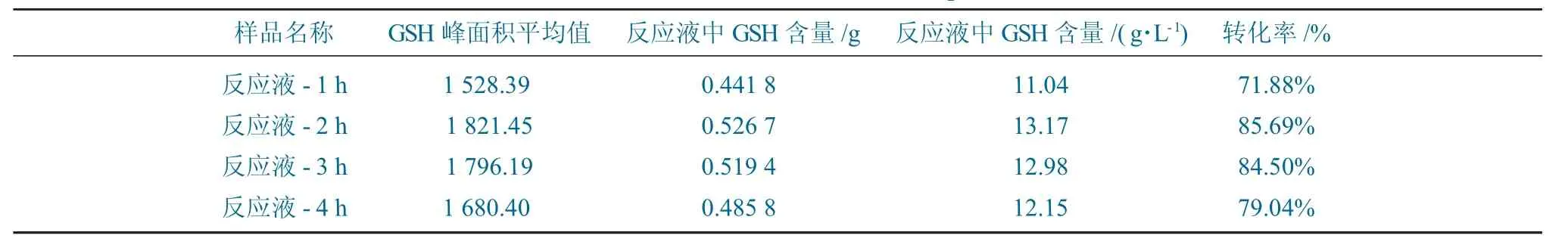
表3 样本转化率Table 3 Conversion rate of the samples
不同时间样品转化率如图8 所示。
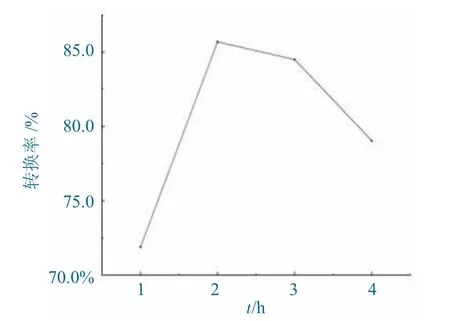
图8 不同时间样品转化率Fig.8 Conversion rate of samples at different times
3 结语
研究初期,依据常用缓冲盐体系及药典提及添加庚烷磺酸钠离子对的方法进行了尝试。常用缓冲盐磷酸二氢钾体系,对反应底物L-半胱氨酸、L-谷氨酸钠、甘氨酸不能完全分离。药典方法虽然可以实现目标峰可完全分离,但检测时间较长,不利于日常分析检测;所以2 种方法均不能达到实验目的。本方法针对多酶体系中各组分含量检测建立,与药典方法相比,缩短检测时长,且对体系中各组分均可定量检测。此方法应用初期,甘氨酸、L-半胱氨酸两物质出峰时间较近,后期针对缓冲盐体系的pH 值及有机相比例进行调整。经过验证,优化后的方法分离度更高、简便快捷,可以用于生成还原型谷胱甘肽反应液中GSH、GSSG、Gly、L-Cys、L-Glu、AMP、ADP、ATP 含量的测定,以及转化率的计算,对实际生产有重要的指导意义。
