以腹膜及下颌下腺受累的IgG4相关性疾病一例并文献复习
2023-12-01罗亚丹杨宇齐达静静袁立英
罗亚丹,查 艳,杨宇齐,达静静,袁 静,袁立英,张 唐
(1.遵义医科大学第三附属医院 肾内科, 贵州 遵义 563000;2.贵州省人民医院 肾内科, 贵州 贵阳 550002;3.国家卫生健康委员会肺脏免疫性疾病诊治重点实验室,贵州 贵阳 550002)
IgG4相关性疾病(IgG4-related disease,IgG4-RD)是20世纪90年代发现的一类罕见病,“貌似肿瘤,却非肿瘤”,首先于1995年由Yoshida等[1]在研究自身免疫性胰腺炎时提出。2003年由Kamisawa等[2]首次引入IgG4系统性疾病概念,即IgG4相关性疾病。该疾病是一种全身性疾病,累及全身多重器官,如胰腺、唾液腺(下颌下腺、腮腺、舌下腺)、泪腺、甲状腺及腹膜等,病变部位常有大量淋巴细胞和浆细胞浸润。
该病中老年好发,男性多于女性[3-4],病因不明,发病率约0.6/10万[5],由于少见,认识不充分,且容易形成肿块,常被误认为恶性肿瘤。目前依据2011年日本制定的IgG4-RD综合诊断标准及2019年美国风湿病学会(ACR)/欧洲抗风湿病联盟(EULAR)制定的IgG4-RD分类标准,治疗准则是糖皮质激素联合免疫抑制剂,但是具体药物选择及剂量根据患者具体年龄、性别、体重、骨密度、累及器官及其损伤程度和有无并发症等情况,用药时密切评估患者状态及病情缓解情况调整激素及免疫抑制剂剂量,避免药物副作用的出现。绝大多数IgG4-RD对激素反应快,效果好[6]。现对遵义医科大学第三附属医院肾内科收治的1例同时累及下颌下腺及腹膜的IgG4-RD病例进行报道。
1 病例介绍
男性,62岁,退休干部,因“右侧双J管置入术1月”于2019年6月28日收入遵义医科大学第三附属医院泌尿外科。患者1月前因双肾积水及肾功能受损于泌尿外科行双J管置入术,住院期间左侧双J管自行脱落,术后感右侧腰部隐痛,为更换双J管再次入院。在诊疗过程中出现尿量减少至0 mL/24 h、血肌酐增高至1 441.5 μmol/L,于2019年7月7日转入肾内科。既往“左肺肿瘤”切除10年,病理提示“假性瘤”;“2型糖尿病”8年,服用阿卡波糖等控制血糖;“高血压”病史6年,服用依拉普利等控制血压。2019年2月因“双颌下包块”于我院乳甲外科手术,病理石蜡切片结果:涎腺组织慢性炎症,其内淋巴组织增生伴淋巴滤泡形成。病理冰冻切片结果:良性病变。出院后1周切口大出血再次入院手术止血,无烟酒嗜好,婚育家族史无特殊。体格检查:体温36.8 ℃,脉搏89次/min,呼吸20次/min,血压127/87 mmHg,神志清楚,安静面容,查体合作,步入病房,全身皮肤黏膜无苍白、黄染、出血点,颈部见2条长约3 cm陈旧性手术疤痕,双肺呼吸音清,未闻及干、湿罗音,心界不大,心率89次/min,律齐,心音有力,各瓣膜听诊区未闻及杂音。腹软,无明显压痛、反跳痛、肌紧张,肝脾双肾未扪及,右肾区轻叩痛,左肾区无叩痛,移动性浊音阴性,双下肢无水肿。入院后腹部B超:双肾轻度积水、输尿管梗阻;腹部CT:腹主动脉周围不规则软组织密度影,腹膜后纤维化?(图1A、B、图3A);尿素氮(BUN)12.5 mmol/L,血清肌酐(sCr)389.6 μmol/L,血清IgG4 11.7 g/L(正常值0.03~2.01 g/L),血清IgG 16.6 g/L(正常值7.51~15.6 g/L),红细胞沉降率(ESR)水平显著升高;尿常规:潜血可疑,白细胞可疑,蛋白阴性,白细胞12个/μL。结合患者以上资料,高度怀疑IgG4-RD,将2019年2月在我院乳甲科住院所切下颌腺包块组织送广州金域医学检验中心行免疫组化:IgG散在阳性(10~20个/HPF),IgG4/IgG阳性细胞比值约为0.7(图2A、B)。考虑患者10年前诊断“肺部假性瘤”,将10年前我院切除的肺部组织再次送广州金域医学检验中心行免疫组化提示IgG4/ IgG:0(图2C)。结合血清检测、腹部B超及CT检查显示双肾积水、输尿管梗阻、腹膜后纤维化及下颌腺组织病理学检查结果,依据2011年日本制定的IgG4-RD综合诊断标准该患者诊断IgG4-RD,予静脉输注甲泼尼龙80 mg/次,每天1次,3 d后改为40 mg/d口服,联合静脉输注环磷酰胺1 g/月(连续6个月),共输注6 g,期间甲强龙逐渐减量,同时给予更换双J管、血液透析2次及对症、支持等治疗。经上述治疗,患者3 d后尿量恢复至2 800 mL/24 h,血肌酐降至155.7 μmol/L,19 d后复查血清IgG4明显下降,23个月复查腹部CT,腹膜后纤维化范围与入院时比较明显缩小(图3B、图4)。2020年3月取出左侧双J管,尿量无明显减少,2020年8月取出右侧双J管,肌酐及尿量无明显变化,2022年11月19日复查血清IgG4 0.3 454 g/L,血肌酐124.4 μmol/L,甲泼尼龙4 mg/8 mg交替服用维持治疗。

A、B:下颌下腺组织IgG4细胞阳性(红色箭头,×400);C:肺部组织IgG4细胞阴性(×200)。图2 下颌下腺及肺部包块切除术后标本免疫组化
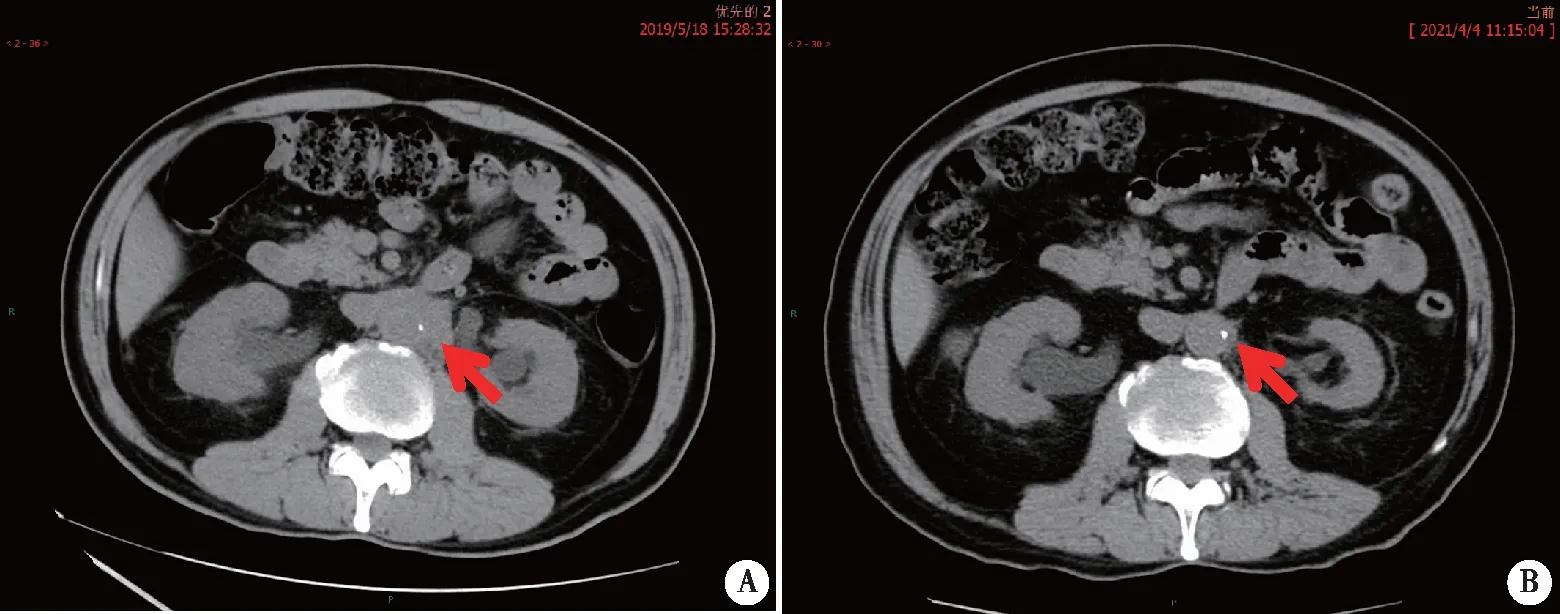
A:2019年6月腹主动脉周围不规则软组织密度影,腹膜后纤维化(红色箭头);B:2021年5月复查腹部CT,腹膜后纤维化范围与入院时比较明显缩小(红色箭头)。图3 腹膜受累CT表现
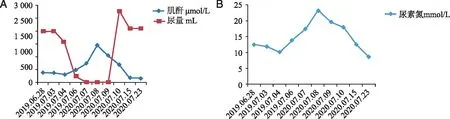
A:蓝色线条表示血肌酐、红色线条表示尿量;B:蓝色线条表示尿素氮。图4 尿量、肌酐、尿素氮时间线流程
2 讨论
IgG4是人类血清中的抗体,是免疫球蛋白IgG4种分型中的一种亚型,占免疫球蛋白IgG的5%左右,具有独特的生物学特性,能够进行Fab-arm交换,产生双特异性功能单价抗体,限制形成免疫复合物和激活补体的能力,存在于一系列不同的疾病中[7-8],但是它对IgG4-RD的发病机制仍不太清楚,推测可能为血清中IgG4含量增高,IgG4阳性浆细胞浸润不同器官所致炎性增生。
IgG4-RD是目前人类罕见的自身免疫性疾病之一[9],近年来成为国内外研究热点,随着医疗技术的日益发展及临床医师对罕见病认识的提高,漏诊率及误诊率也逐渐降低。因此,临床表现多种多样,可以有胰腺、唾液腺(下颌下腺、腮腺、舌下腺)、泪腺、甲状腺及腹膜后等全身不同器官损害[10],且发病慢,隐匿,故仍有可能被误诊(包括诊断错误和延误诊断)。部分患者可以为单一的器官受累(如泪腺、淋巴腺、肾上腺、硬化性胆管炎、耳部症状),且在病程中几乎无发热、乏力等全身症状,因早期不易发现导致易发生漏诊,有经验的专科医师会怀疑该疾病而进一步检查发现血清IgG4增高[11],而如果累及肾脏则为IgG4-RD(IgG4-RKD),主要常见表现为肾脏组织内大量IgG4+浆细胞浸润、席纹状纤维化,肾小管间质炎症 (IgG4-related tubulointerstitial nephritis, IgG4-TIN) 、膜性肾病 (IgG4-related membranous nephropathy, IgG4-MN)[12]。本病例为下颌下腺受累以及腹膜后发生纤维化引起梗阻性肾病,该情况较为少见。由于该患者合并多年糖尿病、高血压、肺部假性瘤基础病史,且病程中突发的无尿和严重肾功能障碍,医师未及时发现并诊断IgG4-RD。然而,影像学检查常常能帮助我们寻找到相关的关键线索,计算机断层扫描(CT)、正电子发射断层扫描(PET)进行的CT、磁共振(MR)成像、MR胰胆管造影和超声内镜是评估IgG4-RD的常用方法[13]。结合患者的腹部计算机断层扫描(CT)提示腹膜后纤维化,血清IgG4明显增高以及病理切片提示IgG4阳性浆细胞,根据2011年日本的诊断标准,故诊断为IgG4-RD[14-15]。
IgG4-RD一旦确诊,接下来则需根据器官受累情况以及相应病理机制选择合适的治疗和随访策略。早期规范治疗可避免重要器官不可逆的损伤,减少并发症。2021年我国《IgG4相关性疾病诊治中国专家共识》中指出激素和细胞毒药物是治疗IgG4-RD及预防其复发的主要药物,激素的有效率在90%以上[16],可单独使用,也可联合应用。本病例采取长期激素联合环磷酰胺治疗后,高滴度血清IgG4与血沉等反应指标呈进行性下降并一直稳定在正常水平。推测ESR及IgG4水平是一些患者疾病活动性的有用的指标,相关文献也提示可以根据监测其水平调整激素疗程及剂量,以避免复发[11, 17]。Matsumura等[18]和Doumen等[19]总结的病例中,使用以糖皮质激素为核心的药物治疗均能使患者获得一定的缓解甚至改善。当患者存在较高的复发风险时,可在糖皮质激素基础上联合免疫抑制剂如环磷酰胺、硫唑嘌呤和吗替麦考酚酯等进行治疗。循证医学研究表明,糖皮质激素联合免疫抑制剂治疗的患者可获得较单用糖皮质激素治疗更佳的缓解效果[9]。同时,本例患者通过激素治疗缓解后并联合环磷酰胺治疗后,腹部CT提示腹膜后纤维化范围减小,提示影像学的变化可能与血清IgG4的水平有正相关关系,但由于仅为个案报道,还需要更大样本量的临床研究证实。此外,患者腹膜后纤维化导致发生梗阻性肾病引发的急性肾损伤情况非常凶险,提示我们加强临床上对IgG4的早期认识及诊治,可能减少和避免并发症的出现。随着精准医学发展,生物制剂在临床疾病中的应用越来越广泛,目前对于常规治疗方案失败、激素治疗效果不佳或重症的IgG4-RD患者,有应用前景的生物靶向治疗包括:B 细胞清除治疗[如:抗 CD20 单抗(利妥昔单抗)、抗 CD19 单抗(奥贝利单抗)、B淋巴细胞活化因子抑制剂(贝利尤单抗)、布鲁顿氏酪氨酸激酶抑制剂(泽布替尼)、硼替佐米]、靶向 T 淋巴细胞[T细胞共刺激调节剂(阿巴西普)、信号淋巴细胞激活分子家族成员 7单克隆抗体(埃罗妥珠单抗)]和靶向细胞因子[IL-4受体α单克隆抗体(度普利尤单抗)],但生物制剂的疗效及用法尚缺乏大规模的研究去证实[20]。
总之,IgG4-RD累及下颌下腺及腹膜后纤维化的情况少见,且患者后期还出现由于腹膜后纤维化所致的急性肾损伤,通过激素联合免疫抑制剂治疗后,病情有明显好转,由于该病临床表现多样,发病隐匿,临床上不容易被及时诊治,可能病情持续进展出现更多或严重的并发症。提高临床医生对IgG4-RD的认识及关注,给予及时诊治显得尤为重要。另外,该患者诊断IgG4-RD,但病程中未行肾脏病理检查,通过治疗后病情好转稳定,故没有进一步行肾脏病理检查,为诊断IgG4相关性肾病留下遗憾。
