结构导向的对比教学法在有机化学教学中的应用
——以“醛酮的化学性质”为例*
2023-11-29林丽萍李家玉
林丽萍,李家玉
(福建农林大学生命科学学院,福建 福州 350002)
“有机化学”是众多农林院校为农学、林学、植物学、化工、动物科学、动物医学、生物学、生态学等专业大一新生设置的必修基础课。根据新高考的政策,部分学生仅在高一年级选修了化学相关课程,化学基础相对薄弱。而有机化学涉及到的化合物种类繁多,结构多样,理化性质和反应机理也相对复杂。这就导致了大学有机化学课堂上学生学习积极性不高,参与度不够,学习成效不好,教学效果较低等问题。因此,在有机化学教学过程中选择合适的教学方法对解决上述问题,提高教学效果和学生的学习效率尤为重要。
对比教学法是指在教学过程中将两个或多个具有某种联系或者区别的教学内容放在一起进行讲解,促进学生理解、掌握和巩固教学内容,达到帮助学生理解掌握教学内容的一种教学方法[1]。基于“结构决定性质”这一理念及其有机化合物中有很多类似的结构和性质的特点,通过采用对比教学法进行教学,不仅可以帮助学生巩固学过的知识点,还有利于学生更好的理解记忆新的知识点,同时还培养学生的逻辑思维和分析并解决问题的能力[2-4]。本文以“醛酮的化学性质”这一教学内容为例,探讨结构导向的对比教学法在有机化学教学过程中的应用及其对提高学习效果的重要意义。
1 综合分析,提纲挈领
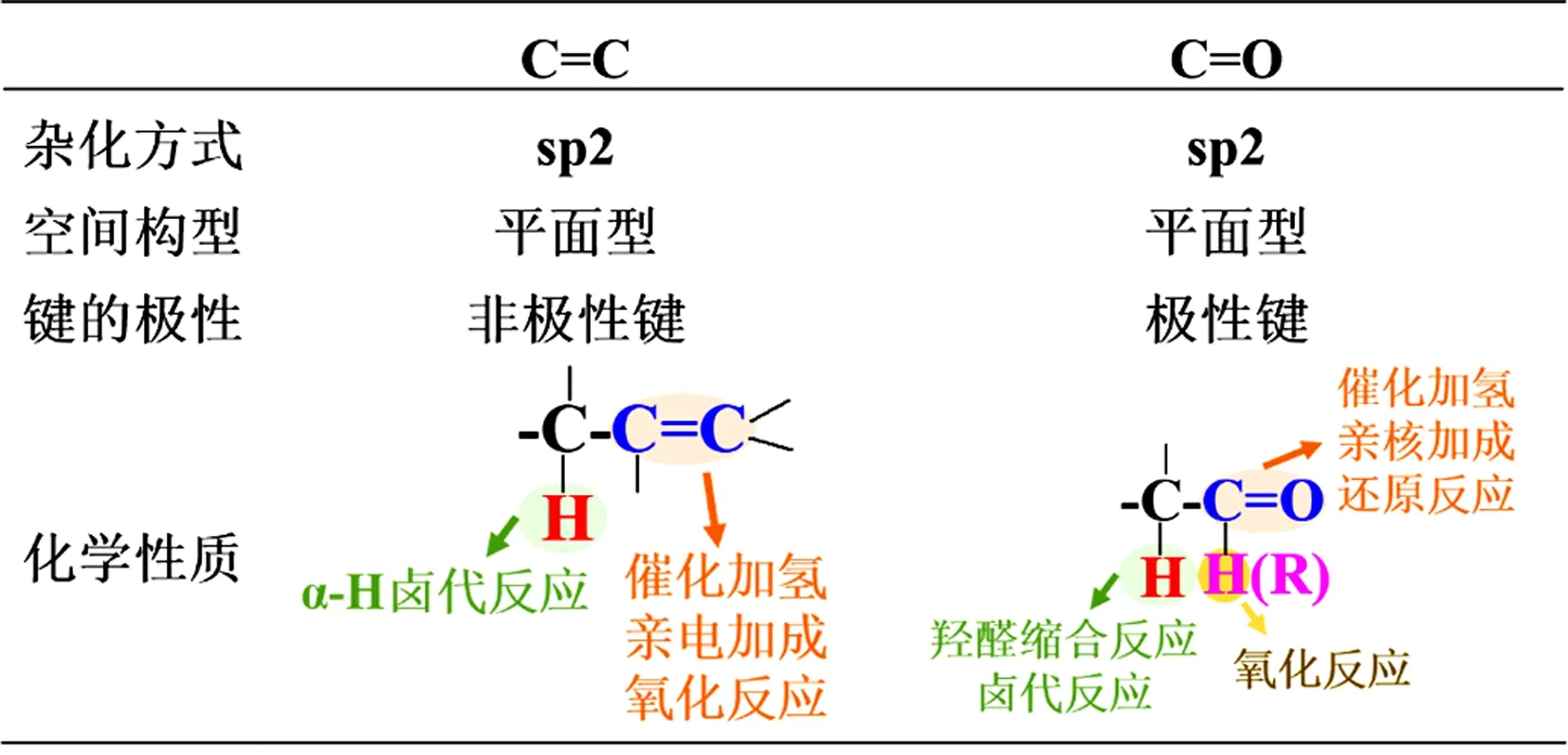
图1 烯烃中碳碳双键与醛酮中羰基的比较
2 分毫析厘,各个击破
2.1 亲核加成反应
2.1.1 醛酮的亲核加成反应活性的比较

2.1.2 亲核加成反应机理的比较
除了醛酮进行亲核加成反应的反应活性不一样外,醛酮与不同的亲核试剂如HCN、饱和NaHSO3、格氏试剂(RMgX)、醇(ROH)、含氮亲核试剂(Y-NH2)等发生亲核加成反应时,具体的反应机理却不尽相同。主要可以分为三类:①简单加成,即亲核试剂中带负电的部分直接加在醛酮羰基中表现缺电性的C原子上,带正电荷部分加在O原子上,如与HCN、饱和NaHSO3、RMgX的反应(如图2a所示)。②先加成后取代,即醛酮先与一分子的亲核试剂进行简单的亲核加成反应后,得到的加成产物不稳定,会与另一分子亲核试剂发生取代反应,如与ROH的反应(如图2b所示)。在醛(酮)与一分子的醇反应得到的产物半缩醛(酮)中,原来的羰基C原子变成连着一个羟基-OH和一个烷氧基-OR,这就导致整个半缩醛(酮)不稳定,半缩醛(酮)中的羟基会继续与另一分子的醇反应得到具有双醚结构的缩醛(酮),而醚的化学性质是比较稳定的,即得到的缩醛(酮)是最后的产物。③先加成再消除,即醛酮先与亲核试剂进行简单的亲核加成反应,得到的加成产物中,原来的羰基变成连着一个羟基-OH和一个-NH-Y键,这一化合物相对不稳定,很容易发生消除反应,失去一分子的水得到含有C=N键的最终产物,如与含氮亲核试剂Y-NH2的反应(如图2c所示)。
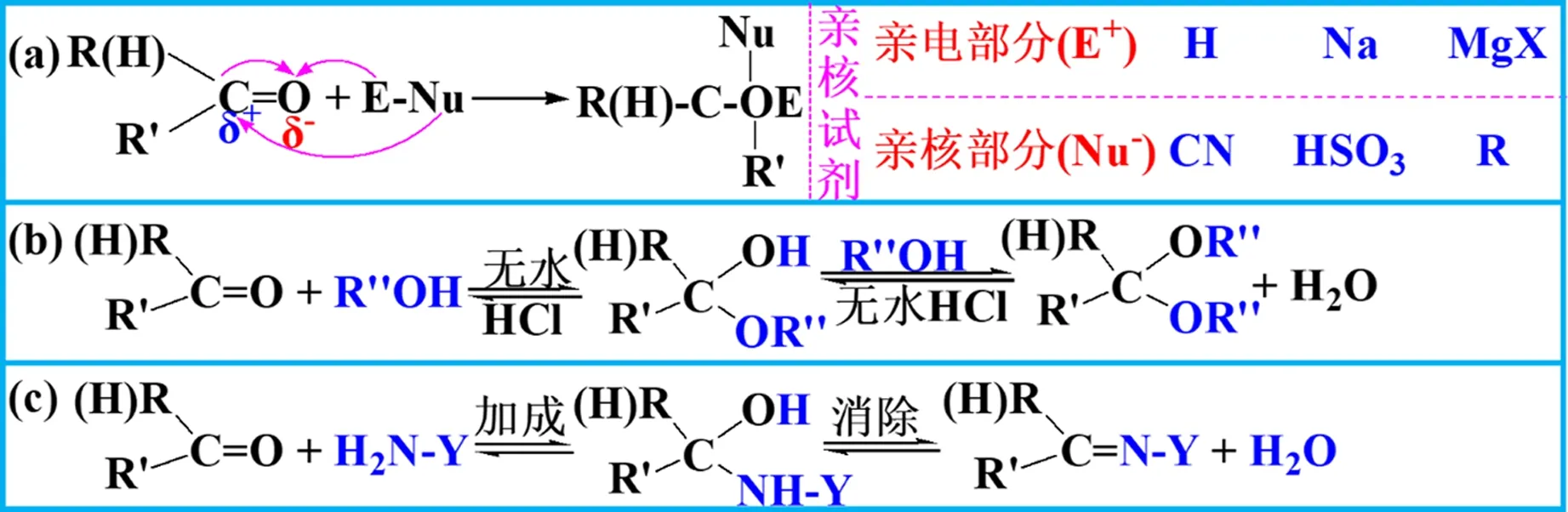
(a)简单加成;(b)先加成后取代;(c)先加成后消除图2 醛酮进行亲核加成反应的机理
2.2 氧化反应
2.2.1 醛酮氧化反应活性的比较
在氧化反应中,醛和酮中羰基结构的不同仍会引起它们发生氧化反应的活性不同。如在在弱氧化剂(如托伦试剂、斐林试剂和本尼迪特试剂等)的条件下,醛因其羰基结构上连着一个H原子,会被氧化生成羧酸,酮则不发生氧化反应(如图3a所示)。而在强氧化剂(如H+/K2Cr2O7、H+/KMnO4、HNO3等)条件下,醛和酮虽然都会被氧化形成羧酸,但是醛是被氧化成碳总数不变的羧酸,而酮则是通过羰基两侧的碳链断裂得到是碳总数减少的多种羧酸,产物为混合物(如图3b所示)。
2.2.2 歧化反应

2.3 还原反应
羰基中的C原子处于中间价态,所以除了氧化反应,醛酮还可以发生还原反应,具体可以分为四种情况。如图4所示,醛酮中的羰基在Ni、Pd、Pt等催化条件下进行催化加氢反应还原成对应的羟基。若选择金属氢化物如NaBH4和LiAlH4作为还原剂,也可以实现从羰基到羟基的转变。但是二者之间也存在不同点,即催化加氢可以同时还原碳碳双键和羰基,而金属氢化物只能还原羰基而不还原碳碳双键。此外,利用克莱门森还原法和武尔夫-吉日聂尔-黄鸣龙还原法可以将羰基还原成亚甲基。但这两种方法的反应条件则完全不同,克莱门森还原法是醛酮在锌汞齐和浓盐酸的条件进行还原的,而武尔夫-吉日聂尔-黄鸣龙还原法则是醛酮在水合肼、氢氧化钠和高沸点溶剂如乙二醇条件下进行还原的,二者适用范围不同,之间形成良好的互补关系。
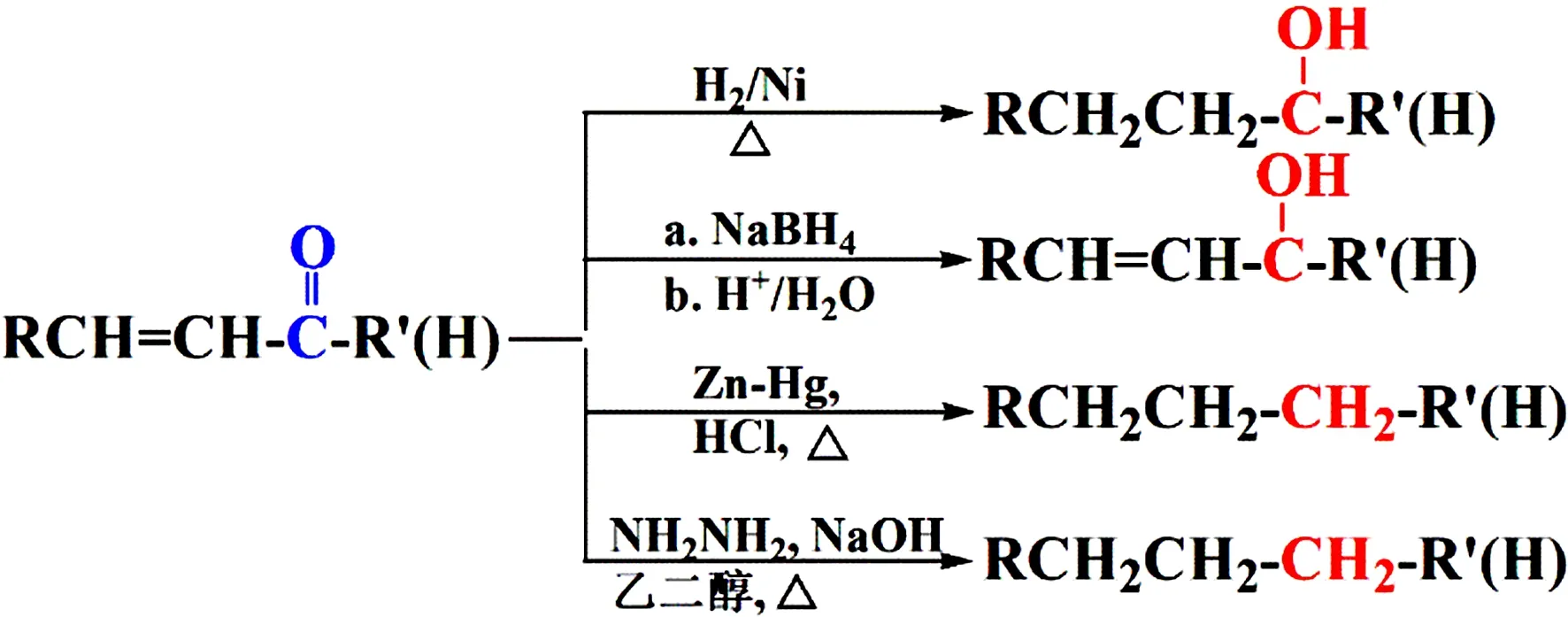
图4 醛酮在不同反应条件下的还原反应
2.4 α-H的反应
由于羰基吸电子的诱导效应和α—C上C—H键对羰基的超共轭效应,导致α—C上C—H键的极性增强,在一定条件下,该H原子可以解离成H+,得到碳负离子,表现出一定的酸性。所得到的碳负离子可以作为亲核试剂进攻另一分子羰基上的C原子,发生羟醛缩合反应,也可以受亲电试剂的进攻发生卤代反应。
2.4.1 羟醛缩合反应
进行羟醛缩合反应的醛酮必须至少有一分子醛或酮要含有α-H,且在稀碱条件下进行反应。如图5所示,含有α-H的醛酮中α-H表现出一定的酸性,在稀碱条件下,得到了带负电荷的烯醇负离子,烯醇负离子再进攻另一分子的醛酮中的羰基,发生亲核加成反应,并夺取溶剂中的质子,得到了β-羟基醛或酮。此时,继续加热,则β-羟基醛或酮会发生分子内脱水反应得到α,β-不饱和醛或酮。此外,要注意区分羟醛缩合反应和歧化反应的反应条件,羟醛缩合反应是含有α-H的醛酮在稀碱条件下进行,歧化反应则是无α-H的醛酮在浓碱条件下进行的,虽然二者本质上都是亲核加成反应,但是稀碱条件下是OH-主要表现出碱性,与表现出酸性的α-H反应,而浓碱条件下则是OH-则是作为亲核试剂先与羰基上的C原子反应(如图3c所示),反应机理完全不同,适用范围也不同。
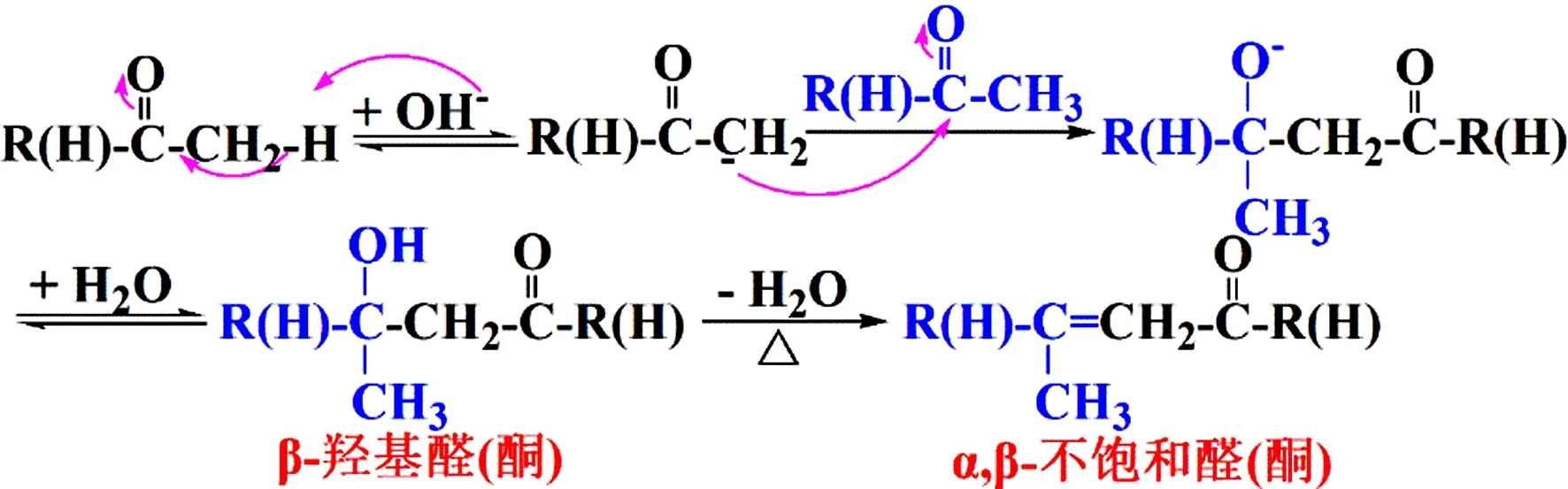
图5 羟醛缩合反应机理示意图
2.4.2 卤代反应
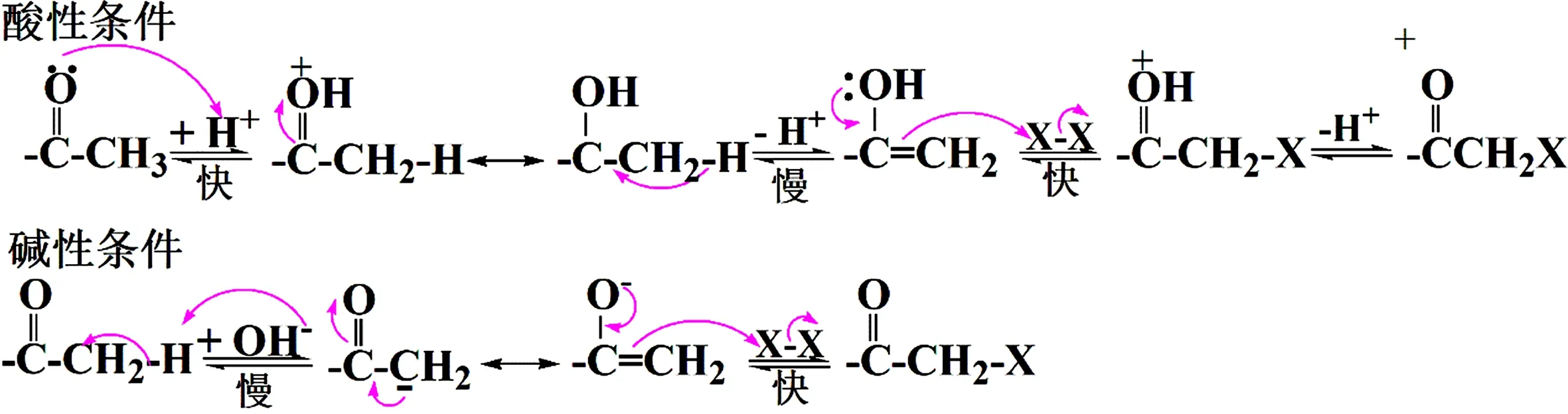
图6 在酸性和碱性条件下醛酮发生卤代反应的反应机理
2.5 α,β-不饱和醛酮的亲电加成反应和1,4-加成反应
除了饱和醛酮外,α,β-不饱和醛酮的结构与共轭二烯烃也很类似,因此在学习α,β-不饱和醛酮的化学性质时也可以类比共轭二烯烃的化学性质进行学习。通过回忆共轭二烯烃与HX发生亲电加成反应且主要为1,4-加成反应,并满足马氏规则,即H原子加在含H多的碳上。向学生提问“那么α,β-不饱和醛酮可以进行哪些反应呢?”通过分析α,β-不饱和醛酮的结构可知,α,β-不饱和醛酮既含有碳碳双键又有羰基,所以既可以发生亲电加成反应也可以发生亲核加成反应。那亲电加成反应和亲核加成反应又是如何进行的呢?如图7所示,以丙烯醛为例,由于碳碳双键与羰基形成共轭体系,羰基的吸电子效应,使碳碳双键上的电荷分布发生变化,与HX进行亲电加成反应是反马加成的结果。同时羰基上发生的亲核加成反应,要特别注意其1,4-加成反应的产物,若产物里存在烯醇式结构,则要将烯醇式结构转为酮式结构。

图7 α,β-不饱和醛酮的亲电加成反应和1,4-加成反应机理示意图(以丙烯醛为例)
3 结语
总之,基于“结构决定性质”这一理念,以结构导向的对比教学法启发学生利用已有的知识分析和解决问题,增加了师生间的互动性,培养学生分析和解决问题的能力,让学生获得独立解决问题的成就感,增强他们学好有机化学的自信心,同时还能培养学生的学习思维,并用于其他有机化合物和学科的学习,提高了学生的学习效果和学习兴趣。
