超重对急性Stanford A型主动脉夹层术后并发症的影响分析*
2023-11-29杨少峰张圣强沈崇文刁文杰陈宏志
杨少峰,张圣强,沈崇文,石 宇,刁文杰,陈宏志,刘 戈,施 超
蚌埠医学院第一附属医院心脏外科,安徽蚌埠 233000
急性Stanford A型主动脉夹层是外科中最凶险且致命的一种疾病,发病后每小时病死率为0.5%,48 h病死率为23.7%[1]。急诊外科手术可明显降低急性Stanford A型主动脉夹层的病死率,优于药物保守治疗[2]。但该手术具有创伤大、时间长、术中需深低温停循环等特点,使患者术后可能产生相应器官功能损伤,导致术后并发症的增多及恢复时间的延长。虽然随着手术方式、术中器械及术中止血材料的进步,手术成功率及疗效也在不断提高,但术后并发症的发生仍然困扰着临床。引起术后恢复时间延长及并发症增多的因素有很多,本研究主要针对超重对术后并发症的影响进行探讨。
1 资料与方法
1.1一般资料 选取2021年1月至2022年12月本院心脏外科收治的64例急性Stanford A型主动脉夹层并接受急诊手术治疗患者为研究对象。(1)纳入标准:①年龄18~80岁;②经影像学检查确诊为Stanford A型主动脉夹层;③发病到手术时间<14 d。(2)排除标准:①术前存在肝、肾等脏器功能障碍;②资料记录不完全;③术后2 d内死亡。体质量指数(BMI)计算公式:BMI=体质量(kg)/身高(m)2。将研究对象按照BMI分组,41例BMI≥24.0 kg/m2患者纳入超重组,23例BMI<24.0 kg/m2患者纳入非超重组。超重组平均年龄(53.90±10.58)岁,合并高血压病史16例,糖尿病病史4例,有吸烟史10例;非超重组平均年龄(55.22±10.29)岁,合并高血压病史10例,糖尿病病史3例,有吸烟史5例。所有研究对象均自愿参与本研究,并签署知情同意书,本研究经本院医学伦理委员会审核批准。
1.2手术方法 患者进入手术室后,常规进行右侧颈内静脉穿刺置管,上下肢动脉穿刺测压,常规麻醉诱导后消毒铺巾,常规游离右侧腋动脉,股动脉游离根据情况备用。胸正中开胸止血后,游离头臂血管并套带备用。建立体外循环,降温,并于主动脉根部灌注HTK液进行心搏骤停,保护心肌,阻断升主动脉,根据根部受夹层累及情况选择根部手术方式,根部处理后,分别阻断头臂血管,深低温停循环期间选择右侧腋动脉以5 mL/(kg·min)流量进行选择性脑灌注。再次游离主动脉弓部并横断头臂血管,结扎夹夹闭左侧锁骨下动脉的近端。测量主动脉直径后放置象鼻支架至降主动脉真腔内。经四分叉人工血管供血管插管恢复躯干循环,单泵双管半流量转机。采用5-0 prolene线四分叉人工血管分支与左颈总动脉吻合恢复脑灌注,后恢复单泵双管转机,同时复温。四分叉人工血管近端与主动脉近端吻合。充分排气后开放升主动脉,恢复心脏血液循环。心脏自动复跳后,依次进行左侧锁骨下动脉-人工血管、无名动脉-人工血管吻合。吻合全部血管后,渐停体外循环,鱼精蛋白1.0∶1.2中和肝素,无特殊反应后拔除动脉插管,彻底手术创面止血,置心包、纵隔引流管,常规关胸。患者术毕送回科室重症监护室(ICU)进一步监护治疗。
1.3数据收集 收集患者基本资料及术前是否合并高血压病、糖尿病等合并症情况,以及术中体外循环时间、深低温停循环时间、手术输血量、是否有低氧血症[术后6 h动脉血氧合指数(PaO2/FiO2)≤200 mm Hg]。术后恢复情况主要统计是否出现术后肺部感染、是否出现切口愈合、机械通气时间、术后ICU停留时间、住院天数、是否死亡、术后抗菌药物使用时间等。

2 结 果
2.1两组基本资料及围术期情况比较 超重组体外循环时间明显长于非超重组,差异有统计学意义(P<0.05)。超重组与非超重组年龄,有高血压病史、糖尿病病史、吸烟史比例,停循环时间,手术输血量比较,差异无统计学意义(P>0.05)。见表1。

表1 两组基本资料及围术期情况比较或n(%)]
2.2两组术后基本情况比较 超重组的住院时间、呼吸机使用时间、ICU停留时间、抗菌药物使用天数长于非超重组,低氧血症、肺部感染及切口愈合不良发生率均高于非超重组,差异有统计学意义(P<0.05)。两组病死率比较,差异无统计学意义(P>0.05)。见表2。
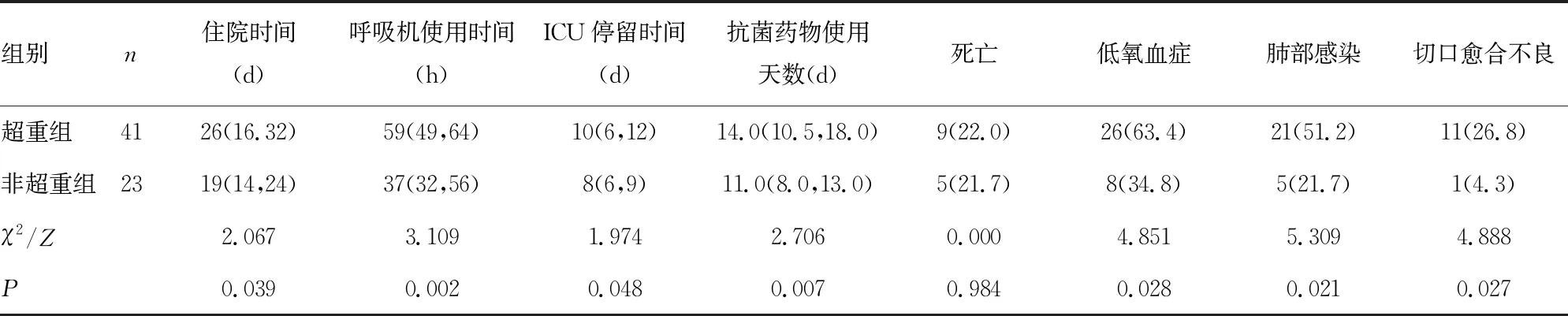
表2 两组术后基本情况比较[M(P25,P75)或n(%)]
3 讨 论
急性Stanford A型主动脉夹层因其病死率高,一经确诊急需进行手术治疗,但由于其手术创伤大,手术时间长及深低温停循环的手术特点导致手术后患者出现各种手术并发症的可能性较其他心脏手术高,对患者预后产生较大影响[3]。既往诸多研究均对主动脉夹层术后死亡的危险因素进行了相关报道,认为体外循环时间、肾功能不全、术后脑血管意外等均会增加手术死亡风险[4-5]。本文主要针对BMI对手术并发症的影响进行分析,以期对辅助临床工作,减少主动脉夹层手术并发症,加快术后恢复,提高手术成功率。
本研究结果显示,超重组的住院时间、呼吸机使用时间、ICU停留时间、抗菌药物使用天数长于非超重组,差异均有统计学意义(P<0.05)。既往的研究报道BMI是主动脉夹层术后发生低氧血症的危险因素[6]。本研究结果显示,超重组术后低氧血症发生率高于非超重组,差异有统计学意义(P<0.05),这与既往研究相符,究其原因可能与绝大多数BMI高的患者为腹型肥胖,在手术过程中,腹腔内脏器向上挤压至胸腔,腹腔压力增加,使横膈上抬,导致胸腔内压力增加,使肺小气道闭塞,造成压迫性肺不张[7]。又因手术时间长,麻醉过程中长时间吸入高浓度的氧后容易造成肺泡表面活性物质的功能障碍,从而容易诱发气体吸收性肺不张,在接受高浓度吸氧的患者中,肥胖患者出现肺不张的概率更高[8-9],各种肺不张均对术后患者肺功能的恢复造成影响,从而加重术后低氧血症的发生。另外,对体外循环相关急性肺损伤的研究显示,急性肺损伤也与全身炎症反应综合征有关,炎症因子的过度释放与抗炎因子的减少在急性肺损伤中起着重要的作用[10],而关于肥胖对机体的影响机制的研究发现,脂肪组织内富含大量炎症因子,手术后炎症因子升高,炎症因子的升高使肺泡表面活性物质减少,肺顺应性下降,加重肺内分流,导致术后低氧血症[11]。而低氧血症延长了患者呼吸机辅助通气时间,进而延长ICU停留时间[12]。
相关文献报道显示,肥胖患者切口愈合不良发生率高于非肥胖患者[13]。本研究结果显示,超重组的切口愈合不良发生率明显高于非超重组,差异有统计学意义(P<0.05)。切口愈合是一个复杂的病理、生理过程,主要经历炎症期、增生期及重塑期[14],炎症期患者通过局部组织变质、渗出和增生来使炎症介质吸收、排出,急性Stanford A型主动脉夹层患者由于手术时间长,切口组织长时间暴露导致脂肪组织的脱水分解,另外手术过程中需要反复使用胸骨撑开器撑开胸骨,过程中可能反复挤压损伤脂肪组织,同时脂肪组织由于血液供应相对较少,手术后更容易出现脂肪坏死,坏死的脂肪组织释放大量的脂质代谢产物[15],诱发切口炎症反应,增加患者切口脂肪液化坏死的发生风险。因此,术中应注意提高手术操作效率,缩短手术时间,减少反复撑开胸骨等操作。缝合时注意保护脂肪组织血供,术后及时发现脂肪液化可能,及时通畅引流,使切口炎症介质及时排出,缩短切口愈合不良恢复时间。
综上所述,超重患者急性Stanford A型主动脉夹层术后的并发症发生率增加,但是在病死率上与非超重患者未见明显差异,提示可以针对超重的患者术前、术后分别制订相应的临床治疗措施,提前干预以减少术后并发症的发生,提高临床治疗效果。
