酶解絮凝耦联对咸蛋清脱盐及理化性质的影响
2023-11-26李晶晶蔡为荣王璐
李晶晶,蔡为荣,朱 樱,王璐
(安徽工程大学 生物与食品工程学院 安徽芜湖 241000)
咸鸭蛋清的主要成分是蛋清蛋白,因具有起泡、乳化、保水等功能而在食品加工业被广泛应用,然而咸蛋清含盐量高、分子质量大、黏度高,不便直接利用,每年约有千万吨咸鸭蛋清被丢弃[1-3]。研究表明,酶解法在降低蛋清蛋白的分子质量及黏度的同时,可以提高蛋清的理化性质[4]。如:涂勇刚等[5]利用木瓜蛋白酶提高蛋清蛋白起泡性能。此外,添加多糖也可以提高蛋清理化性质。如:Erçelebi等[6]向蛋清中添加不同的多糖,蛋清理化性质均有提升。将两种方法耦联,与单一的酶解相比,耦联技术更能提高所得蛋清的理化性质。如:Chang等[7]在酶解的蛋清蛋白中添加多糖,所得产物的功能特性均有提升。刘雪[8]向咸鸭蛋蛋清酶解物中添加麦芽糖糊精,同样得到具有功能性的蛋清粉。
壳聚糖是一种天然高分子絮凝剂,也是一种天然阳离子多糖[9],因适用范围广、无毒等优点而广泛应用于食品领域[10]。对比其它脱盐方法——膜过滤[11]、离子交换法[12]和电渗析法[13],以壳聚糖为絮凝剂脱盐操作简单,然而相关文献研究少。基于此,本研究以咸蛋清酶解液为原料,将酶解与絮凝技术耦联。选取壳聚糖作絮凝剂,优化絮凝脱盐工艺,并测定所得蛋清粉的理化性质,评估耦联对其影响。本研究旨在得到含盐量低且具有功能特性的蛋清粉,为咸蛋清回收利用、开发和应用提供理论参考。
1 材料与方法
1.1 材料与试剂
鸭蛋、咸鸭蛋,市售;氢氧化钠(AR)、柠檬酸(AR)、十二烷基硫酸钠(SDS)、壳聚糖(脱乙酰度>90%)、橄榄油(CP),国药集团化学试剂有限公司;木瓜蛋白酶(Papain,酶活4×104u/g),合肥博美生物公司。
1.2 仪器与设备
胶体磨,南洋防爆电机有限公司;D-160 手持式均质分散仪,大龙兴创实验仪器有限公司;CP214 电子天平,奥豪斯仪器有限公司;SB2000数显盐度计,韩国HM 有限公司;UVmini-1280 紫外分光光度计,日本岛津有限公司;PHSJ-5 雷磁pH 计,上海雷磁仪器厂;HP-C210 精密色差仪,深圳汉谱有限公司;DSC-60 差示扫描量热仪,日本岛津有限公司;Mastersizer 2000 型激光粒度仪,英国马尔文有限公司;真空冷冻干燥机,松源华兴科技发展有限公司。
1.3 蛋清粉的处理及制备
1.3.1 样品预处理 咸鸭蛋、鸭蛋清洗表面后擦干,分离蛋清、蛋黄,蛋清经3 层纱布过滤除去颗粒杂质,经胶体磨(刻度调制1 μm)均质化处理,冻干得咸蛋清粉、鲜蛋清粉。
1.3.2 咸蛋清酶解 酶水解参照文献[14],并作一定修改,具体如下:取均质后咸鸭蛋蛋清稀释至500 mL(质量分数5%),木瓜蛋白酶酶添加量为1×104U/g,55 ℃恒温酶 解处理,用0.5 mol/L NaOH/柠檬酸保持水解过程中维持pH=7.0±0.1,水解1 h,制备低水解度的酶解液。水解结束后,于沸水浴15 min 灭酶。取冷却酶解液,冻干得酶解咸蛋清粉。
水解度(DH):采用SN-TCA 指数法测定水解度[15]。
1.3.3 絮凝脱盐单因素实验 取100 mL 酶解液调节pH 值后,以壳聚糖溶液(1%乙酸为溶剂)作为絮凝剂,磁力搅拌一定时间,于水浴锅恒温静置30 min,4 000 r/min 离心15 min,离心沉淀为回收蛋白,上清液中含盐量为脱除盐分记作脱盐率,含盐量采用盐度计测定[16]。以脱盐率为指标,考察搅拌时间(3,5,10,20,30 min)、料液温度(5,10,20,30,40,50 ℃)、壳聚糖添加量(0.1,0.2,0.3,0.4,0.5 g·L-1)、料液pH 值(5,5.5,6,6.5,7,7.5,8)对脱盐率的影响。
1.3.4 絮凝脱盐响应面优化 单因素实验的基础上,进行Box-Behnken 建立模型,选取pH 值(A)、搅拌时间(B)、絮凝温度(C)、壳聚糖添加量(D)为试验因素,以脱盐率为响应值进行优化。并在工艺参数下制备脱盐蛋清粉,冻干得酶解脱盐蛋清粉。
1.4 蛋清粉理化性质的测定
1.4.1 含盐量及蛋白质含量 咸蛋清及絮凝上清液中盐含量均采用盐度计测定[16]。蛋清粉中盐含量测定的具体方法为,将1 g 蛋清粉溶于100 mL超纯水中,150 r/min 转速条件下搅拌1 h,用盐度计测定溶液中盐含量。本试验各样品中氮、蛋白质含量均采用GB/T 5009.5-2016 测定。
1.4.2 起泡性 采用机械搅打法评估起泡能力[17],将各蛋清粉溶于pH=7 的磷酸缓冲液(0.2 mol PBS)配置成不同浓度的样液,取20 mL 蛋液记作V0,磁力搅拌器搅拌(1 500 r/min,3 min),搅打结束后立即转入量筒,记录泡沫体积V1,静置30 min 后再次记录泡沫体积V2。起泡能力(foaming capacity,FC)和泡沫稳定性(foaming stability,FS),按照下式计算:
1.4.3 乳化性 乳化性评估参考Guo等[18]的方法,并略作修改,取不同浓度的样液,室温下将样液与橄榄油(V/V=3∶1)均匀混合,均质分散仪分散(18 000 r/min,1 min)后,立即从溶液底部吸取50 μL 乳化液用0.1% SDS 溶液稀释至5 mL。SDS 溶液作空白对照,于500 nm 处测定其吸光值,静置10 min 后,重复上述操作。以0 min 测定吸光度A0表示乳化活性(emulsifying activity,EA);乳化稳定性(emulsifying stability index,ESI)按下式计算:
式中,A0——0 min 的吸光值;Δt——时间差(10);Ax——10 min 的吸光值。
1.4.4 热变性温度 称取3~5 mg 待测样置于铝盒中,以空铝盒为空白对照,使用差示扫描量热仪(DSC)进行测定,测定条件初温40 ℃,终温110℃,升温速率5 ℃/min,样品吹扫气20 mL/min[19]。
1.4.5 粒度 取各样品涡旋振荡1 min 后再进行粒度分布测定,测定条件:激光粒度仪设置分散剂为水,转速1 800 r/min,测定模式为手动,分散模式为多分散,每个样平行测5 组。摇匀样品,移液枪吸取后缓慢注入分散剂中,直至遮光度在10%~20%之间,开始测定粒度分布状况[20]。
1.4.6 色度 采用色度计直接测量蛋清粉的L*、a*、b*值(国际照明委员会实验室色度模式)。L*表示亮度,a*表示红色(+)或绿色(-),b*表示黄色(+)或蓝色(-)。ΔE 为各样品经冻干后与对照样品(冻干鲜鸭蛋蛋白粉)的色差,按下式计算:
1.4.7 氨基酸组分分析 按照GB/T 5009.124-2016 《食品中氨基酸的测定》 对FDEWP、SDEWP、EH-DDEWP 中氨基酸组分进行分析。
1.5 统计分析
本研究中除特殊说明均做3 次重复试验,数据采用SPSS 25.0 进行统计,结果以平均值±标准差表示,响应面试验采用Expert-Design 完成,差异性显著采用ANOVA 分析,图表绘制采用GraphPad Prism 8.0.2 软件完成。
2 结果与分析
2.1 酶解液的脱盐
2.1.1 絮凝脱盐单因素实验 各因素对壳聚糖絮凝脱盐效果见图1,pH=6 时絮凝效果最好,pH值的改变影响了酶解液中蛋白及多肽分子所带电荷的性质和数量,溶液接近中性至碱性时,壳聚糖分子表面阳离子减少中和能力下降,絮凝效果也逐渐下降[21]。搅拌时间(图1b)过长絮凝脱盐效果反而下降,因此,选取5 min 作为搅拌时间。图1c中絮凝脱盐效果随添加量上升,添加量达到0.3 g/L 时絮凝效果最优,当壳聚糖添加量超过0.3 g/L絮凝效果开始下降,溶液沉降速度变慢且开始浑浊,絮凝剂浓度过高反而会影响絮凝效果。在许永安等[22]、褚绍霞等[23]利用壳聚糖絮凝分离蛋白的研究中,也得到一致的结论。图1d 中温度对脱盐率呈先上升后下降的趋势,30 ℃效果最好。随着温度的升高分子运动加强,絮凝剂与蛋白及多肽分子间碰撞增多,发生脱稳沉淀呈现上升趋势。而壳聚糖的黏度在絮凝中起主要作用,温度升高其黏度所有下降,絮凝效果及脱盐率均下降[24]。因此,选取30 ℃作为絮凝温度。

图1 pH 值(a)、搅拌时间(b)、絮凝剂添加量(c)、絮凝温度(d)对脱盐率的影响Fig.1 Influence of pH(a),stirring time(b),flocculant amount(c)and flocculation temperature(d)on desalination rate
2.1.2 絮凝脱盐条件响应面优化
2.1.2.1 响应面试验结果 响应面模型设计方案及结果见表1,回归方差分析见表2。利用Design-Expert 8.0.6 软件构建各因素pH 值(A)、搅拌时间(B)、絮凝温度(C)、絮凝剂添加量(D)与脱盐率(Y)的二次多项回归方程:Y=93.93+0.37A-0.66B+1.19C-0.32D+0.55AB-0.031AC-0.45AD-0.39BC+0.16BD-0.43CD-0.76A2-0.71B2+0.02C2-0.66D2。

表1 Box-Behnken 试验设计及结果Table 1 Box-Behnken experimental design and results
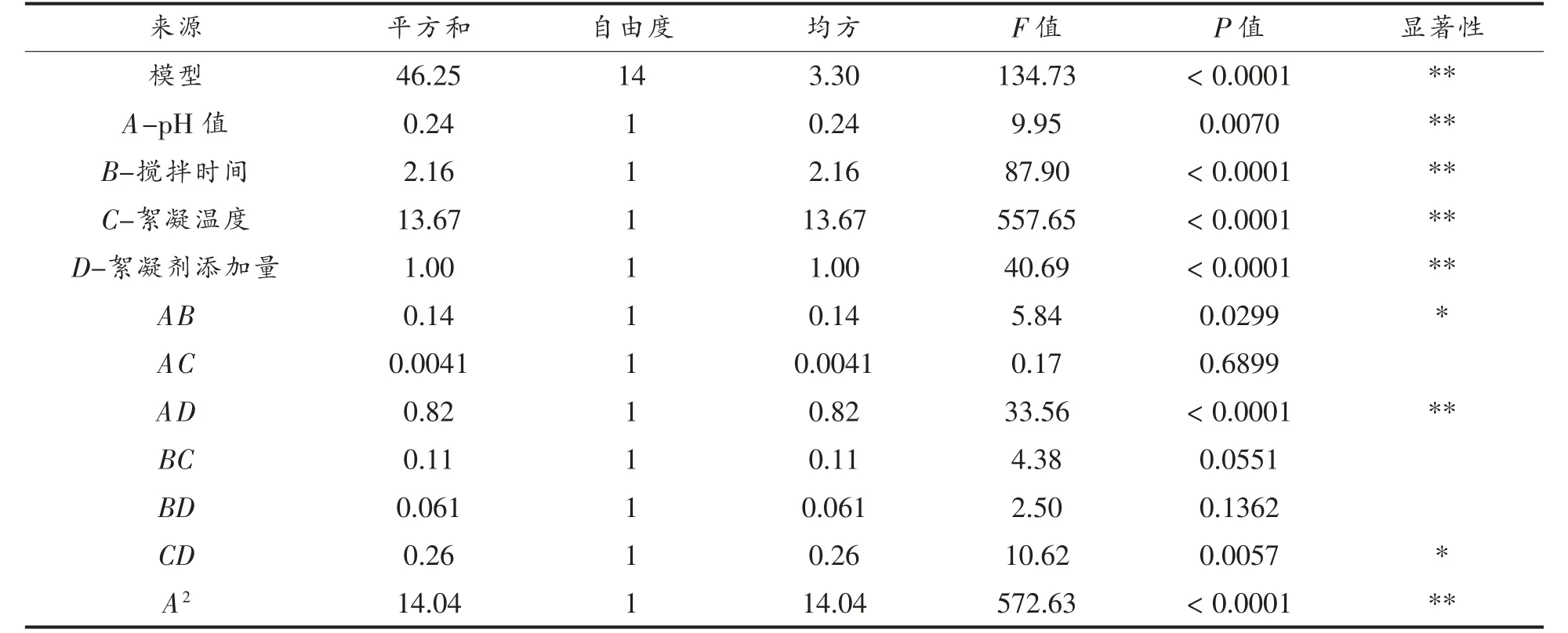
表2 回归模型方差分析Table 2 Analysis of variance of regression model
如表2 方差分析结果显示,模型P<0.0001,回归模型极显著,失拟项P=0.0854>0.05,模型失拟项水平上不显著,该回归方程能较好的拟合模型选择是较合适的。回归方程相关系数R2=99.26%、R2Adj=98.53%,表明方程回归效果较好,且响应面数据有98.53% 来自表内因素,该模型能够解释响应值的变化,可用于预测絮凝作用下脱盐率的变化。各因素对脱盐率影响的次序为:絮凝温度>搅拌时间>絮凝剂添加量>pH 值。
2.1.2.2 各因素交互及验证试验 通过各因素响应面三维图(图2),下图a、图b、图c 中,曲面随絮凝温度的增加而上升,最高点落在40 ℃处。整个响应面曲面呈坡面,3 组交互作用中均含有絮凝温度因素,3 组交互主要受絮凝温度影响,最大值落在中心。图d、图e、图f 中各因素变化呈先上升后下降的趋势,在交互作用下形成的曲面呈抛物形曲面开口向下,等高线闭合最大值落在等高线内。各因素交互图随着曲面上升颜色均呈现加深趋势,最佳考察范围在此范围内。
利用软件对回归方程求解得到絮凝的最优工艺为:pH=6.04、絮凝温度为40 ℃、搅拌时间5.56 min、添加量0.27 g/L,脱盐率为96.0173%。结合实际情况,将最优工艺参数定为pH=6、絮凝温度为40 ℃、搅拌时间5.5 min、添加量0.27 g/L。利用上述最优工艺重复3 次进行验证,产物平均脱盐率为96.18%,试验值与理论预测值基本相吻合,该模型合理有效,得到的工艺参数有实用价值。
2.2 蛋清粉的理化性质
2.2.1 蛋清粉的盐度及蛋白质含量 各蛋清粉中氮含量及含盐量见表3,未脱盐的两种蛋清粉含盐量均超过30%,酶解蛋清粉经脱盐浓缩干燥后,100 g 蛋清粉含1.4 g NaCl 已经处于较低范围。酶解后蛋清通过絮凝脱盐含盐量由30.15 g/100 g低至1.44 g/100 g,处理后蛋清粉中含盐量约降低了96%,实现对咸蛋清的高效脱盐。

表3 各蛋清粉成分Table 3 Composition of each egg white powder
2.2.2 起泡性 除比较咸蛋清粉、鲜蛋清粉、酶解咸蛋清粉、酶解脱盐蛋清粉4 种蛋清粉外,另根据絮凝脱盐优化条件制备未经酶解的脱盐蛋清粉。各蛋清粉起泡性能见图3a,不同浓度下,脱盐蛋清和咸蛋清起泡性无明显差距,酶解咸蛋清起泡性较咸蛋清有所提升,酶解可以提高蛋清的起泡性能,如涂勇刚等[5]使用木瓜蛋白酶对蛋清蛋白改性使起泡性提高2.09 倍。而酶解后再添加壳聚糖絮凝脱盐的样品起泡性能最优,当样品质量浓度为4 g/100 mL 时,鲜蛋清的起泡性达210%,而酶解脱盐蛋清粉的起泡性达295%。这与刘超[25]的研究,先酶解后添加增稠剂等方法对蛋清蛋白改性得到一致结论,样品起泡性也超过100%。

图3 各蛋清粉起泡能力(a)、泡沫稳定性(b)及各蛋清粉乳化活性(c)及乳化稳定性(d)Fig.3 Foaming ability(a)and foam stability(b)of each egg white powder and emulsifying activity(c)and emulsion stability(d)of each egg white powder
各蛋清粉形成泡沫稳定性见图3b,酶解咸蛋清粉形成的泡沫稳定性最差,泡沫在静置过程中消失极快,而鲜蛋清粉和酶解脱盐蛋清粉搅打后形成的气泡均匀细腻,30 min 后泡沫结构变化不大,稳定性分别达到81.6%和88.5%,酶解改变了蛋清结构造成起泡性有所改变,但絮凝剂的添加增加了蛋白质的聚集程度提到了其起泡性及泡沫稳定性[26]。
2.2.3 乳化性 图3c 中各蛋清粉乳化活性均随浓度提高,酶解脱盐蛋清粉的乳化活性随样品浓度呈线性上升的趋势,样品质量浓度为4 g/100 mL 时,鲜蛋清粉和脱盐蛋清粉的乳化活性分别为0.65 和0.62。根据Paulson等[27]的报道,乳化活性与溶解性呈正相关。添加絮凝剂脱盐使得样品溶解度有所降低,可能是酶解脱盐蛋清粉的乳化活性略低于鲜蛋清的原因。
乳化稳定性见图3d,样品在形成乳化液后,维持乳状液的稳定主要依靠蛋白质的疏水性,疏水性越强乳化液的稳定性越强[28]。酶解会释放蛋白中疏水基团,但酶解咸蛋清粉乳状液稳定性却较差,可能是因为样液里含大量的NaCl,大量电子存在破坏了乳状液稳定。酶解脱盐蛋清粉的乳化稳定性则远高于其它样品,样品质量浓度为4 g/100mL 时乳化稳定性高达392%。
2.2.4 热变性温度 蛋清蛋白在吸热过程中,通常存在卵转铁蛋白(61~65 ℃)和卵清蛋白(75~84℃)的特征峰[19],蛋清粉热变性曲线见图4,蛋清粉DSC 数据见表4,鲜蛋清粉(b)两个吸收峰的热变性温度分别为63.80,80.39 ℃,咸蛋清粉(c)两个吸收峰的热变性温度分别为60.18,76.94 ℃,咸蛋清的变性温度向左偏移,可能是咸蛋清中存在大量的NaCl 对蛋清热变性有诱导作用,有研究表明NaCl 对蛋白质结构有扰乱[29],且在董华伟等[1]的研究中,对咸蛋清通过电渗析脱盐后,其热变性温度也较咸蛋清粉提高,蛋清粉中存在NaCl 会影响蛋清粉的热稳定性。酶解脱盐蛋清粉(a)的热变性曲线呈平缓下降趋势,在温度范围内没有出现变化峰无热变性温度,热稳定性提高。
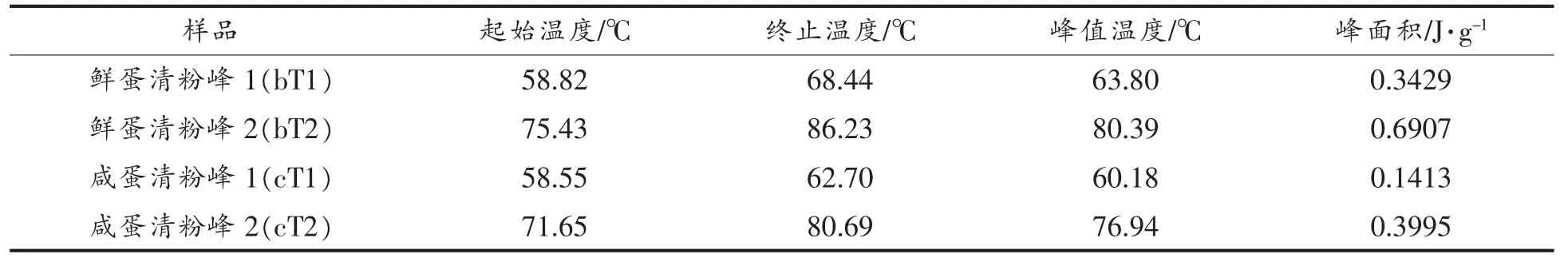
表4 各蛋清粉的DSC 分析结果Table 4 DSC analysis results of egg white powder
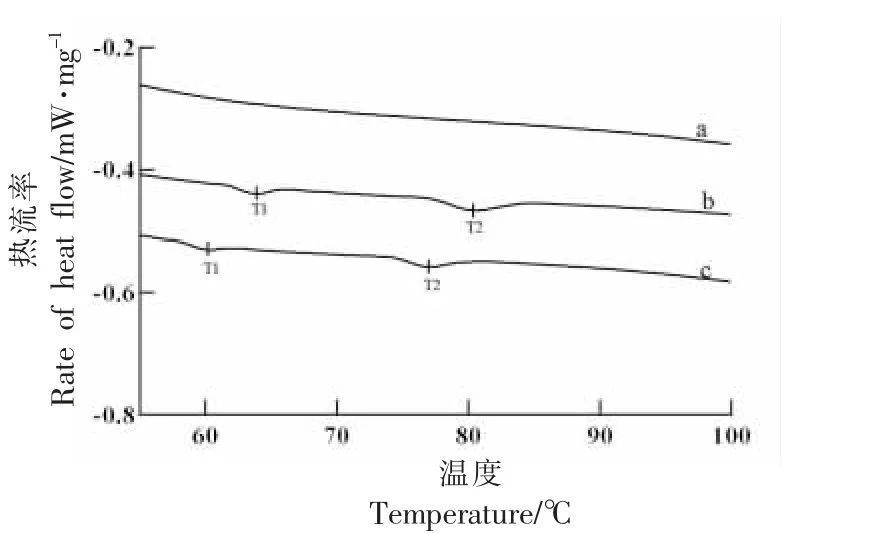
图4 各蛋清粉的DSC 曲线Fig.4 DSC curves of egg white powders

图5 各蛋清粉粒径分布图Fig.5 Particle size distribution of egg white powder
2.2.5 粒度 表5 中咸蛋清粉、鲜蛋清粉和酶解脱盐蛋清粉粒径的中值平均粒径D50 分别为65.80,51.04 和25.61 μm,咸蛋清粒径平均粒径最大,粒径分布范围最宽20.73~82.52 μm,D(3,2)和D(4,3)的差值越大,粒度分布越宽[30]。可能蛋清粉中高含盐量会促使蛋清粉中蛋白质颗粒变大[29]。酶解后蛋清粉平均粒径下降,但粒径分布较宽13.19~41.51 μm,可能不完全酶解或者酶切位点的不同使得酶解得到不同颗粒大小产物。该研究中所得产物粒径同样高于其它研究,可能由于蛋清酶解后经壳聚糖絮凝与蛋清交联,提高了酶解蛋清粉整体粒径大小。
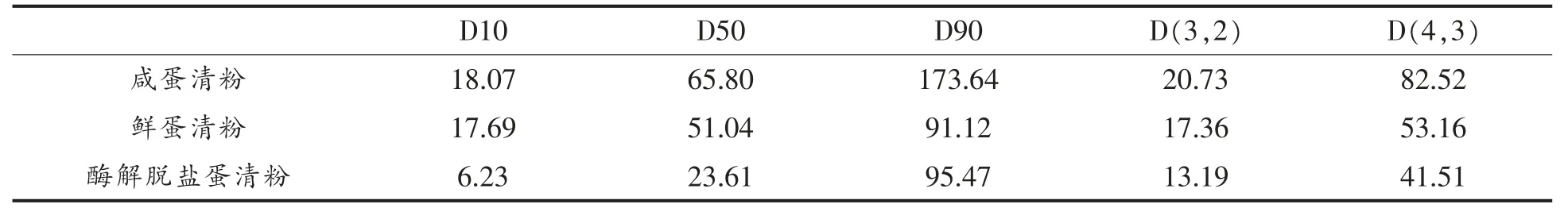
表5 蛋清粉粒径分布结果表(μm)Table 5 Results of particle size distribution of egg white powder(μm)
2.2.6 色度分析 表6 中,鲜蛋清粉相比,脱盐蛋清粉的L*、a*值均无显著变化,b*值有所升高,酶解脱盐后蛋清粉偏黄。可能是由于在酶解处理时,蛋清热处理过程中产生褐变导致颜色发生变化;咸鸭蛋清粉的L*、a*值较鲜蛋清粉有所差异可能是由于含盐量较高,NaCl 是一种白色晶体,提高了咸蛋清粉的亮度。由于△E*均较小,说明与鲜鸭蛋清粉相比颜色均较为接近,样品在视觉上都是白色,不影响蛋清粉的使用。

表6 蛋清粉的色度分析Table 6 Chroma analysis of egg white powder
2.2.7 氨基酸组分分析 氨基酸组分见表7,咸蛋清粉中NaCl 含量较高,氨基酸总量较低,脱盐后酶解蛋清粉氨基酸占比增加。3 种蛋清粉中各氨基酸组分占比较为接近,酶解脱盐蛋清粉的氨基酸组成中每日必须摄入氨基酸的含量与新鲜蛋清基本接近。从氨基酸组分来说,酶解蛋清经絮凝脱盐后,对氨基酸组成的影响不明显。

表7 蛋清粉的氨基酸分析Table 7 Amino acid analysis of egg white powders
3 结论
本研究以咸蛋清为原料,使用木瓜蛋白酶制备得低水解度的蛋清酶解液,利用壳聚糖作絮凝剂,将酶解与絮凝技术耦联制备得到酶解脱盐蛋清粉。壳聚糖絮凝脱盐经单因素及响应面优化,得到最优工艺参数为pH=6、絮凝温度为40 ℃、搅拌时间5.5 min、添加量0.27 g/L。处理后的蛋清粉含盐量由咸蛋清粉33.09 g/100 g 低至1.44 g/100 g,含盐量约降低了96%,实现高效脱盐。与鲜蛋清粉、咸蛋清粉作对比,酶解絮凝耦联制备蛋清粉粒径较小,样品质量浓度为4 g/100 mL 时,形成的泡沫细密均匀稳定性高,起泡性提高2.95 倍,30 min 后还有88%泡沫存在。絮凝后样品溶解度有所降低,乳化活性略低于鲜蛋清粉为0.62,乳化稳定性大幅提升,高达392%。从DSC 热变性分析和粒度可看出,蛋清粉中NaCl 的存在会降低热稳定性且使样品颗粒变大,而经酶解脱盐后的蛋清粉热稳定性提高,粒径变小。蛋清粉颜色视觉上为白色不影响,营养成分也与鲜蛋清接近。通过将酶解与絮凝耦联,可以实现高效脱盐,并得到具有起泡性、乳化性、高热稳定性的改性蛋清粉,为提高咸鸭蛋清利用率及附加值提供了试验依据和工艺参考。
