组织Wnt/β-catenin通路蛋白表达水平与卵巢子宫内膜异位症组织恶变的关系分析
2023-11-25张喜红宋晓霞
田 金,张喜红,宋晓霞,郑 岩,马 莉
(郑州人民医院,河南 郑州450053)
卵巢子宫内膜异位症(ovarian endometriosis,OEjavascript:void(0);)是由遗传、环境、免疫功能等多种因素导致的妇科疾病,病因至今尚未明确,患者以继发性痛经为主要临床特征,对女性的身心健康造成严重影响[1]。子宫内膜异位症相关性卵巢癌(endometriosis associated ovarian cancer,EAOC)为OE恶变转化而来,是一种特殊的卵巢癌,恶性程度较卵巢癌更低,但是EAOC也会影响女性正常的排卵过程,甚至会造成不孕[2-3]。有研究指出,Wnt/β-catenin信号通路可以控制细胞生长发育,在多种肿瘤的发生和发展中具有重要作用,但在EAOC中的作用机制尚不明确,猜测与Wnt/β-catenin通路蛋白的表达有关[4]。Wnt/β-catenin信号通路蛋白中,β-catenin为Wnt/β-catenin信号通路的开关,基质金属蛋白酶-9(matrix metalloproteihase-9,MMP-9)能降解细胞外基质和基底膜,促进肿瘤侵袭[5-6]。本研究通过分析β-catenin和MMP-9在EAOC组织中的表达,旨在为EAOC的早期诊疗提供理论研究。
1 资料与方法
1.1 一般资料
选取2016年10月至2018年10月在郑州人民医院就诊的46例EAOC患者为研究对象,设为EAOC组,患者年龄23~69岁,平均(47.63±7.38)岁;FIGO分期[7]:Ⅰ期10例,Ⅱ期19例,Ⅲ期14例,Ⅳ期3例。纳入标准:(1)符合EAOC诊断标准[8],且经病理学确诊;(2)年龄18周岁以上。排除标准:(1)术前3个月使用激素治疗;(2)合并其他恶性肿瘤;(3)放置宫内节育器;(4)子宫肌瘤;(5)妊娠或哺乳期妇女;(6)内分泌或生殖道疾病;(7)子宫肌瘤剔除术史或剖宫产;(8)精神类疾病。另取同期入院的34例OE患者为OE组,患者年龄23~67岁,平均(46.29±7.43)岁。两组患者的基础资料差异无统计学意义(P>0.05)。本研究符合《世界医学协会赫尔辛基宣言》要求,所有患者或者家属知情并签署知情同意书。
1.2 方法
采集两组患者的病变组织,使用免疫组化染色,观察β-catenin和MMP-9在组织中的表达情况。β-catenin和MMP-9阳性为细胞质或胞核中可以看到棕黄色颗粒,随机取10个视野,用光镜观察,根据着色程度和阳性细胞百分比判定结果:着色程度,3分(棕黄色)、2分(中度黄色)、1分(淡黄色)、0分(阴性);阳性细胞百分比,3分(>50%)、2分(10%~50%)、1分(≤10%);着色程度和阳性细胞百分比得分的乘积为总分,总分≥3分为阳性,反之为阴性[3]。
1.3 观察指标
(1)比较两组患者组织中β-catenin和MMP-9表达水平;(2)分析EAOC组织中β-catenin和MMP-9表达水平与临床病理特征的关系;(3)对患者进行长达36个月的随访,通过电话等形式了解患者的生存状况,分析不同β-catenin和MMP-9表达水平与EAOC患者预后的关系。
1.4 统计学分析
2 结果
2.1 两组患者组织中β-catenin和MMP-9表达水平比较
EAOC组β-catenin阳性表达率为63.04%,高于OE组的23.53%,MMP-9阳性表达率为69.57%,高于OE组的44.12%(P<0.05)。见表1。

表1 两组患者组织中β-catenin和MMP-9表达水平比较(例,%)
2.2 EAOC组织中β-catenin和MMP-9表达水平与临床病理特征的关系
β-catenin的阳性表达率在不同分化程度、淋巴结转移、临床分期、铂敏感性的EAOC组织中比较,差异具有统计学意义(P<0.05);MMP-9的阳性表达率在不同分化程度、淋巴结转移、临床分期EAOC组织中比较,差异具有统计学意义(P<0.05)。见表2。

表2 EAOC组织中β-catenin和MMP-9表达水平与临床病理特征的关系
2.3 不同β-catenin和MMP-9表达水平与EAOC患者预后的关系
对46例EAOC患者进行随访,随访36个月,以患者EAOC复发死亡为观察终点,死亡20例,3年总生存率是56.52%(26/46)。β-catenin阴、阳性患者3年生存率分别是68.97%(20/29)、35.29%(6/17),差异有统计学意义(χ2=4.945,P=0.026),见图1。MMP-9阴、阳性患者3年生存率分别是68.75%(22/32)、28.57%(4/14),差异有统计学意义(χ2=6.398,P=0.011),见图2。

图1 不同β-catenin表达EAOC患者生存曲线图
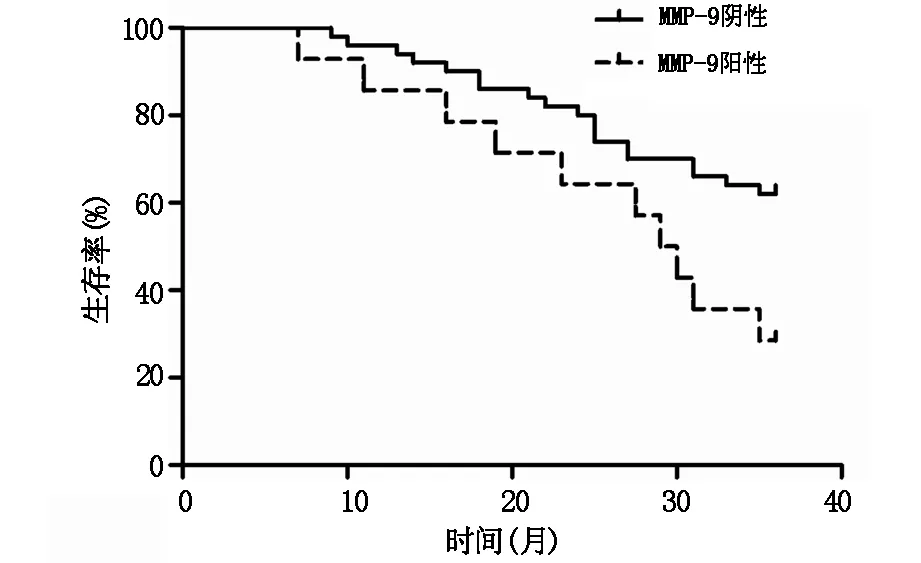
图2 不同MMP-9表达EAOC患者生存曲线图
3 讨论
OE患者子宫内膜组织生长异常,侵犯到卵巢,该病虽为良性病变,但同样具有浸润、转移、复发等特征[9]。有研究显示,OE会有1.3%~1.9%的机率发生恶变[10]。但是,在临床实际中,由于种种原因,病理医师在确诊患者为OE后,可能会忽视癌细胞取代OE病灶的影响,OE恶变真实的发生率会更高[11]。EAOC即OE恶变,患者发病年龄和病变期比其他类型的卵巢癌更早[12]。Wnt/β-catenin信号通路在多种恶性肿瘤中扮演重要角色,高俊彦[13]研究发现,miR-139-5p的过度表达,能调节Wnt/β-catenin信号通路,降低卵巢癌细胞的活性,从而削弱癌细胞增殖和迁徙的能力,抑制卵巢癌的进展。李委佳等[14]同样发现,NDRG4通过对Wnt/β-catenin信号通路的调节作用,降低卵巢癌细胞的侵袭和迁移能力。但是,Wnt/β-catenin信号通路是否参与OE恶变尚未明确,了解Wnt/β-catenin信号通路与OE恶变的关系,有助于设计作用靶点的药物,通过对Wnt/β-catenin信号通路的调节,起到抑制癌细胞增殖的作用,延长患者生存期。
β-catenin是Wnt/β-catenin信号通路的关键转录因子,主要位于细胞膜,其水平的表达能反映该信号通路的激活状态,β-catenin为阳性表达,Wnt/β-catenin信号通路开启,反之关闭[15]。本研究结果发现,EAOC组β-catenin阳性表达率为63.04%,高于OE组的23.53%(P<0.05),提示β-catenin阳性表达水平的升高,可以促进OE恶变为EAOC。在β-catenin参与OE恶变的过程中,Wnt/β-catenin信号通路可能发挥重要作用,β-catenin的阳性表达激活Wnt/β-catenin信号通路,通过调控上游Wnt、Frizzled和下游信号靶基因MMP-9 mRNA,促进癌细胞的侵袭和转移。β-catenin的阳性表达率在不同分化程度、淋巴结转移、临床分期、铂敏感性的EAOC组织中比较,差异具有统计学意义(P<0.05),说明β-catenin水平的阳性表达可以诱导EAOC组织分化,促进癌细胞转移和侵袭。此外,β-catenin在铂耐药EAOC组织中表达更高,提示β-catenin还与EAOC患者铂耐药的发生有关,这对于临床研究铂耐药的机制,以及避免铂耐药的药物研制具有重要意义。
MMP-9为Wnt/β-catenin信号通路的下游靶基因,也是MMPs家族重要的蛋白水解酶,可以降解细胞外基质中的大部分成分以及基底膜,为肿瘤的侵袭创造条件,因此,MMP-9的异常表达可以反映肿瘤侵袭的程度[16]。本研究中,MMP-9阳性表达率为69.57%,高于OE组的44.12%(P<0.05),证实MMP-9能参与OE恶变过程,且发挥着重要作用。MMP-9与EAOC组织的临床病理特征分析显示,MMP-9的阳性表达率在不同分化程度、淋巴结转移、临床分期EAOC组织中比较,差异具有统计学意义(P<0.05),说明MMP-9参与EAOC的进展,其水平的阳性表达可以刺激EAOC癌细胞增殖、转移和侵袭。MMP-9的阳性表达破坏了腺体基底膜,可以促进EAOC癌细胞向周围结缔组织和腹膜侵袭,此外MMP-9还可以促进血管内皮生长因子的表达,刺激血管的生成,有助于癌细胞增殖。
生存曲线显示,β-catenin阴、阳性患者3年生存率分别是68.97%(20/29)、35.29%(6/17),差异有统计学意义(χ2=4.945,P=0.026),MMP-9阴、阳性患者3年生存率分别是68.75%(22/32)、28.57%(4/14),差异有统计学意义(χ2=6.398,P=0.011),说明β-catenin和MMP-9可以评估EAOC患者的预后,其水平的阳性表达表示预后不良。通过抑制β-catenin和MMP-9水平的阳性表达,阻断Wnt/β-catenin信号通路,有可能阻止OE恶变。
综上所述,Wnt/β-catenin信号通路与OE恶变密切相关,β-catenin激活通络,促进下游靶基因MMP-9的表达,参与OE恶变过程,β-catenin和MMP-9这两个指标可以作为OE恶变的潜在检测指标,其水平的阳性表达提示EAOC患者预后不良。
