过氧化氢气体灭菌生物监测失败原因及应对策略
2023-11-25蔡婷婷赵锡丽
蔡婷婷,赵锡丽,李 静,柏 莉
(重庆医科大学附属第二医院消毒供应中心,重庆 401336)
过氧化氢气体灭菌是一种常见的低温灭菌方法,以汽化的过氧化氢作为主要微生物杀灭因子实现灭菌[1]。根据分解残留过氧化氢的方式不同,可以进一步分为过氧化氢低温等离子体灭菌和汽化过氧化氢灭菌。这种灭菌方法因适用于不耐湿和不耐热的医疗器械而在医院得到广泛应用[2-3]。生物监测是验证该方法灭菌效果的首选,但国内调查[4-6]显示,过氧化氢气体灭菌的生物监测失败率相对较高。根据行业标准,一旦生物监测失败,应尽快召回前次生物监测合格以来所有尚未使用的灭菌物品,检查灭菌过程的各个环节,分析原因并改进;已使用的器械应对相应患者进行密切观察[7]。因此,生物监测失败不仅会影响手术顺利进行,增加耗材和人力成本,还会带来极大的医院感染风险。本文旨在全面分析过氧化氢气体灭菌生物监测失败的原因,提出具体的策略和建议,降低监测失败率,为实践提供理论依据。
1 过氧化氢气体灭菌生物监测原理
GB/T 33417—2016《过氧化氢气体生物指示物检验方法》[1]要求,用于制作过氧化氢气体灭菌生物指示物的菌株为嗜热脂肪杆菌芽孢(ATCC 7953或SSI K31)。第一代菌片式生物指示物将菌片和培养基分别封装在生物指示管中,灭菌后混合,再进行培养。第二代生物指示物为慢速生物指示物,其原理是在培养基中使用酸碱指示剂。当孢子萌发后,其代谢产生的酸性物质会改变培养基pH值,从而改变培养基的颜色,观察培养基的颜色变化可判断灭菌效果。此产品需1~7 d培养时间。第三代生物指示物为快速生物指示物,具有双读系统。快速部分可在几十分钟内通过生物阅读器判断灭菌结果[8]。这种指示物使用非荧光物质甲基伞形酮α-D-葡萄糖苷(α-MUG)作为培养基,嗜热脂肪杆菌芽孢在萌发和生长过程中产生α-葡萄糖苷酶,与α-MUG发生水解反应,产生荧光物质甲基伞形酮(MU)。生物阅读器内荧光接收器可以捕捉到荧光信号,从而显示阳性培养结果。反之,若细菌芽孢及其合成酶在灭菌过程中被破坏,无法产生荧光物质,那么显示培养结果为阴性[9]。目前,行业内已停止使用第一代菌片式生物指示物,取而代之的是第二、第三代自含式生物指示物,大型三甲综合医院普遍采用第三代生物指示物。
2 过氧化氢气体灭菌生物监测失败原因及应对策略
2.1 缺乏相关明确标准 压力蒸汽灭菌和环氧乙烷气体灭菌领域已经建立了明确的使用准则,包括设备参数配置、操作流程及监测方法等,但过氧化氢气体灭菌作为一种相对年轻的技术,其具体规范和操作程序的明确标准仍处于研究开发阶段。目前各品牌灭菌器的生产工艺、灭菌剂装载方式、灭菌剂浓度及用量存在差异。国际上关于过氧化氢气体灭菌器的标准目前仅为草案[10],国内虽然发布了过氧化氢气体等离子体低温灭菌器卫生要求[11],但多项指标与非等离子体式灭菌器无相关性,因此不适用于此类设备。首版关于灭菌过程的开发、验证和常规控制要求的国际标准[12]于2022年发布,但与之对应的国内标准尚未发布。生物指示物能否准确监测灭菌效果,取决于其抗力[8]。目前生物指示物的生产仅遵循通用标准,因此其适用性尚不明确[5,13-14]。尽管GB/T 33417[1]规定了过氧化氢气体灭菌生物指示物的检验方法,但测试D值时使用的生物指示物抗力测试仪并无对应标准,故灭菌器制造商各自开发适用于其设备的生物指示物,而这些指示物的抗力及阅读器的稳定性均不一致,无法使用标准监测器材比较不同指示物之间的抗力[1,5,15-16]。此外,用于评价灭菌器性能和灭菌过程的标准仍未正式发布。应用方面,AAMI ST 58[17]中涵盖了过氧化氢气体灭菌的特性和应用,但我国现行行业标准[18]、《医疗机构消毒技术规范》[19]和《消毒供应中心管理与技术指南》[20]仅对过氧化氢低温等离子体灭菌的操作给予了指导。因此,国家相关机构应尽快制定相关规范和指南,完善过氧化氢气体灭菌各类标准,增加汽化过氧化氢灭菌设备要求和应用规范,为生产企业和临床操作提供指导;同时,使用部门也应加强相关的循证研究。
2.2 人员操作因素
2.2.1 灭菌物品的装载量和装载方式 装载量是影响过氧化氢气体灭菌效果的重要因素[21-23],装载量过多可造成灭菌剂不足。栗英等[23]用过氧化氢等离子体同一程序对3种不同装载量的器械灭菌30批次后发现,当装载量>80%时,生物监测失败率高达86.67%,而装载量<80%时,失败率为0。WS/T 367—2012[19]及灭菌器说明书均明确规定,灭菌包应避免叠放和接触灭菌腔内壁。重叠放置、特卫强包装物品朝向不一致等状况,不利于过氧化氢的扩散和穿透。此外,装载物品如果触碰到灭菌舱内壁或电极,会妨碍等离子体产生[17];装载物品距灭菌剂注射口过近,也可能影响过氧化氢气体的释放和扩散。因此,医疗机构可组织相关培训,帮助专职人员理解灭菌器的结构及灭菌原理,并要求严格按照灭菌器说明书要求装载,质控组长及科室负责人指导并监督装载情况。
2.2.2 灭菌物品和包装材料的选择 材料兼容性和穿透目标表面的能力是过氧化氢气体灭菌用于医疗器械最终灭菌的决定性因素[24]。两种因素对灭菌效果的影响主要表现在:第一,当包装或灭菌物品中含有与过氧化氢气体灭菌不兼容的材质时,可降低灭菌效果。例如,具有吸附或分解过氧化氢性质的物品可造成过氧化氢气体浓度降低,从而影响灭菌[25]。蔡碧兰等[26]对221批因过氧化氢浓度过低致灭菌失败的情况统计分析后发现,61.1%由吸附性物品所致。研究[27]显示,无纺布包装对过氧化氢的吸附性大于特卫强包装,且当无纺布放在上层时,其吸附性大于放在下层。第二,对于表面灭菌,过氧化氢被消耗时容易接触到新补充的过氧化氢气体,有助于杀灭微生物。然而过氧化氢气体穿透性较低,只能通过管腔开口进入内部,若待灭菌物品形状或结构复杂,特别是细长的管腔器械,可能达不到可靠的灭菌效果[6,21-22,28]。Noh等[21]的研究发现管腔的材料和结构对灭菌性能有明显影响。
GB 27955—2020[11]规定,过氧化氢等离子体灭菌器不得用于吸收液体的、不能承受真空的、盲端等10种对象的灭菌。对此,应对策略包括遵循医药行业标准[29]及AAMI标准[30]规定的过氧化氢灭菌的材料适应性评价指南,确认灭菌器械的材质与灭菌方式的兼容性和适应性;重视包装材料的兼容性,包括评估材料是否会吸收或促进过氧化氢气体的分解[12];关注托盘、附件、垫子、支架、标签、器械盒等部件对过氧化氢的相容性,并遵守医疗器械和灭菌器制造商的使用说明。
2.2.3 清洗不彻底 医疗器械上残留的蛋白质、盐和污垢能为微生物提供防护,阻止其与灭菌剂直接接触,也有利于细菌黏附和生物膜形成[31]。临床实践中,因器械未彻底清洗导致灭菌失败,造成手术部位感染的案例时有发生[32-36]。过氧化氢气体灭菌对清洗质量要求高,器械上的有机物和无机物污染可能会降低其灭菌效果[8,25]。器械表面的有机物不仅会保护细菌芽孢,还会消耗过氧化氢灭菌因子,导致灭菌失败。Rutala等[37]在存在盐和血清污染的器械接种细菌芽孢后,分别用汽化过氧化氢、环氧乙烷、过氧化氢气体等离子体和压力蒸汽4种方式进行灭菌,灭菌失败率为76.3%、1.9%、1.9%和0,提示过氧化氢气体灭菌前充分清洁的重要性。无机盐类(如氯化钠)在灭菌过程中因压力变化导致水分快速蒸发,结晶体析出并附着在待灭菌物品表面,也可导致灭菌失败。对此,可考虑的策略包括:参考AAMI ST 79[38]指南,使用超声清洗后的自动清洗消毒器对大多数手术器械进行再处理;至少每周监测一次(最好每天监测)自动清洗消毒器的清洁效果;遵守制造商的使用说明书进行器械再处理,并与制造商探讨器械设计是否能有助于器械的充分清洗;科室定期组织培训和考核;清洗管腔器械时,先进行预刷洗及酶液超声清洗,再使用减压沸腾、脉动真空清洗消毒器等设备,有效提高清洗效率[39-40]。清洗质量的检测建议使用目测法结合定量检测,对于管腔器械,建议使用白通条和管道镜进行检查[38,41]。
2.2.4 干燥不充分 灭菌前彻底干燥可提高灭菌成功率[23]。水分可吸收过氧化氢,阻碍其接触微生物并对微生物造成破坏,影响灭菌效果。而抽真空过程中,水分汽化会带走大量热量,导致过氧化氢冷凝,同时降低灭菌对象的温度,也不利于灭菌。因此,对难以干燥的器械可使用高压气枪干燥→低温真空干燥→高压气枪干燥的处理流程,并使用管道镜及试纸法检测是否残留水分[23,42-43]。
2.2.6 灭菌程序的选择 过氧化氢灭菌剂注入量、扩散时间、压力、温度等都是影响灭菌器性能的重要过程参数,尤其是灭菌剂注入量,对灭菌成功率影响显著[21]。灭菌剂注入量越多,灭菌效果越好,但过氧化氢注入量过多,可能导致汽化不充分,从而影响穿透性并对灭菌物品和患者造成伤害[24],因此,过氧化氢注入量应保持经过验证的固定值。栗英等[23]发现,当选择短循环程序对管腔器械进行灭菌时,灭菌失败率高达40.00%,而使用长循环程序,失败率可降至4.75%。因此,应根据灭菌物品的材质、结构及灭菌器说明书选择正确的灭菌程序。
2.3 灭菌器 过氧化氢灭菌剂具有强氧化性,可能会氧化和腐蚀传输管道、阀门等内部元件,甚至导致泄漏;盛装过氧化氢溶液的蒸发器内部可能出现结垢、结晶现象,影响其加热效果[45]。赵燕等[46]对2010—2020年的2 866起过氧化氢等离子体灭菌器不良事件进行统计分析,发现灭菌器故障占92.6%,主要表现为灭菌剂泄露、灭菌失败等,这些问题与元件故障、维护使用不当关系密切。长期使用的灭菌器可能因设备老化增加灭菌失败概率[6]。此外,即使在使用过程中出现故障,这种“带病”灭菌器也并不总会报警或中止程序,其对异常状况监测不灵敏,进一步增加了灭菌失败率。黄锡[45]报道了一起过氧化氢气体灭菌器显示“灭菌成功”,而指示卡却显示灭菌失败的案例,检查设备后发现进液阀泄露。为应对这些问题,应购买符合国际、国内标准的灭菌器,严格按照灭菌器说明书要求对设备进行保养和维护;认真观察每批次灭菌记录,发现问题后及时分析并处理;按照制造商的参数规定及行业标准,正确判断物理监测关键指标和化学指示物的变化。
2.4 生物指示物
2.4.1 管腔生物过程挑战装置(PCD)抗力差异大 根据国家强制性标准GB 27955—2020[11],使用过氧化氢低温等离子体灭菌管腔器械时,应使用PCD或等效验证装置进行监测。使用管腔生物PCD可以真实反映管腔器械的灭菌效果,但监测失败率远高于普通生物监测,且不同材质、形状、管腔内径和长度的生物PCD抗力差异大[6,21-22,25,47-48]。管腔越细长,生物监测失败率越高;管腔较长且细的灭菌失败率高;单通道灭菌剂开口结构比双通道开口结构难灭菌;由全氟烷氧基树脂制成的软式PCD在灭菌器达最大装载量时也不易出现生物监测失败[21];一侧盲端的生物PCD不适用于该灭菌方式[25]。灭菌时,应正确选择管腔PCD与非管腔PCD;监测管腔器械时,应依据管腔器械的实际直径、长度、结构、材质等选择合适的管腔PCD[49]。
2.4.2 快速与慢速生物指示物判读结果不一致 大多数情况下,快速生物指示物的荧光判读与慢速培养结果一致(一致性≥97%)[50-51]。两种判读结果不一致的情况较少,往往是快速荧光判读结果阳性,慢速培养结果阴性。其原因可能是灭菌过程有效性处于临界状态,体系中残留芽孢数量极少或无残留,微生物的酸性产物数量不足以使指示剂变色,但尚存在α-葡萄糖苷酶并发挥了催化作用,故提示存在微生物残留,有致病风险[52]。极少数情况下,不一致性表现为快速荧光阅读显示阴性,而慢速培养结果显示阳性的“假荧光阴性反应”。这种判读结果可能是由于少量残留芽孢结构受损,被损伤的芽孢并没有死亡,只是不能(或非常缓慢地)萌发,但可以在培养基上修复后生长[53],荧光监测期间没有产生荧光物质,阅读器误报阴性,之后孢子通过修复再次生长,改变了指示剂的颜色。当发现“假荧光阴性反应”时,未成功灭菌的物品可能已经使用,增加了疾病传播的风险,应引起高度重视,并明确快速生物阅读结果后是否还需要进行慢速培养的相关标准。
2.4.3 生物指示物质量问题 广东省6所医院出现时间聚集性生物监测失败现象,经调查推断可能是因生物指示物自身质量问题造成的假阳性[48],建议在接收产品时,检查其相关测试证书,并按照说明书规范存储生物指示物。
2.5 生物阅读器 生物阅读器滤光片腐蚀或损坏会导致光的波长和强度发生变化,使阅读器无法精确判读[44];阅读器孔内的杂物、漏液、灰尘等也会影响阅读结果。此外,生物指示物与化学指示物直接接触,或监测人员的手接触了带有荧光标记的物品,都可能导致生物阅读器误报阳性[54]。以下措施有助于避免上述问题:阅读器放在远离强光处,加防尘盖;使用生产商建议的清洗剂;触摸生物指示物前洗手;定期对阅读器进行效验和维护。
过氧化氢气体灭菌生物监测失败原因主要总结为缺乏相关明确标准、人员操作因素、灭菌器因素、生物指示物因素和生物阅读器因素5个方面,见表1。
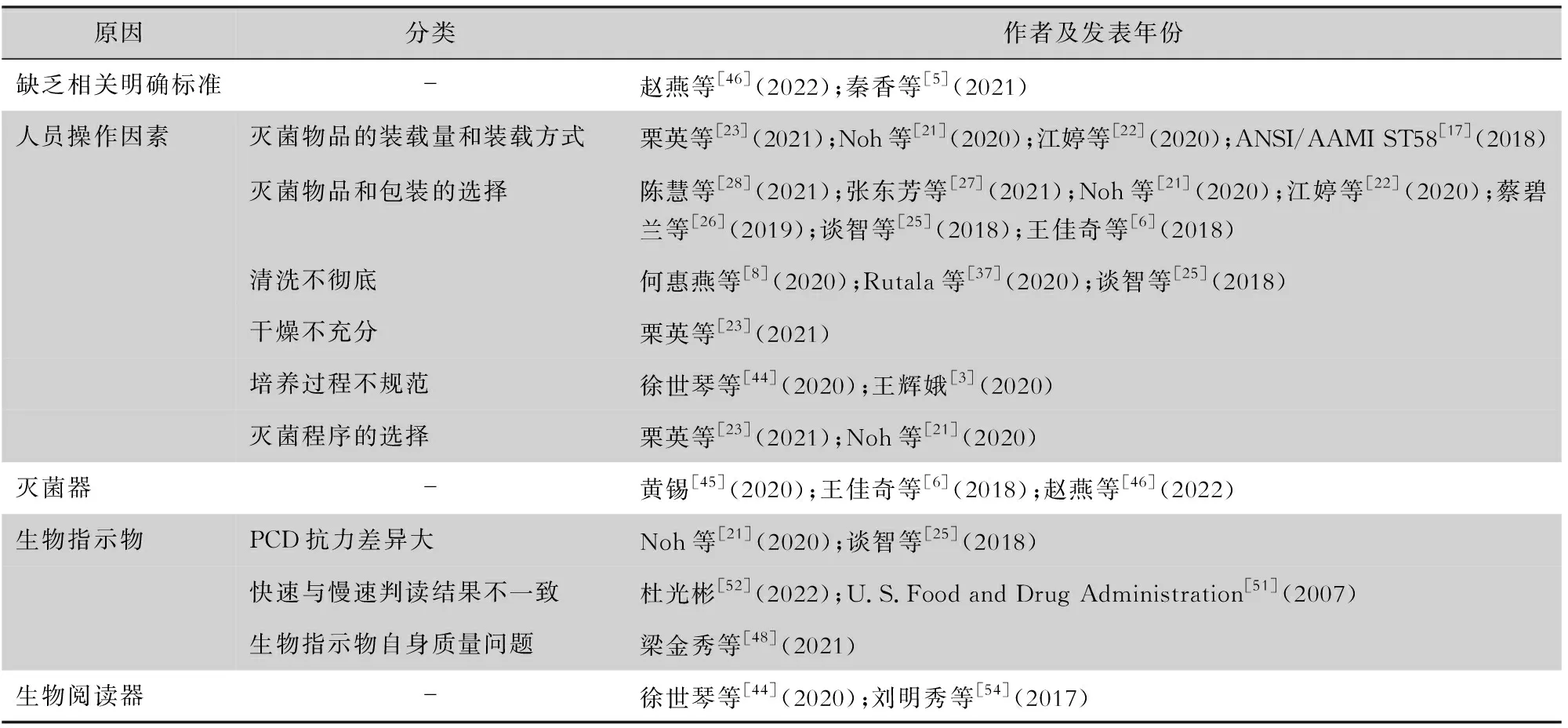
表1 生物监测失败原因及参考文献总结
3 总结
可靠的灭菌效果对患者安全至关重要。尽管过氧化氢气体灭菌在医疗机构中被普遍使用,但各项标准和指南还未完善。此外,过氧化氢气体的穿透力和材料兼容性增加了生物监测失败的复杂度。专业技术人员需要综合考虑各种影响因素,准确分析监测失败的原因,鉴别“真阳性”“假阳性”“假荧光阴性反应”,及早采取针对性措施,确保为患者提供安全可靠的器械保障。
利益冲突:所有作者均声明不存在利益冲突。
