基于I-FABP的鲫肠道通透性检测方法的建立
2023-11-22王靖雯邹振江李莉娟顾泽茂袁军法
王靖雯,邹振江,李莉娟,2,顾泽茂,2,袁军法,2*
基于I-FABP的鲫肠道通透性检测方法的建立
王靖雯1,邹振江1,李莉娟1,2,顾泽茂1,2,袁军法1,2*
(1. 华中农业大学水产学院,武汉 430070;2. 华中农业大学水生动物疫病专业实验室,武汉 430070)
肠道通透性与肠道稳态及个体健康状况直接相关,目前尚缺乏鱼类肠道通透性的定量评价方法及试剂。血清中肠脂肪酸结合蛋白(intestinal fatty acid binding protein,I-FABP)是肠道通透性的重要血清生物学指标,可用于肠道通透性的定量评价。为建立鲫()血清I-FABP的定量检测方法,克隆了鲫I-FABP基因,经原核表达和纯化,并利用重组蛋白分别免疫新西兰白兔(New Zealand white rabbit)及小鼠(),制备了兔源及鼠源多克隆抗体,其效价均为1∶80 000。以纯化的兔源多克隆抗体作为包被蛋白,以辣根过氧化物酶(horseradish peroxidase,HRP)标记的鼠源多克隆抗体作为酶标抗体,通过优化各反应条件建立了基于鲫I-FABP的双抗体夹心酶联免疫检测方法(double antibody sandwich ELISA,DAS-ELISA)。标准曲线的线性回归方程为=0.003 5+0.036 7,拟合度较高2为 0.999 1,临界值为0.090 6。批内及批间变异系数分别为1.17%~5.50%及0.16%~4.78%,具有较好的重复性。以该方法对54份样品进行检测,与商业化试剂盒对比,符合率为100%。构建的DAS-ELISA检测方法可用于鲫肠道通透性的定量评估。鉴于鱼类I-FABP的保守性,该方法或可用于其他鱼类肠道通透性的定量评价。
肠脂肪酸结合蛋白;肠道通透性;双抗体夹心ELISA;原核表达;多克隆抗体;鲫
肠道是重要的消化吸收器官,兼具分泌、代谢和免疫等功能[1]。肠黏膜受损、肠道通透性的增加与溃疡性结肠炎(ulcerative colitis,UC)[2]、克罗恩病(Crohn's disease,CD)[3]等肠道疾病的发生、发展密切相关。因存在肠肝轴、肠肾轴、肠脑轴等多器官的交流,肠道的病变往往还会引起其他器官的损伤[4],如酒精性肝病(alcoholic liver disease,ALD)[5]、慢性肾脏病(chronic kidney disease,CKD)[6]及抑郁症[7]等疾病。在鱼类养殖中,肠道不仅被认为是鱼类弧菌病[8]、肠道败血症[9]等疾病的主要发生器官,还是食源性有毒物质的第一靶器官[10]。除病原感染外,饲料内植物源成分(皂苷)的添加[11]、真菌毒素的产生[12]以及过度投喂等,都会造成鱼类肠道的炎症及损伤。因此,及时、准确的肠道健康状况评估是经济鱼类肠道疾病防控的关键环节。但目前,根据经验或采用组织学的方法对鱼类肠道健康进行评估,主观性强、操作复杂,尚缺乏有效的定量指标。
脂肪酸结合蛋白(fatty acid binding protein,FABP)是一类相对分子质量为14~16 kDa的可溶性小分子蛋白,广泛存在于心脏、脑、肠道等多种组织中[13],与机体的能量贮存、信号传导和细胞的增殖分化等多种生命过程息息相关[14]。肠型脂肪酸结合蛋白(intestinal fatty acid binding protein,I-FABP)是脂肪酸结合蛋白家族的一员,参与脂肪酸的扩散、运输与分解代谢,大量且特异性的表达于肠道黏膜细胞[15]。通常情况下,I-FABP存在于细胞内,但当肠黏膜受损时,I-FABP将快速释放到循环系统中,导致血液、尿液中的I-FABP水平显著升高[16]。因此,血清I-FABP指标可用于肠道通透性的定量检测。
I-FABP作为评估肠黏膜损伤和炎症的非侵入性生物标志物,具有特异性强、灵敏度高、稳定性好等特点[17],已在医学中用于肠道损伤的早期检测[13]。但目前尚无以鱼类I-FABP为抗原设计并建立的肠道通透性检测方法。本实验通过制备重组鲫()I-FABP蛋白和多克隆兔抗、鼠抗,初步建立了DAS-ELISA检测方法,为鱼类肠道健康的评估以及疾病防治提供了科学依据。
1 材料与方法
1.1 试材与试剂
实验所用大肠杆菌表达载体pET-32a为本实验室保存,实验所用鲫血清样品采集自健康鲫或本实验室构建的肠损伤鲫模型。
2X M5 HiPer plusHiFi PCR mix (with blue dye) 、胶回收试剂盒购自北京聚合美生物科技有限公司;DNA Marker、Protein Marker、DH5α菌株、Rosetta(DE3)菌株购自北京擎科新业生物技术有限公司;限制性内切酶购自TaKaRa公司;T4 DNA连接酶购自武汉爱博泰克生物科技有限公司;SDS-PAGE凝胶配置试剂购自Biosharp公司;酶标二抗HRP-山羊抗兔IgG(H+L)购自武汉爱博泰克生物科技有限公司;牛血清白蛋白(BSA)购自Gibco公司;ELISA试验中TMB显色液和TMB显色终止液均购自上海碧云天生物技术有限公司;His亲和层析柱、鼠抗HRP标记试剂盒(过碘酸盐法)、抗体纯化用Protein A/G 琼脂糖纯化树脂和ELISA酶标板购自上海生工生物工程有限公司;人I-FABP检测试剂盒(DAS-ELISA法)购自上海羽朵生物科技有限公司;引物合成与测序由北京擎科新业生物技术有限公司完成。
1.2 试验方法
1.2.1 鲫I-FABP的生物信息学分析 利用NCBI数据库(National Center for Biotechnology Information (nih.gov))获取鲫(NCBI Reference Sequence: XM_026204449.1)的mRNA序列及氨基酸序列,利用SignalP5.0在线软件(SignalP - 5.0 - Services - DTU Health Tech)进行氨基酸序列的信号肽预测;利用TMHMM2.0在线软件软件(TMHMM - 2.0 - Services - DTU Health Tech)进行跨膜区分析。利用ESPript3.0在线软件(ESPript 3.x / ENDscript 2.x (ibcp.fr))和Megalign软件对不同物种的I-FABP进行保守域预测及氨基酸相似度分析。参考氨基酸序列如下(NCBI Reference Sequence):XP_026060234.1(鲫),XP_018962588.1(鲤),AAF00925.1(斑马鱼),AYP66989.1(泥鳅),NP_001187833.1(斑点叉尾鮰),XP_014051032.1(大西洋鲑),XP_021474749.1(虹鳟),AWP05540.1(大菱鲆),EDL12315.1(小鼠),EAW73666.1(人类)。
1.2.2 pET-32a-I-FABP重组质粒的构建 根据鲫的序列设计扩增引物,进行PCR扩增,片段扩增引物如下:正向引物,5′-ATAAT GACCTTCAACGGGACCTG-3′;反向引物,5′-CGCTTAGCTCCTCTTGAAAATCC-3′,上下游引物的酶切位点以下划线表示。PCR 产物经 1.0% 的琼脂糖凝胶电泳检测有明亮单一条带后切胶回收。将纯化后的扩增产物与pET-32a 载体进行双酶切处理。回收纯化后的启动子片段和载体按物质的量 3∶1 混合,T4 DNA 连接酶 16℃连接 12 h,转化入DH5α 感受态细胞,涂布氨苄西林(Amp)抗性的平板,37 ℃倒置培养12 h。对单菌落进行菌液PCR检测及双酶切鉴定,将阳性菌送测序,验证序列是否正确。
1.2.3 鲫I-FABP的诱导表达及纯化 将测序比对结果正确的重组质粒,转化入表达菌株Rosetta(DE3)中,挑取单菌落接种于含Amp的LB液体培养基中振荡过夜培养。次日取上述菌液按1∶100的比例接种于含Amp的LB液体培养基中,培养至对数生长期后加入异丙基硫代-β-D-半乳糖苷(Isopropyl β-D-Thiogalactoside,IPTG)至终浓度为0.4 mmol·L-1,转移至16 ℃恒温培养箱中诱导表达12 h。空载pET-32a采用同样的方法处理作对照。将诱导完全的菌液离心,弃上清,用 PBS洗涤沉淀并将沉淀重悬。经高压破碎后在4 ℃,10 000 g条件下离心为上清和沉淀。全液、上清和沉淀加入SDS上样缓冲液,95 ℃变性10 min,SDS-PAGE检测其表达情况和可溶性。使用0.45 μm的滤器过滤上述所得上清样品,并按Ni-NTA预装重力柱(货号:C600791-0005)说明中的重力法组氨酸标签蛋白纯化步骤纯化重组标签蛋白,利用SDS-PAGE检测纯化所得蛋白的纯度。
1.2.4 抗体的制备与检测 将纯化所得的可溶性蛋白免疫实验用兔及实验用鼠。实验用兔每只每次免疫600~800 μg蛋白,免疫3次后从颈动脉放血,分离血清。实验用鼠每次按50~100 μg·只-1的剂量进行免疫,4次免疫后眼眶取血获得鼠源抗血清。利用Protein A/G 4FF 预装重力柱(货号:C600981-0005)的操作说明分别纯化兔源及鼠源抗血清,SDS-PAGE检测纯化效果。将表达的重组蛋白用 PBS 重悬后进行 SDS-PAGE 电泳,兔源多克隆抗体按1∶20 000、1∶40 000和1∶80 000的比例稀释作为一抗,AP标记的羊抗兔抗体按1∶10 000稀释作为二抗,进行Western-Blot 检测。按照HRP偶联试剂盒(货号:D601047-0001 )的操作步骤对纯化后的鼠源多克隆抗体进行标记,利用直接ELISA方法检测纯化且标记后的鼠源抗体效价。
1.2.5 最佳工作浓度的测定 兔多抗按1∶1 000、1∶5 000、1∶10 000、1∶20 000、1∶40 000和 1∶80 000进行倍比稀释加入酶标板中,100 μL·孔-1,4 ℃过夜包被。37 ℃封闭2 h后加入I-FABP(用PBS-T以1∶5 000稀释)和阴性对照(PBS-T),100 μL·孔-1,37 ℃孵育1 h。将HRP标记的鼠多抗按 1∶1 000、1∶5 000、1∶10 000、1∶20 000和1∶40 000进行倍比稀释,100 μL·孔-1,37 ℃孵育40~60 min。经避光显色后加入ELISA终止液,利用酶标仪测定OD450值并进行分析,计算P/N值,取P/N最高值时的抗体工作浓度为兔抗及鼠抗最佳工作浓度。
1.2.6 最佳工作条件的选择 利用DAS-ELISA法,按已确定的包被浓度对酶标板进行包被和封闭,包被条件分别设为4 ℃ 2 h、4 ℃ 24 h、37 ℃ 1 h、37 ℃ 2 h和25 ℃(室温)2 h。利用酶标仪测定OD450值并计算P/N值,以确定最佳包被条件。
以最佳抗原包被浓度和包被条件包被酶标板,酶标抗体分别在 4 ℃ 2 h、4 ℃ 24 h、37 ℃ 15 min、37 ℃ 30 min和37 ℃ 60 min的条件下孵育,利用酶标仪测定OD450值并计算P/N值,以确定最佳反应条件。
1.2.7 标准曲线的构建 按0、50、100、200、400和800 pg·mL-1的浓度稀释I-FABP蛋白作为待检测标准品,按上述优化条件对标准品进行测定,读取OD450值,构建标准曲线。
1.2.9 重复性及符合率检测 进行批间重复试验,按照已确定的最佳包被浓度及包被条件,对不同批次酶标板进行包被,按已构建的方法分别对已知阴性和阳性样品进行检测,通过测定的OD450值计算变异系数。
进行批内重复试验,用同一批次包被的酶标板分别对已知阴性和阳性样品分别进行3次重复实验,通过测定的OD450值计算变异系数。
使用商业化检测试剂盒与本实验构建的I-FABP双抗体夹心ELISA检测方法分别对54份样本进行检测,比较这两种抗原检测方法的符合率情况,对构建的ELISA检测方法的符合率进行评估。
1.2.10 统计分析 所有实验数据均采用双样本等方差检验进行处理,*,< 0.05; **,< 0.01 或 ***,< 0.001。
2 结果与分析
2.1 鲫i-fabp基因的序列分析与克隆
I-FABP在不同物种中较为保守,氨基酸序列中存在多处保守位点(图1A)。鲫长399 bp,编码133个氨基酸,与人和小鼠的相似度较高,均为67.4%。鲫与其他鱼类的相似度更高,达80.3%~97%(图1B)。对目的基因鲫的全长进行扩增,其片段大小与预期一致(图2A)。将扩增的鲫基因克隆至pET- 32a载体,经双酶切鉴定可见两条与载体及目的基因大小一致的特异性条带,成功获得 pET- 32a-I-FABP重组质粒(图2B)。
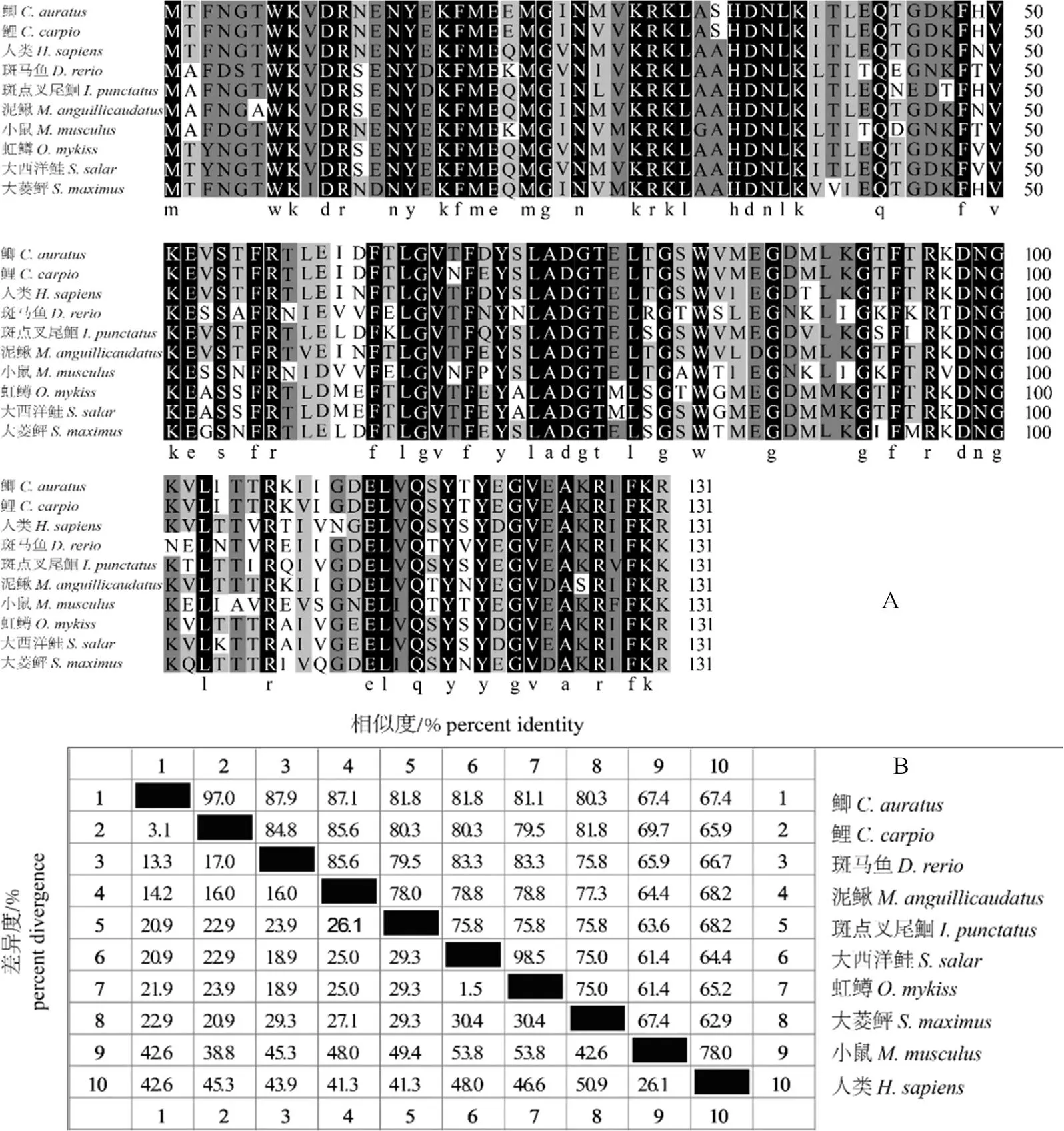
图1 不同物种I-FABP的氨基酸序列比对(A)及相似度分析(B)
Figure 1 Amino acid sequence alignment (A) and similarity analysis (B) of I-FABP of different species
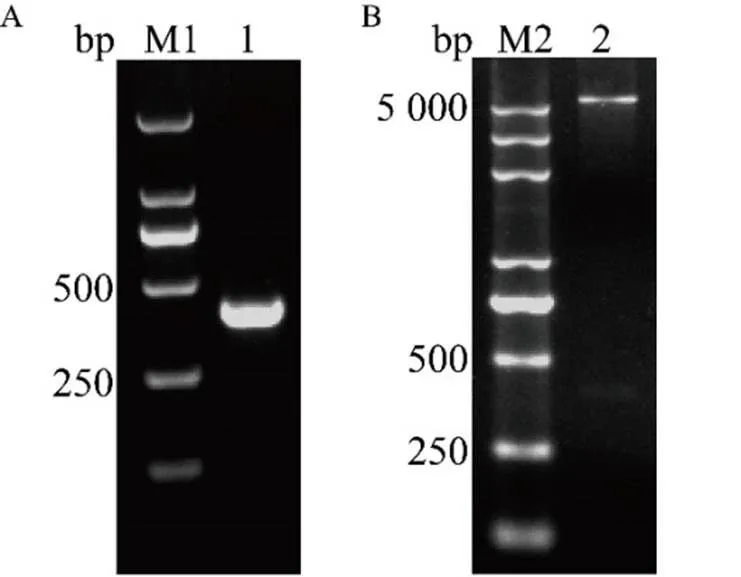
A. M1.分子质量标准 DL2 000;1. i-fabp 基因扩增
Figure 2 Amplification ofand identification of the recombinant plasmid pET-32a-I-FABP
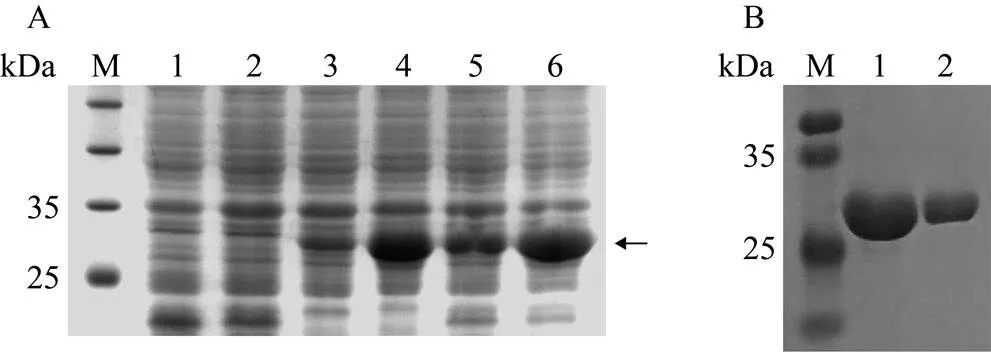
A. SDS-PAGE 分析 pET-32a-I-FABP在 16 ℃下的表达,M. 预染标准分子量蛋白;1. 不加入 IPTG 的空载对照组;2. 加入 IPTG 的空载对照组;3. 不加入 IPTG 的重组对照组;4. 加入 IPTG 全菌蛋白实验组;5. 实验组的沉淀;6. 实验组的上清;箭头指示表达的蛋白条带
Figure 3 Induced expression of pET-32a-I-FABP and purification of I-FABP
2.2 I-FABP的原核表达及纯化
将上述构建所得的重组质粒转化入表达菌株Rosetta(DE3),并诱导表达。与空载组和未诱导组相比,经诱导的pET- 32a-I-FABP重组质粒在32 kDa处出现明显的蛋白条带,可溶性分析显示该融合蛋白大多存在于上清中,呈可溶性表达(图3A)。利用His层析柱对该可溶性蛋白进行亲和纯化,SDS- PAGE凝胶电泳结果显示,目的蛋白条带明亮且单一,获得纯度及浓度均较高的重组融合蛋白(图3B)。
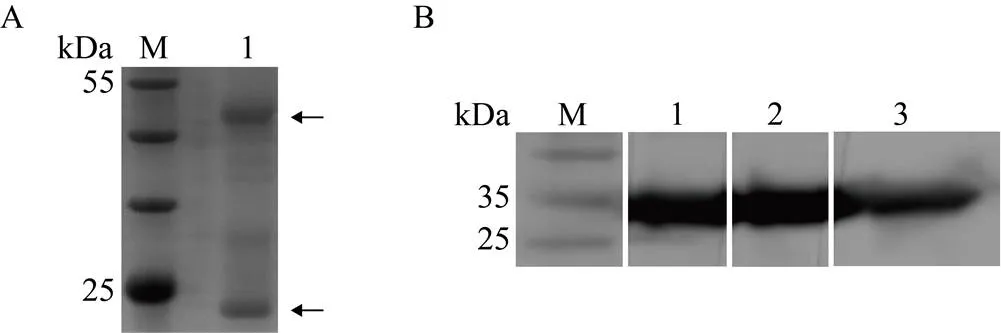
A. SDS-PAGE 检测兔多抗纯度,M. 预染标准分子量蛋白;1. 兔源抗I-FABP的多克隆抗体
Figure 4 Purification and titer detection of I-FABP rabbit polyclonal antibody
2.3 抗体的纯化及效价检测
以上述纯化后的重组蛋白免疫实验用兔,抗血清经Protein A/G层析柱亲和纯化,SDS-PAGE分析可见明确、清晰的条带,即获得了较为纯净的兔源多克隆抗体(图4A)。以兔多抗为一抗,商业化抗体羊抗兔为二抗,检测制备所得兔多抗的效价。结果显示(图4B),本实验制备的兔多抗在1∶20 000~1∶80 000 的稀释倍数下均有清晰的免疫印迹,表明该兔源I-FABP多克隆抗体具有较高效价。
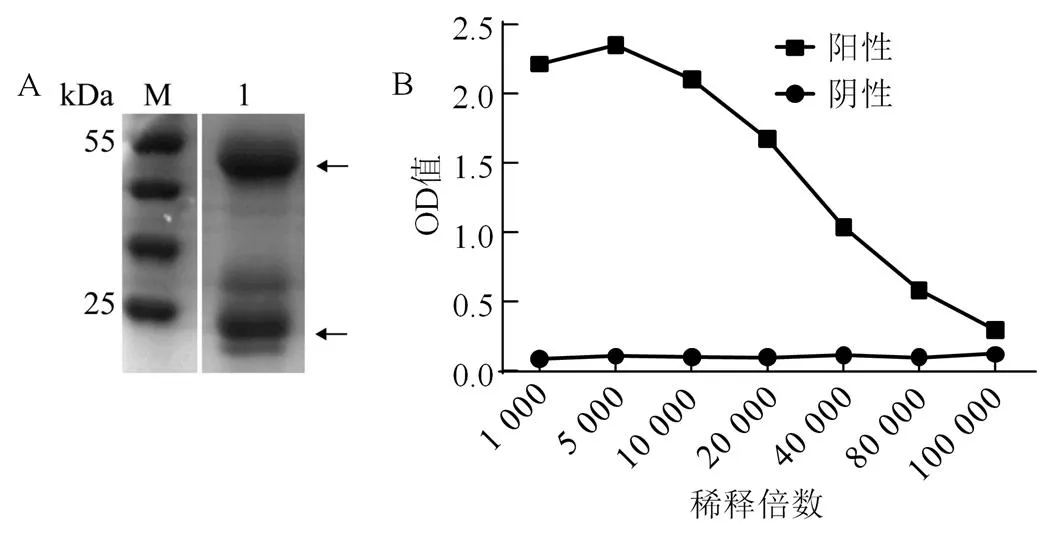
A. SDS-PAGE 检测鼠多抗纯度,M. 预染标准分子量蛋白;1. 鼠源抗I-FABP的多克隆抗体;B. 酶标法检测鼠源抗体效价
Figure 5 Purification and titer detection of I-FABP mouse polyclonal antibody
以纯化的重组蛋白免疫实验用鼠,抗血清经Protein A/G层析柱亲和纯化,获得较为纯净的鼠源I-FABP多克隆抗体(图5A)。以ELISA法测定经HRP标记后的鼠抗效价,(图5B),当稀释倍数为1∶80 000时,鼠抗仍具有反应性,表明本实验制备的鼠源I-FABP多克隆抗体效价为1∶80 000。

表1 包被抗体与酶标抗体最佳工作浓度的确定
2.4 最佳包被浓度及工作浓度的筛选
使用DAS-ELISA检测法和棋盘法确定包被抗体(兔源I-FABP多克隆抗体)及酶标抗体(鼠源I-FABP多克隆抗体)的最佳工作浓度。结果如表1所示,当两种抗体的稀释倍数均为1∶1 000时,P/N值最大(32.625 3),抗体反应性最好,但此时抗体利用率较低。综合P/N值及抗体利用率,认为P/N值为29.622 7时的稀释倍数为最佳,此时包被抗体及酶标抗体的稀释倍数分别为1∶10 000和1:5 000。
2.5 包被条件及抗体反应条件的确定
在包被条件及抗体反应条件的筛选中,不同温度、时间处理下抗体的反应性不同(图6)。当兔抗作为包被蛋白,4 ℃下包被24 h时,OD值与P/N值最高,反应性最好,故选择4 ℃ 24 h作为最佳包被条件(图6(a))。而鼠抗作为酶标抗体,与抗原抗体复合物在37 ℃,反应30~60 min时,OD值与P/N值均较高,均具有较好的反应性,故酶标抗体的最佳反应条件为37 ℃,30 ~60 min(图6(b))。
2.6 标准曲线的构建
基于上述工作条件的优化,建立DAS-ELISA检测方法,并利用该方法对已知浓度的I-FABP标准品进行检测,获得=0.003 5+0.036 7,2>0.999的标准曲线(图7)。

图6 最佳包被条件(a)及抗体反应条件(b)的确定
Figure 6 Determination of coating conditions (a) and antibody reaction conditions (b)
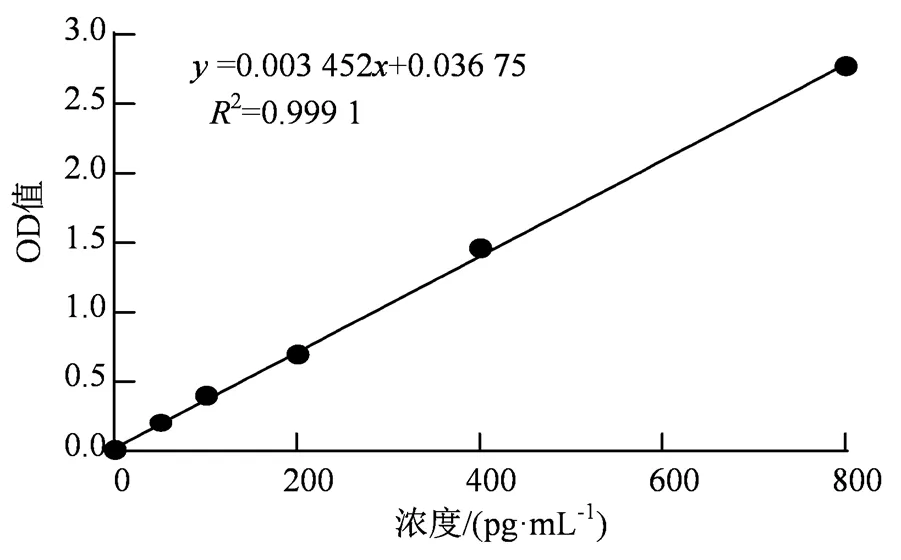
图7 基于DAS-ELISA的I-FABP标准曲线
Figure 7 Standard curve of I-FABP based on DAS-ELISA
2.7 临界(CUT-OFF)值的确定
为确定检测样品阴、阳性的临界值,本实验利用DAS-ELISA检测方法,对36份健康鲫样品进行检测,经计算可得,健康鲫样品的平均OD值为0.065 1,标准差为0.008 5,即临界值CUT-OFF= 0.090 6。
2.8 重复性及符合率检验
为检测基于DAS-ELISA检测方法检测所得结果的重复性,本实验对部分已知样品进行了检测。研究结果显示(表2),肠损伤模型鲫样品的批内变异系数为1.17%~3.82%,批间变异系数为0.16%~4.55%;健康鲫样品的批内变异系数为1.84%~5.50%,批间变异系数为2.70%~4.78%。所有检测结果的变异系数均远小于15%,表明该DAS-ELISA方法的检测结果重复性良好。符合率检验的结果显示(表3),DAS-ELISA检测法共检18例样品高于临界值,而36份样品低于临界值与商业化试剂盒检出结果一致,检验符合率为100%。
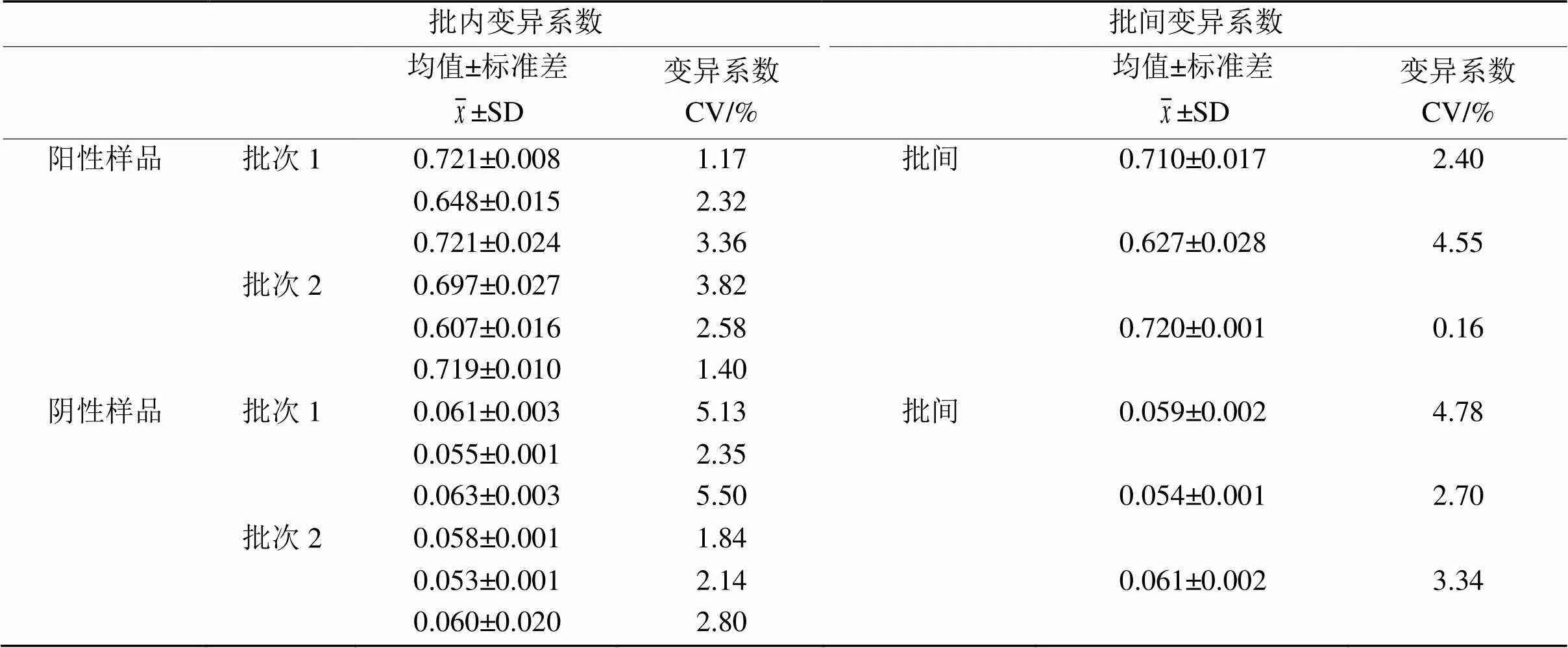
表2 重复性检验结果

表3 符合率检验结果
3 讨论与结论
肠道是鱼类病原体入侵的主要途径之一[18]。病原体可以影响肠道屏障完整性,诱导炎症反应,促进肠黏膜上皮细胞的损伤和凋亡[19]。迟缓爱德华氏菌()[20]、嗜水气单胞菌()[21]等引起的细菌性肠炎是养殖鱼类最常见的肠道疾病。嗜水气单胞菌感染可损害草鱼肠道黏膜屏障的结构和功能,出现炎性细胞浸润、黏膜下层水肿等现象[22]。大西洋鲑在感染传染性胰腺坏死病毒(infectious pancreatic necrosis virus,IPNV)后,肠道屏障通透性显著升高[23]。肠道通透性的增加还进一步增强了肠道对病原体的易感性,从而促进致病菌通过肠道屏障进行易位[24]。因此,肠道通透性在维持肠道正常生理功能和机体稳态方面发挥重要作用,对鱼类肠道通透性和肠道健康状况的评估将有助于疾病的防控。
目前用于评估肠道通透性的方法主要有基于光镜和电镜的组织学检测、基于分子生物学的紧密连接蛋白的表达分析以及基于血液、尿液及粪便的生物标志物检测[25]。相较于其他检测方法,乳果糖、甘露醇及I-FABP等生物标志物的检测方法取样方便,测定方法也更为快捷,应用广泛[26]。
I-FABP分子量低、稳定性强、组织特异性高,参与脂肪酸的转运与代谢。除调节糖、脂代谢外,I-FABP还与代谢性、炎症性等疾病相关。先前多数临床研究集中于I-FABP作为急性肠损伤的诊断标志上。近来研究显示,I-FABP对慢性肠道疾病也具有指示作用。此外,I-FABP的高亲和力及转运特性也为亲脂性药物的溶解及运输提供了便利,为药物的开发及慢性代谢性疾病的治疗提供了新的思 路[27]。目前,I-FABP已应用于坏死性小肠结肠炎,肠系膜梗死和溃疡性结肠炎等疾病的预前检测[28]。研究发现,I-FABP可以在艾滋病病毒感染造成的胃肠道炎症和肠黏膜损伤检测中发挥指示作用[15],鸡I-FABP也可作为由球虫病引起的鸡肠道病变的生物标志物,因此I-FABP还是评估病原感染造成的肠道损伤的重要指标[13]。
本实验利用原核表达制备了可溶性I-FABP重组蛋白及多克隆抗体,通过优化包被浓度、反应时间等建立了DAS-ELISA无损检测方法,具有良好的重复性,可用于鲫I-FABP的定量检测。鉴于I-FABP已在多种鱼类中被鉴定[29],如鲫、鲤、大西洋鲑、斑马鱼[30]、虹鳟[31],其氨基酸序列相似度高达80.3%以上,提示基于鲫I-FABP构建的检测方法或适用于其他鱼类的I-FABP检测,为鱼类肠道通透性和肠道健康状况的评估提供了方法及工具。
[1] PETERSON L W, ARTIS D. Intestinal epithelial cells: regulators of barrier function and immune homeostasis[J]. Nat Rev Immunol, 2014, 14(3): 141-153.
[2] UNGARO R, MEHANDRU S, ALLEN P B, et al. Ulcerative colitis[J]. Lancet, 2017, 389(10080): 1756-1770.
[3] TORRES J, MEHANDRU S, COLOMBEL J F, et al. Crohn's disease[J]. Lancet, 2017, 389(10080): 1741-1755.
[4] 翟少伟, 史庆超, 陈学豪. 饲料中添加抗菌肽Surfactin对吉富罗非鱼肠道健康的影响[J]. 水生生物学报, 2016, 40(4): 823-829.
[5] SZABO G. Gut-liver axis in alcoholic liver disease[J]. Gastroenterology, 2015, 148(1): 30-36.
[6] VAZIRI N D, ZHAO Y Y, Pahl M V. Altered intestinal microbial flora and impaired epithelial barrier structure and function in CKD: the nature, mechanisms, consequences and potential treatment[J]. Nephrol Dial Transplant, 2016, 31(5): 737-746.
[7] WU Y D, MURRAY G K, BYRNE E M, et al. GWAS of peptic ulcer disease implicatesinfection, other gastrointestinal disorders and depression[J]. Nat Commun, 2021, 12(1): 1146.
[8] MACPHERSON H L, BERGH Ø, BIRKBECK T H. An aerolysin-like enterotoxin frommay be involved in intestinal tract damage and mortalities in turbot,(L.), and cod,L., larvae[J]. J Fish Dis, 2012, 35(2): 153-167.
[9] ABDELHAMED H, LAWRENCE M L, KARSI A. Development and characterization of a novel live attenuated vaccine against enteric septicemia of catfish[J]. Front Microbiol, 2018, 9: 1819.
[10] BOUHET S, OSWALD I P. The intestine as a possible target for fumonisin toxicity[J]. Mol Nutr Food Res, 2007, 51(8): 925-931.
[11] VASANTH G, KIRON V, KULKARNI A, et al. A microbial feed additive abates intestinal inflammation in Atlantic salmon[J]. Front Immunol, 2015, 6: 409.
[12] LIU X, WU P, JIANG W D, et al. Effects of dietary ochratoxin A on growth performance and intestinal apical junctional complex of juvenile grass carp ()[J]. Toxins, 2020, 13(1): 11.
[13] CAHYANINGSIH U, SATYANINGTIJAS A S, TARIGAN R, et al. Chicken I-FABP as biomarker of chicken intestinal lesion caused by coccidiosis[J]. IOP Conf Ser: Earth Environ Sci, 2018, 196: 012032.
[14] VEERKAMP J H, PAULUSSEN R J, PEETERS R A, et al. Detection, tissue distribution and (sub)cellular localization of fatty acid-binding protein types[J]. Mol Cell Biochem, 1990, 98: 11-18.
[15] SKOWYRA A, MIKUŁA T, SUCHACZ M, et al. The role of serum I-FABP concentration in assessment of small intestine mucosa among HIV-infected patients[J]. Eur J Inflamm, 2015, 13(2): 75-81.
[16] COELHO A M M, SAMPIETRE S, MACHADO M C, et al. Intestinal fatty acid binding protein (I-FABP) is a marker of bacterial translocation in experimental acute pancreatitis[J]. HPB, 2016, 18(S1): e333.
[17] LAU E, MARQUES C, PESTANA D, et al. The role of I-FABP as a biomarker of intestinal barrier dysfunction driven by gut microbiota changes in obesity[J]. Nutr Metab, 2016, 13: 31.
[18] ZHANG X J, YANG W M, ZHANG D F, et al. Does the gastrointestinal tract serve as the infectious route ofin crucian carp ()?[J]. Aquac Res, 2015, 46(1): 141-154.
[19] GROSCHWITZ K R, HOGAN S P. Intestinal barrier function: molecular regulation and disease pathogenesis[J]. J Allergy Clin Immunol, 2009, 124(1): 3-20.
[20] LIU X, CHANG X, WU H, et al. Role of intestinal inflammation in predisposition ofinfection in zebrafish ()[J]. Fish Shellfish Immunol, 2014, 41(2): 271-278.
[21] SONG X, ZHAO J, BO Y, et al.induces intestinal inflammation in grass carp (): An experimental model[J]. Aquaculture, 2014, 434: 171-178.
[22] KONG W G, LI S S, CHEN X X, et al. A study of the damage of the intestinal mucosa barrier structure and function ofwith[J]. Fish Physiol Biochem, 2017, 43(5): 1223-1235.
[23] SUNDH H, OLSEN R E, FRIDELL F, et al. The effect of hyperoxygenation and reduced flow in fresh water and subsequent infectious pancreatic necrosis virus challenge in sea water, on the intestinal barrier integrity in Atlantic salmon,L.[J]. J Fish Dis, 2009, 32(8): 687-698.
[24] JUTFELT F, SUNDH H, GLETTE J, et al. The involvement ofvirulence factors in bacterial translocation across the rainbow trout,(Walbaum), intestine[J]. J Fish Dis, 2008, 31(2): 141-151.
[25] VANCAMELBEKE M, VERMEIRE S. The intestinal barrier: a fundamental role in health and disease[J]. Expert Rev Gastroenterol Hepatol, 2017, 11(9): 821-834.
[26] 高鹏, 张旭光, 刘雪来. 肠道黏膜屏障功能评估的研究进展[J]. 发育医学电子杂志, 2019, 7(1): 70-74.
[27] HUANG X, ZHOU Y, SUN Y, et al. Intestinal fatty acid binding protein: A rising therapeutic target in lipid metabolism[J]. Prog Lipid Res, 2022, 87: 101178.
[28] VOTH M, LUSTENBERGER T, RELJA B, et al. Is I-FABP not only a marker for the detection abdominal injury but also of hemorrhagic shock in severely injured trauma patients?[J]. World J Emerg Surg, 2019, 14(1): 1-9.
[29] 隋修磊, 张玉茹. 鱼类脂肪酸结合蛋白研究进展[J]. 水产科学, 2019, 38(4): 563-574.
[30] ZHANG W, ZHANG Y T, ZHANG H X, et al. Sex differences in transcriptional expression of FABPs in zebrafish liver after chronic perfluorononanoic acid exposure[J]. Environ Sci Technol, 2012, 46(9): 5175-5182.
[31] BAYIR M, BAYIR A, WRIGHT J M. Divergent spatial regulation of duplicated fatty acid-binding protein (fabp) genes in rainbow trout ()[J]. Comp Biochem Physiol D Genom Proteom, 2015, 14: 26-32.
DAS-ELISA method of detecting intestinal permeability based on I-FABP in crucian carp()
WANG Jingwen1, ZOU Zhenjiang1, LI Lijuan1,2, GU Zemao1,2, YUAN Junfa1,2
(1. College of Fisheries, Huazhong Agricultural University, Wuhan 430070;2. National Aquatic Animal Diseases Para-reference Laboratory, Huazhong Agricultural University, Wuhan 430070)
Intestinal permeability is directly related to intestinal homeostasis and individual health. At present, there is a lack of quantitative evaluation methods and reagents for intestinal permeability of fish. Serum intestinal fatty acid binding protein (I-FABP) is an important serum biological index for quantitative evaluation of intestinal permeability. In order to establish a quantitative detection method of serum I-FABP concentration in crucian carp (), the I-FABP gene of crucian carp was cloned, expressed and purified in prokaryote. The rabbit and mouse polyclonal antibodies were prepared by immunizing New Zealand white rabbit and mouse with the recombinant protein, and their titers were 1:80 000. The rabbit polyclonal antibody was used as the coating protein, and the mouse polyclonal antibody labeled with HRP was used as the enzyme labeled antibody. By optimizing the reaction conditions, a double antibody sandwich ELISA (DAS-ELISA) method based on rI-FABP was established. The linear regression equation of the standard curve was=0.003 5+0.036 7, the fitting degree was high,2was 0.999 1, and the cut-off value was 0.090 6. The intra- and inter-assay coefficient of variation was 1.17%-5.50% and 0.16%-4.78% indicating the good repeatability of established DAS-ELISA. Compared with a commercial kit, the coincidence rate among 54 samples was 100%. The DAS-ELISA detection method constructed in this study can be used for the quantitative evaluation of the intestinal permeability of crucian carp. In view of the conservatism of fish I-FABP, this method may be used for quantitative evaluation of intestinal permeability of other fish.
intestinal fatty acid binding protein(I-FABP); intestinal permeability; double antibody sandwich ELISA(DAS-ELISA); prokaryotic expression; polyclonal antibody; crucian carp()
S917
A
1672-352X (2023)05-0809-08
10.13610/j.cnki.1672-352x.20231030.010
2023-10-31 07:41:52
[URL] https://link.cnki.net/urlid/34.1162.S.20231030.0955.018
2022-09-22
国家自然科学基金(32073013)资助。
王靖雯,硕士研究生。E-mail:953913796@qq.com
袁军法,博士,副教授。E-mail:jfyuan@mail.hzau.edu.cn
