物理化学教学中药物制剂热力学相图案例分析
2023-11-02吉远辉占慧琳
吉远辉 陈 俏 葛 凯 占慧琳 霍 尧
(1. 东南大学 化学化工学院,江苏省生物药物高技术研究重点实验室,江苏 南京 211189;2. 南京工业大学 海外教育学院,江苏 南京 211816)
化工生产中对产品进行分离提取时离不开蒸馏、结晶、萃取等各种单元操作,而这些单元操作过程中的理论基础就是相平衡原理[1]。很多学生对“物理化学”课程中相平衡章节的学习感到枯燥、抽象、难学。为了让学生更好学习这一知识难点,结合近些年来相图在药物制剂开发过程中的应用,作者编写、收集了多个案例,以期起到抛砖引玉的作用。
1 药物制剂中的二元相图案例分析
二元相图[2]是表示系统中两个组元在热力学平衡状态下组分和温度、压力之间的关系简明图解。最初,相图通过大量实验得到。随着计算材料学的发展,以分子动力学为基础的计算相图成为得到相图的一种高效手段。当存在两个组元时,成分也是变量,通常只考虑在常压下的结晶过程,则取两个变量温度和成分,横坐标用线段表示成分,纵坐标表示温度。平面上按平衡状态下存在的相来分隔。
对二组分体系,至少有一个相,根据相律,该体系的最大自由度为3,即体系的状态由三个独立变量(温度、压力和组分)所决定。其相图为三个坐标的立体图。对于二组分体系,常常保持一个变量为常量,可得到三种平面图p-X(压力—组分)图,T-X(温度—组分)图和T-p(温度—压力)图。最常用的是前两种。
案例一:非晶态药物的溶解度优势
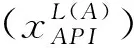

图1 API/溶剂二元体系热力学相行为[4]
由于非晶态API的溶解度通常很难测量,确定溶解度优势的常用方法是构建热力学模型。在本案例中,研究者基于扰动链统计缔合流体理论(perturbed-chain statistical associating fluid theory, PC-SAFT)对API进行建模,预测了五种水溶性差的API(格列本脲、灰黄霉素、氢氯噻嗪、吲哚美辛和伊曲康唑)在水中的相图,结果如图2所示。
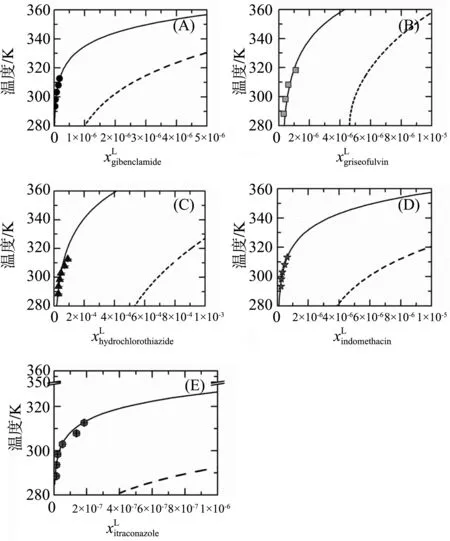
实线表示结晶态API在水中的预测溶解度;虚线表示预测的非晶态API的溶解度(基于PC-SAFT建模)图2 API/水体系相图[4]:格列本脲(A)、灰黄霉素(B)、氢氯噻嗪(C)、吲哚美辛(D)和伊曲康唑(E)
通过PC-SAFT模型成功预测了药物晶态和非晶态在水中溶解度,曲线组成了API/水二元相图,与图1概念化结构图基本一致。预测得到的晶体药物的溶解度与实验结果具有很好的吻合性。API/水二元相图形象直观地说明温度对药物晶态和非晶态相行为的影响,为制药过程中难溶药物剂型开发设计提供辅助。
案例二:提高API的生物利用度研究中的相分析
为了提高API生物利用度,通常将API集成到载体聚合物基质中,得到的混合物称为固体分散体[7]。而通过研究固体分散体的相行为可为固体分散体剂型开发提供可行性分析,包括辅料类型筛选、辅料分子量设计以及载药比设定。如图3所示,固体分散体中可能包含晶态和非晶态API,从热力学角度来看非晶态是一种过冷态,我们将它看作一种特殊液态。
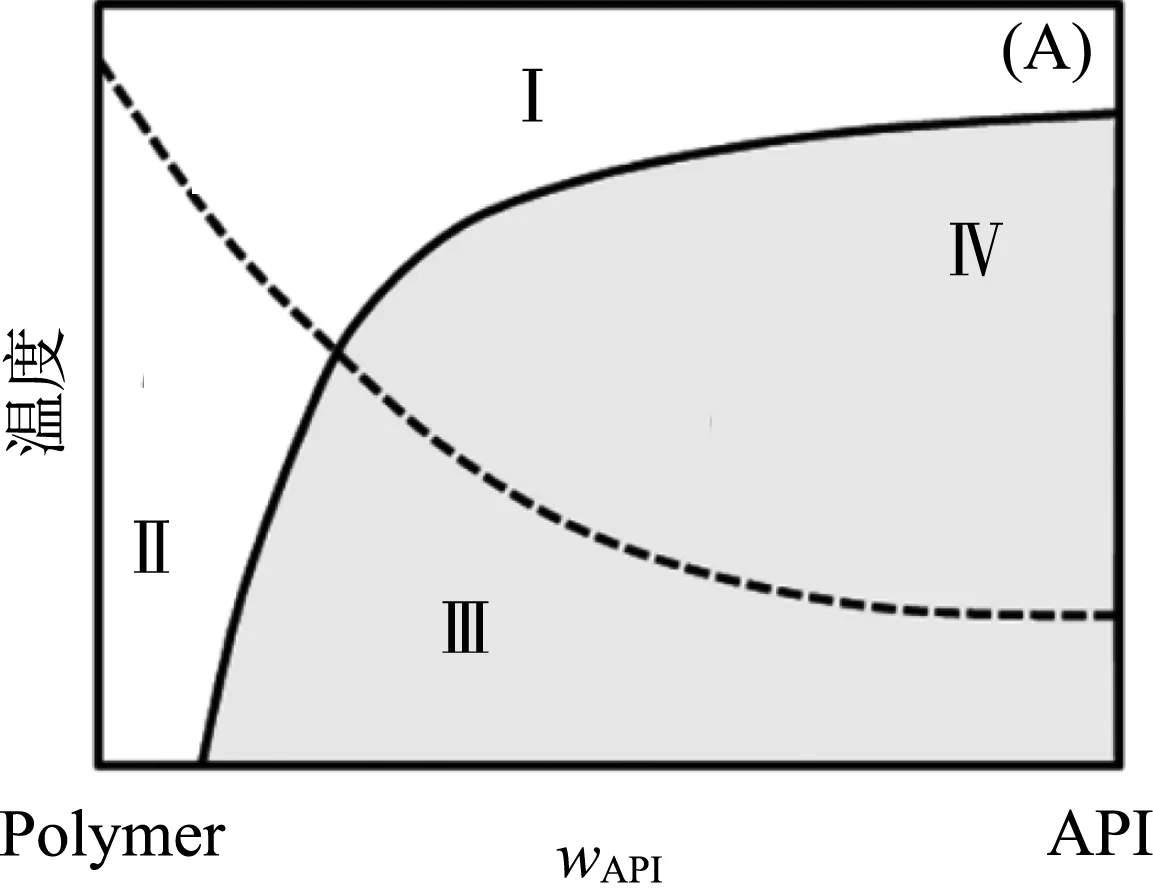
图3(A)中黑色实线描述了晶态API在聚合物中的溶解度,即固液相平衡线。所考察的聚合物(ploymer)是无定形或处于熔融状态(例如高于熔点的PEG),聚合物就充当溶剂,晶态API充当溶质。在固液平衡线以上(Ⅰ区+Ⅱ区),药物和聚合物辅料是热力学稳定的熔融态,不存在重结晶的风险。在固液平衡线以下(Ⅲ区+Ⅳ区)热力学性质不稳定,且药物倾向于重结晶。除了热力学因素外,动力学因素对药物的重结晶也起到了重要作用,这与玻璃化转变温度有关[8]。
玻璃化转变温度曲线(图3中的短虚线)是将相图划分出分子迁移率高的区域(Ⅰ区+Ⅳ区)和分子迁移率低的区域(Ⅱ区+Ⅲ区)的界限。在分子迁移率高的区域Ⅰ,药物与高分子辅料是稳定的熔融态,在分子迁移率高的区域Ⅳ,药物与高分子辅料形成的无定形固体分散体将发生相分离,甚至发生重结晶。在分子迁移率低的区域Ⅲ,药物与高分子辅料形成的无定形固体分散体即使会发生相分离或再结晶,但其发生相分离或再结晶的速率较低,在一定时间内无定形固体分散体也可能维持一定的稳定性,从而维持药剂的药用效果。
图3(B)在高药物比例时,相图中含有由液-液相平衡曲线围成的无定型相分离区,该区域内药物以无定形状态存在,理论上微小局部波动都可以引发固体分散体的液-液相分离,形成药物富相和溶剂富相。
本案例中,作者测定了青蒿素和吲哚美辛在不同分子量聚乙二醇(PEG400、PEG6000和PEG35000)中的溶解度,结合PC-SAFT预测了磺胺类药物在PEG中的溶解度,用于预测API/聚合物固体分散体的整个相图(图4)。
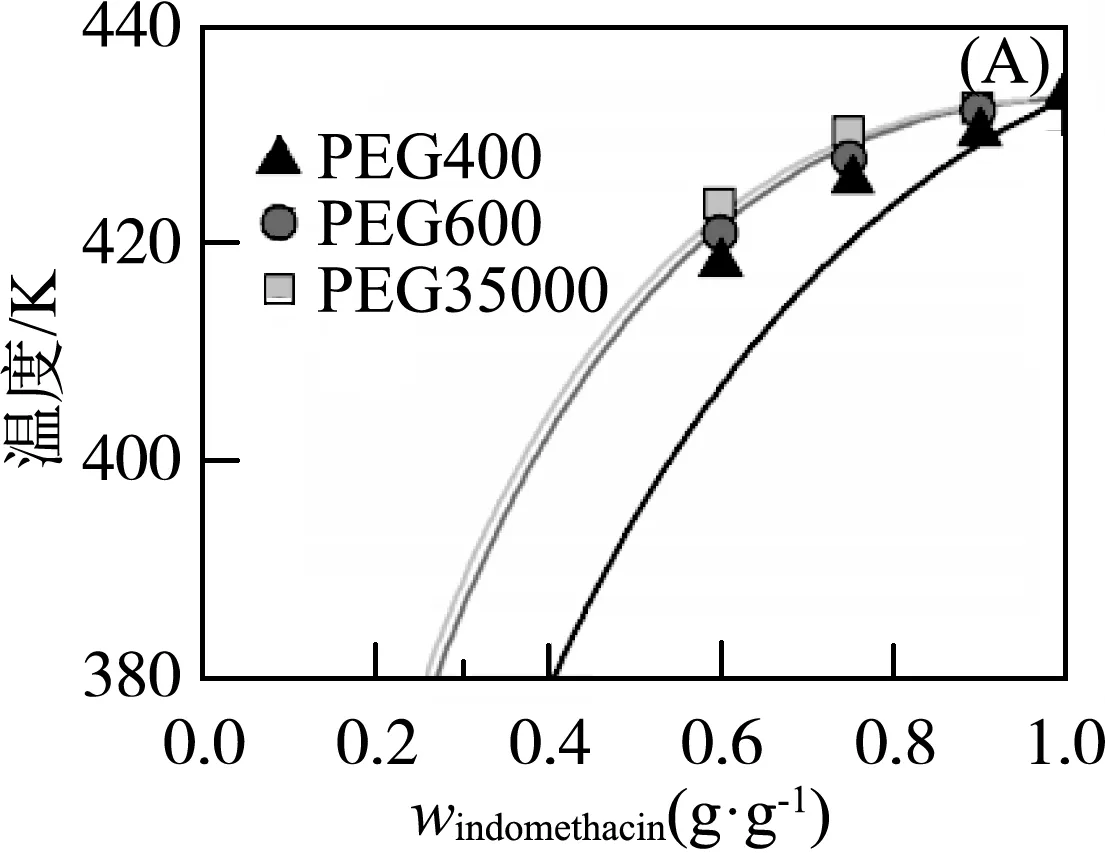
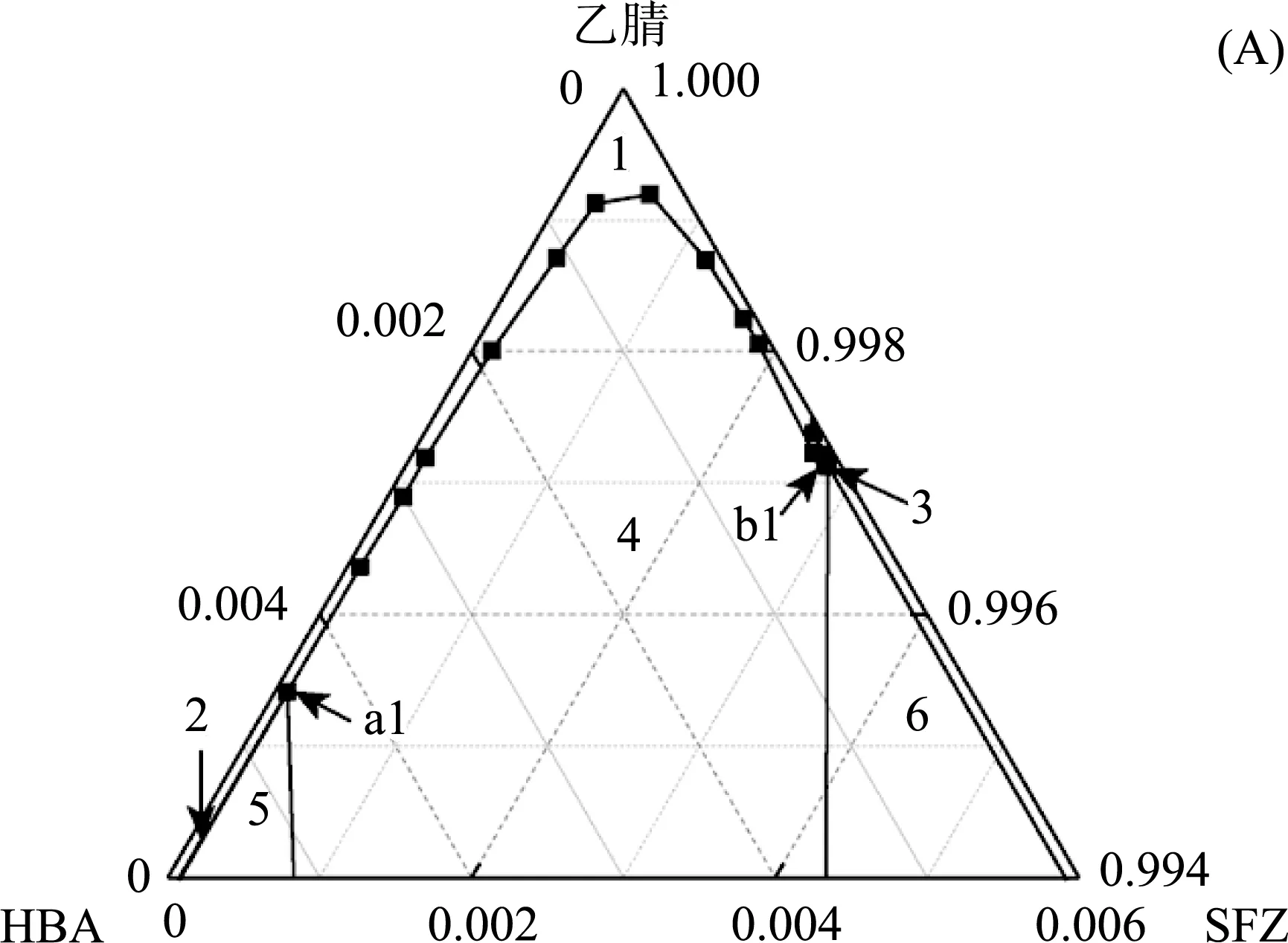
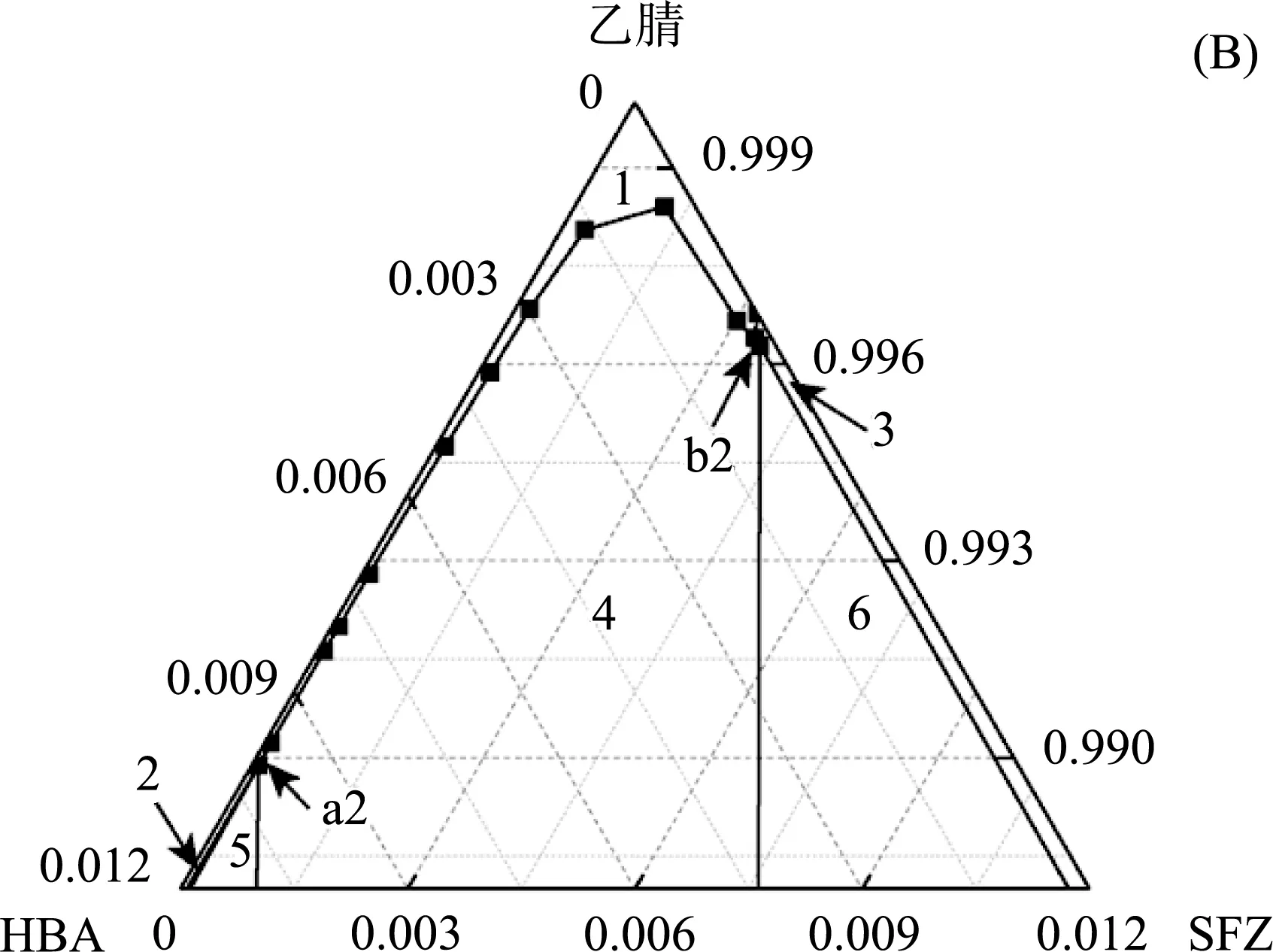
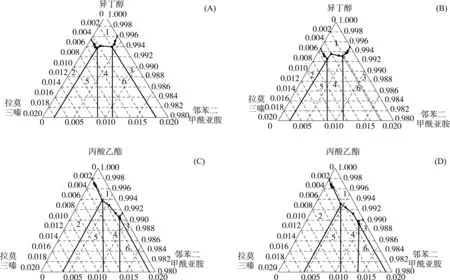
通过分析,吲哚美辛和青蒿素在PEG中的溶解度是PEG分子量的函数,并按以下顺序增加:PEG35000 三元系统是包括三个独立单元的系统,三元相图即三元系统的相图。三元相图是表示在恒压下以温度变量为纵坐标,两个成分变量为横坐标的三维空间图形,由一系列空间曲面及平面将三元相图分成很多相区。冷却结晶法为药物生产常用方法,往往可获得高收率。但在结晶过程存在共晶与单一组分同时析出的风险。因此三元相图的构建与溶剂的选择对结晶工艺的设计至关重要[10]。 案例三:磺胺二甲嘧啶-对羟基苯甲酸共晶在乙腈溶剂中的三元相图测定 药物共晶是由活性药物分子和共晶形成体通过氢键或其他非共价键相互作用形成的,能够改善高渗透性、低溶解度药物存在的低溶解性问题。本案例中,作者采用溶液法制备磺胺二甲嘧啶(SFZ)-对羟基苯甲酸(HBA)共晶,分别在 298.15 K、303.15 K时,建立共晶体在乙腈中的三元相图(图5)。然后又采用XRD、DSC、SEM对SFZ和HBA在298.15 K时部分干燥固相进行表征分析。通过一系列的表征结果与相图进行比较,得到了可利用相图规律制备药物共晶[11]。 图5 SFZ-HBA-乙腈三元体系相图:298.15 K (A);303.15 K(B)[11] 如图5所示,SFZ-HBA-乙腈体系在298.15和303.15 K时的三元相图为对称相图。当温度升高时,SFZ、HBA、SFZ-HBA共晶的溶解度均会增大,进而造成平衡液相线向下移动,不饱和区域(即区域1)面积增大,纯共晶区域(即区域4)面积也同时变大,这是由于温度的升高增大了溶质和溶剂间的相互作用力,从而提高了溶质的溶解度,有利于共晶的形成。此外,在不同温度下的两个不变点a1、b1和a2、b2的相对位置变化不明显,说明温度的变化不能改变相图的对称性,只能促使相图向远离相图顶点的方向移动。 案例四:拉莫三嗪-邻苯二甲酰亚胺药物共晶在有机溶剂中溶解度及三元相图测定 本案例中,研究者分别测定了拉莫三嗪-邻苯二甲酰亚胺共晶在298.15 K和303.15 K温度下,在异丁醇、丙酸乙酯溶液体系下的三元相图,三元相图见图6[12]。 1:不饱和区;2:拉莫三嗪(LAM)+溶液;3:邻苯二甲酰亚胺(PTL)+溶液;4:共晶(1∶1LAM/PTL)+溶液;5:共晶+拉莫三嗪+溶液(同时对共晶和拉莫三嗪饱和);6:共晶+邻苯二甲酰亚胺+溶液(同时对共晶和邻苯二甲酰亚胺饱和)图6 拉莫三嗪+邻苯二甲酰亚胺+溶剂三元相图[12]:298.15 K(A)、(C),303.15 K(B)、(D) 当温度升高时,拉莫三嗪、邻苯二甲酰亚胺和拉莫三嗪-邻苯二甲酰亚胺共晶的溶解度会提高,因而造成平衡液相线向下移动,不饱和区域面积随之增大,从图中也可以分析得到纯共晶区域面积也增大了。此外在相同溶剂不同温度下的两个不变点的相对位置的变化不明显,这也可以说明温度对拉莫三嗪-邻苯二甲酰亚胺共晶的三元相图对称性的影响很小。不仅温度对三元相图会造成影响,不同的溶剂也是影响三元相图的一个主要因素。从拉莫三嗪-邻苯二甲酰亚胺共晶在异丁醇中的三元相图可以得到,三元相图的共晶稳定区域是对称的,再通过对比拉莫三嗪-邻苯二甲酰亚胺共晶在丙酸乙酯中的三元相图,会发现相图不对称,共晶稳定区域会偏向于邻苯二甲酰亚胺侧。造成这一现象的最主要的原因是各固体组分在溶液中溶解度的差异性。在异丁醇中,当温度为298.15 K时,拉莫三嗪和邻苯二甲酰亚胺的溶解度分别是0.004 6和0.003 88,两组分的溶解度差异不大,因此使得相图的对称性很好。但是,在丙酸乙酯中。当温度为298.15 K时,拉莫三嗪和邻苯二甲酰亚胺的溶解度却为0.002 04和0.008 67,两组分的溶解度差异很大,所以相图中共晶的稳定区域开始显著偏向溶解度更大的邻苯二甲酰亚胺一侧。综上,各固体组分在溶剂中溶解度的差异性大小会影响相图的对称性。 相平衡是热力学在化学领域中的重要应用之一,研究多相系统的平衡在化学,化工的科研和生产中具有重要意义,例如:溶解、蒸馏、重结晶、萃取、提纯及金相分析等方面都要用到相平衡的知识。随着新冠疫情席卷全球,药物制剂、药物设计等领域的研究与开发已然变成了当下最热门的话题之一。 作者着重于将学生课堂上的物理化学基础内容中的相图分析与药物制剂案例进行结合,通过前沿热门的药物研究,让同学们深刻体会到相图、相平衡在科研中作为分析方法的基础作用。以此将枯燥、抽象难懂的物理化学理论知识变成一个个生动的实例,培养学生自主地演绎推演,案例分析能力,从而达到激发学生兴趣、提高学习效率、深化学生记忆的目的。 “物理化学”教学任重而道远,文中案例也仅在广阔的药物制剂领域拾取零光片羽,但仍希望能够在当今教育改革的趋势中增砖添瓦,贡献自己的一份微薄力量,愿同广大教师队伍一起,为物理化学科研与教学事业提供更广的前景。2 药物制剂中的三元相图案例分析
3 结语
