五岭龙胆化学成分及其抗炎活性研究
2023-11-02彭江丽彭求贤李顺祥
彭江丽,王 鹏,彭求贤,李 娟*,李顺祥*
1湖南中医药大学药学院;2湖南省中药活性物质筛选工程技术研究中心;3湖南省中美老年性退行性疾病治疗药物国际联合研究中心,长沙410208
五岭龙胆为龙胆科龙胆属五岭龙胆(GentianadavidiiFranch.)的全草[1],生于350~2 500 m的山坡草丛及林下,主要分布于湖南、浙江、福建和江西等地,夏或秋季采收,洗净,晒干或鲜用。据清代《文堂集验方》和《全国中草药汇编》记载,五岭龙胆又名九头青[2],《中华本草》中又称其为落地荷花[3],并在各地民族医药书籍中均有所记载。其味苦,性寒,具有清热解毒、利湿的功效,主治小儿惊风、目赤、咽痛、肝炎、痢疾、淋证、化脓性骨髓炎、痈疮肿毒和毒蛇咬伤[2]。五岭龙胆作为民间用药,其用药历史悠久、疗效显著,主要用于治疗肺热咳嗽[4]、子宫内膜炎[5]和化脓性骨髓炎[6]等炎症相关疾病,但目前其化学成分和药理作用研究比较薄弱。同属植物龙胆研究报道[7]较多,其主要含有环烯醚萜类、黄酮类和三萜类等成分[8],所含成分具有抗炎、保肝和抗氧化等药理活性[9]。本实验根据龙胆的研究基础,采用柱色谱、波谱技术和细胞活性筛选方法,研究五岭龙胆抗炎药效物质基础,为五岭龙胆药材的开发提供实验依据。
1 材料与方法
1.1 仪器与材料
INOVA-600MHz核磁共振波谱仪(瑞士Bruker公司);HR-ESI-TOF-MS光谱仪(美国Agilent公司);Varioskan LUX多功能酶标仪(Thermo 公司);TS2倒置生物显微镜(日本尼康公司);3111型二氧化碳培养箱(美国赛默飞世尔科技有限公司);Sephadex LH-20葡聚糖凝胶填料(瑞士GE Healthcare公司);反相ODS柱填料(日本YMC公司);甲醇等试剂均为分析纯(湖南汇虹试剂有限公司);胎牛血清(批号:164210-50)、DMEM高糖培养基(批号:PM150210)、PBS磷酸缓冲液(批号:PB180327)和胰蛋白酶(批号:SV300371)(Hyclone公司);噻唑蓝(批号:M2128)、脂多糖(批号:L2630)和二甲基亚砜(批号:D2650)(Sigma公司);NO Griess试剂盒(批号S0021M,南京碧云天生物科技有限公司);地塞米松(dexamethasone,DXMS)(批号D8041,纯度>98.5%,北京索莱宝科技有限公司);小鼠单核巨噬细胞(RAW 264.7)(批号CL-0190,武汉普诺赛生命科技有限公司)。
五岭龙胆于2019年12月采自湖南省浏阳大围山,经中药鉴定教研室刘塔斯教授鉴定为龙胆科植物五岭龙胆(GentianadavidiiFranch.)全草,凭证标本(20191211)保存于湖南中医药大学中药活性物质筛选工程技术研究中心。
1.2 实验与方法
1.2.1 提取分离
五岭龙胆干燥全草(7.5 kg),粉碎成粗粉,加入适量70%乙醇浸润,装入渗漏装置中,70%乙醇洗脱至渗滤液无色。药渣继续用70%乙醇回流提取二次,合并渗漏液与提取液,50 ℃减压浓缩至无醇味,得五岭龙胆提取物(1.2 kg)。提取物加适量蒸馏水使悬浮,依次用石油醚、乙酸乙酯和正丁醇萃取6次,每次加入2 L溶剂,分别合并不同极性萃取液,50 ℃减压浓缩,制得石油醚萃取部位(浸膏30.0 g)、乙酸乙酯萃取部位(浸膏150.0 g)、正丁醇萃取部位(浸膏135.0 g)和水层(浸膏约500.0 g)。
乙酸乙酯萃取部位(150.0 g)加适量乙酸乙酯溶解,硅胶(80~100目)拌样后上样,装进硅胶柱色谱(硅胶柱7.0 cm×60.0 cm)上,用石油醚-乙酸乙酯系统(30∶1→10∶1→5∶1→1∶1→0∶1)梯度洗脱,得到5个流分(Fr.1~Fr.5)。Fr.1(8.3 g)经反复硅胶柱层析、Sephadex LH-20 凝胶柱及重结晶,分离得到化合物3(5.5 mg)、8(4.5 mg)和12(10.3 mg)。Fr.2(22.5 g)经硅胶柱层析,石油醚-乙酸乙酯(7∶1)系统等度洗脱,得到10个流分(Fr.2.1~Fr.2.10);Fr.2.1经反复硅胶柱分离得化合物6(5.7 mg)和14(10.1 mg);Fr.2.5经反复硅胶柱分离得化合物4(10.4 mg)和5(40.2 mg);Fr.2.7经ODS柱,甲醇-水(20%→100%)系统梯度洗脱,分离得到化合物1(6.1 mg)和2(5.2 mg)。Fr.4(4.9 g)经ODS柱,甲醇-水(20%→100%)系统梯度洗脱,得到10个流分;Fr.4.5经反复硅胶柱和Sephadex LH-20 凝胶柱分离,得到化合物11(5.7 mg);Fr.4.7经硅胶柱层析,三氯甲烷-甲醇(7∶1)系统等度洗脱,得到化合物7(4.3 mg)。Fr.5(23.6 g)经ODS柱,甲醇-水(20%→100%)系统梯度洗脱,得到10个流分;Fr.5.2经硅胶柱层析,三氯甲烷-甲醇(8∶1)系统等度洗脱,得到化合物9(6.9 mg);Fr.5.3经反复ODS柱和硅胶柱分离得化合物15(7.4 mg);Fr.5.8组分经反复硅胶柱层析,分离得到10(7.2 mg)。正丁醇萃取部位(135.0 g)用适量正丁醇溶解,硅胶(80~100目)拌样后上样,装入已干法装柱的硅胶柱(8.0 cm×55.0 cm)上,用二氯甲烷-甲醇(30∶1→10∶1→5∶1→1∶1→0∶1)系统梯度洗脱,得到5个流分(Fr.A~Fr.E);Fr.B(4.3 g)经ODS柱,甲醇-水(20%→100%)系统梯度洗脱,得到10个流分。Fr.B.3经Sephadex LH-20 凝胶柱和硅胶柱分离,得到化合物13(7.9 mg)。
1.2.2 抗炎活性筛选
不同化合物对RAW 264.7细胞的毒性作用。取生长状态良好且处于对数生长期的RAW 264.7细胞,用DMEM完全培养基配制成单细胞悬液,细胞计数,以3×105个/mL,每孔100 μL均匀接种于96孔板中,于37 ℃,5% CO2细胞培养箱中培养24 h。设置空白组不加细胞、对照组加入含细胞的DMEM完全培养基、样品组加入不同浓度(1、10、25、50和100 μmol/L)化合物的DMEM完全培养基,每组3个复孔。继续培养24 h后,弃去旧培养基,每孔加入20 μL MTT,培养4 h,弃去液体,加入150 μL DMSO溶液,低速振荡10 min后,酶标仪490 nm测定各孔吸光值(OD值),计算细胞存活率。计算公式为:细胞存活率=[(样品组OD值-空白组OD值)/(对照组OD值-空白组OD值)]×100%。
不同化合物对LPS诱导的RAW 264.7细胞中NO释放量的影响。采用LPS诱导RAW 264.7细胞炎症模型,分别设置空白组(无细胞)、对照组(仅DMEM培养基)、模型组(1 μg/mL LPS)[10]、阳性药物组(1 μg/mL LPS +1、10、25和50 μmol/L地塞米松)、实验组(1 μg/mL LPS+1、10、25和50 μmol/L化合物1~15)每组3个复孔。培养24 h,取其上清液于离心管中,采用Griess试剂盒说明书中操作方法,按步骤顺序加入各试剂,检测细胞培养液中NO的含量,根据标准曲线计算各组浓度。将各剂量和抑制率等参数用非线性回归拟合计算IC50[11]。
1.3 统计学方法
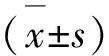
2 结果
2.1 结构鉴定
化合物1无色针状结晶(三氯甲烷);mp.273~275 ℃;ESI-MS:m/z455[M-H]-,分子式为C30H48O3;1H NMR(600 MHz,CDCl3)δ:5.18(1H,t,J= 3.6 Hz,H-12),3.60(1H,m,H-3),2.15(1H,d,J= 10.8 Hz,H-18),0.98(3H,s,H-23),0.95(3H,d,J= 6.1 Hz,H-29),0.91(3H,s,H-27),0.88(3H,s,H-26),0.82(3H,d,J= 6.1 Hz,H-30),0.78(3H,s,H-24),0.73(3H,s,H-25);13C NMR(150 MHz,CDCl3)δ:39.2(C-1),27.0(C-2),79.0(C-3),39.0(C-4),55.6(C-5),18.0(C-6),33.3(C-7),42.4(C-8),47.8(C-9),37.2(C-10),23.5(C-11),125.8(C-12),138.5(C-13),39.7(C-14),28.2(C-15),23.7(C-16),48.1(C-17),53.1(C-18),37.1(C-19),39.7(C-20),31.0(C-21),39.4(C-22),28.3(C-23),15.6(C-24),15.8(C-25),17.1(C-26),23.5(C-27),181.0(C-28),17.2(C-29),21.3(C-30)。以上数据与文献[12]报道基本一致,故鉴定化合物1为熊果酸。
化合物2无色针状结晶(乙酸乙酯);mp.208~210 ℃;ESI-MS:m/z441[M-H]-,分子式为C30H50O2;1H NMR(600 MHz,CDCl3)δ:5.16(1H,t,J= 3.6 Hz,H-12),3.56(1H,d,J= 10.8 Hz,H-28a),3.25(1H,dd,J= 10.8,3.6 Hz,H-3),3.22(1H,d,J= 10.8 Hz,H-28b),1.36(3H,s,H-27),1.31(3H,s,H-26),1.13(3H,s,H-25),0.97(3H,s,H-23),0.96(3H,d,J= 6.0 Hz,H-29),0.83(3H,d,J= 6.0 Hz,H-30),0.82(3H,s,H-24);13C NMR(150 MHz,CDCl3)δ:38.9(C-1),28.3(C-2),79.2(C-3),38.2(C-4),55.3(C-5),18.5(C-6),31.6(C-7),40.2(C-8),47.8(C-9),35.3(C-10),26.2(C-11),125.2(C-12),138.9(C-13),42.2(C-14),27.4(C-15),23.5(C-16),37.0(C-17),54.2(C-18),39.6(C-19),39.5(C-20),30.8(C-21),32.9(C-22),30.3(C-23),15.8(C-24),15.8(C-25),17.5(C-26),23.5(C-27),70.1(C-28),16.9(C-29),21.5(C-30)。以上数据与文献[13]报道基本一致,故鉴定化合物2为乌发醇。
化合物3白色粉末;ESI-MS:m/z485[M-H+HCOOH]-,分子式为C30H48O2;1H NMR(600 MHz,CDCl3)δ:9.31(1H,d,J= 1.1 Hz,H-28),5.30(1H,t,J= 3.5 Hz,H-12),3.20(1H,dd,J= 11.4,4.9 Hz,H-3),1.08(3H,s,H-27),0.97(3H,s,H-23),0.95(3H,d,J= 6.5 Hz,H-30),0.91(3H,s,H-26),0.86(3H,d,J= 6.5 Hz,H-29),0.77(3H,s,H-25),0.75(3H,s,H-24);13C NMR(150 MHz,CDCl3)δ:38.8(C-1),28.3(C-2),79.1(C-3),38.8(C-4),55.3(C-5),18.4(C-6),33.2(C-7),38.9(C-8),47.7(C-9),37.1(C-10),23.4(C-11),126.3(C-12),137.9(C-13),42.3(C-14),27.3(C-15),27.0(C-16),50.3(C-17),52.7(C-18),39.9(C-19),39.1(C-20),30.3(C-21),32.0(C-22),29.8(C-23),16.8(C-24),15.6(C-25),17.3(C-26),23.4(C-27),207.6(C-28),15.8(C-29),21.2(C-30)。以上数据与文献[14]报道基本一致,故鉴定化合物3为ursaldehyde。
化合物4白色粉末;ESI-MS:m/z457[M-H+HCOOH]-,分子式为C29H48O;1H NMR(600 MHz,CDCl3)δ:5.31(1H,t,J= 3.3 Hz,H-12),3.25(1H,dd,J= 12.3,4.7 Hz,H-3),2.85(1H,dd,J= 13.4,4.2 Hz,H-18),0.98(3H,s,H-23),0.97(3H,d,J= 7.2 Hz,H-28),0.95(3H,s,H-27),0.94(3H,s,H-26),0.90(3H,d,J= 7.2 Hz,H-29),0.80(3H,s,H-25),0.78(3H,s,H-24);13C NMR(150 MHz,CDCl3)δ:38.5(C-1),23.5(C-2),79.1(C-3),37.2(C-4),55.3(C-5),18.4(C-6),32.7(C-7),38.9(C-8),46.1(C-9),33.9(C-10),26.1(C-11),123.1(C-12),139.01(C-13),39.4(C-14),28.2(C-15),27.3(C-16),47.7(C-17),46.7(C-18),41.2(C-19),41.8(C-20),30.8(C-21),33.2(C-22),32.7(C-23),17.2(C-24),15.5(C-25),15.7(C-26),27.8(C-27),23.7(C-28),23.1(C-29)。以上数据与文献[15]报道基本一致,故鉴定化合物4为28-norurs-12-en-3β-ol。
化合物5白色粉末;ESI-MS:m/z501[M-H+HCOOH]-,分子式为C30H48O3;1H NMR(600 MHz,CDCl3)δ:5.23(1H,t,J= 3.4 Hz,H-12),3.20(1H,dd,J= 11.4,4.9 Hz,H-3),2.80(1H,dd,J= 13.9,4.1 Hz,H-18),1.12(3H,s,H-27),0.95(3H,s,H-23),0.90(3H,s,H-25),0.89(3H,s,H-30),0.87(3H,s,H-29),0.77(3H,s,H-24),0.74(3H,s,H-26);13C NMR(150 MHz,CDCl3)δ:39.1(C-1),27.2(C-2),79.2(C-3),39.2(C-4),55.9(C-5),18.9(C-6),33.1(C-7),39.8(C-8),48.2(C-9),37.5(C-10),23.8(C-11),122.9(C-12),144.4(C-13),42.3(C-14),28.2(C-15),23.9(C-16),46.9(C-17),41.9(C-18),46.5(C-19),31.1(C-20),34.4(C-21),33.3(C-22),28.4(C-23),15.9(C-24),15.6(C-25),17.2(C-26),26.2(C-27),181.3(C-28),33.4(C-29),23.5(C-30)。以上数据与文献[12]报道基本一致,故鉴定化合物5为齐墩果酸。
化合物6白色粉末;ESI-MS:m/z485[M-H+HCOOH]-,分子式为C39H68O;1H NMR(600 MHz,CDCl3)δ:5.15(1H,t,J= 3.2 Hz,H-12),3.67(2H,t,J= 4.9 Hz,H-1′),3.20(1H,dd,J= 11.9,4.7 Hz,H-3),1.45~1.23(14H,m,H-2′~H-8′),1.09(3H,s,H-27),1.03(3H,s,H-28),1.02(3H,s,H-23),0.98(3H,s,H-25),0.95(3H,s,H-30),0.90(3H,s,H-29),0.87(3H,t,J= 4.9 Hz,H-9′),0.82(3H,s,H-24),0.81(3H,s,H-26);13C NMR(150 MHz,CDCl3)δ:38.9(C-1),23.5(C-2),79.2(C-3),37.1(C-4),55.2(C-5),18.5(C-6),32.1(C-7),39.8(C-8),41.5(C-9),33.9(C-10),17.6(C-11),122.5(C-12),142.3(C-13),40.1(C-14),29.8(C-15),27.4(C-16),59.1(C-17),47.8(C-18),39.7(C-19),41.7(C-20),31.4(C-21),42.2(C-22),28.2(C-23),16.9(C-24),15.8(C-25),15.7(C-26),23.4(C-27),22.8(C-28),14.3(C-29),21.5(C-30),63.2(C-1′),26.7(C-2′),25.9(C-3′),28.3(C-4′),28.9(C-5′),29.8(C-6′),32.9(C-7′),23.5(C-8′),15.8(C-9′)。以上数据与文献[16]报道基本一致,故鉴定化合物6为β-amyrin-n-nonyl ether。
化合物7无色针状结晶(甲醇);mp.235~237 ℃,ESI-MS:m/z198[M-H]-,分子式为C10H14O4;1H NMR(600 MHz,CD3OD)δ:6.78(1H,d,J= 1.8 Hz,H-2),6.72(1H,d,J= 7.8 Hz,H-5),6.65(1H,dd,J= 7.8,1.8 Hz,H-6),3.83(3H,s,H-3-OCH3),3.80(1H,m,H-8),3.51(1H,dd,J= 10.8,4.2 Hz,H-9a),3.43(1H,dd,J= 10.8,6.6 Hz,H-9b),2.71(1H,dd,J= 13.8,6.0 Hz,H-7a),2.61(1H,dd,J= 13.8,7.2 Hz,H-7b);13C NMR(150 MHz,CD3OD)δ:130.9(C-1),113.6(C-2),148.2(C-3),145.3(C-4),115.7(C-5),122.5(C-6),40.1(C-7),74.2(C-8),66.2(C-9),56.1(3-OCH3)。以上数据与文献[17]报道基本一致,故鉴定化合物7为vanillyl glycol。
化合物8白色粉末;ESI-MS:m/z437[M+Na]+,分子式为C29H50O;1H NMR(600 MHz,CDCl3)δ:5.38(1H,d,J= 5.1 Hz,H-6),3.73(1H,m,H-7),3.55(1H,m,H-3),1.13(3H,d,J= 6.6 Hz,H-21),1.03(3H,s,H-19),0.95(3H,d,J= 7.2 Hz,H-29),0.87(3H,d,J= 7.1 Hz,H-26),0.86(3H,d,J= 6.6 Hz,H-27),0.82(3H,s,H-18);13C NMR(150 MHz,CDCl3)δ:39.9(C-1),32.1(C-2),71.9(C-3),42.4(C-4),140.9(C-5),121.9(C-6),31.8(C-7),29.3(C-8),50.3(C-9),37.4(C-10),21.2(C-11),40.6(C-12),45.9(C-13),56.2(C-14),24.5(C-15),28.4(C-16),56.9(C-17),12.0(C-18),19.9(C-19),36.7(C-20),19.2(C-21),34.1(C-22),26.2(C-23),40.7(C-24),29.1(C-25),19.6(C-26),18.9(C-27),23.2(C-28),12.1(C-29)。以上数据与文献[18]报道基本一致,故鉴定化合物8为β-谷甾醇。
化合物9白色粉末;ESI-MS:m/z599[M+Na]+,分子式为C35H60O6;1H NMR(600 MHz,CD3OD)δ:5.33(1H,d,J= 7.8 Hz,H-6),5.07(1H,m,H-1′),4.37(1H,d,J= 7.8 Hz,H-3),3.82~3.80(2H,m,H-6′),1.18(3H,d,J= 6.5 Hz,H-21),1.03(3H,s,H-19),0.95(3H,s,H-29),0.91(3H,d,J= 7.1 Hz,H-26),0.87(3H,d,J= 6.8 Hz,H-27),0.81(3H,s,H-18);13C NMR(150 MHz,CD3OD)δ:38.5(C-1),29.5(C-2),78.9(C-3),42.2(C-4),140.3(C-5),121.9(C-6),33.8(C-7),31.8(C-8),50.2(C-9),37.2(C-10),20.9(C-11),39.7(C-12),45.8(C-13),56.7(C-14),24.2(C-15),28.1(C-16),55.9(C-17),11.6(C-18),18.7(C-19),36.6(C-20),18.5(C-21),36.1(C-22),25.9(C-23),49.3(C-24),29.1(C-25),19.1(C-26),19.5(C-27),22.9(C-28),11.6(C-29),101.08(C-1′),73.6(C-2′),76.5(C-3′),70.2(C-4′),76.1(C-5′),61.6(C-6′)。以上数据[19]与文献报道基本一致,故鉴定化合物9为β-胡萝卜苷。
化合物10白色粉末;ESI-MS:m/z601[M-H]-,分子式为C37H62O6;1H NMR(600 MHz,CD3OD)δ:5.33(1H,d,J= 5.4 Hz,H-6),4.37(1H,d,J= 7.8 Hz,H-1′),3.81~3.80(2H,m,H-6′),1.22(3H,s,H-31),0.99(3H,s,H-18),0.89(3H,d,J= 6.0 Hz,H-24),0.85(3H,d,J= 7.2 Hz,H-28),0.80(3H,t,J= 6.9 Hz,H-30),0.65(3H,s,H-19);13C NMR(150 MHz,CD3OD)δ:37.6(C-1),29.4(C-2),79.4(C-3),42.7(C-4),140.7(C-5),122.4(C-6),32.3(C-7),30.0(C-8),50.6(C-9),34.3(C-10),21.4(C-11),46.2(C-12),40.1(C-13),57.1(C-14),24.6(C-15),56.4(C-16),49.6(C-17),19.6(C-18),12.1(C-19),26.3(C-20),28.6(C-21),23.4(C-22),37.1(C-23),12.1(C-24),20.0(C-25),36.5(C-26),39.0(C-27),19.2(C-28),29.9(C-29),18.9(C-30),32.2(C-31),101.5(C-1′),73.9(C-2′),76.9(C-3′),70.6(C-4′),76.3(C-5′),62.1(C-6′)。以上数据与文献[20]报道基本一致,故鉴定化合物10为anemarrhenoside B。
化合物11白色无定型粉末;ESI-MS:m/z365[M-H]-,分子式为C26H54;1H NMR(600 MHz,CDCl3)δ:1.27~1.29(44H,m,H-3~H-24),0.86(6H,m,H-1,H-26);13C NMR(150 MHz,CDCl3)δ:32.3(C-1),30.1(C-2),30.0~29.9(C-3~C-23),29.7(C-24),23.1(C-25),14.3(C-26)。以上数据与文献[21]报道基本一致,故鉴定化合物11为正二十六烷。
化合物12白色无定型粉末;ESI-MS:m/z434[M-H2O]+,406[M-H2O-C2H4]+,392[M-H2O-C2H4-C2H4]+,分子式为C31H64O;1H NMR(600 MHz,CDCl3)δ:3.56(2H,t,J= 6.6 Hz,H-1),1.55(2H,m,H-2),1.27~1.31(56H,m,H-3~H-30),0.88(3H,t,J= 7.2 Hz,H-31);13C NMR(150MHz,CDCl3)δ:61.8(C-1),32.1(C-2),31.5(C-3),29.2~28.9(C-4~C-28),25.4(C-29),22.2(C-30),13.3(C-31)。以上数据与文献[22]报道基本一致,故鉴定化合物12为正三十一烷醇。
化合物13白色粉末;ESI-MS:m/z515[M-H]-,分子式为C24H36O12;1H NMR(600 MHz,CD3OD)δ:7.11(1H,d,J= 8.4 Hz,H-3),6.92(1H,dd,J= 9.0,3.0 Hz,H-4),6.91(1H,d,J= 2.4 Hz,H-6),5.34(1H,t,J= 7.2 Hz,H-2′),4.82(1H,d,J= 7.2 Hz,H-1′′),4.80(1H,d,J= 7.2 Hz,H-1′′′),4.07(1H,dd,J= 14.4,7.2 Hz,H-6a′′′),3.90(1H,dd,J= 11.8,1.8 Hz,H-6a′′),3.75(1H,dd,J= 11.8,1.8 Hz,H-6b′′),3.71(1H,dd,J= 13.2,6.9 Hz,H-6b′′′),3.39(2H,m,H-1′),1.76(3H,s,H-5′),1.73(3H,s,H-4′);13C NMR(150 MHz,CD3OD)δ:152.1(C-1),133.7(C-2),117.5(C-3),115.7(C-4),154.4(C-5),119.0(C-6),29.2(C-1′),123.7(C-2′),133.5(C-3′),25.9(C-4′),17.9(C-5′),103.4(C-1′′),75.0(C-2′′),78.2(C-3′′),71.3(C-4′′),77.9(C-5′′),62.5(C-6′′),103.0(C-1′′′),74.8(C-2′′′),77.9 (C-3′′′),71.2(C-4′′′),78.0(C-5′′′)和62.4(C-6′′′)。以上数据与文献[23]报道基本一致,故鉴定化合物13为1,5-bis-β-D-glucopyranosyloxy-2-(3′,3′-dimethylallyl)benzene。
化合物14淡黄色针晶(三氯甲烷);mp.51~53℃;ESI-MS:m/z205[M-H]-,分子式为C14H22O;1H NMR(600 MHz,CDCl3)δ:7.35(1H,d,J= 2.5 Hz,H-3),7.12(1H,dd,J= 8.2,2.3 Hz,H-5),6.62(1H,d,J= 8.2 Hz,H-6),1.47(9H,s,H-12~H-14),1.34(9H,s,H-8~H-10);13C NMR(150 MHz,CDCl3)δ:151.9(C-1),135.4(C-2),123.7(C-3),143.1(C-4),124.2(C-5),116.1(C-6),34.9(C-7),31.8(C-8~C-10),34.4(C-11),29.8(C-12~C-14)。以上数据与文献[24]报道基本一致,故鉴定化合物14为2,4-二叔丁基苯酚。
化合物15无色针晶(甲醇);mp.108~110 ℃;ESI-MS:m/z393[M-H]-,分子式为C28H42O;1H NMR(600 MHz,CDCl3)δ:7.54(2H,d,J= 8.4 Hz,H-6,H-6′),7.36(2H,d,J= 2.3 Hz,H-3,H-3′),7.13(2H,dd,J=8.4,2.4 Hz,H-5,H-5′),1.33(18H,s,H-8~H-10,H-8′~H-10′),1.28(18H,s,H-12~H-14,H-12′~H-14′);13C NMR(150 MHz,CDCl3)δ:147.2(C-1,C-1′),147.8(C-2′),147.7(C-2),124.6(C-3,C-3′),138.5(C-4),138.6(C-4′),124.1(C-5,C-5′),119.2(C-6),119.2(C-6′),35.2(C-7,C-7′),31.6(C-8~C-10,C-8′~C-10′),34.7(C-11,C-11′),30.3(C-12~C-14,C-12′~C-14′)。以上数据与文献[25]报道基本一致,故鉴定化合物15为2,2′-oxybis(1,4-di-tert-butylbenzene)。
化合物1~15结构见图1。
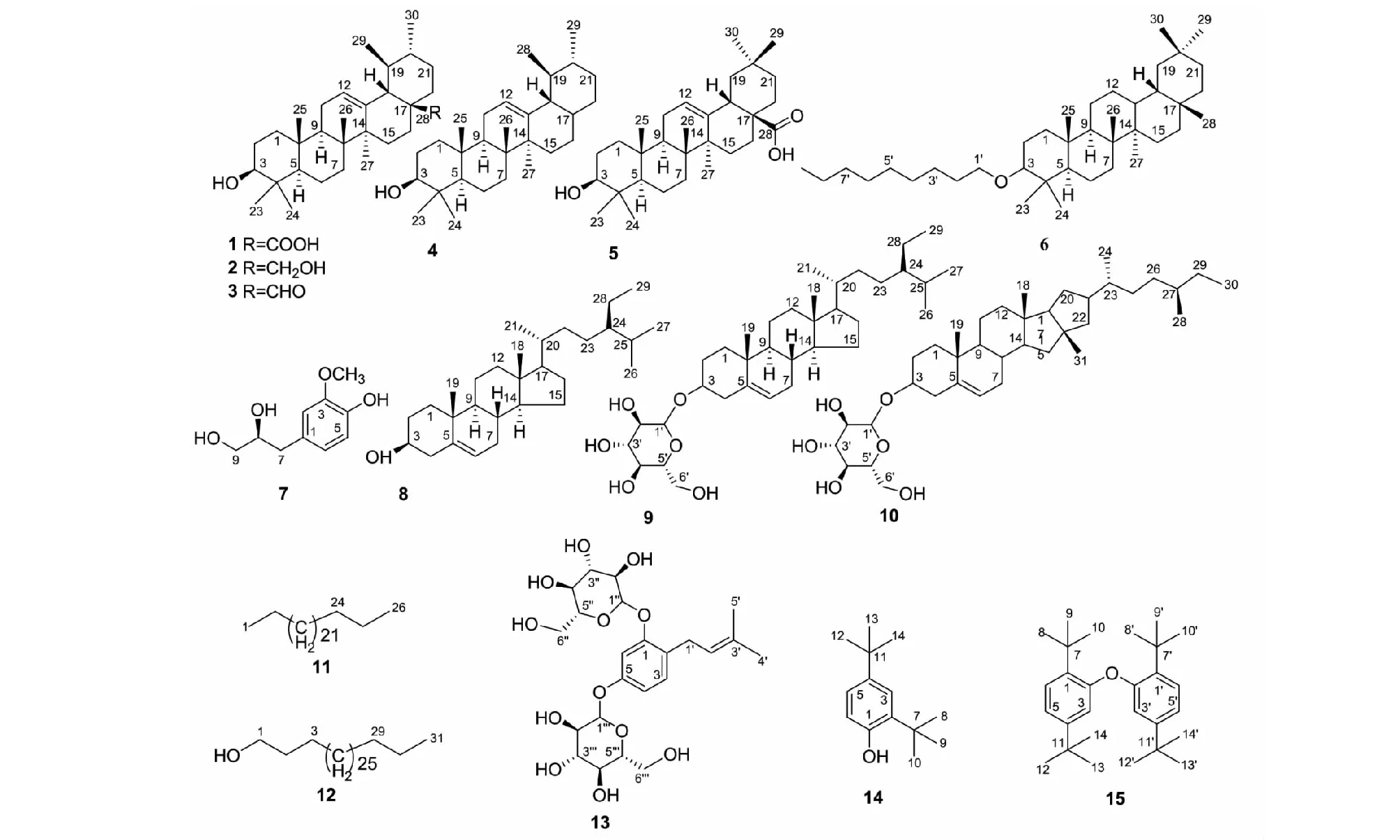
图1 化合物1~15的化学结构
2.2 化合物的抗炎活性筛选结果
2.2.1 对细胞活力的影响
MTT法测定15个化合物对RAW 264.7细胞毒性发现,与对照组(control group,CON)相比,各单体化合物在浓度50 μmol/L时,均未发现明显的细胞毒性,故可选浓度为50 μmol/L进行抗炎活性筛选(见图2)。

图2 不同浓度的化合物1~15对RAW 264.7细胞活力的影响
2.2.2 对LPS诱导RAW 264.7细胞释放的NO影响
体外抗炎活性筛选结果表明,与CON相比,模型组(LPS)释放NO显著增加(P< 0.01)。与模型组相比,化合物1、5、9和DXMS能显著抑制LPS诱导RAW 264.7释放NO量(P< 0.01),其半数抑制浓度IC50分别为26.23±4.67、25.20±1.30、20.86±3.57和10.16±4.37 μmol/L,化合物4、6和10对LPS诱导的RAW 264.7细胞释放的NO具有抑制作用,其余化合物对释放NO抑制作用不明显(见图3、表1)。

表1 化合物1~15对LPS诱导RAW 264.7细胞释放NO的抑制活性
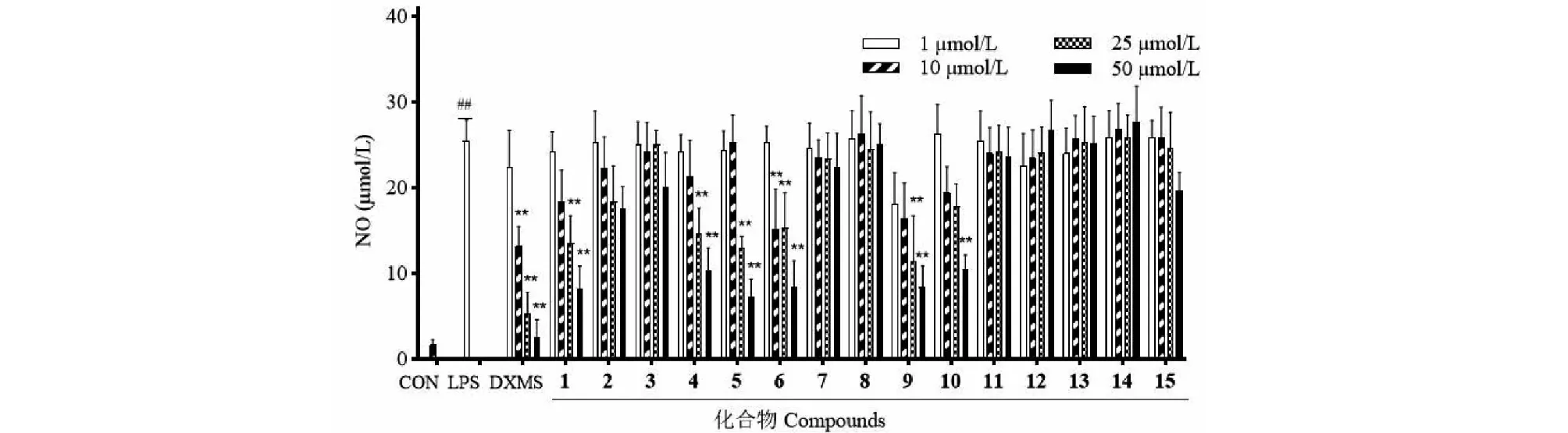
图3 不同浓度的化合物1~15对LPS诱导RAW 264.7细胞释放NO的影响
3 结论
通过对五岭龙胆进行提取分离,共得到15个化合物,包括6个三萜类、1个苯丙素、3个甾醇类及5个其他类化合物,其中7、14和15为首次从龙胆属植物中分离得到,其余化合物为首次从五岭龙胆中分离得到。三萜类化合物为龙胆属植物的重要组成成分,以五环三萜的齐墩果烷型和乌苏烷型最常见,具有抗炎、抗菌、免疫调节及保肝等作用[8,26-29],为龙胆属植物的药效物质。通过抗炎活性筛选发现,五岭龙胆中分离得到的齐墩果酸和熊果酸具有一定的抗炎活性,为五岭龙胆抗炎活性的药效物质。本论文分离的化合物主要来源于五岭龙胆乙酸乙酯萃取部位,龙胆属中环烯醚萜类和黄酮类成分主要为其苷类成分,如龙胆苦苷、獐牙菜苦苷和木犀草素等成分,苷类成分极性较大,故推测五岭龙胆环烯醚萜类和黄酮类成分存在于正丁醇萃取部位,后续将继续相关研究。综上,本研究丰富了五岭龙胆化学成分和药理活性研究,阐明了其发挥抗炎活性的物质基础,为其进一步的研究开发提供参考依据。
