含1,3,4-噻二唑结构的酰胺类衍生物的合成及生物活性研究
2023-10-31苏子钦高田田梁馨文胡继亮张建龙吴玉宇刘玮炜
苏子钦, 高田田, 邱 敏, 梁馨文, 胡继亮, 刘 强, 张建龙, 吴玉宇, 陈 超, 刘玮炜
(江苏海洋大学 药学院,江苏省海洋生物资源与环境重点实验室,江苏省海洋生物产业技术协同创新中心,江苏海洋生物技术重点实验室,江苏省海洋药物活性分子筛选重点实验室,江苏 连云港 222005)
近年来,我国海水养殖种类和养殖模式越来越多样化,养殖技术逐渐成熟,养殖面积不断扩大,但随着集约化养殖程度的不断提高,养殖水域的污染也逐渐加重,致病性弧菌所引起的病害已被认为是海水动物养殖的“灾祸之源”[1-5],主要包括副溶血弧菌(Vibrioparahaemolyticus)、哈维氏弧菌(Vibrioharveyi)、霍乱弧菌(Vibriocholerae)和创伤弧菌(Vibriovulnificus)等,均为海洋环境中最常见的细菌类群。这些菌群广泛分布于近岸、河口海区的海水和水产养殖环境之中,不仅会引起水产动物发病造成巨大经济损失,某些弧菌更是会造成人或其它动物发病[6-8]。
目前,水产动物弧菌病的药物防治主要包括青霉素、硫酸链霉素、诺氟沙星和新诺明等,但长期使用会出现耐药性菌株[9-10]。因此,寻找新的先导化合物或化合物骨架修饰、简化并开发出新型水产抗菌药是当前水产病害防控研究的热点之一。1,3,4-噻二唑是一类含氮硫的五元杂环化合物,具有抗菌、抗氧化、抗病毒和调节植物生长等多种生物活性[11-21]。国内外公司基于噻二唑结构,陆续研发出了多种含1,3,4-噻二唑结构的药物,如除草剂氟噻草胺、丁噻咪草酮和噻黄隆等,杀菌剂噻枯唑,抗菌药头孢唑啉和头孢卡奈等[22-25],该类化合物在化学和生物学研究领域一直具有广泛的应用。
XIAO等[26]设计并合成了2-氨基-5-(2,4-二氯苯氧基)甲基-1,3,4-噻二唑酰胺类化合物(图1),初步活性测试结果发现,大部分化合物具有一定的抑菌活性,其中对麦类黑变病菌的抑制率达到了70%以上,对炭疽菌抑制率达到了60%以上。王德志等[27]基于1,3,4-噻二唑类化合物的抑菌活性,以芳香醛和氨基硫脲为原料,合成了6个2-氨基-5-芳基-1,3,4-噻二唑类化合物。抑菌结果表明,所有目标化合物均对小麦赤霉病菌和番茄灰霉病菌具有一定的抑菌活性。通过分析构效关系得出,该类化合物中对氟苯基取代的化合物抑菌活性优于其它取代基化合物,对应化合物对小麦赤霉病菌和番茄灰霉病菌的半数有效浓度(EC50)值分别为23.17 μg·mL-1和20.22 μg·mL-1(图2)。袁海燕等[28]以硫代氨基脲、甲酸为原料,通过脱水环化、Knoevenagle缩合等多步反应,合成一类具有1,3,4-噻二唑基团的酰胺类化合物。通过生长速率法进行抑菌活性测试,研究结果表明,部分化合物在50 mg·L-1浓度下对稻瘟病菌和番茄早疫病菌均具有良好的抑制活性,且抑菌率达到了80%以上(图3)。万金林等[29]以5-氨基-1,3,4-噻二唑-2-硫醇为起始原料,设计合成了一系列从未报道的含1,3,4-噻二唑结构的查尔酮缩氨基脲类化合物。实验研究发现,该类化合物对水稻白叶枯病菌、烟草青枯病菌和柑橘溃疡病菌均具有较好的抑制活性,部分化合物在100 mg·L-1浓度下对以上3种植物病菌的抑制率均达到100%(图4)。 PATTANAYAK等[30]基于1,3,4-噻二唑结构的活性,设计并合成出2-氨基-5-磺酰基-1,3,4-噻二唑类衍生物,经初步活性测试结果表明,该类化合物具有良好抗焦虑、抗抑郁和抗惊厥活性(图5)。薛蒙伟等[31]以二硫化碳和氨基硫脲为原料,设计并合成一系列2-氨基-5-巯基-1,3,4-噻二唑席夫碱类化合物,初步活性研究发现,部分化合物对番茄灰霉病菌、油菜菌核病菌和大豆灰斑病菌均表现出高于85%的抑制率(图6)。目前,新型杂环酰胺类化合物的合成与相关药物研发逐渐成为医药领域的热点。基于以上分析,本研究根据活性子叠加以及生物等排取代的原理,通过化学合成手段,将酰胺键引入到具有良好抑菌活性的1,3,4-噻二唑类化合物中,设计合成了6个含1,3,4-噻二唑结构的酰胺类衍生物(图7)。其结构经IR、1H NMR以及HR-MS(ESI)确证,并用牛津杯法初步测试了化合物对霍乱弧菌及哈维氏弧菌的抑制活性。

图1 2-氨基-5-(2,4-二氯苯氧基)甲基-1,3,4-噻二唑酰胺类化合物的结构
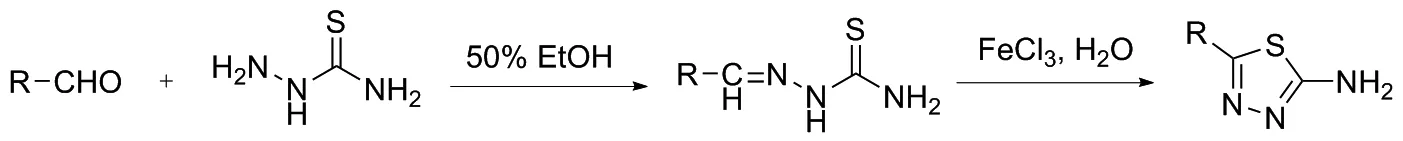
图2 2-氨基-5-芳基-1,3,4-噻二唑类化合物的合成路线

图3 含1,3,4-噻二唑结构的酰胺类衍生物的合成路线

图4 含1,3,4-噻二唑结构的查尔酮缩氨基脲类化合物的合成路线
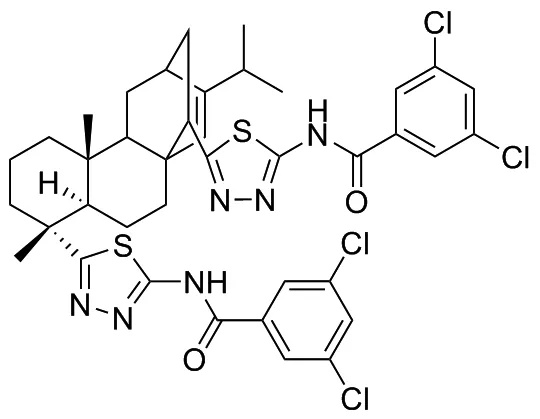
图5 2-氨基-5-磺酰基-1,3,4-噻二唑类衍生物的结构
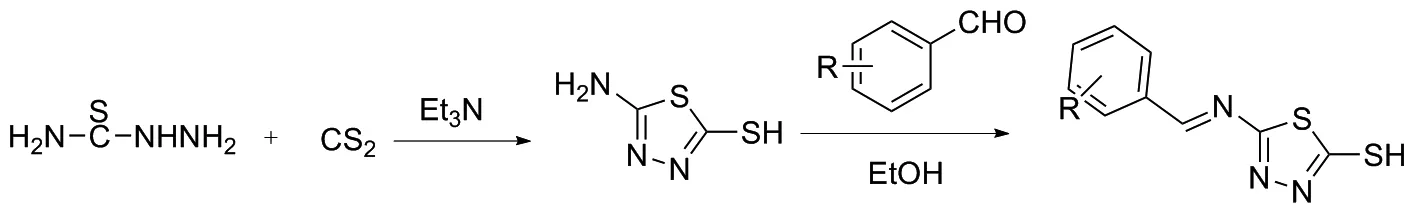
图6 2-氨基-5-磺酰基-1,3,4-噻二唑类化合物的合成路线
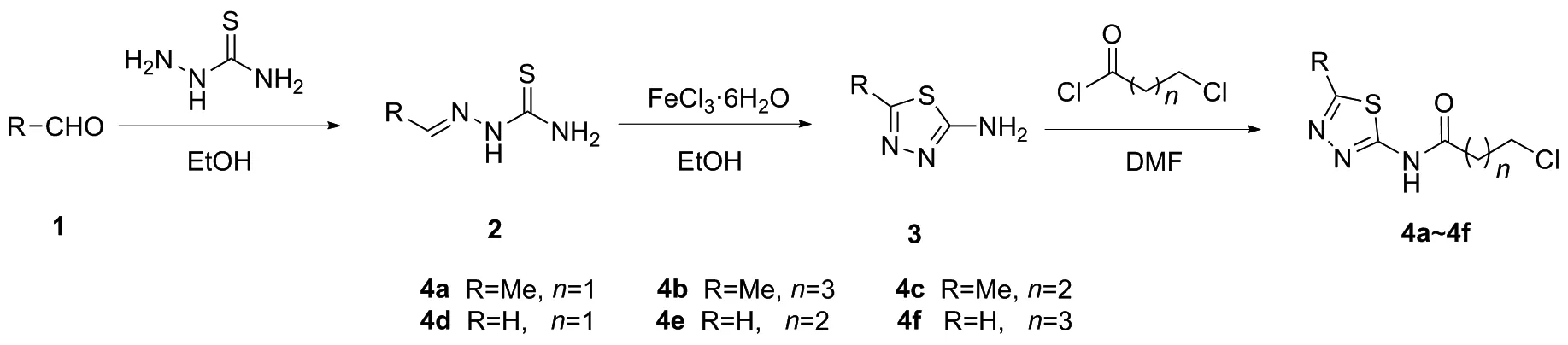
图7 含1,3,4-噻二唑结构的酰胺类衍生物的合成路线
1 实验部分
1.1 仪器与试剂
X-4B型数字显微熔点仪;WFH-203型三用紫外分析仪;AVANCE型核磁共振氢谱仪(DMSO-d6为溶剂,TMS为内标);Cary630型傅里叶红外光谱仪(KBr压片);Agilent 6230型液质联用仪;SW-CJ-1D型单人净化工作台。
酰氯类化合物(98%,上海易恩化学技术有限公司);六水合三氯化铁(99%,上海阿拉丁试剂有限公司);硫酸链霉素(98%,上海麦克林生化科技有限公司);三乙胺(化学纯,上海阿拉丁试剂有限公司),其余试剂均为分析纯。
1.2 化合物的合成
(1) 2-取代-氨基硫脲类化合物(2)的合成
依次称取硫代氨基脲(11 mmol)、取代醛类化合物1(10 mmol)于50 mL的圆底烧瓶中,加入20 mL的无水乙醇溶解。80 ℃油浴搅拌3 h, TLC检测反应至结束,冷却至室温,大量固体析出,静置30 min,抽滤,用蒸馏水洗涤滤饼,得粗品,并用无水乙醇重结晶,得纯品化合物2。
(2) 5-取代-1,3,4-噻二唑-2-胺类化合物(3)的合成
于50 mL圆底烧瓶中依次加入化合物2(6 mmol)、六水合三氯化铁(12 mmol)及20 mL无水乙醇,80 ℃加热回流8 h, TLC监测反应至结束,冷却至室温,倒入装有40 mL蒸馏水的烧杯中,加入5%(质量分数)的氢氧化钠水溶液,调节pH至8,用二氯甲烷(3×30 mL)萃取,取有机相,旋蒸除溶剂,得粗品,无水乙醇重结晶,得纯品化合物3。
(3) 氯-N-(1,3,4-噻二唑-2-取代)酰胺类化合物(4a~4f)的合成
称取化合物3(6 mmol)、酰氯类化合物(7.2 mmol)于50 mL圆底烧瓶中,加入15 mLN,N-二甲基甲酰胺(DMF)溶解,冰水浴下搅拌,加入3滴三乙胺至反应液中,撤去冰水浴,继续搅拌2 h, TLC监测反应至结束。向烧瓶中加入蒸馏水15 mL,有大量固体析出,静置30 min,抽滤得滤饼。用二氯甲烷和甲醇重结晶,得纯品目标化合物4。
2-氯-N-(5-甲基-1,3,4-噻二唑-2-基)乙酰胺(4a):白色固体,收率85.0%, m.p.239~240 ℃; IR(KBr),ν: 3417, 1698, 1596, 1415, 1385, 1066, 840, 774, 613 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.77(s, 1H, NH), 4.43(s, 2H, CH2), 2.63(s, 3H, CH3); HR-MS(ESI)m/z: calcd for C5H7ClN3OS+{[M+H]+}191.9993, found 191.9969。
4-氯-N-(5-甲基-1,3,4-噻二唑-2-基)丁酰胺(4b):白色固体,收率87.0%, m.p.210~212 ℃; IR(KBr)ν: 3416, 1687, 1598, 1411, 1366, 848, 775, 678, 668 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.42(s, 1H, NH), 3.68(t,J=6.5 Hz, 2H, CH2), 2.63(d,J=7.3 Hz, 2H, CH2), 2.60(d,J=3.4 Hz, 3H, CH3), 2.08~2.01(m, 2H, CH2); HR-MS(ESI)m/z: calcd for C7H11ClN3OS+{[M+H]+}220.0306, found 220.0288。
3-氯-N-(5-甲基-1,3,4-噻二唑-2-基)丙酰胺(4c):浅黄色固体,收率83.0%, m.p.206~208 ℃; IR(KBr)ν: 3447, 1688, 1594, 1418, 1365, 848, 777, 681, 648 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.42(s, 1H, NH), 3.68(t,J=6.5 Hz, 2H, CH2), 2.63(d,J=7.3 Hz, 2H, CH2), 2.60(d,J=3.4 Hz, 3H, CH3), 2.08~2.01(m, 2H, CH2); HR-MS(ESI)m/z: calcd for C6H9ClN3OS+{[M+H]+}206.0150, found 206.0123。
2-氯-N-(1,3,4-噻二唑-2-基)乙酰胺(4d):白色固体,收率84.0%, m.p.194~196 ℃; IR(KBr)ν: 3414, 3058, 1711, 1597, 1400, 1364, 820, 776, 715, 603 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.95(s, 1H, NH), 9.23(s, 1H, thiadiazole), 4.46(s, 2H, CH2); HR-MS(ESI)m/z: calcd for C4H3ClN3OS-{[M-H]-}175.9681, found 175.9694。
3-氯-N-(1,3,4-噻二唑-2-基)丙酰胺(4e):棕色固体,收率81.0%, m.p.177~178 ℃; IR(KBr)ν: 3443, 1600, 1423, 1384, 1137, 1067, 953, 825, 778, 619 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.71(s, 1H, NH), 9.18(s, 1H, thiadiazole), 3.90(t,J=6.2 Hz, 2H, CH2), 3.01(t,J=6.3 Hz, 2H, CH2); HR-MS(ESI)m/z: calcd for C5H5ClN3OS-{[M-H]-}189.9836, found 189.9840。
4-氯-N-(1,3,4-噻二唑-2-基)丁酰胺(4f):白色固体,收率82.0%, m.p.174~175 ℃; IR(KBr)ν: 3417, 1687, 1597, 1444, 1385, 1138, 878, 797, 749, 699 cm-1;1H NMR(500 MHz, DMSO-d6)δ: 12.60(s, 1H, NH), 9.15(s, 1H, thiadiazole), 3.69(t,J=6.5 Hz, 2H, CH2), 2.65(t,J=7.3 Hz, 2H, CH2), 2.06(p,J=6.8 Hz, 2H, CH2); HR-MS(ESI)m/z: calcd for C6H7ClN3OS-{[M-H]-}203.9992, found 204.0000。
1.3 待测定药液的配制
待测样品均用乙酸乙酯溶解,配制成浓度为2 mg·mL-1的1 mL样品溶液,并以溶剂乙酸乙酯溶液1 mL作对照,阳性对照药硫酸链霉素用蒸馏水配置成1 mg·mL-1溶液。牛津杯外径7.80 mm,对于抑菌圈直径大于14 mm的化合物,用相应的溶剂按二倍稀释法进行稀释,进一步测定其最小抑菌浓度(MIC)。
1.4 生物活性测定
预热固体MH肉汤培养基,沸腾后取出。温度稍低后,向每个平板中倒入约30 mL MH肉汤培养基,室温静置30 min,待其凝固。吸取活化后的菌悬液200 μL至固体培养基上,在酒精灯附近用涂布棒缓慢将菌液抹匀。静置约10 min后,用镊子夹取牛津杯垂直放置于平板规划的位置,取200 μL待测样品溶液于牛津杯孔径中,每个样品需做3次平行样,在32 ℃恒温培养箱中培养20 h后测定抑菌圈直径。
2 结果与讨论
表1研究结果表明,化合物4b对霍乱弧菌的抑制效果最好,抑菌圈直径为11.79±0.15 mm,化合物4a和4d对哈维氏弧菌的抑菌效果最好,最小抑菌浓度均达到了0.250 mg·mL-1。分析构效关系表明,杂环噻二唑酰胺类衍生物的抗菌活性受连接酰胺键的脂肪链长短的影响。鉴于此,今后的研究工作可以选择噻二唑基团的5位进行结构修饰。

表1 目标化合物体外抑制哈维氏弧菌和霍乱弧菌的活性测试结果
3 结论
本文以醛类化合物为原料,与硫代氨基脲生成希夫碱类化合物,成环后生成1,3,4-噻二唑类衍生物,并与不同链长的酰氯反应,合成6个含1,3,4-噻二唑结构的酰胺类衍生物。抑菌活性结果表明:部分目标化合物对哈维氏弧菌和霍乱弧菌表现出一定的抑制活性,其中化合物4b对霍乱弧菌的抑制效果最好,抑菌圈直径为11.79±0.15 mm,化合物4a和4c对哈维氏弧菌的抑制效果最好,抑菌圈直径分别为17.53±0.08 mm、 19.37±0.56 mm,且MIC均为0.250 mg·mL-1。构效关系表明:酰胺键的脂肪链长短对化合物的弧菌抑制活性影响较大,脂肪链越短活性越好。化合物4a、4b和4d可作为先导化合物进一步研究,为后续水产抗菌药物的研发提供了理论基础。
