非小细胞肺癌肝转移患者预后影响因素分析
2023-10-25管毛敏丁秋平王森凤
管毛敏 丁秋平 王森凤
据2020 年中国癌症统计报告显示,肺癌发病率仅低于乳腺癌,居第2 位,死亡人数达180 万,居所有癌症首位[1]。非小细胞肺癌(NSCLC)为肺癌最常见类型,在我国NSCLC 发病率与病死率均位居首位,5 年生存率<20%[2]。临床发现,导致NSCLC 高病死率主要原因局部复发与远处转移[3]。肝转移为NSCLC 远处转移类型之一,约20% NSCLC 患者随病情进展可产生肝转移[4]。临床研究报道,发生肝转移肺癌患者病情进展快,生存预后差,中位生存时间仅3~6 个月[5]。尽管如此,与骨转移、脑转移相比,临床对肺癌肝转移的重视程度较低。但目前国内尚未见关于NSCLC 肝转移患者预后影响因素的研究报道。本研究拟分析NSCLC 肝转移患者预后的有关影响因素,并构建风险预测模型,以期为临床个体化治疗方案制定、预后判断提供参考。
1 资料与方法
1.1 临床资料 回顾性分析2016 年1 月至2022 年10月本院106 例NSCLC 肝转移患者的临床资料。(1)纳入标准:①符合NSCLC 诊断标准[6],且经病理学或者细胞学检查证实;②经MRI、CT 检查证实出现肝转移;③年龄≥18 岁;④采取化疗或化疗联合免疫、靶向治疗;⑤有客观可测定病灶;⑥随访资料、临床资料完整。(2)排除标准:①合并其他原发肿瘤;②多脏器功能衰竭;③合并凝血功能障碍、严重精神疾病。
1.2 方法 收集患者性别、年龄、体质量指数(BMI)、吸烟史、高血压、糖尿病、肺癌类型、病理分型、Karnofsky功能状态(KPS)评分[7]、肝转移灶数量、合并其他部位转移、原发病灶控制情况、治疗方式等临床资料。以电话、住院/门诊复查等形式完成12 个月的随访时间,研究终点为总生存期(由确诊NSCLC 肝转移到死亡时间)。依据患者总生存期评价预后,以1 年生存情况为分界点,将患者分为死亡组、生存组。
1.3 统计学方法 采用SPSS21.0 统计软件。符合正态分布计量资料以(±s)表示,组间比较用t检验;计数资料以n(%)表示,组间比较用χ2检验;患者预后的独立危险因素采用Logistic 回归分析;受试者操作特征(ROC)曲线分析各独立危险因素及风险预测模型对预后的预测效能;采用交叉验证法检验风险预测模型的预测价值;生存曲线绘制应用Kaplan-Meier 曲线。P<0.05 为差异有统计学意义。
2 结果
2.1 NSCLC 肝转移患者生存情况 本组106 例NSCLC肝转移患者1 年死亡77 例(死亡组),平均死亡时间为6 个月;生存29 例(生存组)。见图1。
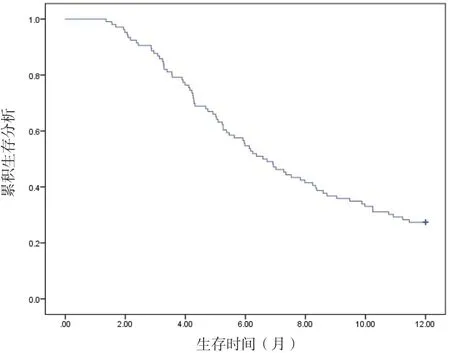
图1 NSCLC肝转移患者生存曲线
2.2 两组临床资料 两组患者年龄、KPS 评分、肝转移灶数量、合并其他部位转移、原发病灶控制情况、治疗方式比较,差异有统计学意义(P<0.05)。见表1。
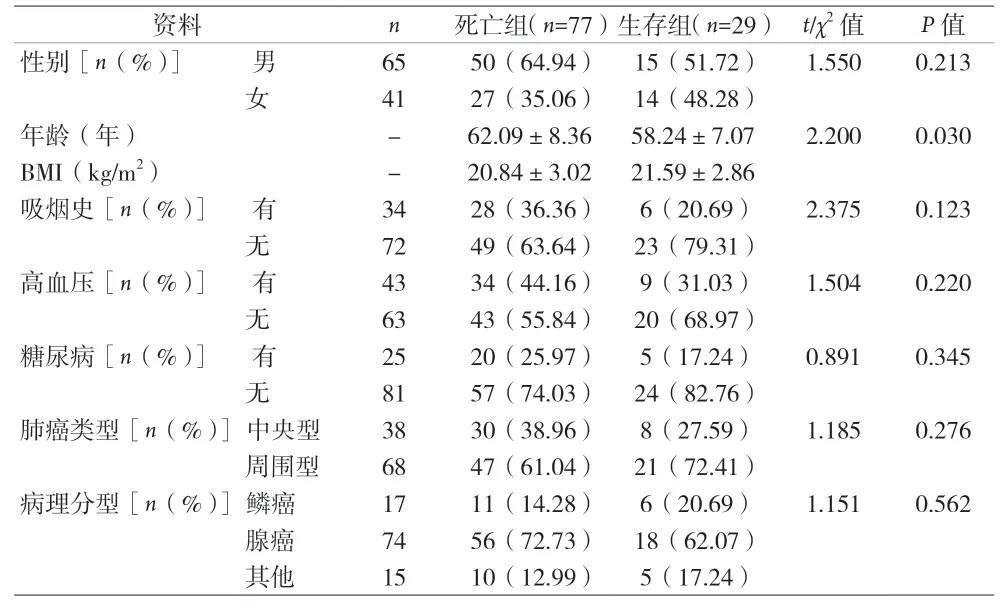
表1 两组临床资料比较
2.3 NSCLC肝转移患者预后的影响因素 Logistic回归分析显示,年龄、KPS 评分、合并其他部位转移、原发病灶控制情况、治疗方式均为患者预后死亡的独立危险因素(P<0.05),肝转移灶数量不是患者预后死亡的独立危险因素(P>0.05),见表2。
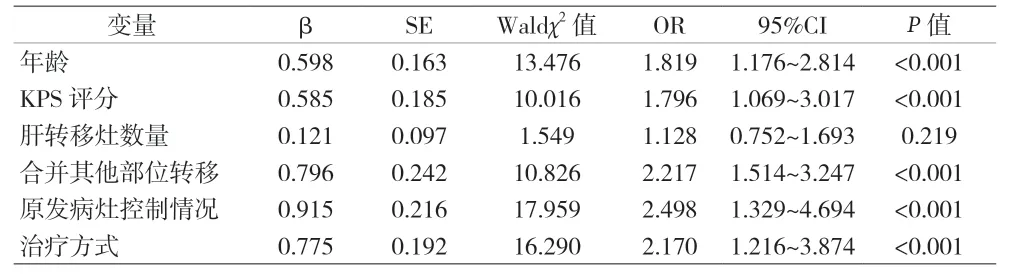
表2 NSCLC肝转移患者预后的影响因素
2.4 各独立危险因素对NSCLC 肝转移患者预后的预测效能 以死亡组设置为阳性样本,生存组设置为阴性样本,ROC 曲线分析显示,年龄、KPS 评分、合并其他部位转移、原发病灶控制情况、治疗方式均对NSCLC肝转移患者预后死亡具有一定预测意义,AUC 分别为0.679、0.635、0.626、0.646、0.624。见表3 和图2。
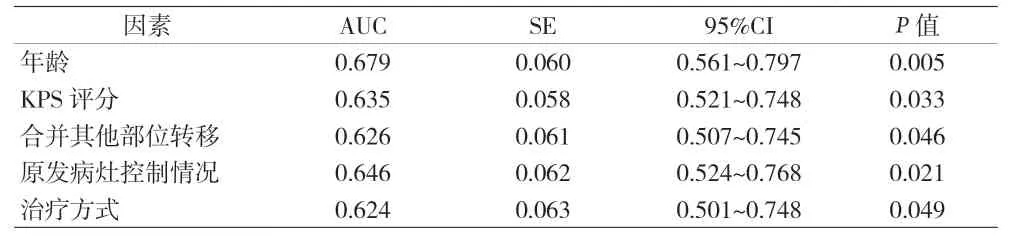
表3 各独立危险因素对NSCLC肝转移患者预后的预测效能
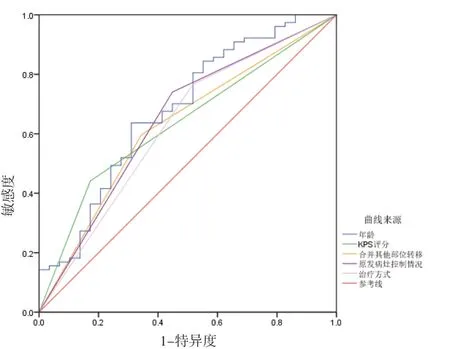
图2 各独立危险因素对NSCLC肝转移患者预后预测的ROC曲线
2.5 风险预测模型对预后的预测效能 依据独立危险因素构建风险预测模型,以预测概率值P 为检验变量,预后情况为状态变量。经ROC 曲线分析显示,风险预测模型的AUC 为0.919,标准误差为0.028,95%CI 为0.863~0.975,P<0.001。见图3。
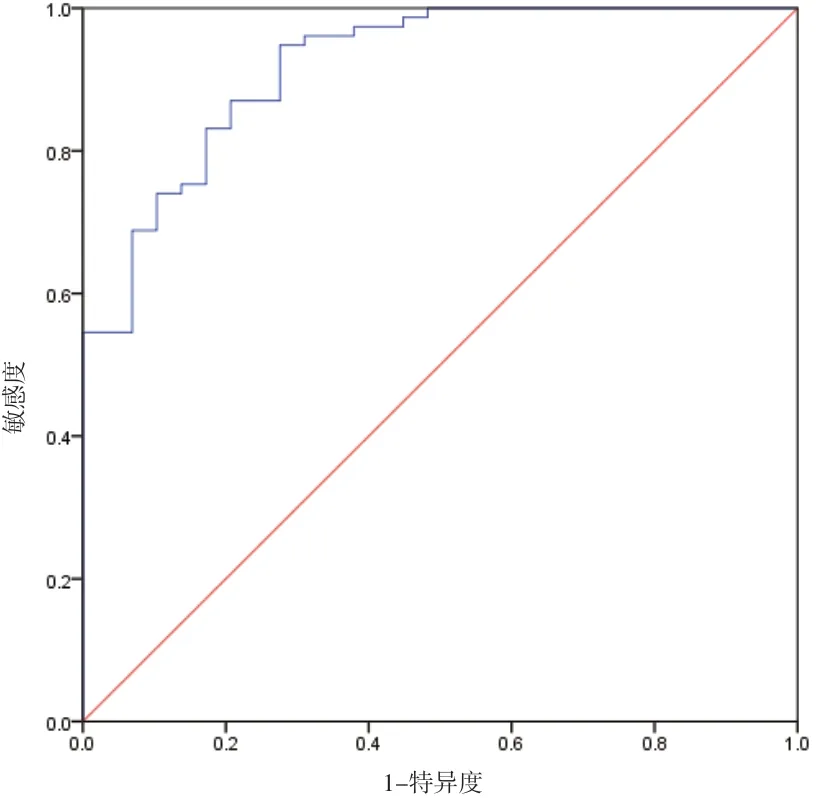
图3 风险预测模型对预后的预测ROC曲线
2.6 风险预测模型的预测价值检验 将预测概率值P为自变量,预后情况为分类变量,应用交叉验证法检验风险预测模型的预测预后分组与实际预后分组一致性。检验显示,风险预测模型分类准确率为88.68%。见表5。

表5 风险预测模型的预测价值检验[n(%)]
3 讨论
NSCLC 肝转移属一种被明显低估远处转移类型,实际上其预后较差,甚至明显差于备受关注的肺癌脑转移患者[8-9]。张国伟等[10]研究报道,伴肝转移晚期NSCLC 患者行纳武利尤单抗治疗后的中位无进展生存时间为3.7 个月,短于无肝转移患者的5.6 个月。SRIDHAR 等[11]研究报道,肝转移是NSCLC 患者总生存期、无进展生存期的独立危险因素,且伴肝转移可导致患者对度伐鲁单抗治疗的客观反应率降低。ASHOUR等[12]、KANAJI 等[13]研究也证实,伴肝转移与晚期肺癌患者不良生存结局有关。本研究显示,本组106 例NSCLC 肝转移患者1 年死亡77 例,死亡率72.64%,平均死亡时间为6 个月,也提示NSCLC 肝转移患者预后较差。
本研究单因素及进一步Logistic 回归分析显示,年龄、KPS 评分、合并其他部位转移、原发病灶控制情况、治疗方式均为患者预后死亡的独立危险因素。年龄越大、KPS 评分越低、合并其他部位转移、原发病灶未控制、治疗方式为单纯化疗患者预后死亡风险大。年龄是影响人体生理功能的关键因素,高龄患者生理功能减退,常合并多种基础疾病,对临床治疗的耐受性降低,易产生不良反应,影响治疗进展与治疗效果,不利于患者预后[14-15]。CAMPOS-BALEA 等[16]通过SEER 数据库中选出46,030 例肺腺癌患者,经统计分析,年龄为患者生存预后不良的独立危险因素。KPS 评分为评价癌症患者病情、日常活动与生活自理程度的重要工具,其分值越高,会影响预后生存期[17]。YANG 等[18]、LIAO等[19]基于SEER 研究均证实,相较于单一脏器转移NSCLC 患者,多器官转移患者有更差的生存率。原发肿瘤病灶控制情况也为影响患者预后的关键因素,分析机制:原发肿瘤得到早期干预可降低远处转移风险,抑制病情进展;有效的控制原发肿瘤病灶也可缓解患者临床症状,改善耐受性,有利于患者预后。马伟锋等[20]通过单中心研究发现,原发病灶未控制是肺腺癌脑膜转移患者预后不良独立危险因素(OR:4.186),侧面提示原发病灶控制不良可能会影响远处转移肺癌患者预后。NSCLC 肝转移患者已处于肝癌晚期,患者多需采取化疗治疗,但近期研究指出,单一采取化疗治疗对NSCLC肝转移患者长期疗效欠佳,可能与肝脏中化疗药物浓度较低有关[21]。而靶向药物、免疫治疗药物在NSCLC 肝转移中的应用效果得到临床证实,联合应用化疗与免疫/靶向药物进行综合治疗可由不同机制控制肿瘤病灶,提高临床疗效,延长患者生存周期[22]。提示在患者可耐受的情况下采取个体化综合治疗可对改善患者预后起到积极意义。肝转移灶数量在单因素分析中差异有统计学意义,而在多因素分析中显示并非患者预后死亡的独立危险因素。推测原因可能与该因素受到其他条件的影响,对患者预后起到更大影响的因素将其排除。本研究结果还显示,年龄、KPS 评分、合并其他部位转移、原发病灶控制情况、治疗方式均对NSCLC 肝转移患者预后死亡具有一定预测意义。也再次证实上述因素与患者预后的密切关系,有望作为预后评估的候选指标。
本研究另依据上述独立危险因素构建风险预测模型,经ROC 曲线显示,该风险预测模型的AUC 为0.919,95%CI 为0.863~0.975,预测效能良好。应用该风险预测模型可早期识别预后不良患者,且具有可靠性高、操作性强的特点,可为临床评价患者预后提供更为可靠的参考依据。本研究应用交叉验证法检验显示,该风险预测模型分类准确率为88.68%。
综上所述,年龄、KPS 评分、合并其他部位转移、原发病灶控制情况、治疗方式是NSCLC 肝转移患者预后死亡的独立危险因素,据此建立的风险预测模型对患者预后死亡的预测效果较好。但本研究为小样本量、回顾性研究,结论仍需今后大样本前瞻性研究进一步探讨。
