电感耦合等离子体质谱法测定生活饮用水中钡的不确定度评定
2023-10-25张颖唐琳吴梦溪黄文耀
张颖,唐琳,吴梦溪,黄文耀
(湖北省疾病预防控制中心,应用毒理湖北省重点实验室,武汉 430079)
测量不确定度是表征合理地赋予被测量值的分散性,与测量结果相联系的参数[1-3]。对检测结果进行不确定评定是评价分析质量的重要手段,也是国家计量技术规范中的规定[4-6]。
目前,关于电感耦合等离子体质谱(ICP-MS)法测定生活饮用水中各种元素不确定度的研究已有报道[7-9],但对不确定度的来源分析只针对实验室检测部分,忽略了采样及样品保存过程的不确定度。笔者按照GB/T 5750.2—2023 《生活饮用水标准检验方法 水样的采集与保存》[10]采集并保存样品,依据GB/T 5750.6-2023 《生活饮用水标准检验方法 金属和类金属指标》[11]电感耦合等离子体质谱法对生活饮用水中的钡进行检测,从采样到实验室检测,系统分析不确定来源,对整个过程的不确定度进行评定。
1 实验部分
1.1 主要仪器与试剂
电感耦合等离子体质谱仪:Agilent 7900 型,美国安捷伦科技有限公司。
超纯水仪:Milli-Q Advantage A10型,美国密立博公司。
钡单元素溶液标准物质:100 μg/mL,编号为GBW(E) 080243,中国计量科学研究院。
硝酸:UP级,苏州晶瑞化学有限公司。
质谱调谐液:铈、钴、锂、钇、铊混合标准溶液,各元素质量浓度均为10 μg /mL,介质为2%(质量分数)的硝酸溶液,安捷伦科技(中国)有限公司。
内标储备液:100 μg /mL 铟标准溶液,介质为10%(质量分数)的硝酸溶液,安捷伦科技(中国)有限公司。
实验用水为Milli-Q Advantage A10实验室水纯化系统制备的高纯水(电阻率大于18.2 MΩ·cm)。
1.2 测定方法
按照GB/T 5750.2—2023 《生活饮用水 标准检验方法 水样的采集和保存》[10]进行采样、运输和保存。用聚乙烯瓶现场采集10 份样品,均以每500 mL加入0.4 mL浓硝酸,调节pH至不大于2,运送至实验室保存,于14天内进行测定。
依据GB/T 5750.6—2023 《生活饮用水标准检验方法 金属和类金属指标》[11]电感耦合等离子体质谱法对生活饮用水中的钡进行检测。
1.3 溶液配制
钡标准使用液:1 000 μg/L,移液器吸取1.00 mL 钡标准溶液于100.0 mL 容量瓶中,用1%(体积分数,下同)硝酸定容至标线。
钡系列标准工作溶液:用移液器分别吸取0.00、0.10、0.20、0.30、0.40、0.50、1.00 mL 于10.0 mL 容量瓶中,用1%硝酸定容至标线,配制成质量浓度分别为0、10.0、20.0、30.0、40.0、50.0、100 μg/L 的钡系列标准工作溶液。即使用100 μL 移液器分别移取100 μL 标准使用液0 次、1 次、2 次、3 次、4 次、5 次,使用1 mL移液器1次。
1.4 测定
用调谐液调整仪器各项指标,仪器灵敏度、氧化物、双电荷、分辨率等各项指标达到测定要求后,以铟(115In)作为内标元素,依次将试剂空白、钡系列标准工作溶液、样品溶液分别测定。
以钡元素的质量浓度为横坐标,以元素钡的质谱信号与内标元素铟的质谱信号的强度比为纵坐标,绘制标准工作曲线,按照标准曲线法得到样品中钡元素的质量浓度。
2 数学模型
按1.2样品的保存和测定方法,由标准曲线法得到样品中钡的质量浓度,数学模型如式(1):
式中:ρ——水样中钡的质量浓度,μg/L;
I—钡的质谱信号强度;
I0—内标铟的质谱信号强度;
a——标准曲线截距;
b——校准曲线斜率。
3 不确定度来源分析
参考JJF1059.1—2012《测量不确定评定与表示》[12],结合实验过程,被测量不确定度主要来源有:
(1)样品采集引入的不确定度;
(2)水样保存稳定性引入的不确定度;
(3)样品采集时加保存剂引入的不确定度;
(4)有证标准物质引入的不确定度;
(5)钡系列标准溶液配制过程引入的不确定度;
(6)标准曲线拟合引入的不确定度;
(7)测量重复性引入的不确定度。
4 不确定度评定
4.1 采样引入的相对标准不确定度urel(X)
平行测定现场采集的10份平行样,平行样测定结果见表1。
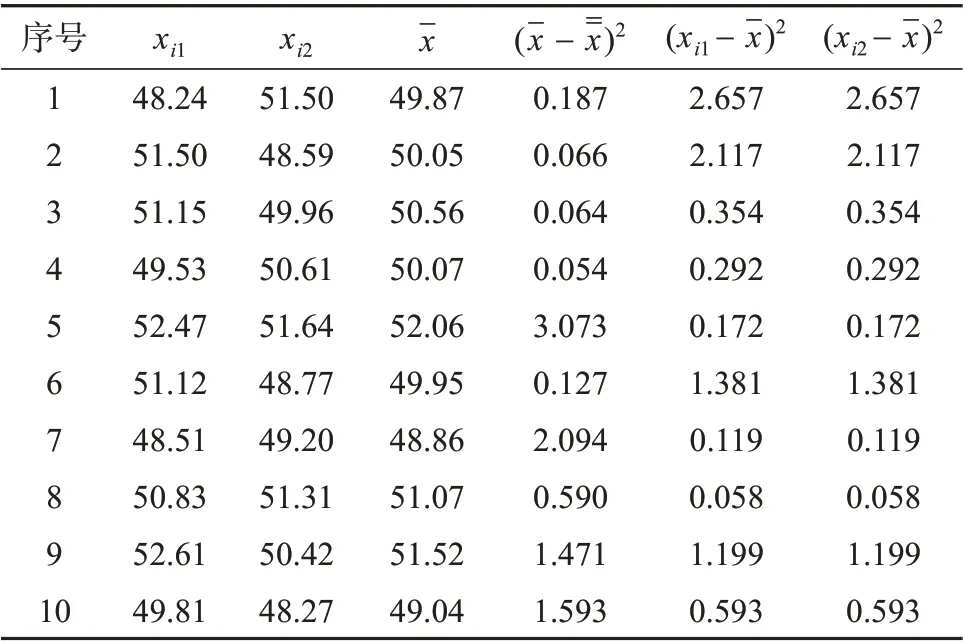
表1 平行样测定结果
根据JJF 1343—2012《标准物质定值的通用原则及统计学原理》[13]的规定,按式(2)~式(5)计算采样引入的相对标准不确定度urel(X)。
m——平行样品测定次数,m=10;
n——样品重复测定次数,n=2;
由表1 中的数据结合式(2)~(5)计算得到测得值的平均值为50.30 μg/L,组间方差为2.017,组内方差为1.788,采样方差为0.142,则采样引入的相对标准不确定度
4.2 水样保存稳定性引入的相对标准不确定度urel(St)
水样采集后,不能立即测量,在运输途中、储存过程可能影响水中钡的稳定性。为了测定水样放置过程稳定性引入的不确定度,将其中1份水样分成8份,分别放置0、2、4、6、8、10、12、14d后测量,钡的质量浓度测定值分别为49.87、49.53、50.81、50.61、51.50、49.83、50.42、48.99 μg/L,波动范围为48.99 ~51.50 μg/L,平均值为 50.20 μg/L。按照均匀分布采用极差法估算[14],水样放置过程中产生的相对标准不确定度为:
4.3 水样采集时加保存剂引入的相对标准不确定度urel(fD)
4.3.1 0.5 mL吸量管引入的标准不确定度u(V1)
(1)示值误差引入的不确定度。根据JJG 196—2006《常用玻璃量器》检定规程[15],0.5 mL 标线吸量管的最大允许误差为±0.005 mL,假设为三角分布,k=,故该项引入的标准不确定度为0.005/k=0.002 04 mL。
(2)体积变化引入的不确定度。实验室温度变化在±2 ℃范围内,硝酸在25 ℃的体积膨胀系数约为1.04×10-3℃-1,则引起的溶液体积变化:0.4 mL×1.04×10-3℃-1×2 ℃=0.000 832 mL,按矩形分布计算,k=,标准不确定度为0.000 832/k=0.000 480 mL。
以上两项合成得到0.5 mL 刻度吸量管引入的标准不确定度:
4.3.2 500 mL量筒引入的标准不确定度u(V2)
(1)示值误差引入的不确定度。500 mL量筒的最大允许误差为±5 mL,假设为三角分布,k=,故标准不确定度为5/k=2.041 mL。
(2)体积变化引入的不确定度。温度变化在±2 ℃范围内,水在25℃的体积膨胀系数为257.3×10-6℃-1,温度变化产生的体积最大变化为:500 mL×257.3×10-6℃-1×2 ℃=0.257 mL,按矩形分布计算,k=,则体积变化引入的标准不确定度为0.257/k=0.148 mL。
以上两项合成得到500 mL 量筒引入的标准不确定度:u(V2)==2.046 mL。
4.3.3 加入保存剂引入的相对标准不确定度
水样采集时的稀释因子为(V1+V2)/V2。采样时加保存剂引入的标准不确定度u(fD)按以下公式计算。

4.4 钡单元素溶液标准物质引入的相对标准不确定度urel(ρstd)
采用的钡单元素标准溶液的质量浓度为100 μg/mL,相对扩展不确定度为1%(k=2),则钡标准物质引入的相对标准不确定度为urel(ρstd)=1%/k=0.005。
4.5 标准系列溶液配制过程引入的相对标准不确定度urel(Vstd)
标准系列溶液配制过程用到了100 mL 单标线容量瓶1 次,10 mL 单标线容量瓶7 次,100 μL 移液器15次,1 mL移液器2次。
4.5.1 100 mL 容量瓶定容引入的相对标准不确定度urel(V100)
(1)示值误差引入的不确定度。100 mL 容量瓶的最大容量允许误差为±0.1 mL,按照三角分布估算,k=,则标准不确定度为0.1/k=0.040 8 mL。
(2)体积变化引入的不确定度。与4.3.2(2)同法评定,温度变化产生的体积最大变化为100 mL×257.3×10-6℃-1×2 ℃=0.051 5 mL,按照矩形分布计算,k=,则体积变化引入的标准不确定度为0.051 5/k= 0.029 7 mL。
则100 mL 容量瓶定容过程引入的相对标准不确定度:
4.5.2 10 mL容量瓶定容引入的相对标准不确定度urel(V10)
(1)示值误差引入的不确定度。10 mL容量瓶的最大容量允许误差为±0.020 mL,按三角分布估算,k=,则标准不确定度为0.020/k=0.008 2 mL。
(2)体积变化引入的不确定度。按照4.3.2(2)同法评定,温度变化产生的体积最大变化为10 mL×257.3× 10-6℃-1×2 ℃=0.005 15 mL,按矩形分布计算,k=,则体积变化引入的标准不确定度为0.005 15/k=0.002 97 mL。则10 mL容量瓶定容过程引入的相对标准不确定度:
4.5.3 移液器引入的相对标准不确定度urel(Vpip)
移液器按照JJG 646—2006《移液器检定规程》的规定[16],引入的相对标准不确定度见表2。其中容量误差引入的标准不确定度,按照三角分布,k=,允差/6;温度波动按矩形分布,k=,u(VΔT)=(V×ΔT×α)/3,则移液器引入的相对不确定度:
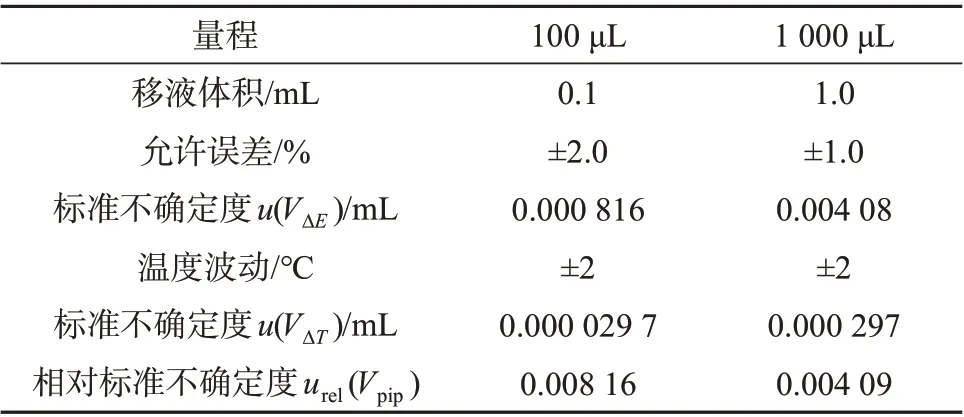
表2 移液器引入的相对标准不确定度
将以上三项合成,则钡系列标准溶液配制过程引入的相对标准不确定度urel(Vstd)=0.019 7。
4.6 标准曲线拟合引入的相对标准不确定度urel(curve)
以钡元素的质量浓度为横坐标,以钡与铟的响应值的比值为纵坐标,得到拟合标准曲线为y=0.016 7x+0.002 7,相关线性系数r=0.999 9。标准曲线拟合引入的标准不确定度按式(9)~(11)计算:
式中:u(curve) ——标准曲线拟合引入的不确定度,μg/L;
SR——标准曲线的残差标准差;
b——标准曲线斜率,b=0.016 7;
p——水样测定次数,p=2;
n——标准溶液测定的总次数,n=7;
ρ0——水样中钡的平均质量浓度,μg/L;
ρj——标准曲线中各浓度点的值,μg/L;
-ρj——标准曲线中各浓度点的平均值,μg/L;
yj——标准曲线中各浓度点的实际强度比值;
a——标准曲线截距,a=0.002 7。
标准曲线中各浓度点的平均值为35.714 μg/L,根据表1计算,水样中钡的平均质量浓度ρ0为49.87 μg/L,根据表3中的数据结合式(9)(10)计算得到标准曲线的残差标准差SR为0.009 89,标准曲线拟合引入的不确定度u(curve)为0.486 μg/L,故标准曲线拟合引入的相对标准不确定度:
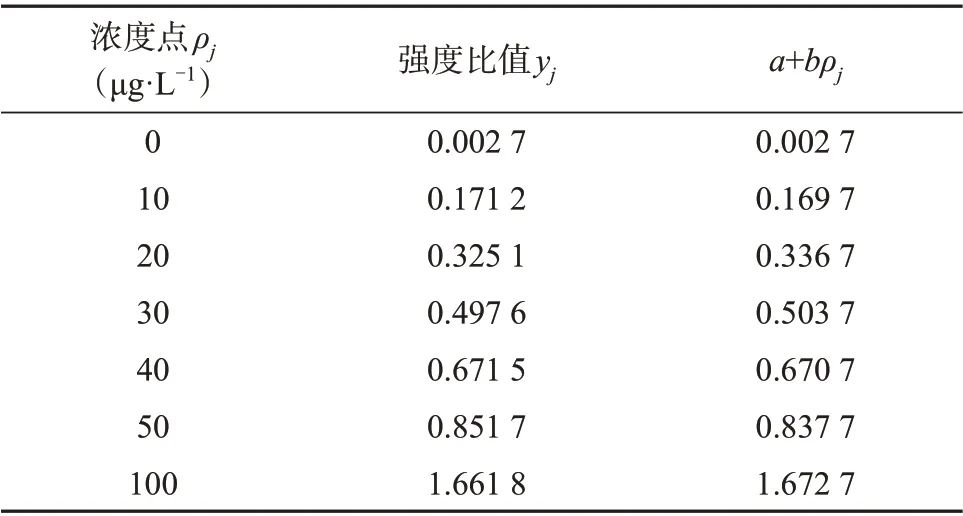
表3 标准曲线测定结果
4.7 测量重复性引入的相对标准不确定度urel(r)
10 份平行水样的测定结果见表1,水样所有测量结果的平均值ρˉ=50.30 μg/L,标准偏差为s=1.018 μg/L,故由重复性引入的标准不确定度:
则相对标准不确定度:
4.8 合成相对标准不确定度urel(ρ)
ICP-MS测定生活饮用水中钡的合成相对标准不确定度:
则钡的标准不确定度:
4.9 扩展不确定度
取置信水平为95%,包含因子k=2时,则扩展不确定度:
电感耦合等离子体质谱法测定生活饮用水中钡的含量为(50.3±2.9) μg/L(P=95%,k=2)。
5 结语
对ICP-MS法测定生活饮用水中钡的整个过程(从采样到实验室检测)进行不确定度评定。结果表明,测定的饮用水中钡的含量为50.3 μg/L,其扩展不确定度为2.9 μg/L(P=95%,k=2)。测定结果的不确定度主要来源为标准系列溶液配制过程引入的不确定度,因此配制标准系列溶液时,应选用经校正后的A 级容量瓶和高精度的移液器具,并尽量减少稀释次数[3]。其次是水样保存过程中钡的稳定性引入的不确定度,说明水样采集后应尽快完成实验室检测,以减小该不确定度分量,提高测定结果的可靠性。
