黄铁矿在酸性镍(Ⅱ)溶液中的电化学氧化行为
2023-10-23毛王彬李佳蕊唐家华李栢庄顾云贵
毛王彬,李佳蕊,唐家华,李栢庄,顾云贵,何 琳, 张 炎
(昆明理工大学理学院)
引 言
黄铁矿(FeS2)是一种常见的硫化矿[1-2],在细菌和氧气等各种因素作用下,会发生氧化反应,导致酸性矿山废水(Acid Mine Drainage,AMD)的形成[2]。AMD不仅会通过水循环进入湖泊、河流等进而破坏水体生态环境,甚至可能通过食物链传入人体,危害人类身体健康[3]。目前,控制AMD污染扩散和从源头上防止金属硫化物氧化是治理AMD的2种主要思路。然而,仅仅依靠控制AMD污染扩散的效果并不显著,并且可能引起二次污染。因此,深入研究黄铁矿表面氧化机理对从源头上治理AMD污染具有理论指导意义,可以为制定更有效的治理策略提供依据。
尽管黄铁矿在各种电解质溶液中的氧化机理得到广泛研究,但其在酸性Ni2+溶液中的氧化机理报道较少。因此,试验期望通过多种电化学技术对黄铁矿电极在酸性Ni2+溶液中的氧化行为进行深度探索,拓宽对黄铁矿在酸性Ni2+溶液中氧化行为的研究,在源头上对其防腐与治理提供新见解。
1 试验药剂及方法
1.1 电解液
用电子天平称取不同量的NiCl2·6H2O和NaCl于烧杯中(用于调整Cl-的浓度),并用0.5 mol/L的H2SO4溶液溶解,定容于500 mL容量瓶中配制成0.5 mol/L H2SO4+18 mmol/L Cl-+xmmol/L Ni2+(x=1,3,5,7,9)的酸性溶液。
1.2 电极及仪器
试验以饱和甘汞电极为参照电极,铂电极为辅助电极,黄铁矿电极为工作电极,将3根电极一起浸泡在电解液中,并使用上海辰华电化学工作站及CHI660e软件进行测量。
试验所用的黄铁矿购自中国地质博物馆。XRF检测结果表明,黄铁矿的纯度为98.6 %,主要杂质为SiO2。为了制备工作电极,将高纯度的天然黄铁矿切割成半径为1 cm、高度为0.2 cm的圆柱块。其中一个底面用砂纸进行抛光,以确保与电解液接触良好。将黄铁矿埋于石墨中,只露出一个面积为0.8 cm2的抛光面作为工作表面与电解质相接触。通过铜线连接到未抛光的黄铁矿表面。在每次试验开始前与每次测量结束后,使用镊子取出黄铁矿样品,用砂纸打磨抛光面并用蒸馏水清洗以去除杂质或反应产物。
2 结果与讨论
2.1 开路电位
为了保证电化学测量体系的稳定性,开路电位(OCP)的数值通常应在±5 mV的范围内变化[5]。在总时长为800 s,时间间隔为0.1 s的条件下,测试不同浓度Ni2+对黄铁矿电极OCP值的影响,试验结果见图1。
由图1可知:在400~800 s,OCP值呈现出±5 mV波动的相对稳定状态。这表明3个电极体系满足了电化学测试的要求,并且具有较好的稳定性。此外,Ni2+浓度为1 mmol/L、3 mmol/L、5 mmol/L、7 mmol/L、9 mmol/L时,黄铁矿电极的OCP值分别在430.5 mV、429.3 mV、425.2 mV、421.4 mV、419.3 mV附近波动。
综上所述,在此试验条件下,Ni2+浓度会影响黄铁矿电极的OCP值,即OCP值随着Ni2+浓度的增加而减小。
2.2 CV曲线
在电位为-0.70~0.80 V时,对黄铁矿电极在不同浓度Ni2+酸性溶液中的CV曲线进行测试,扫描圈数为3圈,试验结果见图2。
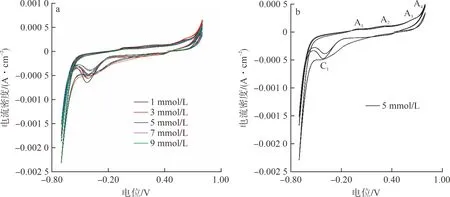
图2 黄铁矿电极在不同浓度Ni2+酸性溶液中的CV曲线
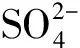

(1)

(2)

(3)

(4)

(5)
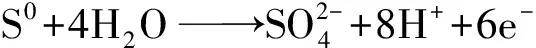
(6)
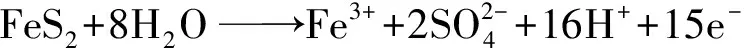
(7)
2.3 Tafel极化曲线
在测试电压为0~0.60 V,扫描速率为10 mV/s的条件下,使用Tafel极化曲线测试了黄铁矿电极随Ni2+浓度变化时的电化学行为,并对Tafel 极化曲线进行计算,得到了黄铁矿电极在不同浓度Ni2+酸性溶液中的电化学腐蚀动力学参数,包括腐蚀电位(Ecorr)和腐蚀电流密度(jcorr),试验结果见图3和表1。
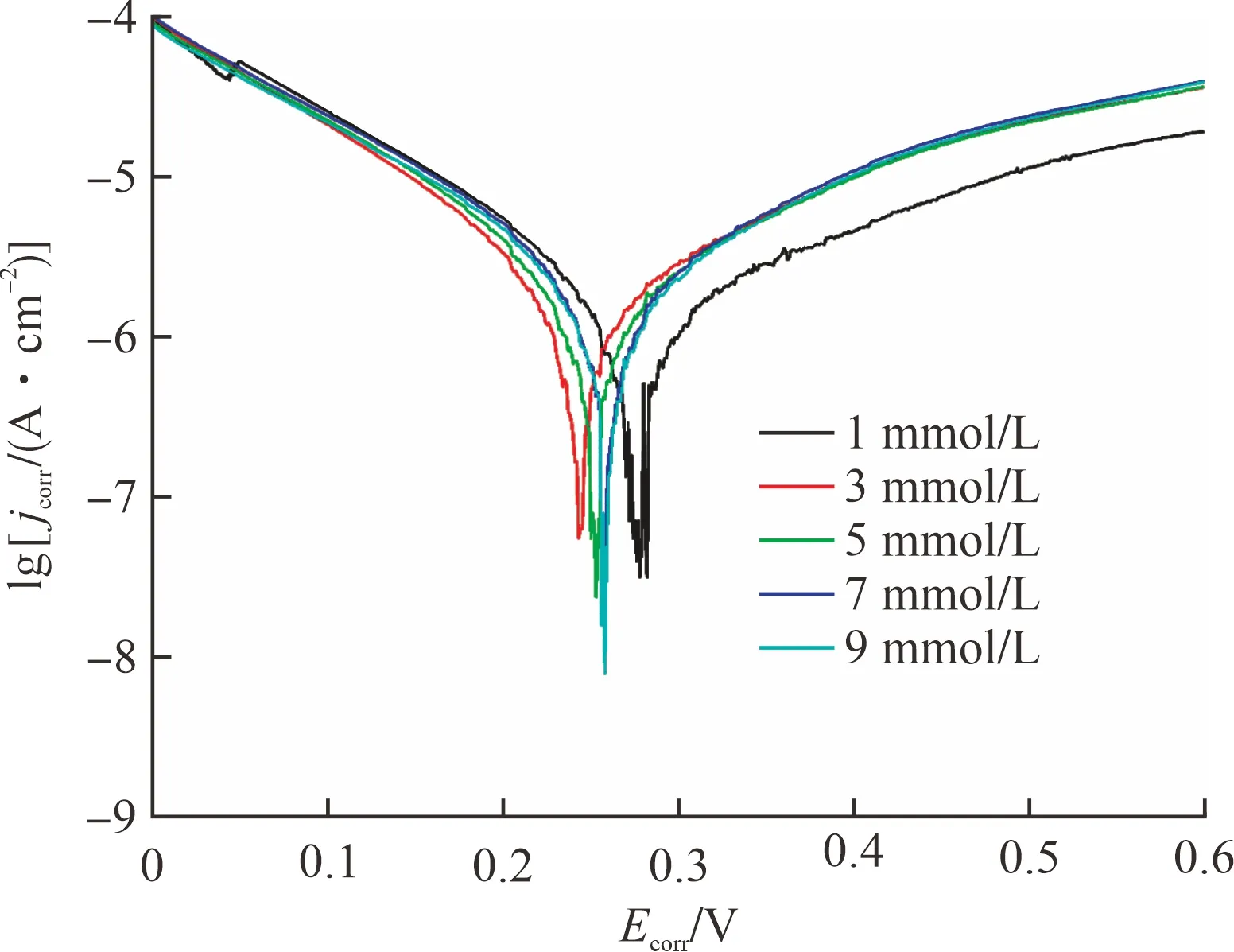
图3 黄铁矿电极在不同浓度Ni2+酸性溶液中的Tafel极化曲线
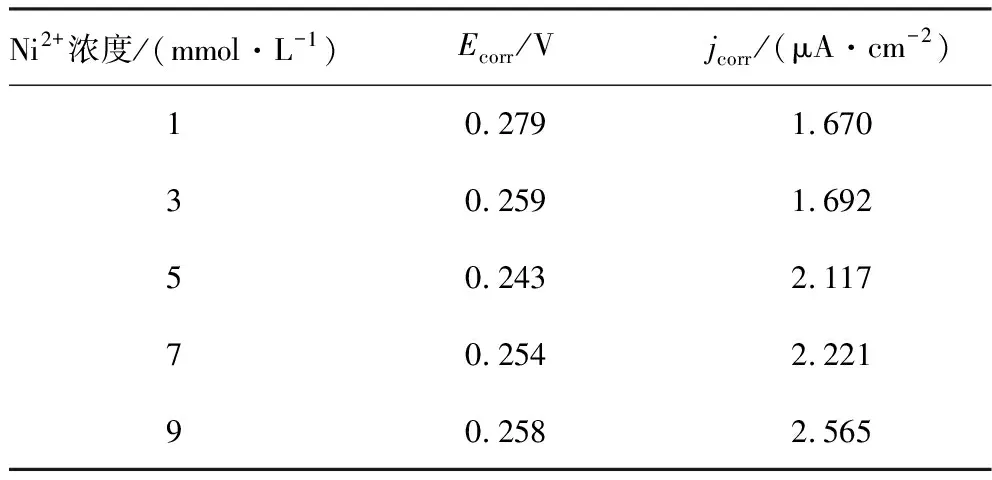
表1 黄铁矿电极在不同浓度Ni2+酸性溶液中的Tafel曲线参数
根据前人的研究,腐蚀电流密度(jcorr)越大,氧化作用越强[1,5]。由表1可知:jcorr随着Ni2+浓度的增加而升高。即当Ni2+浓度从1 mmol/L增加到9 mmol/L时,jcorr从1.670 μA/cm2逐渐增大至2.565 μA/cm2。这表明在试验条件范围内,增加Ni2+的浓度可以提高黄铁矿的氧化速率。
2.4 EIS曲线
电化学阻抗谱(EIS)是一种测量电化学系统阻抗与频率关系的方法,通过给系统施加一个小振幅的正弦波电位,测量电位与电流信号之间的相位差和幅值,从而绘制出阻抗随频率变化的图谱。目前,该方法广泛应用于黄铁矿表面氧化反应动力学过程的研究。在本试验中,测量电压为0.60 V,频率测试范围为10-1~105Hz,振幅为5 mV,测定了不同浓度Ni2+酸性溶液的EIS曲线。此外,对试验测得的电化学阻抗谱进行拟合,得到了相应的电化学等效电路图。黄铁矿电极在不同浓度Ni2+酸性溶液中的奈奎斯特图谱和等效电路图分别见图4和图5,试验结果见表2。
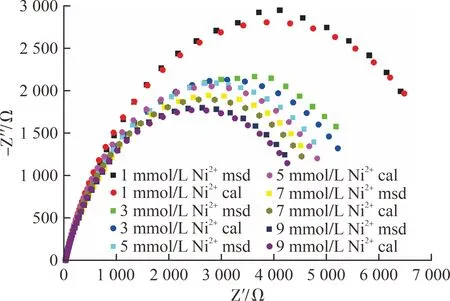
-Z″—电极虚部阻抗 Z′—电极实部阻抗cal—拟合模拟值 msd—试验测量值图4 黄铁矿电极在不同浓度Ni2+酸性溶液中的奈奎斯特图谱
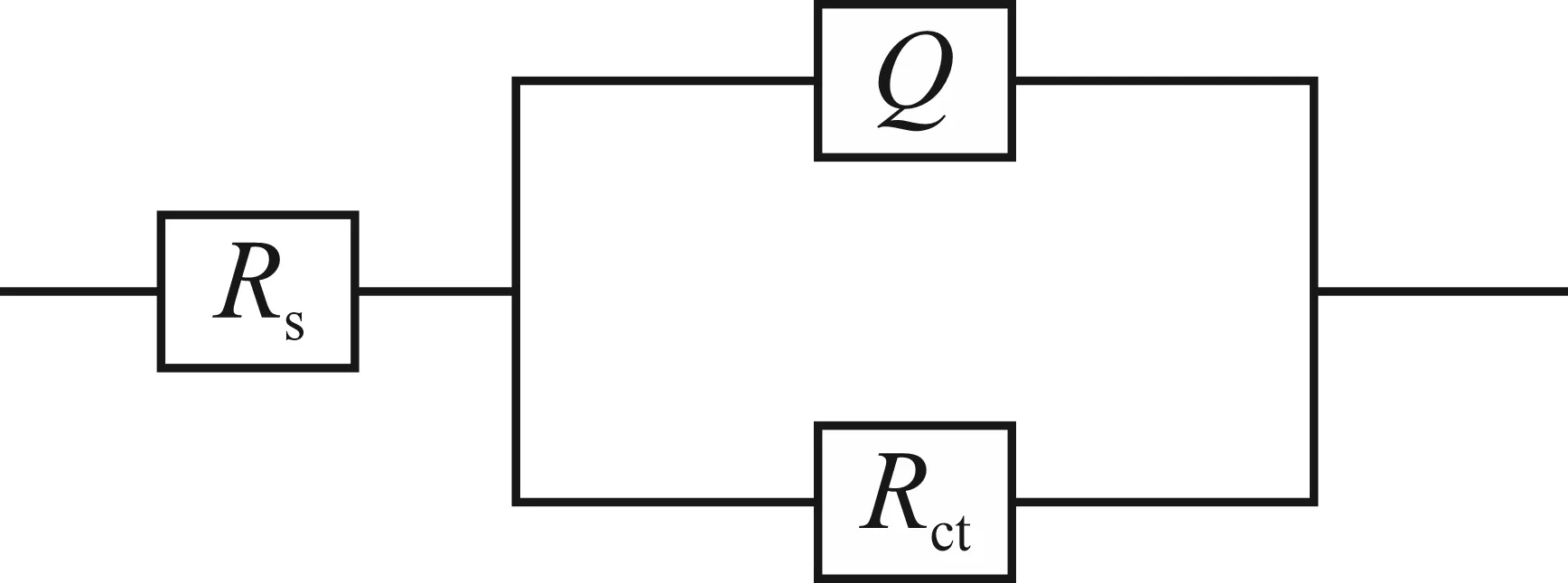
Rs—溶液电阻(Ω·cm2)Q—表面层-电极界面的双电层电容(sn/(Ω·cm2))Rct—电子转移电阻 (Ω·cm2)图5 黄铁矿电极在不同浓度Ni2+酸性溶液中的等效电路图
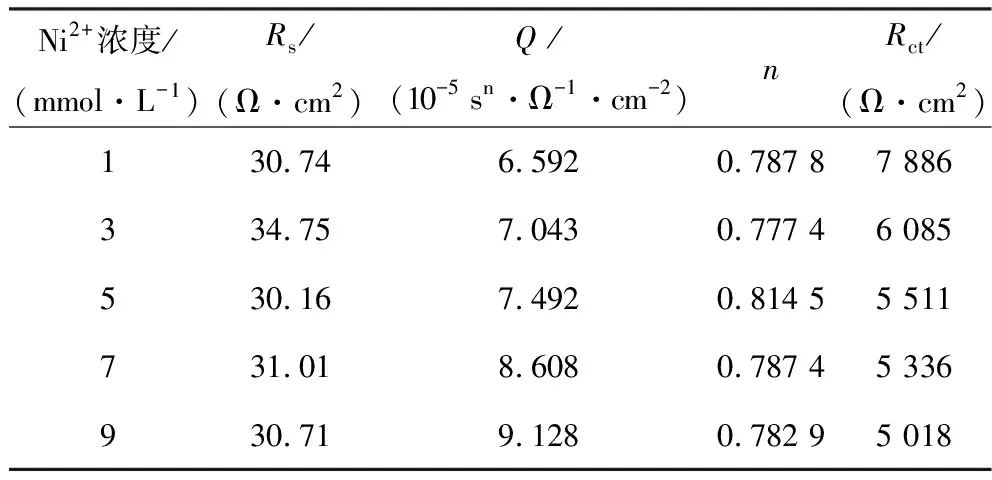
表2 等效电路图中各元件参数
在等效电路图中,电荷转移电阻Rct用于表示电极表面氧化速率的快慢[15]。由表2可知:Rct值随添加的Ni2+浓度的增大而减小。该试验数据表明,随着Ni2+浓度的增大,黄铁矿电极表面氧化速率加快,与图4中的半圆弧越来越小相对应。
3 结 论
1)试验测得的OCP值表明,随着Ni2+浓度的增加,黄铁矿电极的OCP值逐渐减小。
2)Tafel极化曲线动力学试验数据表明,腐蚀电流密度随Ni2+浓度的升高而增大。
3)通过对奈奎斯特图和等效电路图中元件的Rct值进行分析,发现随着加入Ni2+浓度的增加,黄铁矿电极表面氧化速率也随之加快。
