二甲基亚砜有机溶液中Sb-Te薄膜热电材料的电沉积制备
2023-10-19胡佳琦王亚妮秦若轩赵婧炜李菲晖
胡佳琦,邱 爽,王亚妮,秦若轩,赵婧炜,李菲晖
(天津商业大学 生物技术与食品科学学院,天津 300134)
工业的迅猛发展,石油、煤炭等传统化石能源的大量使用,工业废热的大量排放以及能量的低效使用等对环境造成了严重的污染。全球对可再生能源和能源转换效率的需求不断增长,热电材料作为一种可以实现热能和电能相互转化的能源转换技术材料,备受人们关注[1-3]。其作为热电领域的关键组成部分,在提高能源利用效率、减少能源浪费以及实现可持续发展方面发挥着重要作用。
无机半导体Sb2Te3材料在室温条件下具有较高的热电优值[4-6],还具有较高的能量转换效率,成为目前应用较为广泛的热电材料[7-8]。热电薄膜材料的研究热潮也促进各种制备方法的产生与发展,如磁控溅射法[9]、离子束溅射法[10]、化学气相沉积法[11]、电化学沉积法[12-13]等。而其中电化学沉积法因其制备方便、工艺成本低、设备要求和操作要求低、生产效率高等优点,在薄膜热电材料领域潜力巨大[14]。研究者们为提高材料性能,投入大量研究在关于材料的掺杂改性、材料复合等方面[15-17],仅有为数不多的文献报道改变了溶液体系,尝试在有机体系中制备材料,以期提高材料性能[18-19]。Sb(III)、Te(IV)等离子在有机体系中的沉积电位及沉积的相对难易程度较水溶液会有很大的不同,改变溶液体系可能获得性能更佳的薄膜热电材料[20]。本文采用电化学测量技术研究了二甲基亚砜(DMSO)有机体系中Sb(III)、Te(IV)离子的电化学行为。在此基础上深入分析了Sb体系、Te体系以及Sb-Te二元体系的氧化还原机理,根据结果选取了不同的电沉积条件制备薄膜热电材料,并对其进行了塞贝克系数测试及结构表征。
1 实验方法
1.1 溶液配制和材料制备
1.1.1 溶液配制
称取一定量所需溶质转移至干燥洁净的烧杯之中,先加入少量DMSO溶剂,使溶质在室温下溶解,待其完全溶解后使用玻璃棒将溶液转移至干燥洁净的容量瓶之中,定容、摇匀后贴上标签放置待用,测试溶液组成如表1所示。
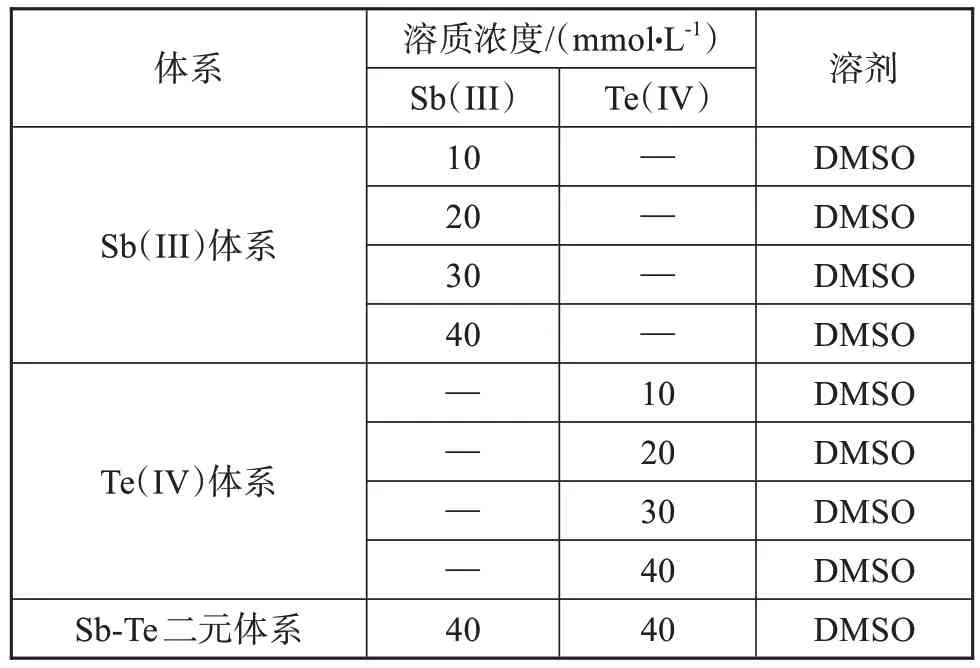
表1 溶液组成Tab.1 Composition of solution
1.1.2 测试所需电极及前处理
研究电极:
(1)金电极:将直径为3 mm的金电极用蒸馏水冲洗干净后,在除油液(80 g/L Na3PO4·12H2O+11.5 g/L Na2SiO3·9H2O+11.5 g/L无水Na2CO3)中进行阴极电化学除油(室温),除油时间为10 s,将除油后的金电极用蒸馏水冲洗干净,然后放入体积比为1∶1的硝酸溶液中进行酸浸处理10 s,将酸浸处理后的金电极用蒸馏水冲洗干净,之后采用DMSO溶剂进行两次润洗,最后放入电解液中组成三电极两回路体系。
(2)镀金铜片:将铜片根据测试要求裁剪成为1 cm × 9 cm规格,将其背面使用胶带封装严密,再将其正面用绝缘胶带封装严密,留出1 cm×1 cm的测试区,然后用蒸馏水冲洗干净,于40 ℃下进行阴极电化学除油0.5~1.0 min,之后用蒸馏水清洗干净,采用DMSO溶剂进行两次润洗,最后放入电解液中组成三电极两回路体系。
辅助电极:选用面积为3 cm2的铂电极作为本实验的辅助电极,前处理方法与镀金铜片相同。
参比电极:采用饱和甘汞电极作为参比电极。
1.2 电化学行为测试
循环伏安曲线测试的扫描速度设置为5、10、20、30、40 mV/s,其中Sb(III)体系的电位测试范围为-2.5~1.0 V,Te(IV)体系的电位测试范围为-2.0~1.0 V,Sb-Te二元体系的电位测试范围为-3.0~1.5 V。阴极极化曲线的测试起始电位为开路电位,终止电位为-2.0 V,扫描速度为1 mV/s,测试过程中施加强制搅拌。
1.3 薄膜热电材料的制备
根据含有Sb(III)、Te(IV)溶液的循环伏安曲线以及二元体系的线性极化曲线的结果分析,选择合适的溶液浓度配比和沉积电位,使用CHI660E电化学工作站进行恒电位沉积薄膜热电材料,工作电极为镀金铜片,沉积过程中施加强制搅拌,在沉积过程中观察铜片上的沉积状态,待电化学工作站中显示的沉积量达到10 C/cm2后停止实验,将电沉积后的材料取出,用蒸馏水冲洗,撕掉封装的胶带,冷风吹干后放入样品袋中,贴好标签后放入干燥器中待用。
1.4 热电材料的性能表征
采用X-射线衍射仪(日本理学Rigaku D型,XRD)进行物相分析,对恒电位法所沉积出的薄膜热电材料进行X射线衍射实验,扫描范围为0~90 °,扫描速度为4 °/min,所得样图使用软件Jade可对所制备的样片进行定性分析。
采用扫描电子显微镜(德国蔡司Sigma300型,SEM)进行形貌分析,通过对样片进行高倍放大而观察样片的微观结构形貌,放大倍数为1000和5000倍。
采用能谱仪(德国蔡司Sigma300型,EDS)进行元素组分分析,选取放大后的薄膜温差电材料的形貌良好平整的部位进行成分分析,可得样品中的元素含量比。
采用TJU-EC2001 塞贝克测试系统(天津大学自主研发)测试电沉积薄膜材料的塞贝克系数,测试在室温下进行,测试方向垂直于材料生长方向,施加的温度差小于10 ℃。
2 结果与讨论
2.1 离子氧化还原行为的研究
2.1.1 Te(IV)、Sb(III)体系的氧化还原行为
图1(a)为DMSO空白溶液在Au电极上的循环伏安曲线图。可以看出,在较宽的电位范围内,DMSO空白溶液并未出现明显的氧化峰和还原峰,且其电流密度约为10-6A·cm-2,可忽略不计。因此可粗略认为,在-1.5~1.0 V的电位范围内,DMSO作为溶剂对溶液中其他离子的氧化还原行为没有干扰性,具有较宽的电化学窗口。图1(b)、图1(c)为采用Au电极,在10 mmol/L Te(IV)或Sb(III)DMSO有机溶剂体系中于不同扫描速度下测得的循环伏安曲线图。图中的氧化还原峰分别对应于Te(IV)或Sb(III)离子得电子还原为Te或Sb单质的还原过程以及Te或Sb单质失去电子氧化为Te(IV)或Sb(III)离子的氧化过程。可以看出,随着扫描速度的增大,还原峰电位负移,峰电流也会随之增大,曲线的氧化峰和还原峰并不对称,且其面积不相等,在曲线测试过程中可明显看出工作电极与对电极上皆有残留物,因此可证明Te(IV)离子、Sb(III)离子在DMSO有机溶剂中的氧化还原行为是完全不可逆的过程。
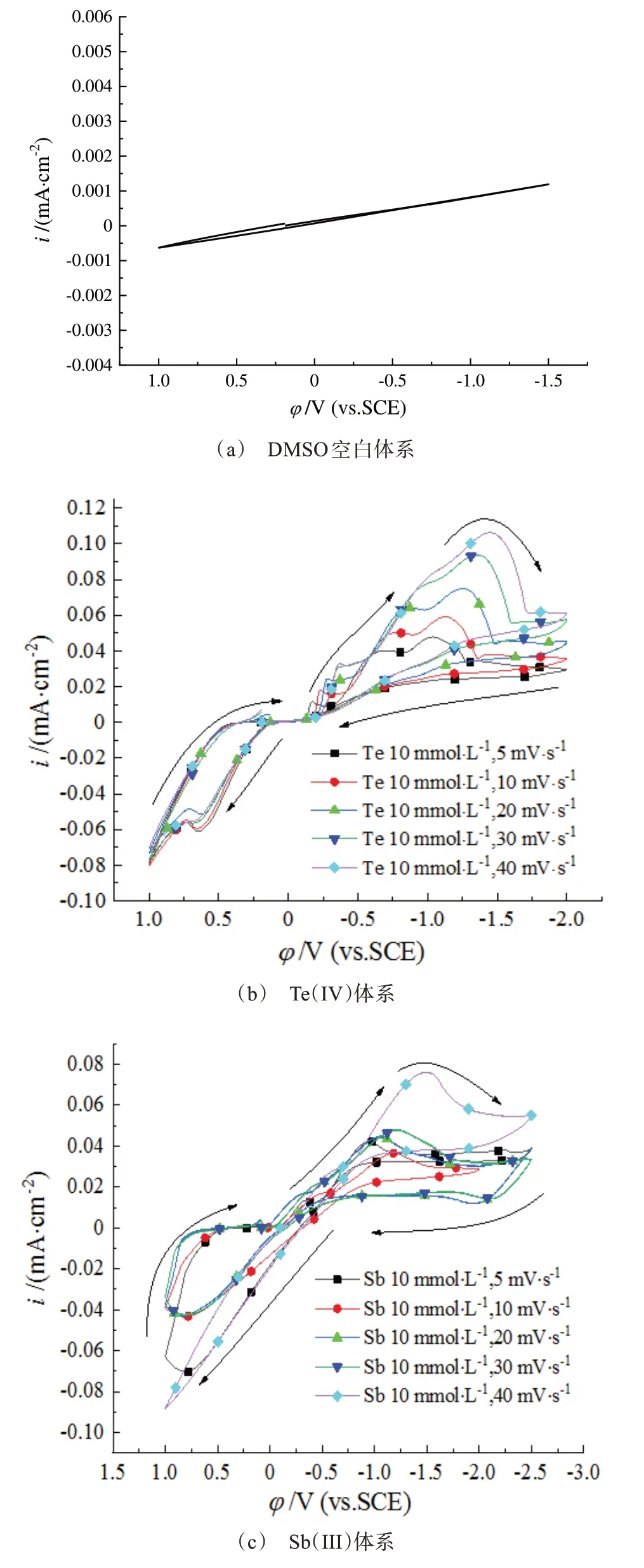
图1 单体系在不同扫速下的循环伏安曲线Fig.1 Cyclic voltammetry curves of single solution system at different scanning rates
图2为采用Au电极在含有不同浓度的Te(IV)或Sb(III)离子的DMSO有机溶剂中测得的阴极极化曲线。可以看出,随着电极电位的不断负移,还原电流密度的数值不断升高,还原速度逐渐加快。对比相同电位下的电流密度,Te(IV)体系的阴极极化曲线的电流密度随着离子浓度的增大明显提高,而Sb(III)体系的电流密度随浓度变化不明显。该现象说明在所测试的电位范围内,Te(IV)离子的还原过程受离子液相传质的影响,当Te(IV)离子浓度增大时,液相传质速度提高,沉积速度加快;而Sb(III)体系的还原过程是由电化学极化占据主导地位,当主盐Sb(III)离子的浓度不断增加时,沉积速率并未出现明显的变化。
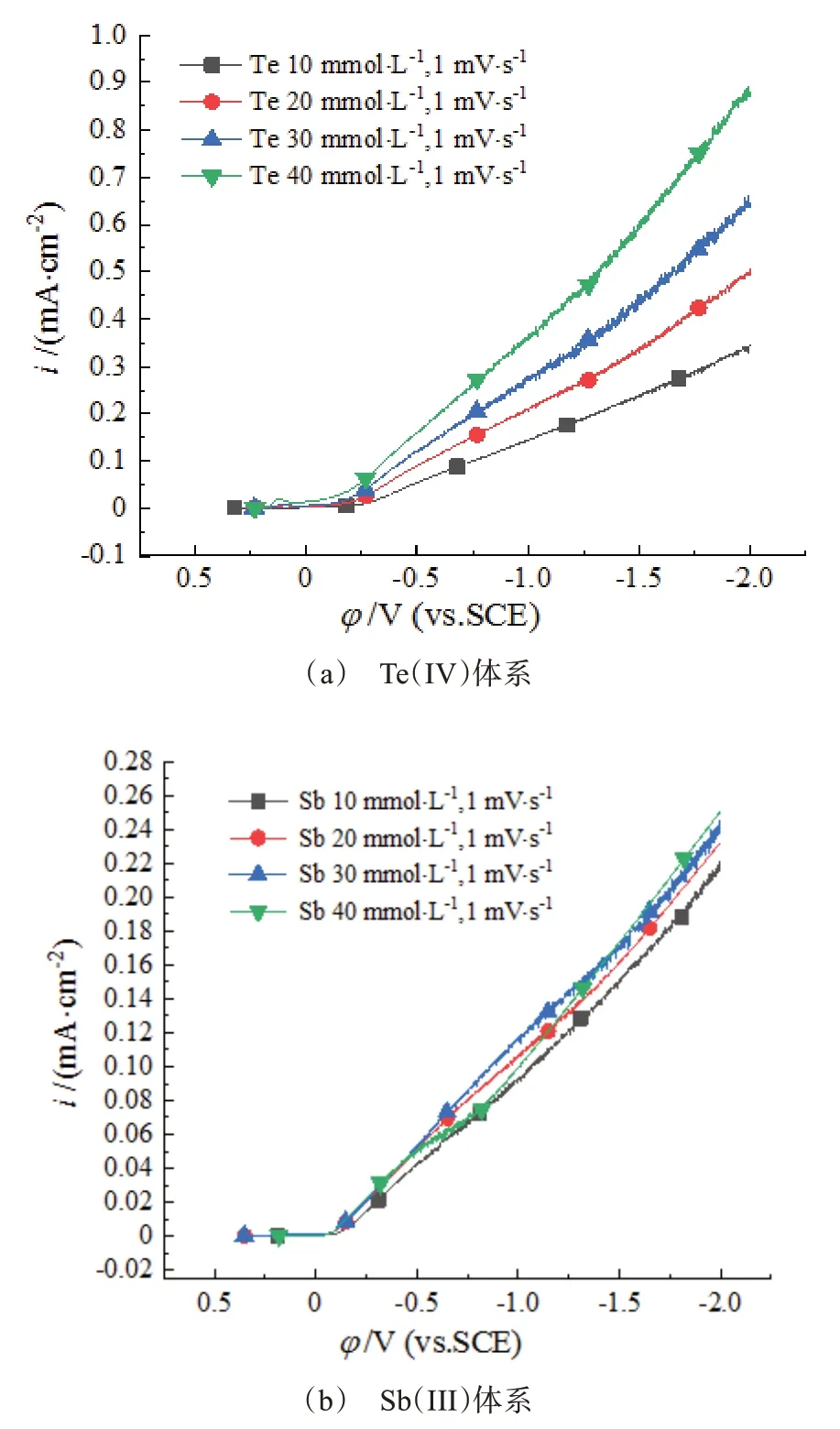
图2 离子浓度不同的单元体系的阴极极化曲线Fig.2 Cathode polarization curves of single solution system with different ion concentrations
2.1.2 Te(IV)、Sb(III)体系的对比
图3和图4分别为Sb(III)、Te(IV)单元体系的循环伏安曲线和阴极极化曲线的对比图。
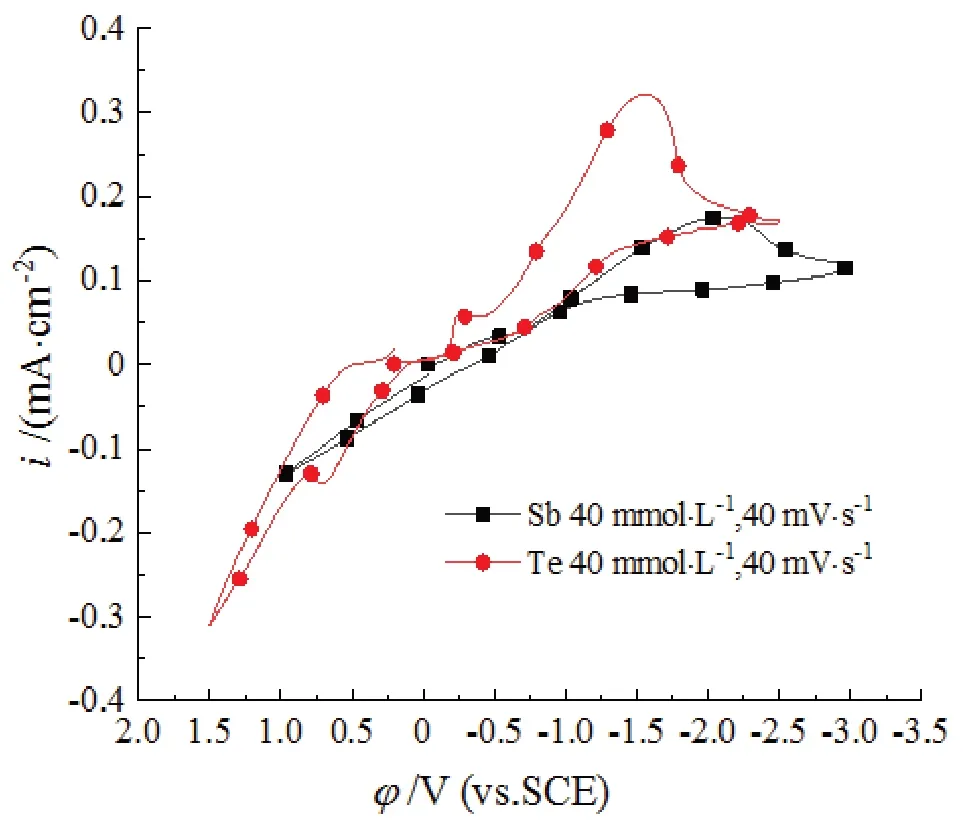
图3 Sb(III)、Te(IV)体系的循环伏安曲线对比图Fig.3 Comparison of cyclic voltammetry curves of Sb(III) and Te(IV) single solution system
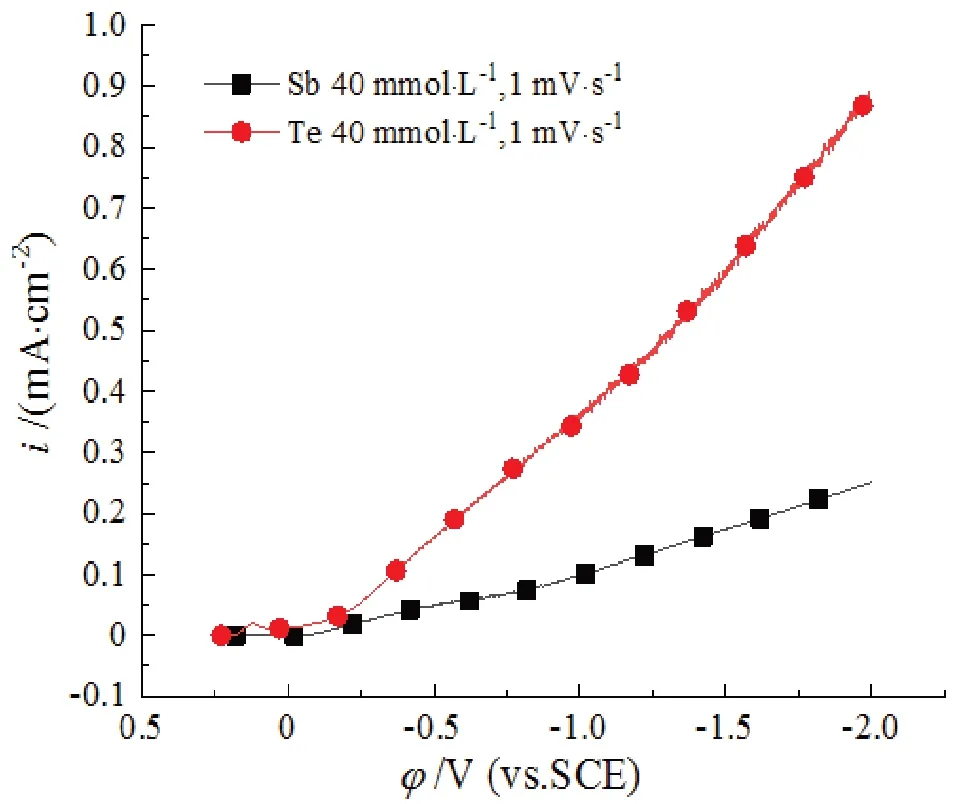
图4 Sb(III)、Te(IV)单元体系的阴极极化曲线对比图Fig.4 Comparison of cathode polarization curves of Sb(III) and Te(IV) single solution system
由图可知,在相同浓度以及电流密度的条件下,Sb(III)离子的还原电位比Te(IV)离子的更负,因此Sb(III)离子更难被还原析出;而在相同电位条件下,Te(IV)单元体系的电流密度大于Sb(III)单元体系的电流密度,即在相同的推动力下,Te(IV)离子的沉积速度比Sb(III)离子更快。由此可见,在同等条件下,Sb(III)比Te(IV)更难被还原,若要通过电化学共沉积的方式获得Sb2Te3(Sb、Te元素原子含量比为1∶1.5)二元合金化合物,需要适当增大镀液中难还原的组分Sb(III)离子的浓度,因此在Sb-Te二元体系中,将Sb(III)、Te(IV)离子的浓度比设置为1∶1。
2.2 薄膜热电材料的制备
图5为Sb-Te二元体系的循环伏安曲线,电位扫描速度为50 mV/s。由图5可得,该二元体系溶液的氧化峰和还原峰上下不对称,面积不相等,因此Sb-Te二元体系在DMSO有机溶剂体系中所进行的氧化还原过程也是完全不可逆的。
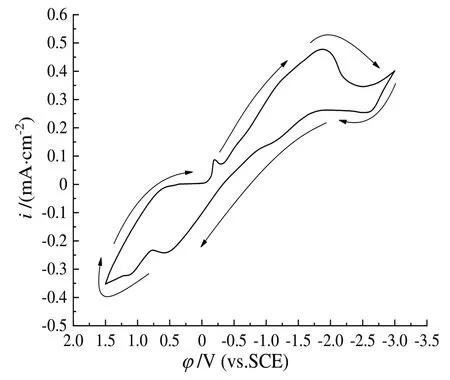
图5 Sb(III)-Te(IV)二元溶液体系的循环伏安曲线Fig.5 Cyclic voltammetry curve of Sb(III)-Te(IV) binary solution system
图6为Au电极在Sb-Te二元体系中测得的阴极极化曲线。由图可得,该体系的电流密度在-0.5 V左右处开始大幅上升,并呈现持续大幅上涨的趋势,阴极极化曲线在测试的电位范围内呈现连续上升趋势,未出现分段上升的现象,说明二元体系中Sb(III)、Te(IV)离子的还原过程并非分步进行,而是同时还原完成共沉积的。结合循环伏安曲线图和极化曲线图,选取-1.2 V、-1.4 V、-1.6 V三个电位,采用恒电位沉积方式进行薄膜热电材料的电化学制备。
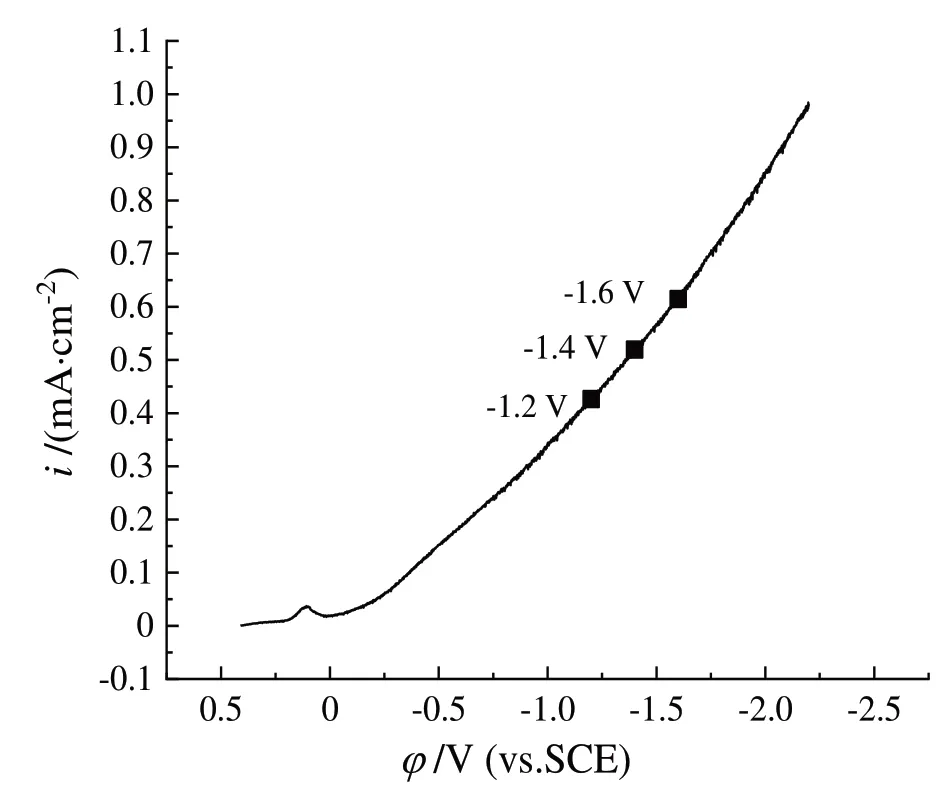
图6 Sb(III)-Te(IV)二元溶液体系的阴极极化曲线Fig.6 Cathode polarization curve of Sb(III)-Te(IV) binary solution system
2.3 薄膜热电材料性能分析
2.3.1 薄膜热电材料的物相分析
图7为在-1.2 V、-1.4 V、-1.6 V三个电位下制备的薄膜热电材料的XRD谱图。
可以看出,不同电位下制备的薄膜材料在2θ=28 °、38 °、45 °等处均可以观察到明显的Sb2Te3二元固溶体合金的衍射峰,说明在这三个沉积电位下制备的薄膜中,均含有Sb2Te3二元固溶体合金,但衍射峰的形状偏矮偏宽,说明Sb2Te3薄膜的电结晶情况不理想。此外,由图7中还可以观察到曲线在2θ=43 °、51 °和74 °等位置处出现明显的Cu单质的衍射峰,这是由于电沉积基体采用的镀金铜片,部分镀层不够致密或局部脱落导致铜基体裸露,因此XRD谱图中检测到了Cu的衍射峰。
2.3.2 薄膜热电材料的形貌分析
图8为在-1.2 V、-1.4 V、-1.6 V三个电位下制备的薄膜热电材料的SEM图。可以看出,在低电位下制备的薄膜的微观形貌为浅鼓包状结晶,随着电位的不断负移,胞状结晶越来越明显,所制备出的薄膜热电材料的表面粗糙度也在不断加大。
2.3.3 薄膜热电材料的组分分析
图9为在-1.2 V、-1.4 V、-1.6 V三个电位下制备的薄膜热电材料的能谱图,测试区域选自扫描电子显微镜图,结果如表2所示。
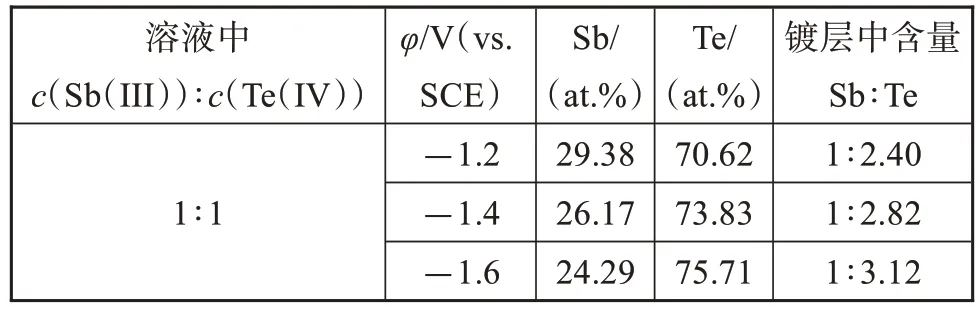
表2 热电薄膜材料的组分分析Tab.2 Component analysis of thermoelectric thin film materials
由图9和表2可得,在c(Sb(III))∶c(Te(IV))为1∶1的溶液体系之中,随着电位的不断负移,Te元素的含量逐渐提高,Sb元素含量逐渐下降,Sb、Te元素在镀层中的原子百分含量的比值不断降低,由1∶2.40下降为1∶3.12。
2.3.4 塞贝克系数测定结果
表3为不同电位下恒电位沉积的热电薄膜材料的塞贝克系数。从表3中可以看出,在-1.2 V至-1.6 V条件下制备的Sb-Te二元材料塞贝克系数均为正值,可证明材料为P型,随着电位的改变,塞贝克系数在35~80 μV/K的范围内变化,塞贝克系数最高的为-1.4 V下制备的薄膜材料,数值为78.8 μV/K。
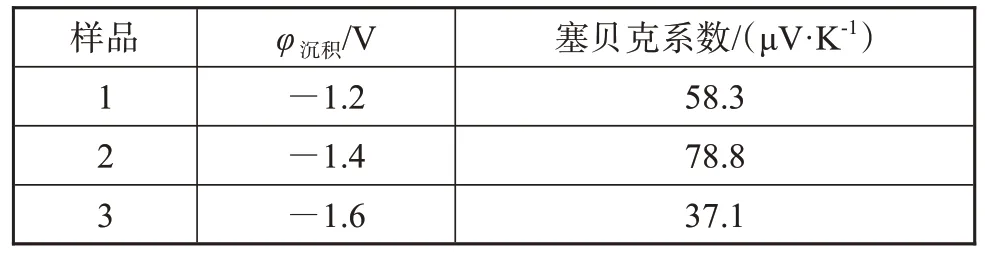
表3 Sb-Te体系热电薄膜材料的塞贝克系数Tab.3 Seebeck coefficient of Sb-Te thermoelectric film materials
3 结 论
通过测试不同溶液体系下的循环伏安曲线和阴极极化曲线,分析了单元和二元体系的氧化还原行为,在此基础上,选择了不同的沉积电位进行恒电位沉积制备材料,通过XRD、SEM、EDS等方法对制备的薄膜热电材料的性能进行了表征,得出以下结论:
(1)Sb(III)、Te(IV)单元及二元体系在DMSO有机溶剂中的氧化还原过程均为完全不可逆过程;
(2)Sb(III)离子在DMSO有机溶剂中于Au电极上的阴极还原电沉积比Te(IV)离子困难;
(3)不同电位下制备出的薄膜热电材料中均含有Sb2Te3二元固溶体合金;随着沉积电位的不断负移,所制备出的薄膜热电材料的表面粗糙度不断加大,薄膜材料中Te元素的占比逐渐提高;不同电位下制备的薄膜热电材料均呈P型,塞贝克系数最高可以达到78.8 μV/K。
