基于PGGB途径优化桫椤组织培养繁殖体系研究
2023-10-17杨卫诚吴高殷车冰洁梁红飞周壁波
杨 姣,杨卫诚,吴高殷,车冰洁,梁红飞,周壁波
(贵州师范大学 生命科学学院,贵州师范大学喀斯特洞穴研究中心,贵阳 550025)
桫椤(Alsophilaspinulosa)属桫椤科(Cyatheaceae)桫椤属(Alsophila),国家二级保护植物,现存唯一的木本蕨类植物,主要生长于温暖潮湿的热带及亚热带地区,中国主要分布于贵州、重庆、四川等地[1]。外形上,桫椤树形高雅飘逸、青翠碧绿,特别是排列整齐的孢子囊群是自然界的奇特景观。桫椤茎、叶含有丰富的黄酮、多酚、多糖、有机酸等活性物质,具有较高的观赏价值和药用价值,运用及开发潜力大[2-5]。然而,桫椤营养叶易被桫椤叶蜂(Rhoptroceroscyatheae)和绿带妒尺蛾(Phthonolbaviridifasciata)幼虫取食和破坏,且其孢子繁殖周期长,生长缓慢。野外调查发现地质表层桫椤幼苗极少,自然更新困难,极大地限制了桫椤种群的发展[6]。植物组织培养技术作为一种高效的无性繁殖方法,具有繁殖周期短、繁殖效率高和不受季节限制等特点。原叶体绿色球状体(prothallus green globular body,PGGB)是由原叶体不断增殖形成似球状的特殊结构。
蕨类植物组织培养中可通过PGGB途径建立高效的繁殖体系,通过相应的生长调节剂及浓度来实现该途径。张港隆等通过芒萁(Dicranopterispedata)孢子诱导萌发的原叶体在6-BA与KT的组合下成功诱导出PGGB,实现PGGB高效增殖,建立了稳定、高效的芒萁繁殖体系[7]。朗月婷等[8]以阴生桫椤(Alsophilalatebrosa)、大叶黑桫椤(Alsophilagigantea)和侯梦丹等[9]以桫椤孢子为外植体,通过不同生长调节剂及比例初步建立其繁殖体系。但孢子萌发率、分化率和生根率均较低,其技术尚未成熟,未能得以推广应用。本文在前人研究基础上进一步优化桫椤孢子萌发条件、配子体增殖、分化以及组培苗移栽等过程,以期构建1个高效的桫椤再生繁殖体系,为进一步探究桫椤体外培养发育机制、新品种培育、规模生产及应用提供技术支持。
1 材料和方法
1.1 桫椤孢子采集与保存
1.2 桫椤孢子预处理与无菌孢子获取
试验前对孢子浸泡12 h后消毒,无菌孢子获取参照郎月婷等[8]的方法,制成无菌孢子悬浮液。
1.3 桫椤孢子诱导配子体
将无菌孢子悬浮液接种至1/8 MS(大量元素浓度为MS的1/8,铁盐、微量元素、有机物浓度与MS等量)基本培养基中,培养基中添加蔗糖20 g/L,琼脂10 g/L,6-BA(0.5,1.0,1.5 mg/L),NAA(0.05,0.10,0.20,0.30 mg/L),以不添加植物生长调节剂作为空白,每皿接种无菌悬浮液400 μL,每个处理接种3皿,重复3次。
培养条件:温度(25±2) ℃,光照强度为3 000 lx,12 h/d,每周观察1次(下同),30 d后记录诱导率。在OLYMPUS SZ体式显微镜(奥林巴斯(深圳)工业有限公司)下任取10个视野观察、记录桫椤孢子诱导配子体情况。
1.4 桫椤配子体诱导PGGB
把处于蝶形原叶体时期的配子体切割成4 mm×4 mm方块,鲜重约0.102 g接种至1/2 MS培养基中,添加6-BA(0.2,0.3,0.5 mg/L),NAA(0.2,0.4,0.6 mg/L),两两对应组合,蔗糖30 g/L,琼脂6 g/L,以不添加植物生长调节剂作为空白,pH 5.8。
每组处理接种10瓶,每瓶接种4个配子体,重复3次。培养2个月后,统计PGGB的诱导率、鲜重、直径以及球状体的颜色与长势情况。
1.5 桫椤PGGB分化
将诱导成功的PGGB分割成直径约为1.2 cm的小球接种于1/2 MS培养基,加入KT(0.3,0.5,0.7 mg/L)、IBA(0.1,0.2,0.3,0.4 mg/L)、蔗糖30 g/L、琼脂6 g/L,以不添加植物生长调节剂作为空白,pH 5.8。每隔15 d用消毒后的喷壶在PGGB表面喷施无菌水0.3 mL。每组接种10瓶,每瓶接种3个,重复3次。培养1个月后统计PGGB分化率、分化的茎芽数,孢子体长势与颜色。
1.6 桫椤孢子体生根
将孢子体接种在1/2 MS培养基中,添加蔗糖30 g/L、琼脂6 g/L、IAA(0.3,0.5,0.7,1.0 mg/L)和IBA(0.3,0.5,0.7,1.0 mg/L),以不添加植物生长调节剂作为空白,pH 5.8。每组接种30瓶,每瓶接种1个,重复3次,培养1个月后统计生根情况。
1.7 桫椤组培苗练苗、移栽培养
将高为5 cm以上的桫椤再生植株在人工气候室进行驯化,练苗1周后移栽至不同灭菌后基质(表1)中,并用保鲜膜覆盖。每组移栽30株,重复3次。每周观察桫椤组培苗的生长情况,培养30 d,统计组培苗成活率。炼苗培养条件:温度(24±2) ℃,湿度(89±2)%,光质为白光,光照周期为16 h/d。
3.大数据管理决策能力。 “互联网+”时代,政府治理主体和对象数据信息呈爆发式增长,局限于传统的监测、管理、应对手段无法摸清经济社会发展及政府行政真实情况,更难做出科学有效的治理决策,只有借助大数据技术获取、处理和分析海量信息,支撑经济管理、政务服务和社会关系塑造等治理活动,才能够保障政府行为的精确度和科学性。
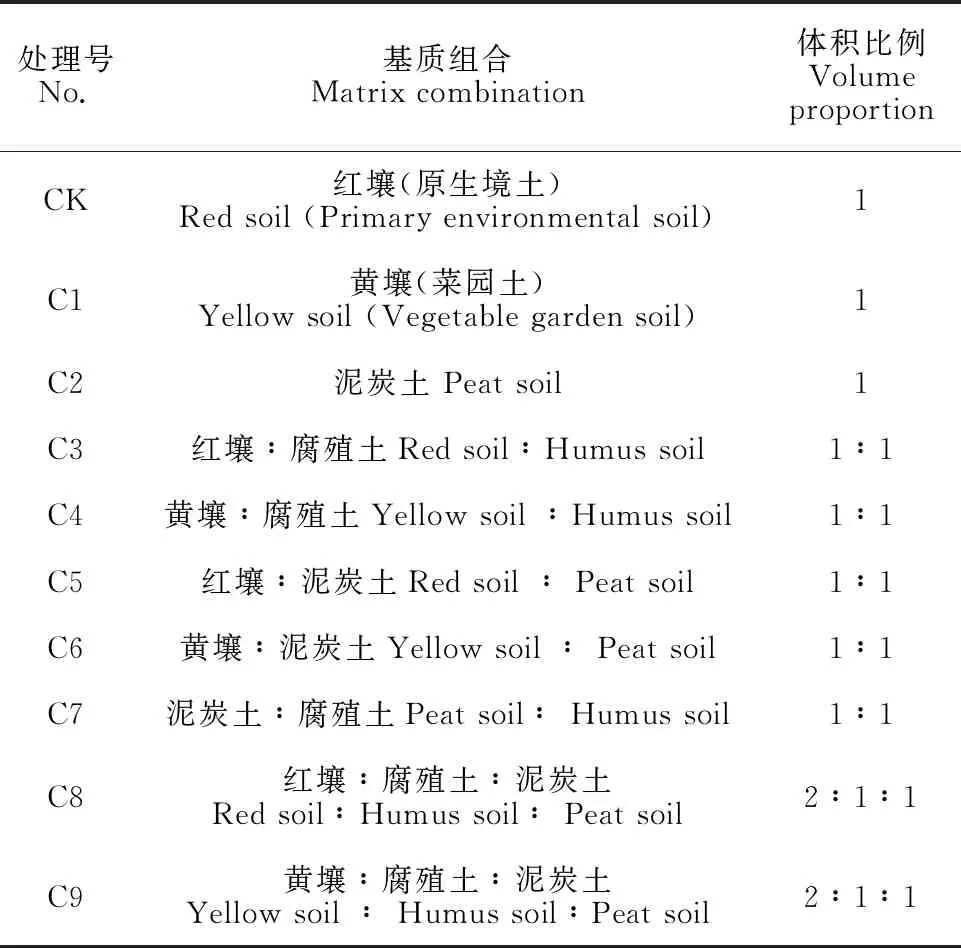
表1 不同的土壤基质及体积比例
1.8 数据收集与统计分析
用Excel 2021和SPSS统计分析数据,Origin作图。数据以平均值±标准误差表示,采用单因素检验进行方差分析,显著性水平P<0.05。
配子体诱导率=视野里诱导形成的配子体数/视野里总的孢子数×100%;PGGB诱导率=诱导形成的PGGB数/接种总数×100%;PGGB分化率=分化的PGGB数/接种总数×100%;生根率=生根的孢子体数/接种的孢子体总数×100%;成活率=成活的桫椤试管苗/移栽的桫椤试管苗×100%;增殖倍数=PGGB的鲜重/0.102,0.102是配子体诱导PGGB前的初始鲜重(g)。
2 结果与分析
2.1 桫椤孢子组织培养过程的形态特征
桫椤孢子(图1,A)接种于培养基上20 d后变绿,诱导形成配子体。首先是绿色细胞增殖发育成丝状体(图1,B),丝状体不断生长发育形成片状体(图1,C)、蝶形原叶体(图1,D)、成熟配子体(图1,E)。

A.孢子;B.丝状体;C.片状体;D.蝶形原叶体;E.成熟配子体;F.PGGB;G.精子器;H.颈卵器;I.配子体分化;J.孢子体;K.孢子体的根;L.幼苗移栽。
配子体后期诱导成PGGB团(图1,F),随PGGB增殖,其配子体腹面上的精子器(图1,G)与生长点上的颈卵器(图1,H)不断发育成熟,经喷施无菌水后,促进受精过程,而生长出无拳卷的叶、叶脉呈二叉状分枝形成孢子体(图1,I),在生根培养基上诱导孢子体生根,并将桫椤再生植株移栽在基质中(图1,J、图1,K和图1,L)。
2.2 桫椤孢子诱导配子体
不同植物生长调节剂对配子体诱导率、诱导时间差异显著(P<0.05)(表2)。同一NAA浓度下,配子体诱导率随6-BA浓度升高逐渐下降,诱导时间延长。同一6-BA浓度下,配子体诱导率随NAA浓度升高整体上呈先升高后降低的趋势,在高浓度6-BA中诱导时间延长,然而,在L2中诱导率最高(64.62%),诱导时间最少(23 d),均与CK差异显著(P<0.05)。

表2 不同生长调节剂浓度组合对桫椤孢子诱导配子体的影响
2.3 配子体诱导PGGB
将处于蝶形原叶体时期的配子体接种于Z1~Z9培养基中诱导PGGB(图2),PGGB诱导率(100%)不具显著性差异(P>0.05),均显著高于CK(P<0.05),其增殖倍数、鲜重差异显著(P<0.05),PGGB直径差异不显著(P>0.05)。同一6-BA浓度下,随着NAA浓度上升,PGGB鲜重、PGGB直径、PGGB增殖倍数均整体下降;同一NAA浓度下,6-BA的浓度上升,PGGB鲜重、PGGB直径、PGGB增殖倍数整体呈现上升趋势。其中,Z5组PGGB鲜重、PGGB直径、PGGB增殖倍数最高,并且与CK有显著差异(P<0.05,见表3)。因此,选取1/2 MS+ 0.3 mg/L 6-BA+0.4 mg/L NAA作为配子体诱导PGGB适宜培养基。

图2 Z1~Z9对应不同培养基下诱导成功的PGGB
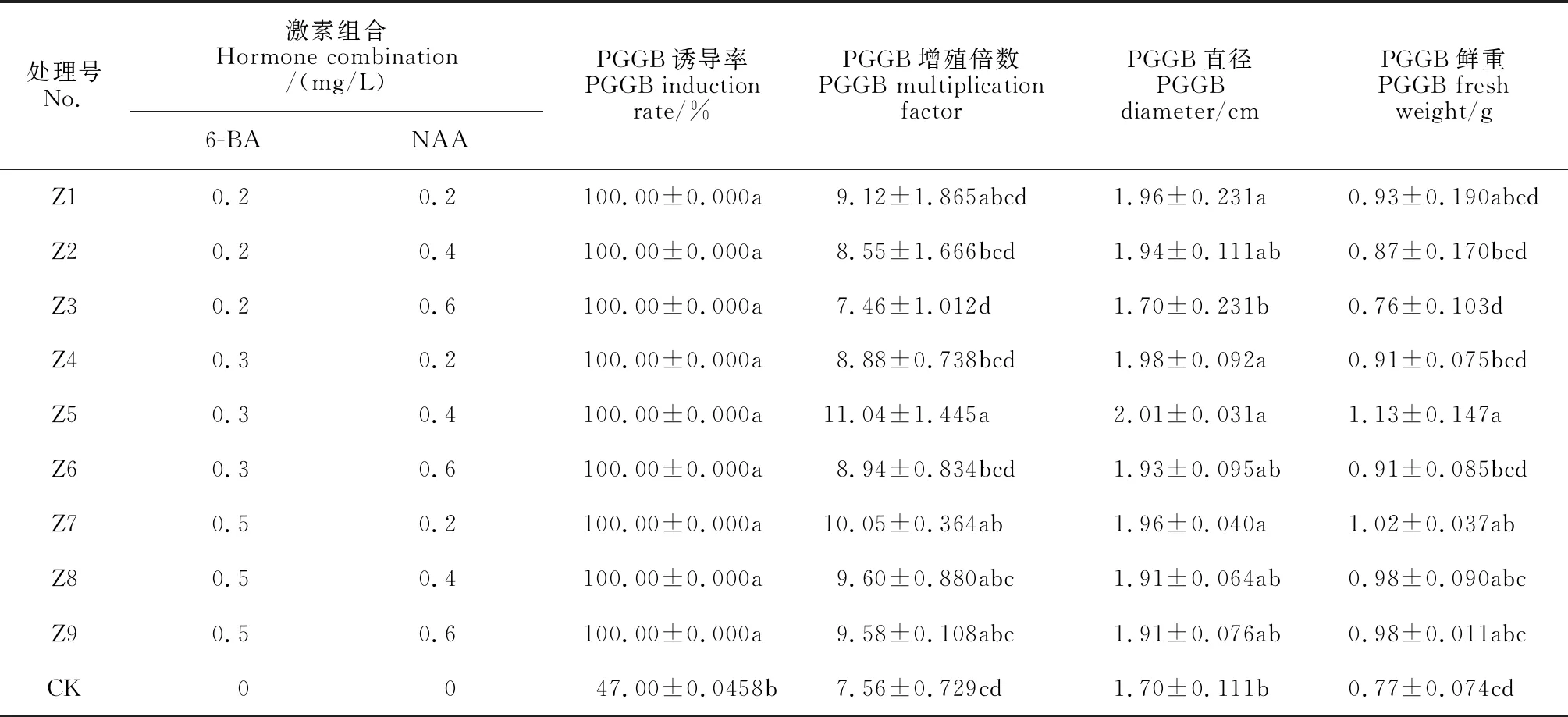
表3 不同生长调节剂浓度组合对PGGB诱导增殖的影响
2.4 植物生长调节剂对PGGB分化的影响
将PGGB转接至H1~H12分化培养基中,其分化率、总茎芽数、株高、茎叶长以及宽均具显著差异(P<0.05)(图3、表4)。随着KT浓度增加,分化率、分化茎芽数、株高、茎叶的长及宽总体上呈现先增加后减少。当KT浓度小于0.5 mg/L时,PGGB分化率、分化茎芽数随着IBA浓度升高而增加;相反,当KT浓度大于0.5 mg/L时,其随IBA浓度升高而降低。综上所述,PGGB在H4组(1/2 MS+0.3 mg/L KT +0.4 mg/L IBA)培养基中的分化率、总茎芽数、株高、茎叶的长及宽是最好的,并且与CK均有显著性差异(P<0.05)。

图3 H1~H12对应不同的培养基的PGGB分化

表4 不同生长调节剂浓度组合对PGGB分化率、总茎芽、株高、茎长及茎宽的影响
2.5 生长调节剂对桫椤孢子体生根及生长发育的影响
将分化的的桫椤孢子体接种于F1~F8生根诱导培养基中,其生根率均为100%(表5),显著高于CK(33.3%)(P<0.05)。随着IBA浓度增加,桫椤植株的根数、根长、株高、叶片数量、叶长、叶宽呈现上升趋势,均在F4中最高;而随着IAA浓度增加,桫椤植株的根数、根长、株高、叶片数量、叶长、叶宽呈现下降趋势,但其根长、生根数、株高、叶片数量、叶长及宽无显著性差异(P>0.05)(表6)。由此可知,H4组(1/2 MS+1.0 mg/L IBA)是桫椤孢子体最适合的生根诱导及生长发育培养基(图4)。

F3、F4孢子体诱导根有分支、有根毛。
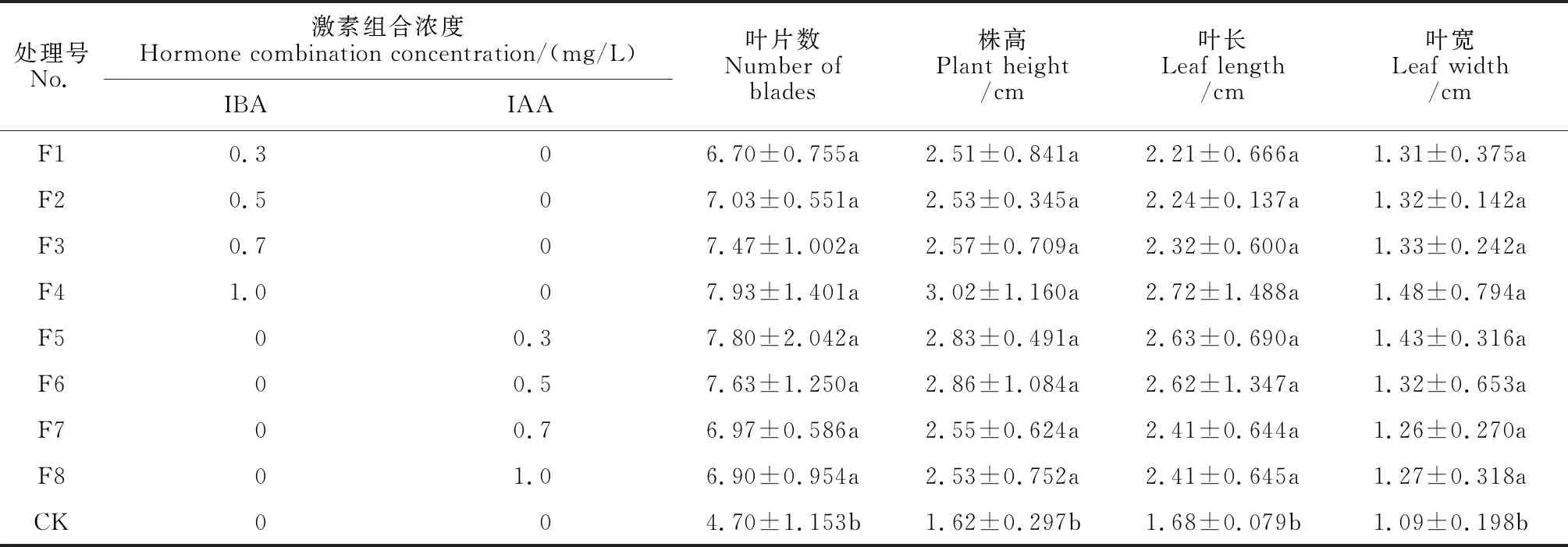
表6 不同生长调节剂浓度组合对桫椤孢子体叶片数量、株高、叶长以及叶宽的影响
2.6 桫椤组培苗练苗、移栽培养
将高为5 cm以上的桫椤组培苗移栽至不同基质中,结果(图5)表明不同基质对桫椤组培苗成活率具有显著性差异(P<0.05)。

A.黄壤∶泥炭土(1∶1)∶桫椤幼苗叶片边缘变黄;B.红壤基质的桫椤幼苗;C.红壤∶泥炭土∶腐殖土(2∶1∶1)的桫椤幼苗。
其中,桫椤组培苗在C8基质中成活率最高达96.3%(表7),显著高于C2基质,与CK、C1、C3~C9无显著差异(P>0.05),但其叶片翠绿,生长势较强。因此,选择C8中红壤∶腐殖土∶泥炭土(2∶1∶1)的基质作为桫椤组培苗适宜的移栽基质。

表7 不同基质对桫椤组培苗移栽的影响
3 讨 论
研究利用PGGB途径与组织培养技术相结合的繁殖方式,以桫椤孢子为外植体进行优化,并构建桫椤快繁体系,提高配子体诱导率、PGGB诱导率、PGGB分化率、孢子体生根率,最后进行移栽。前人研究表明,桫椤孢子诱导配子体、配子体诱导PGGB及分化、孢子体生根等过程受诸多外部因素影响,如温度、湿度、光照强度、光周期、培养基种类、无机盐浓度、糖的种类以及浓度、生长调节剂种类以及浓度、pH值等[10-13]。其中,植物生长调节剂对蕨类植物孢子组织培养过程中的发育及生长具有重要作用。
PGGB途径作为蕨类植物组织培养中特有的繁殖路径,具有用材少、繁殖效率高和增殖系数大等特点。通过PGGB途径来构建桫椤的组培体系,在桫椤配子体诱导PGGB、分化、生根的过程中,生长调节剂的种类与浓度对其诱导、分化、生根有重要作用。赤霉素(gibberellins,GA)、成精子囊素(anteridiogen,An)、细胞分裂素(cytokinin,CK)、生长素(auxin,AUX)、茉莉酸(jasmonic acid,JA)、乙烯(ethylene,Eth)、脱落酸(abscisic acid,ABA)、油菜素内脂(Brassinolide,BR)等不同种类的植物生长调节剂能不同程度地影响蕨类植物孢子萌发、配子体的生长发育、孢子体的形成等过程[14-16]。生长素激活细胞,促进有丝分裂;细胞分裂素能刺激细胞分裂和生长过程;赤霉素协调细胞分裂的过程、性别决定,促进了蕨类植物配子体腹面的精子器形成[17]。细胞分裂素6-BA、生长素NAA在蕨类植物组培中常搭配使用于孢子萌发与配子体的增殖。王阳[18]在研究东北对开蕨(Phyllitisscolopendrium)的组培中发现6-BA对孢子萌发、原叶体增殖中有明显促进作用,特别是0.5 mg/L 6-BA的增殖效果最好;但是,6-BA的浓度越大、原叶体增殖效果不佳、鲜重越小。陈朋等[19]的研究表明6-BA浓度低于1.5 mg/L可观察到粤紫萁(Osmundamildei)孢子萌发,并且6-BA在0.5~1.0 mg/L范围与低浓度NAA组合有利于原叶体增殖,6-BA大于1.5 mg/L时则抑制其增殖,这与本研究桫椤孢子诱导配子体结果一致,表明低浓度6-BA与NAA组合对孢子诱导配子体的诱导率及诱导时间具有显著促进作用。实验中还发现KT、ZT虽然都能使孢子诱导配子体,但存在诱导时间较长,诱导时会出现有绒毛状假根,原叶体增殖停滞,颜色黄绿。然而,0.5 mg/L 6-BA与0.1 mg/L NAA或者0.1 mg/L 2,4-D组合时,都能一定程度上缩短了诱导时间;但是,6-BA与 NAA配合时,配子体颜色碧绿、长势好;而6-BA与2,4-D组合时,配子体颜色变淡,不仅出现假根现象,且部分出现褐化;这与Bonomo等[20]对树蕨(Alsophilaodonelliana)的孢子萌发、配子体发育研究结果相似,在6-BA的浓度为0.01,0.1,1.0 mg/L时,促进了原叶体的形成;0.1 mg/L的2,4-D会缩短丝状体蛋白的形成而促进了丝状体的形成。就PGGB诱导而言,与朗月婷等[8]研究阴生桫椤GGB诱导结果一致,低浓度的6-BA与NAA组合能够缓解PGGB的原叶体碎小、假根现象,PGGB诱导率为100%,特别是0.3 mg/L 6-BA与0.4 mg/L NAA组合使PGGB直径、增殖倍数和鲜重达到最佳,这可能与不同蕨类植物诱导GGB或者PGGB时,对激素种类及浓度适应度不同有关。
在研究蕨类植物的世代交替的繁殖过程中,配子体向孢子体转化的关键是成熟配子体上的精子器与颈卵器能够进行受精作用,故PGGB进行分化前,受精是分化的关键。过去研究表明,赤霉素、成精子囊素、光等因素会影响精子器的形成[21-22]。本研究发现KT是影响PGGB分化的主要因子,与张艳琴等[23]研究铁线蕨(Adiantumcapillus-veneris)孢子体的产生以及朗月婷等[8]研究阴生桫椤GGB分化的结果相似,KT的浓度越大,分化率降低。前人研究表明,不加任何激素也会诱导孢子体的分化。比如粤紫萁[19]、大叶黑桫椤[24]。还有研究表明,波斯顿蕨(Nephrolepisexaltata‘Bostoniensis’)的GGB在1.2 mg/L 6-BA与0.4 mg/L NAA的浓度下能分化出大量孢子体[25],而桫椤配子体在0.1 mg /L NAA 与0.5 mg /L BA组合下分化出大量孢子体[12],这可能与分化前配子体增殖或者PGGB诱导使用的激素不同有关,也与不同物种其内部激素的差异有关。试验中还发现,除了KT能促进PGGB的分化外,ZT也能影响PGGB的分化,不过ZT诱导分化时,会使PGGB增大、分化茎叶少、孢子体不长高、孢子体的叶片变黄。低浓度KT与IBA组合时,IBA的浓度越高,越能促进PGGB分化以及茎叶、茎芽的长及宽、孢子体株高的伸长。
桫椤的孢子体分化后,需对其进行生根诱导,而生长素IBA、NAA、IAA等是植物再生苗常用的生根诱导激素。叶秀仙等[26]与刘偲[27]等报道了生长素NAA对鹿角蕨(Platyceriumwallichii)孢子体的生根有促进作用,并且NAA的浓度越大,既能缩短生根时间,也能促进生根率以及生根数。桂皮紫萁孢子体在IBA 0.5 mg/L中生根率最高,并且生根率随IBA浓度升高呈先增加后减少趋势[28]。大叶黑桫椤在IAA与NAA组合下的生根率最佳,而单一激素IAA的浓度越高,生根数越多、根长越长[8],这与本研究中IAA诱导桫椤孢子体生根的结果一致。许姗[29]在槲蕨(Drynariaroosii)组培中发现,槲蕨在IBA激素下诱导的生根率、生根数、根长有显著差异,其浓度越高,效果越好与本研究桫椤孢子体在IBA诱导生根情况一致。本研究还表明,桫椤孢子体在IAA与IBA组合下诱导生根时,其生根率低,茎芽不伸长,而茎芽下的配子体继续增殖,不如单一的IBA或者IAA效果好,而质量浓度为1 mg/L的IBA,生根率100%,根数、茎叶数、茎芽长、宽以及株高都明显增高,并且根毛丰富、有分支,为炼苗、移栽提供好的基础。
前人研究表明,炼苗基质对桫椤组培苗的成活率影响较大,加上桫椤喜潮湿环境,对其引种、移栽时对湿度、温度的要求高。侯梦丹等[9]使用泥炭土、菜园土、营养土不同配比对桫椤组培苗进行移栽炼苗,发现其移栽后幼苗成活率很低;朗月婷等[8]在泥炭土、菜园土中成功移栽阴生桫椤,其成活率达60%以上;而在同样基质上对大叶黑桫椤(A.gigantea)组培苗的移栽却没有成功。这可能因为不同的桫椤科植物的内部输水系统与根系对不同土壤基质的敏感度不同,也可能与移栽时组培苗的质量和移栽有关。然而,本试验在前人研究基础上,进一步优化移栽炼苗基质,采用赤水桫椤保护区原生境的红壤与腐殖土和泥炭土进行混合对桫椤再生苗进行移栽,其成活率大大提高,这可能与红壤作为桫椤生境土壤,其理化性质和微生物类型对桫椤组培苗的生长具有促进作用有关,从而提高桫椤组培苗移栽成活率。
4 结 论
本研究中桫椤PGGB途径不仅繁殖系数大,而且较稳定、高效,出苗率大。(1)1/2 MS+6-BA 0.5 mg/L+NAA 0.1 mg/L是孢子诱导配子体的最适培养基;(2)1/2 MS+6-BA 0.3 mg/L+NAA 0.4 mg/L是诱导PGGB最合适的培养基;(3)PGGB分化最佳的培养基是1/2 MS+KT 0.3 mg/L+IBA 0.4 mg/L;(3)桫椤孢子体在1/2 MS+IBA 1.0 mg/L培养基里生根诱导效果最好;(4)桫椤组培苗移栽在基质红壤∶腐殖土∶泥炭土=2∶1∶1中成活率最高,且生长良好。
