重庆市1 755 例抗精神病药物药品不良反应分析*
2023-10-17毛文星曾令高
毛文星,王 彦,邓 莉,陈 竹,唐 华,曾令高△
(1. 重庆市食品药品检验检测研究院·国家药品监督管理局麻醉精神药品质量监测重点实验室,重庆 401121;2. 重庆市药品不良反应监测中心,重庆 401120)
精神分裂症是一种严重的慢性致残性精神障碍,以服用抗精神病药物(APDs)治疗为主[1]1-5。APDs根据药理作用可分为典型APDs和非典型APDs,对患者的阴性症状、阳性症状和认知障碍有不同程度的疗效。精神分裂症的病程漫长、病情难控,需要长期甚至终身服药[2]。APDs 导致的药品不良反应(ADR)极大地影响患者的总体功能结局和生活质量,是患者中断治疗的重要原因[3]。药品上市后的ADR 监测是关系用药安全、有效的重要环节,ADR 自发呈报可覆盖较广范围的用药人群,有利于及早发现潜在的ADR 信号,是目前运用较广的监测方式[4]。为了解近年重庆地区APDs 致ADR 的特征,本研究中对重庆市2019 年至2022 年APDs 致ADR 的报告进行回顾性分析,为促进临床合理用药、降低患者用药风险提供参考。现报道如下。
1 资料与方法
1.1 资料来源
收集2019 年至2022 年重庆市医疗机构、药品经营企业等上报至国家药品不良反应监测系统的APDs 致ADR 报告,提取关联性评价结果为“肯定”“很可能”“可能”的报告1 755份。
1.2 方法
按《中华人民共和国药典临床用药须知(2015 年版)》的药品分类纳入本次分析的APDs;ADR 名称和累及系统/器官以世界卫生组织不良反应术语集(WHOART)为基础,参照《药品不良反应术语使用指南(2016年版)》的评定标准进行规整和分类,并根据《药品不良反应报告和监测工作手册》对ADR 的严重程度进行分类;年龄段划分参考《国家药品不良反应监测年度报告(2020)》的分层标准。
1.3 统计学处理
采用Microsoft Excel 2016 软件中的工具表汇总和校对数据,分析患者性别、年龄、药物使用情况、ADR 严重类型及转归、累及系统/器官、临床表现等信息。计数资料以例数及构成比进行统计描述。
2 结果
2.1 患者性别与年龄分布
重庆市2019 年至2022 年的1 755 份APDs 致ADR报告均由医疗机构呈报,涉及患者1 755例,其中2019年376 例,2020 年306 例,2021 年539 例,2022 年534 例。男997 例(56.81%),女758 例(43.19%),男女性别比为1∶0.76;患者年龄6 个月至91 岁,15~44 岁青壮年780例(44.44%)。详见表1。

表1 患者年龄与性别分布(n=1 755)Tab.1 Distribution of patients' age and gender(n=1 755)
2.2 药物使用情况
1 755份ADR报告中,治疗方式为单药治疗1 443份(82.22%),联合用药312 份(17.78%)。单药治疗患者中,怀疑药品为非典型APDs的多于典型APDs(1 296例比147 例),上报频次排名前3 的依次为利培酮、奥氮平和阿立哌唑,详见表2。联合用药中,二联用药260 例(14.81%),三联用药39 例(2.22%),四联用药10 例(0.57%),五联用药1 例(0.06%),六联用药2 例(0.12%);APDs + APDs 联用的患者188 例(10.71%),APDs 与其他种类药物联用的患者124 例(7.07%)。其中,其他种类药物以抗癫痫药、镇静催眠药、抗抑郁药等精神障碍用药最常见。

表2 抗精神病药物单用患者的用药情况(n=1 443)Tab.2 Medication of patients treated with single APDs(n=1 443)
2.3 ADR 严重程度及转归
本研究中报告的ADR 均为首次上报,严重程度以一般ADR 为主(88.49%);202 例(11.51%)报告为严重ADR,其中98 例(5.58%)导致延长住院时间,97 例(5.53%)导致其他重要医学事件,6 例(0.34%)危及生命,1例(0.06%)导致死亡。患者经减药、停药或对症处理后,临床ADR 症状大多在短期内好转(79.94%)和痊愈(12.08%),ADR 转归情况还有未好转(5.01%)、不详(2.74%)、有后遗症(0.17%)、死亡(0.06%)。详见表3。

表3 ADR严重程度及转归分布(n=1 755)Tab.3 Distribution of severity and outcome of ADRs(n=1 755)
2.4 ADR 发生时间
1 755份ADR报告中,上报的ADR发生时间大多集中在用药30 d 内(56.24%)。APDs 导致的ADR 发生时间跨度较广,其中178 例(10.14%)患者用药当日即发生ADR,57 例(3.25%)患者用药1 年后才报告ADR,最长的1例达15年。详见表4。
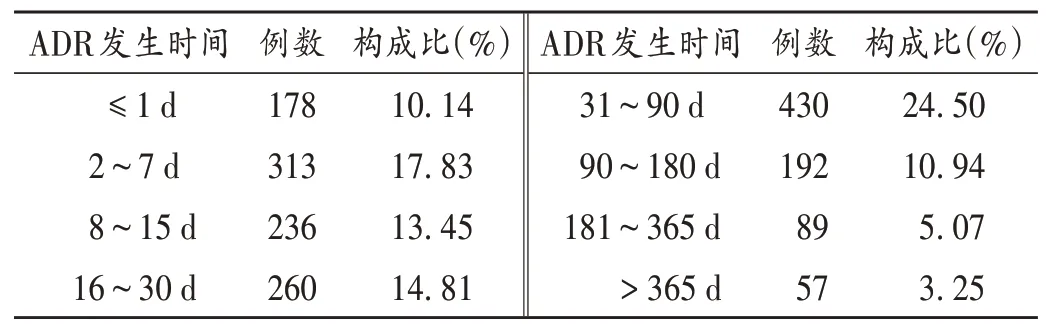
表4 ADR发生时间(n=1 755)Tab.4 Occurrence time of ADRs(n=1 755)
2.5 ADR 累及系统/器官及临床表现
1 755 份报告共发生2 199 例次ADR,ADR 累及多个系统/器官,以神经系统损害最常见(48.48%),其次为消化系统损害(17.46%)和心血管系统损害(9.64%);临床表现主要为锥体外系反应(19.74%),其次为流涎(6.73%)、心动过速(5.28%)、便秘(4.14%)、肌张力亢进(3.73%)、震颤(3.37%)、体质量增加(3.32%)、嗜睡(2.96%)、静坐不能(2.91%)等。详见表5。
3 讨论
3.1 谨慎选择治疗药物
重庆市2019年至2022年的APDs致ADR 报告涉及药品品种基本涵盖了目前国内上市的常用ADPs。典型APDs根据化学结构可分为以氯丙嗪等为代表的吩噻嗪类药物,以氟哌啶醇等为代表的丁酰苯类药物,以氯普噻吨等为代表的硫杂蒽类药物,以舒必利等为代表的苯甲酰胺类药物,非典型APDs 主要包括利培酮、奥氮平、阿立哌唑等,是目前临床治疗精神分裂症的一线用药。非典型APDs 氯氮平因其较高的粒细胞缺乏症发生率,目前已退居二线,主要用于治疗难治性精神分裂症[1]105。典型APDs 具有较强的多巴胺D2受体阻断作用,治疗阳性症状效果较好;非典型APDs 对5 - 羟色胺、多巴胺、肾上腺素、胆碱和组胺受体有不同程度的阻断作用,既能治疗精神分裂症的阳性症状,又能有效改善阴性症状和认知障碍,且锥体外系反应较轻[5]。APDs 药理作用广泛,机制各异,导致的ADR 也不同,治疗精神分裂症应根据临床症状进行个体化选择。
本研究中报告的锥体外系反应、心动过速等高频率ADR 与多项研究结果[6-7]相似,是导致患者依从性低、预后效果不良的重要原因。ADR 严重程度多为一般,报告的236 例新的ADR 转归情况总体较理想。其中1 例患者氯氮平治疗效果不佳,换用氟哌啶醇后引发恶性综合征,导致死亡。该ADR 是APDs 引起的最严重症状之一,临床较少见。所有APDs 均有诱发恶性综合征的可能,其中氟哌啶醇报道最多,且多种APDs 合用风险更大[8]。近年来,有研究尝试将作用机制不同的APDs合用,以求达到改善多种症状或难治性精神分裂症的效果,但其有效性及安全性仍不明确[9]。《中国精神分裂症防治指南(第二版)》指出,只有在单药无效或合并其他问题时才考虑联合用药[1]1-5。本研究中312 例患者的治疗方式为联合用药,形式以APDs + APDs 为主(10.71%),其余患者联用药物多为缓解共患疾病或ADR 症状。不同种类APDs 的联用很可能是导致患者体内药物浓度高的重要原因之一,极大地提高了ADR 发生风险。故应充分掌握药物的药学知识,临床应用时酌情选择合理的联合用药方案。
本研究中发现,有患者换用同品种、不同厂家生产的APDs 后出现ADR。国产仿制奥氮平导致的心电图异常发生率明显高于原研药[10]。带量采购的常态化促进APDs 仿制药物用量增加,而APDs 多治疗指数较窄,药物设计空间有限,药学等效方面的微小差异均可导致严重ADR 发生,不同厂家药品之间的替代是否安全、有效,尚缺乏明确的临床评价,故该类药物治疗安全、有效时应尽量避免换用其他厂家的药品[11-12]。
3.2 加强ADR 监测
报告数量是衡量药品ADR 监测工作水平的重要指标,本研究中2022 年APDs 致ADR 呈报数较2019 年增加42.02%,一定程度上表明重庆市近年的ADR 监测工作颇有成效。上报机构均为医疗机构,这可能与精神分裂症患者较其他疾病患者住院治疗率相对较高、APDs多为处方药等因素有关,患者在医院接受用药治疗后的不良症状可被医护人员第一时间发现并处理。该患者群体多存在认知障碍,依从性低,因神经系统ADR 易与原发疾病混淆,心血管系统、代谢及内分泌系统损害等隐匿性较强的慢性症状需检验才能判断,故可能出现低归因、少报、慢报等情况。本研究中57 例患者药物治疗1 年后上报ADR,非住院患者及家属缺乏对ADR的识别能力和重视度而导致处理不及时是重要原因之一。故服药患者的临床管理亟须开展定期的个体化ADR监测,以确保长期治疗方案的合理性。
由于男女激素分泌、脂肪分布、肝药酶活性等生理结构的差异,不同性别患者的药物疗效和ADR 表现有差异。研究表明,女性患者服用APDs 后锥体外系反应、代谢综合征、催乳素增加等ADR 发生率较高[13]。而本研究中男性患者占比高于女性,可能与重庆市男性精神分裂症患者比例较高、服用APDs 的人数较多等有关,与上海市长宁区某医院的研究结果一致[6]。本研究中ADR 报告患者年龄符合精神分裂症起病时间特征,主要为15~44岁青壮年。值得注意的是,青少年精神疾病的患病人数逐年增加,由于解剖、生理、生化等特点,儿童及青少年较成人更易发生ADR,且危害更大。目前,美国食品和药物管理局(FDA)批准阿立哌唑、奥氮平、喹硫平、利培酮、帕利哌酮和鲁拉西酮可用于儿童及青少年精神分裂症的治疗,而上述多种药物在我国儿童及青少年中尚未获批相应适应证,超药品说明书用药情况普遍[14-15]。本研究中监测到114 例未成年患者发生ADR,警示儿童及青少年精神分裂症患者应作为重点监测人群,科学选择药物、剂量与剂型,充分权衡风险与获益。
精神分裂症的治疗不仅要控制精神疾病的症状,还需改善药物长期治疗引起的ADR 和躯体共病,以提高患者的总体功能结局。故临床治疗应遵循个体化用药,加强该群体的全面ADR 监测,及早诊断和干预,保障患者用药安全、有效。
