沙库巴曲缬沙坦联合芪苈强心胶囊药物治疗慢性心力衰竭的疗效及对其心功能、血清炎性指标的影响
2023-10-10司华峰杜艳丽魏琦
司华峰,杜艳丽,魏琦
许昌市人民医院心内科,河南 许昌 461000
慢性心力衰竭(chronic heart failure,CHF)是各种病因所导致心脏疾病的终末阶段,是一种复杂的临床综合征,也是心血管疾病终末期表现和最主要死因[1-2]。近些年,随着老龄化进程的加快,CHF 患病率日渐增加,超过65岁人群患病率为6%~10%,5年病死率高达50%,给其生命健康带来极大威胁[3]。国外最新指南推荐,沙库巴曲缬沙坦为治疗CHF 首选药物,其可同时拮抗血管紧张素受体、抑制脑啡肽酶而发挥抗心衰作用,显著降低病死风险[4]。中医药作为CHF 重要辅助疗法,在其治疗中具有不可替代优势。已有相关研究表明,芪苈强心胶囊可益气温阳、通络活血、消肿利水,同时能够减缓心室重构、抑制炎症反应、增强心肌收缩力[5]。相关研究指出,组织蛋白酶S (CatS)、可溶性尿激酶型纤溶酶原激活物受体(suPAR)与CHF 病情进展密切相关[6]。为此,本研究以CatS、suPAR 为切入点,旨在探讨沙库巴曲缬沙坦联合芪苈强心胶囊治疗CHF 临床疗效,现将结果报道如下:
1 资料与方法
1.1 一般资料 经本院伦理委员会审核批准,选取2020年4月至2022年6月许昌市人民医院心内科收治的88例CHF患者为研究对象。纳入标准:符合CHF诊断标准[7],如有超声心动图异常、心腔扩大、心脏杂音、第三心音等心脏功能或结构异常等客观证据,胸腔积液、肝脏肿大、心动过速、呼吸急促、外周水肿等体征,呼吸困难、休息或运动时出现下肢水肿、乏力等症状;具有收缩性或舒张性心力衰竭特征;病情稳定;近1 周内未服用改善心功能药物;NYHA 分级Ⅱ~Ⅳ级;患者及家属知晓本研究,并签署知情同意书。排除标准:急性心力衰竭;瓣膜性心肌病;伴有先天性心脏病;合并恶性肿瘤;认知功能障碍;既往接受心脏介入或搭桥手术者;对本研究药物过敏者;患有严重精神疾病,不愿配合者。按随机数表法将患者分为常规组和联合组,每组44 例。两组患者的性别、年龄、纽约心脏病学会(NYHA)分级和体质量指数比较差异均无统计学意义(P>0.05),具有可比性,见表1。
表1 两组患者的一般资料比较[例(%),±s]Table 1 Camparison of general information between two groups of patients[n(%),±s]
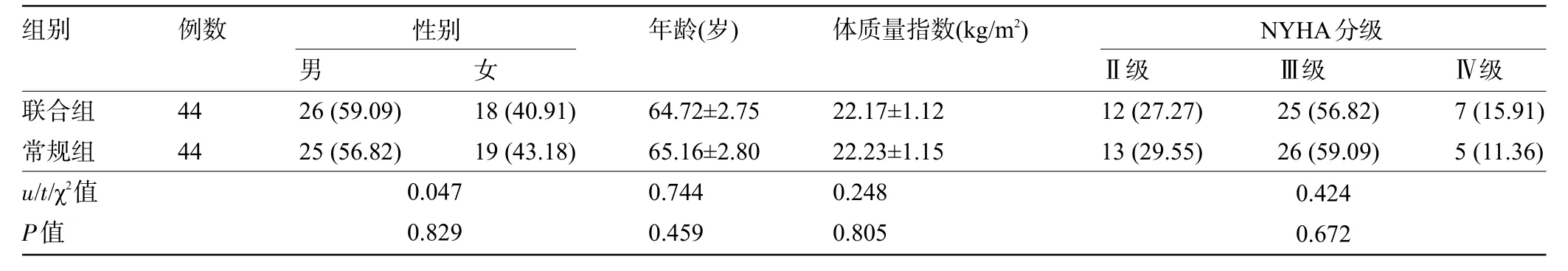
表1 两组患者的一般资料比较[例(%),±s]Table 1 Camparison of general information between two groups of patients[n(%),±s]
组别例数性别年龄(岁)体质量指数(kg/m2)NYHA分级男女联合组常规组u/t/χ2值P值44 44 26(59.09)25(56.82)18(40.91)19(43.18)0.047 0.829 64.72±2.75 65.16±2.80 0.744 0.459 22.17±1.12 22.23±1.15 0.248 0.805Ⅱ级12(27.27)13(29.55)Ⅲ级25(56.82)26(59.09)Ⅳ级7(15.91)5(11.36)0.424 0.672
1.2 治疗方法 两组患者均给予相应对症治疗,如利尿剂、抗血小板聚集、硝酸酯类、他汀类、β受体阻抗剂等。常规组患者同时采用沙库巴曲缬沙坦(生产厂家:北京诺华制药,国药准字J20171054,规格:每片100 mg)治疗,起始剂量100 mg/次,2 次/d,根据患者耐受情况,每2~4 周倍增1 次,直至达到每次200 mg,2 次/d 的目标维持剂量。联合组患者同时给予沙库巴曲缬沙坦(给药方法同常规组)联合芪苈强心胶囊(生产厂家:石家庄以岭药业,国药准字Z20040141,规格:0.36 g,36 粒)治疗,4 粒/次,3 次/d。两组均连续治疗3个月。
1.3 观察指标与评价(检测)方法 (1)疗效[8]:显效:临床症状、体征消失,NYHA分级改善>2级;有效:临床症状、体征明显改善,NYHA 分级改善1~2 级;无效:未达上述标准。(2)左室射血分数(LVEF)、心脏指数(CI)、每搏输出量(SV):治疗前、治疗3个月后采用彩色多普勒超声诊断仪(美国GE公司,型号:Voluson E8)测定CI、SV,并 计算LVEF。(3)肿瘤 坏 死因子-α(TNF-α)、超敏C 反应蛋白(hs-CRP)、白细胞介素-6(IL-6)、IL-1β:治疗前、治疗3 个月后采集两组患者清晨4 mL空腹静脉血,3 000 r/min,离心10 min,取上清液,置于低温环境待检。以酶联免疫吸附法测定。(4)高敏肌钙蛋白(hs-TnT)、组织蛋白酶S(CatS)、可溶性尿激酶型纤溶酶原激活物受体(suPAR)、氨基末端脑钠肽前体(NT-proBNP):取上述血清标本,以酶联免疫吸附法测定hs-TnT、CatS、suPAR,以电化学发光法测定NT-proBNP。(5)不良反应:统计治疗期间两组患者的嗜睡、头晕、口干等不良反应发生情况。
1.4 统计学方法 应用SPSS22.0统计学软件分析数据。计量资料符合正态分布,以均数±标准差(±s)表示,组内比较行配对t检验,组间比较行独立t检验,计数资料比较行χ2检验,等级资料行Ridit 分析,u检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者的临床疗效比较 联合组患者的治疗临床总有效率为95.45%,明显高于常规组79.55%,差异有统计学意义(χ2=5.091,P=0.024<0.05),见表2。

表2 两组患者的临床疗效比较(例)Table 2 Comparison of clinical efficacy between two groups of patients (n)
2.2 两组患者治疗前后的心功能比较 治疗3 个月后,两组患者的LVEF、CI、SV明显高于治疗前,且治疗3 个月后,联合组患者的LVEF、CI、SV 明显高于常规组,差异均有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后的心功能指标比较(±s)Table 3 Comparison of cardiac function indicators between two groups of patients before and after treatment(±s)

表3 两组患者治疗前后的心功能指标比较(±s)Table 3 Comparison of cardiac function indicators between two groups of patients before and after treatment(±s)
注:与本组治疗前比较,aP<0.05。Note:Compared with that before treatment in this group,aP<0.05.
组别例数LVEF(%) CI(L/min) SV(mL)联合组常规组t值P值44 44治疗前37.16±4.27 36.63±4.85 0.544 0.588治疗3个月后66.92±5.03a 59.17±4.92a 7.306 0.001治疗前1.63±0.49 1.68±0.51 0.469 0.640治疗3个月后3.74±0.68a 2.91±0.57a 6.205 0.001治疗前41.58±5.93 42.27±4.86 0.597 0.552治疗3个月后80.46±8.71a 71.52±6.45a 5.472 0.001
2.3 两组患者治疗前后的炎性指标比较 治疗3 个月后,两组患者的血清hs-CRP、IL-6、TNF-α、IL-1β水平明显低于治疗前,且联合组患者的血清hs-CRP、IL-6、TNF-α、IL-1β水平明显低于常规组,差异均有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后的炎性指标比较(±s)Table 4 Comparison of inflammatory indicators between two groups of patients before and after treatment(±s)

表4 两组患者治疗前后的炎性指标比较(±s)Table 4 Comparison of inflammatory indicators between two groups of patients before and after treatment(±s)
注:与本组治疗前比较,aP<0.05。Note:Compared with that before treatment in this group,aP<0.05.
组别例数hs-CRP(mg/L) IL-6(ng/L) TNF-α(mmol/L) IL-1β(mmol/L)联合组常规组t值P值44 44治疗前12.35±3.26 13.08±3.49 1.014 0.313治疗3个月后4.97±1.16a 6.83±2.01a 5.316 0.001治疗前37.49±5.18 38.34±4.72 0.805 0.423治疗3个月后16.43±4.09a 20.17±5.14a 3.777 0.001治疗前15.74±4.43 16.29±4.57 0.573 0.568治疗3个月后5.91±1.27a 7.64±2.31a 4.353 0.001治疗前24.41±5.38 25.69±6.17 1.037 0.303治疗3个月后10.48±3.32a 16.35±4.79a 6.681 0.001
2.4 两组患者治疗前后的疾病相关指标比较 治疗3 个月后,两组患者的血清NT-proBNP、hs-TnT、CatS、suPAR水平明显低于常规组,且联合组患者的血清NT-proBNP、hs-TnT、CatS、suPAR 水平明显低于常规组,差异均有统计学意义(P<0.05),见表5。
表5 两组患者治疗前后的疾病相关指标比较(±s)Table 5 Comparison of disease-related indicators between two groups of patients before and after treatment(±s)
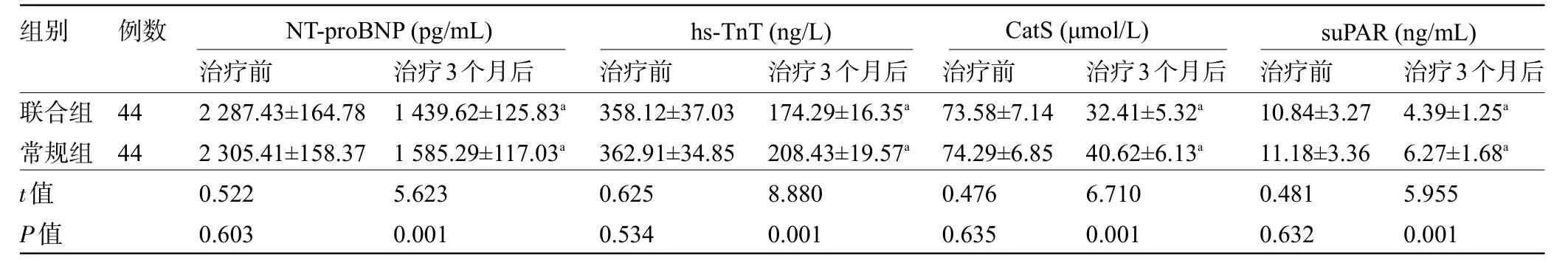
表5 两组患者治疗前后的疾病相关指标比较(±s)Table 5 Comparison of disease-related indicators between two groups of patients before and after treatment(±s)
注:与本组治疗前比较,aP<0.05。Note:Compared with that before treatment in this group,aP<0.05.
组别例数NT-proBNP(pg/mL) hs-TnT(ng/L) CatS(μmol/L) suPAR(ng/mL)治疗前治疗3个月后治疗前治疗3个月后治疗前治疗3个月后治疗前 治疗3个月后联合组常规组t值P值44 44 2 287.43±164.78 2 305.41±158.37 0.522 0.603 1 439.62±125.83a 1 585.29±117.03a 5.623 0.001 358.12±37.03 362.91±34.85 0.625 0.534 174.29±16.35a 208.43±19.57a 8.880 0.001 73.58±7.14 74.29±6.85 0.476 0.635 32.41±5.32a 40.62±6.13a 6.710 0.001 10.84±3.27 11.18±3.36 0.481 0.632 4.39±1.25a 6.27±1.68a 5.955 0.001
2.5 两组患者的不良反应比较 治疗期间,联合组患者的不良反应总发生率为11.36%,略高于常规组的6.82%,但差异无统计学意义(χ2=0.138,P=0.711>0.05),见表6。
3 讨论
现阶段,临床上治疗CHF 主要在于延缓病情进展,缓解临床症状,改善生活质量及远期预后,以降低再住院率及病死率,减轻家庭经济及社会医疗负担。沙库巴曲缬沙坦为治疗CHF 常用药物,其由沙库巴曲、缬沙坦复合而成,具有扩张血管、抑制肾素-血管紧张素-醛固酮系统、利尿、促进排钠及利钠肽表达等诸多作用。但因CHF的发病机制复杂,仅干预神经内分泌,效果有限。因此,寻找新的协同治疗方案对控制病情及改善预后有重要意义。
近年,中医药在CHF 治疗中作用凸显,并取得一定成效,受到临床广泛重视,诸多学者开始探索中西医结合方案治疗CHF 的价值。中医理论认为,气阴两虚为CHF 病机关键,因肺气不足,脾阳不足,肾阳衰弱,致心阳不足,阳虚则周身血运不畅,使心脉瘀滞[9]。芪苈强心胶囊以中医脉络学说为指导、气血理论为切入点,集合泽泻、桂枝、黑顺片、黄芪多种中药制成,具有益气温阳、利水消肿、通络活血作用,现代药理研究表明,其可有效增强心肌收缩力,提升心排血量,降低醛固酮及血管紧张素水平,延缓心室重构,持续改善心功能[10]。本研究结果发现,芪苈强心胶囊联合沙库巴曲缬沙坦治疗CHF 可进一步提升治疗效果,促进心功能恢复,与赵玉清等[11]研究结果一致。究其原因,芪苈强心胶囊联合沙库巴曲缬沙坦能发挥中西药的各自优势,取长补短,不仅能共同促进心功能恢复,还可促进临床症状消退,同时针对中医病机进行根本上调理,进而有效改善预后。因此两者联合可从不同机制发挥叠加效应,提高治疗效果。NT-proBNP、hs-TnT 为反映CHF 患者心肌损伤及预后敏感指标[12-13]。本研究结果显示,联合组患者治疗3个月后的NT-proBNP、hs-TnT水平明显低于常规组,其原因可能与芪苈强心胶囊的抗氧化、抗纤维化及抑制炎症因子表达有关。
炎症反应可促进多种炎症细胞因子大量生成,进而加快心肌细胞纤维化,加重CHF 病情,而CHF 病情加重又可促进炎症介质生成,形成恶性循环[14]。hs-CRP、IL-6、TNF-α、IL-1β为常见促炎因子,可有效反映机体内炎症反应情况。此外,有研究证实,糖尿病合并冠心病患者中体内CatS呈过度表达,可增加糖尿病合并冠心病患者心力衰竭发生风险[15]。Peng等[16]研究表明,抑制CatS表达能通过抑制TNF-α、IL-1β表达和细胞凋亡,减轻心肌缺血/再灌注损伤,保护心脏功能,且在机体炎症反应、组织修复、血管生成及细胞增殖等病理生理中发挥重要调节作用。suPAR是一种炎症生物标志物,当机体受到炎性刺激时,其水平升高,而suPAR通过细胞黏附、趋化等途径使大量炎性介质释放,加剧机体炎症反应,加重心功能损伤[17]。本研究结果表明,联合组患者治疗3 个月后的血清hs-CRP、IL-6、TNF-α、IL-1β、CatS、suPAR 水平明显低于常规组,可见芪苈强心胶囊联合沙库巴曲缬沙坦治疗CHF可有效抑制炎症反应,是其主要治疗机制之一。此外,本研究还发现,两组患者治疗期间不良反应发生率差异无统计学意义,可见两者联合不增加药物不良反应,具有一定安全性。
综上所述,沙库巴曲缬沙坦联合芪苈强心胶囊药物治疗CHF 可有效减轻心肌收缩,抑制炎症反应,促进心功能改善,显著增强疗效,且具有一定安全性。本研究的不足之处在于,未详细探讨沙库巴曲缬沙坦联合芪苈强心胶囊药物治疗CHF 患者对其远期预后的影响,今后将做进一步的随访研究,以获取更为全面的数据支持。
