吡贝地尔缓释片联合盐酸多奈哌齐治疗对帕金森病患者认知功能及血清sLAG3、RANTES水平的影响
2023-10-10陈晓静程曼张雪芳秦慧兵刘红钊
陈晓静,程曼,张雪芳,秦慧兵,刘红钊
南阳市中心医院神经内科,河南 南阳 473000
帕金森病(Parkinson's disease,PD)属于慢性神经系统退行性病变,可导致患者出现运动迟缓、认知障碍、静止性震颤、睡眠障碍等,呈慢性进行性发展,如未及时得到有效治疗,可导致患者生活自理能力逐渐丧失,严重影响患者生活质量[1]。目前,临床对于PD尚无根治性治疗方案,多采用药物治疗以延缓病情进展、减轻临床症状[2]。盐酸多奈哌齐为胆碱酯酶抑制剂,可通过调节脑部代谢,改善患者学习、记忆能力[3]。吡贝地尔缓释片在促进肌肉强直及震颤症状改善方面具有较好作用,还可改善智能缺陷[4]。本研究旨在探究吡贝地尔缓释片联合盐酸多奈哌齐治疗PD对患者认知功能及血清可溶性淋巴细胞活化基因3(sLAG3)、活化T细胞趋化因子(RANTES)水平的影响。
1 资料与方法
1.1 一般资料 选取2020 年3 月至2022 年10月于南阳市中心医院神经内科就诊的134 例PD 患者作为研究对象。纳入标准:(1)符合PD 诊断标准[5];(2)患者及家属知情本研究内容并签署承诺书。排除标准:(1)对本研究相关药物过敏者;(2)伴有其他脑部病变者;(3)严重感染者;(4)精神障碍者;(5)肝肾衰竭者;(6)恶性肿瘤者;(7)急性心脑血管疾病者。采用随机数表法将患者分为对照组和联合组,每组67例。对照组患者中男性36例,女性31例;年龄52~78岁,平均(65.34±6.32)岁;病程1~11 年,平均(6.17±1.59)年;Hoehn-Yahr 分期Ⅰ期11 例,Ⅱ期15 例,Ⅲ期27 例,Ⅳ期14 例。联合组患者中男性38 例,女性29 例;年龄53~79 岁,平均(65.93±6.46)岁;病程2~13 年,平均(6.64±1.54)年;Hoehn-Yahr分期Ⅰ期12例,Ⅱ期17例,Ⅲ期28 例,Ⅳ期10 例。两组患者的一般资料比较差异均无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会审核通过。
1.2 治疗方法 对照组患者采用盐酸多奈哌齐(国药准字H20010723,山东绿叶制药)治疗,口服,5 mg/次,2 次/d。联合组患者在对照组治疗基础上给予吡贝地尔缓释片(国药准字H20130084,珠海联邦制药治疗),口服,50 mg/次,初始用量1 次/d,7 d 后调整为2 次/d,如症状未见改善则继续调整用量至3 次/d。两组患者均连续治疗3个月。
1.3 检测方法 分别于治疗前、治疗1 个月、3个月后采集两组患者晨起外周静脉血,离心处理获取血清样本,采用英国Abcam 公司提供的试剂盒(酶联免疫吸附法)检测血清脑源性神经营养因子(BDNF)、5-羟色胺(5-HT)、神经元特异性烯醇化酶(NSE)、去甲肾上腺素(NE)、白介素-6 (IL-6)、白介素-1β(IL-1β)、sLAG3、RANTES水平。
1.4 观察指标与评价方法 (1)运动功能、认知功能和睡眠质量:治疗前、治疗1个月、3个月后,采用帕金森综合评分量表-Ⅲ(UPDRS-Ⅲ)评估患者的运动功能,总分50 分,分值越高表示运动功能越差;采用智力状态检查量表(MMSE)评估患者的认知功能,总分30 分,分值越高认知功能越高;采用帕金森病睡眠障碍量表(PDSS)评估患者的睡眠质量,总分140分,分值越高睡眠质量越好。(2)临床疗效:治疗后比较两组患者的疗效;①临床痊愈:疗效指数[(UPDRS-Ⅲ评分治疗前-UPDRS-Ⅲ评分治疗后)/UPDRS-Ⅲ评分治疗前×100%]>90%;②显效:90%≥疗效指数≥50%;③有效:50%>疗效指数≥20%;④无效:未达以上标准。总有效率=(总例数-无效)/总例数×100%。(3)血清神经递质:比较两组患者治疗前、治疗1个月、3个月后的血清BDNF、5-HT、NSE、NE 水平。(4)血清IL-6、IL-1β、sLAG3、RANTES 水平:比较两组患者治疗前、治疗1 个月、3 个月后的血清IL-6、IL-1β、sLAG3、RANTES水平。(5)不良反应:统计两组患者治疗期间的恶心呕吐、疲劳、腹泻等不良反应发生情况。
1.5 统计学方法 应用SPSS22.0 统计学软件分析数据。计数资料比较采用χ2检验;计量资料采取Bartlett 方差齐性检验与Kolmogorov-Smirnov 正态性检验,均确认具备方差齐性且服从正态分布,以均数±标准差(±s)表示,组间比较采用t检验。以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组患者的临床疗效比较 联合组患者的临床治疗总有效率为94.03%,明显高于对照组的82.09%,差异有统计学意义(χ2=4.542,P=0.033<0.05),见表1。
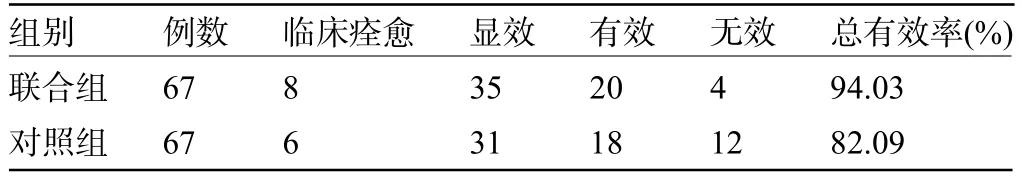
表1 两组患者的临床疗效比较(例)Table 1 Comparison of clinical efficacy between the two groups(n)
2.2 两组患者治疗前后的UPDRS-Ⅲ、MMSE、PDSS 评分比较 与治疗前比较,两组患者治疗1 个月、3 个月后的UPDRS-Ⅲ评分均降低,MMSE、PDSS评分均升高,且联合组患者的变化幅度明显高于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组患者治疗前后的UPDRS-Ⅲ、MMSE、PDSS评分比较(±s,分)Table 2 Comparison of UPDRS Ⅲ, MMSE, and PDSS scores between the two groups before and after treatment (±s,points)

表2 两组患者治疗前后的UPDRS-Ⅲ、MMSE、PDSS评分比较(±s,分)Table 2 Comparison of UPDRS Ⅲ, MMSE, and PDSS scores between the two groups before and after treatment (±s,points)
注:与同组治疗前比较,aP<0.05;与同组治疗1个月后比较,bP<0.05。Note: Compared with that in the same group before treatment,aP<0.05;Compared with that in the same group after 1 month of treatment,bP<0.05.
时间治疗前PDSS 84.26±6.31 82.79±7.02 1.361 0.176 99.62±5.71a 90.46±6.28a 8.841 0.001 121.84±5.93ab 108.43±6.24ab 12.751 0.001例数67 67治疗1个月后67 67治疗3个月后组别联合组对照组t值P值联合组对照组t值P值联合组对照组t值P值67 67 UPDRS-Ⅲ38.16±3.51 37.59±4.14 0.860 0.392 27.44±3.71a 32.85±4.06a 8.052 0.001 21.03±3.42ab 25.78±3.69ab 7.728 0.001 MMSE 13.59±3.24 13.08±3.31 0.901 0.369 19.43±2.15a 16.95±2.43a 6.256 0.001 23.28±2.06ab 20.19±2.55ab 7.716 0.001
2.3 两组患者治疗前后的血清神经递质水平比较 与治疗前比较,两组患者治疗1个月、3个月后的血清BDNF、5-HT、NE 水平明显升高,NSE 水平明显降低,且联合组患者的变化幅度明显高于对照组,差异均有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后的血清神经递质水平比较(±s)Table 3 Comparison of serum neurotransmitter levels between the two groups before and after treatment(±s)

表3 两组患者治疗前后的血清神经递质水平比较(±s)Table 3 Comparison of serum neurotransmitter levels between the two groups before and after treatment(±s)
bb注:与同组治疗前比较,aP<0.05;与同组治疗1个月后比较,bP<0.05。Note:Compared with that in the same group before treatment,aP<0.05;Compared with that in the same group after 1 month of treatment,bP<0.05.
时间治疗前例数67 67治疗1个月后67 67治疗3个月后NE(μg/L)23.38±2.55 24.25±4.62 1.349 0.179 42.64±4.17a 37.59±4.35a 6.860 0.001 55.71±6.34a 50.08±5.12a 5.655 0.001组别联合组对照组t值P值联合组对照组t值P值联合组对照组t值P值67 67 BDNF(ng/L)16.37±2.68 15.94±2.79 0.910 0.365 24.43±3.46a 20.95±3.58a 5.721 0.001 35.45±4.22ab 31.08±3.84ab 6.269 0.001 5-HT(ng/L)21.38±3.62 22.07±4.31 1.003 0.317 40.05±3.66a 36.81±3.78a 5.040 0.001 49.65±5.16ab 43.38±4.64ab 7.396 0.001 NSE(ng/mL)26.78±2.97 27.15±3.11 0.704 0.483 15.52±3.41a 19.78±3.35a 7.295 0.001 8.79±2.05ab 12.43±3.29ab 7.686 0.001
2.4 两组患者治疗前后的血清IL-6、IL-1β、sLAG3、RANTES 水平比较 与治疗前比较,两组患者治疗1 个月、3 个月后的血清IL-6、IL-1β、sLAG3、RANTES 水平均降低,且联合组明显低于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后的血清IL-6、IL-1β、sLAG3、RANTES水平比较(±s,pg/mL)Table 4 Comparison of serum IL-6,IL-1β,sLAG3,and RANTES levels between the two groups before and after treatment(±s,pg/mL)

表4 两组患者治疗前后的血清IL-6、IL-1β、sLAG3、RANTES水平比较(±s,pg/mL)Table 4 Comparison of serum IL-6,IL-1β,sLAG3,and RANTES levels between the two groups before and after treatment(±s,pg/mL)
bb注:与同组治疗前比较,aP<0.05;与同组治疗1个月后比较,bP<0.05。Note:Compared with that in the same group before treatment,aP<0.05;Compared with that in the same group after 1 month of treatment,bP<0.05.
时间治疗前RANTES 42.58±3.76 43.14±5.17 0.717 0.475 30.51±3.44a 35.82±4.39a 7.793 0.001 21.79±3.62a 26.28±4.23a 6.601 0.001例数67 67治疗1个月后67 67治疗3个月后组别联合组对照组t值P值联合组对照组t值P值联合组对照组t值P值67 67 IL-6 28.46±3.87 29.15±3.54 1.077 0.284 14.43±3.72a 19.84±4.21a 7.882 0.001 5.73±1.32ab 7.96±2.24ab 7.021 0.001 IL-1β 168.45±19.31 171.34±20.03 0.850 0.394 101.25±11.46a 125.73±14.68a 10.759 0.001 69.48±7.29ab 83.64±8.11ab 10.629 0.001 sLAG3 958.46±59.43 963.44±60.07 0.482 0.630 819.67±57.31a 867.49±52.06a 5.055 0.001 685.39±54.17ab 737.43±58.64ab 5.336 0.001
2.5 两组患者的不良反应比较 联合组患者的不良反应总发生率为5.79%,略高于对照组的1.49%,但差异无统计学意义(χ2=0.831,P=0.362>0.05),见表5。
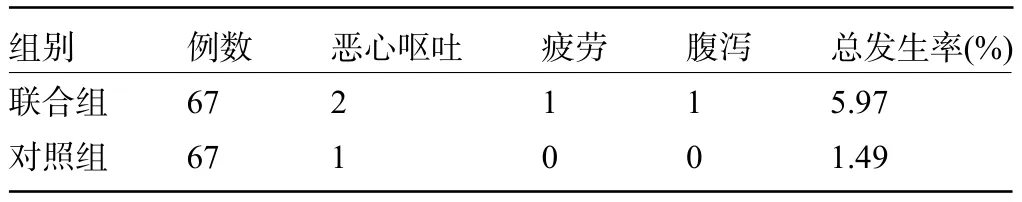
表5 两组患者的不良反应比较(例)Table 5 Comparison on incidence of adverse reactions between the two groups(n)
3 讨论
PD 多见于中老年群体,近年来随着人口老龄化加剧,其发病率也逐年上升,给患者家庭及社会均带来沉重负担[6]。因此,积极探究优化PD 治疗方案意义重大。
盐酸多奈哌齐可通过抑制中枢乙酰胆碱酯酶,提高乙酰胆碱含量,从而保护胆碱能神经元,改善患者学习、记忆功能,提高认知功能;还具有抗氧化作用,可抑制氧化应激反应,降低中枢神经损伤[7-8]。吡贝地尔缓释片作为多巴胺受体激动剂,可促进多巴胺结合受体,恢复乙酰胆碱、多巴胺平衡;还可作用于中脑皮质及黑皮质纹状体突触后D2,调节交感神经张力,促进动脉血流恢复;且半衰期较长,可避免频繁给药造成的药物脉冲式刺激,具有较高安全性[9]。
本研究结果显示,联合组临床总有效率、MMSE、PDSS 评分高于对照组,UPDRS-Ⅲ评分低于对照组。究其原因在于,吡贝地尔缓释片可促进乙酰胆碱、多巴胺恢复平衡,提供多巴胺效应,改善动脉血液循环。而盐酸多奈哌齐作为六氢吡啶类氧化物,可促进突触间隙乙酰胆碱水平升高,抑制活性氧自由基释放,增强中枢神经系统可塑性,提高中枢神经功能。两者联合可产生协同增效作用,进一步保护及修复胆碱能神经元,提高患者运动功能、认知功能、睡眠质量,增强临床疗效。
经与对照组比较发现,联合组治疗1 个月、3 个月后血清BDNF、5-HT、NE 水平均较高,NSE 水平较低。其中BDNF参与神经细胞生长、分化过程,可与多巴胺相互作用,调控多巴胺能行为,修复受损神经细胞[10]。5-HT 作为神经递质,可调节机体睡眠、体温等生理功能[11]。NE 与机体记忆功能相关[12]。NSE 高表达可加重神经细胞损伤[13]。由此可进一步证实采用吡贝地尔缓释片与盐酸多奈哌齐联合治疗PD患者对神经系统功能的促进作用较高,这也是联合用药方案能显著提高疗效的作用机制之一。
本研究结果显示,与对照组相比,联合组可显著下调血清IL-6、IL-1β、sLAG3、RANTES 水平。其中IL-6 为典型炎性因子,参与神经系统疾病的病理过程,可导致多巴胺能神经元变性、坏死[14]。IL-1β可增强单核-巨噬细胞抗原呈递能力,诱导炎症介质释放,引发神经元变性,加重患者睡眠障碍[15]。LAG3 具有调控机体炎症反应及免疫功能的作用,可特异性结合α-突触核蛋白参与PD 发生发展,可裂解为sLAG3 稳定表达于血液中[16]。RANTES可趋化外周T淋巴细胞及单核巨噬细胞,诱发细胞免疫损伤及多巴胺能神经元凋亡,加重神经炎症反应[17]。由此可见,采用吡贝地尔缓释片联合盐酸多奈哌齐治疗PD患者可有效减轻炎症反应,抑制PD病情进展。分析其原因在于,吡贝地尔缓释片与盐酸多奈哌齐联合可降低单核-巨噬细胞抗原呈递能力,抑制促炎因子表达,调节机体免疫功能,减轻神经元细胞损伤,修复受损神经元,从而抑制病情进展。此外,两组间不良反应发生率比较差异无统计学意义,提示在盐酸多奈哌齐基础上联合吡贝地尔缓释片治疗PD 不会显著增加不良反应发生风险,具有一定安全性。
综上所述,采用吡贝地尔缓释片联合盐酸多奈哌齐治疗PD患者可显著提高临床疗效,提高神经功能、运动功能、认知功能、睡眠质量,且具有一定安全性。
