溶胶-凝胶法制备Li3V2(PO4)3电极材料及电化学性能研究
2023-10-09曾建华胡庆兰翁方青欧小文
华 丽,曾建华,胡庆兰,翁方青,欧小文,曹 君
(湖北第二师范学院 化学与生命科学学院;湖北省抗癌活性物质提纯与应用重点实验室,武汉 430205)
正极材料是制约锂电池发展的关键。[1]近年来,锂与过渡金属磷酸盐Li3M2(PO4)3(其中M为多价金属)作为锂离子电池的正极材料引起了人们的广泛关注。其中Li3V2(PO4)3(磷酸钒锂)正极材料具有理论比容量高(197mAh·g-1)[2],而V离子处于3种不等价(+3,+4,+5)的电荷环境中,可以实现5个锂离子的嵌脱,最终可使理论比容量最高达332mAh·g-1。[3]且Li3V2(PO4)3晶体结构稳定,环境友好,有望成为大功率电子产品、新能源汽车或混合动力电车行业电池的正极材料。[4]
当前关于Li3V2(PO4)3合成方法主要有高温固相法、微波法和H/C还原法,高温固相法具有产物颗粒不均匀、晶形无规则、纯度低、电性能差等缺点;微波法与固相法相比有反应时间短、无需惰性气体保护等优点,但过程难以控制,难以工业化大规模生产[5];文献报道较多的是氢气(H2)还原法和碳(C)还原法[6],但将H2作为还原剂时,成本高,H2易燃、易爆等特点而导致危险系数大而不常用。[7]因此一些研究发现,改用碳作还原剂比H更具有可行性,但高温碳还原法[8]烧结温度高,能耗大,对设备操作要求高,产物颗粒大小不一,也进一步限制了其工业应用[9]。因此,本文采用溶胶—凝胶法制备颗粒细小的Li3V2(PO4)3纳米材料并将其作锂电池正极材料,该法能使原料实现分子水平的混合均匀,无需高温高压和惰性气体保护,工艺操作简单,产物粒径均匀,比表面积较大,安全性高等优点[10],适用于商业生产和应用。并进行电化学性能分析,以期获得有用数据,为其进一步工业推广提供基础支撑。
1 实验部分
1.1 仪器和试剂
1.1.1 仪器
电动搅拌器(JJ-1型,上海尚仪仪器设备有限公司);离心机(LC-LX型,上海力辰科技有限公司);集热式磁力搅拌机(HJ-8型,河南胜博仪器设备有限公司);氩气保护的真空手套箱(GRS-1200,武汉格瑞斯新能源有限公司);数显恒温水浴锅(HH-2型,江苏金怡仪器科技有限公司);真空干燥箱(DZF-6020型,常州恩谊贸易有限公司);环境扫描电镜(ESEM,Quanta 200型,FEI公司);X-射线衍射仪(XRD,09 Empyrean型,X'Pert PRO荷兰帕纳科公司PANalytical B.V.(原飞利浦公司));粒度分析仪(YST-100型,厦门易仕特仪器有限公司);带程序升/控温的空气炉(HR-1020型,上海华睿有限公司);电池程控测试仪(Land CT2001A型,河南精迈仪器仪表有限公司);电化学工作站(CHI660D型,北京华科普天科技有限公司和CS350H型,武汉科思特仪器股份有限公司);电子分析天平(FA2104S型,上海精科实业有限公司,能精确到0.1mg)。
1.1.2 试剂
V2O5晶体粉末(AR级,东莞鼎伟靶材有限公司);电解液(体积比为1∶1的1M LiPF6+碳酸乙烯酯(EC)/碳酸二乙酯(DEC)有机溶液(南京莫杰斯能源科技有限公司);正极为合成的Li3V2(PO4)3纳米材料,负极为高纯金属锂片(纯度>99.9%,无锡新锋锂业有限公司);电池隔膜为微孔聚丙烯膜(Ceigad 2400,东莞市科恒包装制品有限公司);N-甲基-2-吡咯烷酮(NMP,CR级,江苏恒祥化学股份有限公司);导电乙炔黑(工业级,天津亿博瑞化工有限公司),无水乙醇/甲醇(AR级,武汉瀚启化工有限公司);聚乙烯吡咯烷酮(PVP,K-30,安徽中弘生物工程有限公司)。聚偏氟乙烯(PVDF,AR级,深圳市华耀塑化实业有限公司)。
1.2 实验方法和步骤
1.2.1 Li3V2(PO4)3的制备
方法见文献[11]:向一定量的V2O5晶体中加入10%的H2O2搅拌4 h,释放出分解的O2,形成红色溶液,室温下静置4d,形成V2O5·nH2O湿凝胶。再将NH4H2PO4、LiOH·H2O等原料加入其中,搅拌8h后再进行真空干燥即可得到Li3V2(PO4)3前驱体。接着研细干燥的Li3V2(PO4)3前驱体,将其置于陶瓷皿在空气炉中程序升温(升温速率为1℃/min)至不同温度条件下(450℃—750℃)烧结12 h即可制备出Li3V2(PO4)3样品。
1.2.2 电池组装及测试
方法见文献[12],将制备的Li3V2(PO4)3材料作为活性物质,按70∶15∶15的质量比将活性物质、PVDF和乙炔黑进行混合,研细并向其中加入数滴NMP调成浆状,然后涂布在铝箔上,烘干后,压制成直径为8mm的圆形电极片,并在80℃下真空干燥15h备用。
电池组装及性能测试:方法见文献[13,14],将上述制备的电极片作为研究电极,电解液为1mol/L LiPF6/EC∶DEC(体积比=1∶1),金属锂片为对电极,在真空手套箱中装配成模拟CR-2032 型纽扣电池。测试参考文献[15]:用Land CT2001A 电池程控测试仪在0.01~4.5V 电压范围内进行恒电流充放电性能测试。电极片中样品的承载量为3~5mg/cm2,充放电循环程序自己编写。
1.2.3 循环伏安测试(CV)
本论文循环伏安测试用两电极体系,高纯金属锂片作为对电极和参比电极。活性物质为工作电极,使用辰华CHI 660D电化学工作站测试。测试方法见文献。[16,17]
1.2.4 交流阻抗测试(EIS)
采用CS350H电化学工作站进行EIS测试来进一步了解电池在恒电流充放电条件下内部阻抗变化从而获得脱嵌锂离子机理,测试条件见文献[15]:交流电压的振幅为5mV,频率范围为10mHz~10KHz,测试采用扣式电池体系。
1.2.5 性能表征
XRD进行产物晶体结构分析。其扫描范围2θ为5°~80°。环境扫描电子显微镜(ESEM)进行形貌表征,在测试之前进行喷金处理。
2 结果与讨论
2.1 ESEM电镜图
图1 是合成的Li3V2(PO4)3锂电池电极材料650oC 条件下锻烧12h 产物的ESEM 电镜图(a,20000X;b,50000X;c,100000X;d,200000X),从中可知形成是类球形的纳米结构,平均粒径约10-20nm 之间,分散性较好,颗粒与颗粒之间无粘结现象。较之文献[18]报道在680oC条件下锻烧后产物不规则且有团聚现象相比,本法能够较好合成粒度均匀细小的纳米材料。
2.2 XRD分析
图2 为不同烧结温度下合成的Li3V2(PO4)3的XRD 图(其中a,450℃;b,550℃;c,650℃;d,750℃),从中可知,在650oC条件下煅烧时所得产物的XRD图谱与单斜晶系结构的Li3Fe2(PO4)3(ICDD43-0526)相一致,空间群为P21/n。[19,20]进一步研究表明,随着锻烧温度的升高,Li3V2(PO4)3产物对应的主要衍射峰相对强度增强,且峰型更为尖锐,说明锻烧温度升高,有利于Li3V2(PO4)3形成较好的结晶度。温度继续升高,达到750oC之后,虽然结晶度较好,但产物晶粒逐渐变得粗大,且易烧结成块,有明显的过烧结行为。若产物存在晶粒粗大和团聚现象,会增加锂离子在电极表面固相传输电阻,使部分活性中心难以参与电化学反应而产生不可逆比容量损耗,最终会影响电池的循环稳定性和使用寿命。因此选择最佳烧结温度为650oC。
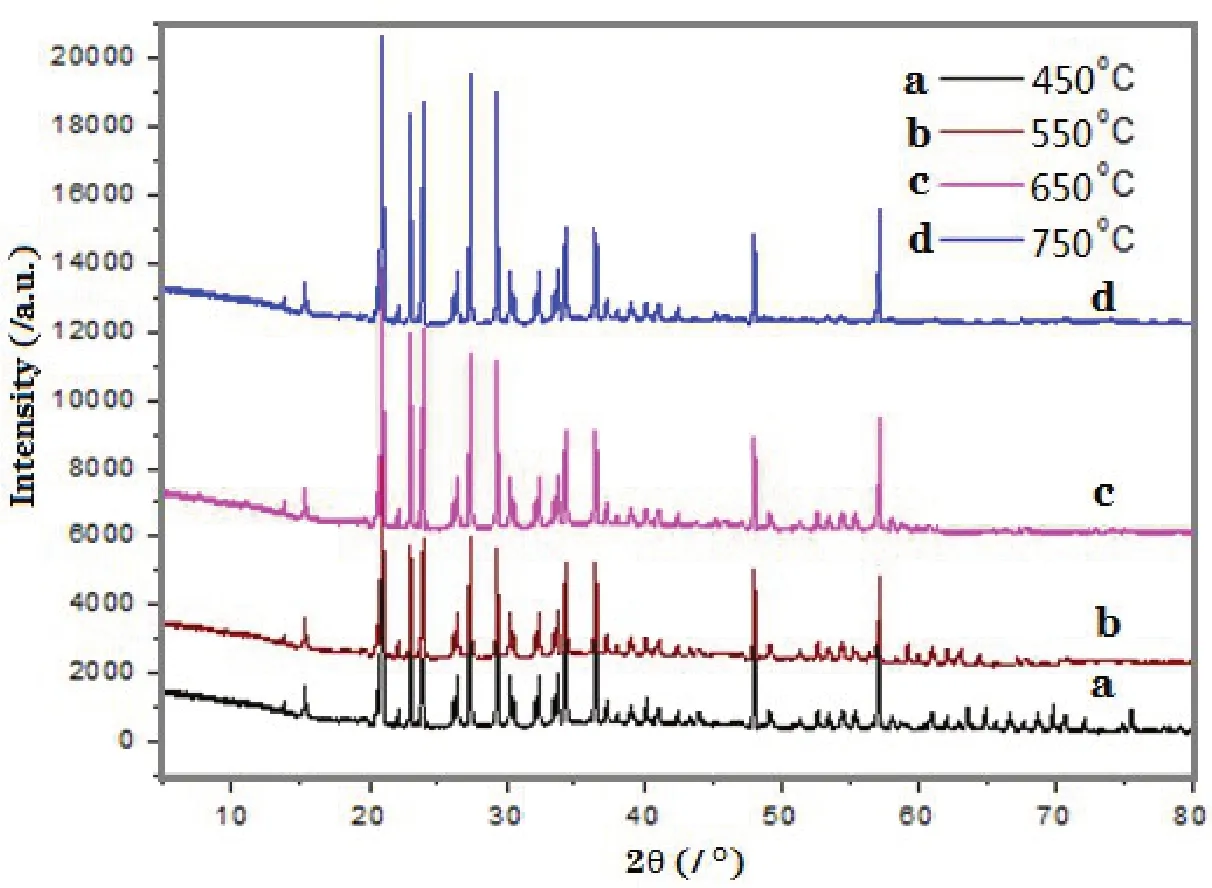
图2 不同烧结温度下合成的Li3V2(PO4)3的XRD图谱(其中a,450℃;b,550℃;c,650℃;d,750℃)Fig.2 X-ray diffraction(XRD)spectrometries of Li3V2(PO4)3in conditions of different calcined temperatures(wherein,a,450℃;b,550℃;c,650℃;d,750℃)
2.3 恒电流下充放电性能测试
图3 为在恒电流条件下Li3V2(PO4)3电极材料的充放电曲线(电流密度为0.2C=50mA/g,其中a,b,c,d,e,f,g分别为1,30,60,100,150,200,250次循环),从中可知,首次充放电比容量分别为170和172mAh/g;30次充放电循环后比容量分别为165和166mAh/g;60次充放电循环比容量为158和162mAh/g;100次充放电循环比容量为157 和161mAh/g;150 次充放电循环比容量为155 和160 mAh/g;200 次充放电循环比容量为140 和141mAh/g;250次充放电循环比容量仍为103和124mAh/g。而文献[11]中低温碳热还原法合成的Li3V2(PO4)3在650oC烧结12h后经30次循环后其放电比容量只有88.5 mAh/g;与另一文献[21]中报道的微波法合成Li3V2(PO4)3电极在0.2C首次放电比容量为145.7 mAh/g,经50次循环后,放电为98 mAh/g相比较,本文合成的电极材料电化学性能较为优异。但达到250次环后充放电比容量变化相对较大,可逆比容量相对下降明显,分析原因可能是与多次充放电后电极材料出现了团聚或粘结现象,导致电极表面电阻变大有关,这一点在交流阻抗分析中得到证实。

图3 恒电流条件下Li3V2(PO4)3电极材料的充放电曲线(电流密度为0.2C=50mA/g,其中a,b,c,d,e,f,g分别为1,30,60,100,150,200,250次循环)Fig.3 The charge-discharge curves of the obtained Li3V2(PO4)3electrode materials at the constant current density of 0.2C=50mA g-1 in the 1st,30th,60th,100th,150th,200th,250th cycle)
2.4 不同倍率下循环稳定性测试
为了分析电极材料在不同倍率条件下的循环性能,进行了0.2C,0.5C,1C高和低倍率0.2C条件下测试,每组循环30次,分析其放电比容量,结果如图4所示(其中:a,0.2C;b,0.5C;c,1C;d,0.2C)。在0.2C(0.2C=50mA/g),比容量在170-172mAh/g 之间,波动幅度为2mAh/g;在0.5C 倍率下,有微小波动,但能相对稳定在166-162mAh/g,幅度为4mAh/g;在1C倍率下,较为不稳定,在162-155mAh/g左右波动且幅度为7mAh/g;经过了多次循环后,再在0.2C倍率下测试,比容量同样能稳定在170-171mAh/g之间。由此可见,Li3V2(PO4)3电极材料在低电流密度(50mA/g)条件下相对稳定,电流密度越大充放电越不稳定,这一结果与文献[11]报道的相似,主要原因可能是在大电流充放电条件下电极材料遭到了一定的破坏,出现粉化所致。

图4 Li3V2(PO4)3电极材料在不同倍率下循环稳定性曲线((其中:a,0.2C;b,0.5C;c,1C;d,0.2C)Fig.4 The cycling performance curves of Li3V2(PO4)3electrode materials at different rates(wherein,a,0.2C;b,0.5C;c,1C;d,0.2C)
2.5 循环伏安(CV)曲线
图5 烧结温度为650℃Li3V2(PO4)3电极材料在50mA/g 电流密度下的循环伏安(CV)曲线图,扫描速率为0.05mA/s,扫描电压范围为3.0-5.5V。从中可知,首次充电过程中,出现了三个氧化峰(标注1,2,3),分别对应着3.69V,4.18V和4.64V,其中前两个峰产生的原因可能是Li3V2(PO4)3脱出1个Li+后,另1个V从+3价氧化成+4价所致;在4.64V处氧化峰,是进一步脱去1 Li+后,1个V再次从+4价氧化成+5价所致。而首次放电过程中出现了两个还原峰(标注4,5),分别对应着3.48V和3.75V,这是由于Li+被嵌入后,V再次被还原从+5价变为+3价和+4价所致。

图5 烧结温度为650℃Li3V2(PO4)3电极材料在50mA/g电流密度下的循环伏安(CV)曲线图Fig.5 Cyclic voltammetry(CV)curves of Li3V2(PO4)3electrode material sintered at 650°C in density of 50mA/g
2.6 交流阻抗(EIS)曲线
交流阻抗谱用于分析比较复杂的电极电化学反应,是电极界面动力学研究中强有力的电化学技术。图6为Li3V2(PO4)3电极材料在0.2C,0.5C,1C 倍率下首次放电后的交流阻抗谱图(EIS)(其中a 为Nyquist 图,b 为Bode 图,c为等效电路图)。从中可知,三条曲线均由高频区(10Hz-10KHz)半圆弧和低频区(100mHz-10Hz)半无限扩散线两个时间常数组成,三种倍率下阻抗谱均可用图6c中的等效电路模拟,拟合数据见表1所示,其电化学参数涵义如下[22]:高频圆弧与阻抗实轴Z’的截距为接触电阻R1,它包括电解液电阻和电极与之接触电阻;高频区的圆弧对应电极界面电化学反应的总的电荷转移电阻R2,此处对应着Li+在Li3V2(PO4)3电极上的电化学嵌入/脱出过程总阻抗;C1为双电层电容;低频区直线是由于Li+在电解液中Wurburg扩散阻抗Ws(包括Ws-T和Ws-p)。从表1中可以看出Li3V2(PO4)3电极材料在不同倍率下的R1、R2、Ws均有较大的差别,变化趋势是R1C>R0.5C>R0.2C,W1C>W0.5C>W0.2C,且这三项阻抗总和(R1+R2+Ws)也满足这个关系。究其原因可能是电流密度越大,锂离子在脱嵌过程中更易形成氧化产物或还原产物附着在电极表面而增大了阻抗或是Li3V2(PO4)3电极材料在大电流条件下更易粉化或团聚,从而引起阻抗增大。这也为进一步了解大电流条件下欠佳的循环稳定性提供了理论依据,这将是今后商业应用需要进一步攻关的方向。

表1 不同倍率下Li3V2(PO4)3电极材料等效电路拟合结果Table 1 Fitting results of the equivalent circuit of Li3V2(PO4)3 electrode materials at different rates

图6 Li3V(2PO4)3电极材料在0.2C,0.5C,1C倍率下首次放电后的交流阻抗谱图(EIS)(其中a为Nyquist 图,b为Bode 图,c为等效电路图)Fig.6 Electrochemical impedance spectroscopy(EIS)of Li3V(2PO4)3 electrode material after first discharge at 0.2,0.5 and 1c rates(where a is Nyquist,b is Bode and c is equivalent)
3 结论
(1)通过溶胶-凝胶法制成的Li3V2(PO4)3锂电池电极材料,ESEM电镜图表明,形成是类球形的纳米结构,平均粒径约10-20nm之间,分散性较好,颗粒与颗粒之间无粘结现象。
(2)不同烧结温度下合成的Li3V2(PO4)3,说明锻烧温度升高,有利于Li3V2(PO4)3形成较好的结晶度。温度达到750oC之后,虽然结晶度较好,但产物晶粒逐渐变得粗大,有明显的过烧结行为。若产物存在晶粒粗大和团聚现象,会增加锂离子在电极表面固相传输电阻,使部分活性中心难以参与电化学反应而产生不可逆比容量损耗,最终会影响电池的循环稳定性和使用寿命。因此选择最佳烧结温度为650oC。
(3)恒电流条件下Li3V2(PO4)3电极材料的充放电,达到250次充放电循环后充放电比容量相对变化较大,可逆比容量相对下降明显,可能是因多次充放电后电极材料粉化,导致电极表面电阻较大所致。
(4)不同倍率条件下的循环性能测试表明,材料在低电流密度下充放电相对较为稳定,高倍率下不稳定,主要原因可能是在大电流充放电条件下电极材料遭到了一定的破坏,出现粉化所致。
(5)阻抗结果显示:材料在不同倍率下的R1、R2、Ws均不同,且电流密度越大,阻抗越大,这可能与锂离子在脱嵌过程中更易形成氧化产物或还原产物附着在电极表面而增大了阻抗或是Li3V2(PO4)3电极材料在大电流条件下更易粉化或团聚,从而引起阻抗增大。这也为进一步了解大电流条件下循环稳定性差提供了理论依据。
