碳量子点敏化二氧化钛纳米管阵列光催化降解草甘膦废水*
2023-10-09黄露露艾子昊樊宇天
黄露露,艾子昊,樊宇天,李 萍,2
(1 武汉工程大学化工与制药学院,绿色化工过程省部共建教育部重点实验室,湖北省新型反应器与绿色化学工艺重点实验室,湖北 武汉 430205;2 磷资源开发利用教育部工程研究中心,湖北 武汉 430205)
草甘膦(glyphosate)作为世界农业生产中最广泛使用的除草剂,常年大规模使用而引发的水污染已成为全世界的一个普遍问题。为改善环境污染与能源危机,大力提倡发展可持续的、清洁环保的能源,光催化技术由此备受关注[2]。二氧化钛纳米管阵列(TNTAs)由于结构独特、比表面积大,作为光催化材料前景可期。但由于TNTAs只能吸收波长小于387.5 nm的紫外光,且光生电子空穴易复合,光催化效率较低,其应用受到限制[3]。现今提高TiO2光催化效率的方法有两种:一种是将其吸光范围延伸至可见光波长,如半导体复合[4-6]、贵金属沉积[7]等;另一种是提高光生载流子的传输效率如离子掺杂、量子点敏化等[8-10]。碳量子点(CQDs)是一种粒径小于10 nm的新型荧光碳纳米粒子,由于其具有光致发光特性、水溶性好、化学稳定性高、成本低廉和低毒性,合成路线简单等优点,应用前景十分广阔[11-12]。通过CQDs敏化,可以有效调节TiO2的能带,同时CQDs可以作为优良的电子给体,从而在光催化过程中促使催化剂的电子与空穴有效地分离[13-14]。
本文采用阳极氧化法经两步氧化获得纳米管阵列结构,制备工艺简单、成本低廉、列管排列均匀,进一步CQDs敏化TNTAs,以拓宽其光响应范围,提高电子-空穴分离效率,从而提高光催化性能。
1 实 验
1.1 实验试剂
氟化铵,山东多聚化学有限公司;乙二醇,国药集团化学试剂有限公司;无水乙醇,郑州派尼化学试剂厂;钛片(纯度99.9%);丙酮,西陇科学股份有限公司;过氧化氢,茂名市雄大化工有限公司;乙二胺,上海颖心化学试剂有限公司;硝酸,西亚化学科技有限公司。所有化学品均为分析纯试剂,未经任何纯化直接使用。
1.2 样品的制备
1.2.1 二氧化钛纳米管阵列的制备
2×3 cm的钛片用乙醇和丙酮超声15 min,放入浓H2SO4中浸泡1 min,再用蒸馏水冲洗并晾干。
石墨电极为阴极,钛片为阳极,含2vol%去离子水和0.5wt%氟化铵的乙二醇溶液为电解液,在40 V的直流电压下第一步阳极氧化1 h,然后将钛片放入5wt%的双氧水中浸泡5 min,继续40 V第二步阳极氧化1 h。将反应后的钛片于450 ℃下焙烧2 h,自然冷却后得到TNTAs。
1.2.2 碳量子点的制备
取3.84 g柠檬酸、1.35 mL乙二胺于40 mL水中;混合液超声5 min,转移至100 mL高压反应釜中,200 ℃下反应5 h,自然冷却至室温。减压抽滤,滤液透析48 h,透析袋中的溶液4 ℃下保存备用。
1.2.3 CQDs/TNTAs的制备
TNTAs浸泡在乙醇溶液中,60 ℃于搅拌300 rpm下逐滴加入CQDs溶液配制得到0.5 mg/mL的溶液,继续搅拌4 h后,60 ℃干燥备用。
1.3 样品的表征
德国布鲁克公司的XRD衍射仪分析晶相组成,管电流80 mA,管电压60 kV。采用JSW-5510LV型扫描电镜(SEM),JEM2100透射电镜(TEM)。采用NICOLET6700傅立叶红外光谱仪(FT-IR)对样品进行红外光谱分析,波长范围4000~5000 cm-1。采用上海美析仪器UV-1700PC型紫外-可见光分光光度计测试样品的吸光谱。
1.4 光催化活性的评估
300 W的PLS-SXE300C氙灯(北京泊菲莱)为光源,将2×3 cm的TNTAs膜分散在100 mL浓度为5 mg/L的草甘膦水溶液中,搅拌下暗反应0.5 h,随后打开光源,于25 ℃下光催化反应,每隔20 min取2 mL样品,用0.22 μm滤膜过滤后的滤液加入到10 mL容量瓶中并加入适量蒸馏水定容,随后滴加50%硫酸0.5 mL,250 g/L溴化钾0.1 mL,和14 g/L的亚硝酸钠0.5 mL。摇匀放置30 min后,用紫外-可见分光光度计测量其在λ=244 nm的吸光度。
2 结果与讨论
2.1 样品形貌
所制备的TNTAs及CQDs/TNTAs样品的形貌如图1所示。TNTAs中具有明显整齐排列的管状结构,管径大约100 nm,壁厚约10 nm,管长超过1 μm。经过CQDs敏化后的CQDs/TNTAs仍保持完整的管状阵列结构,管径与管长基本不变,但管壁与敏化前相比略显粗糙。

图1 TNTAs(a,b)及CQDs/TNTAs (c,d)的SEM图Fig.1 SEM of TNTAs (a ,b)and CQDs/TNTAs (c,d)
所制备CQDs的TEM如图2所示。可以看出CQDs大小均匀,粒径尺寸主要分布在1~4 nm之间,平均粒径为3.36 nm。
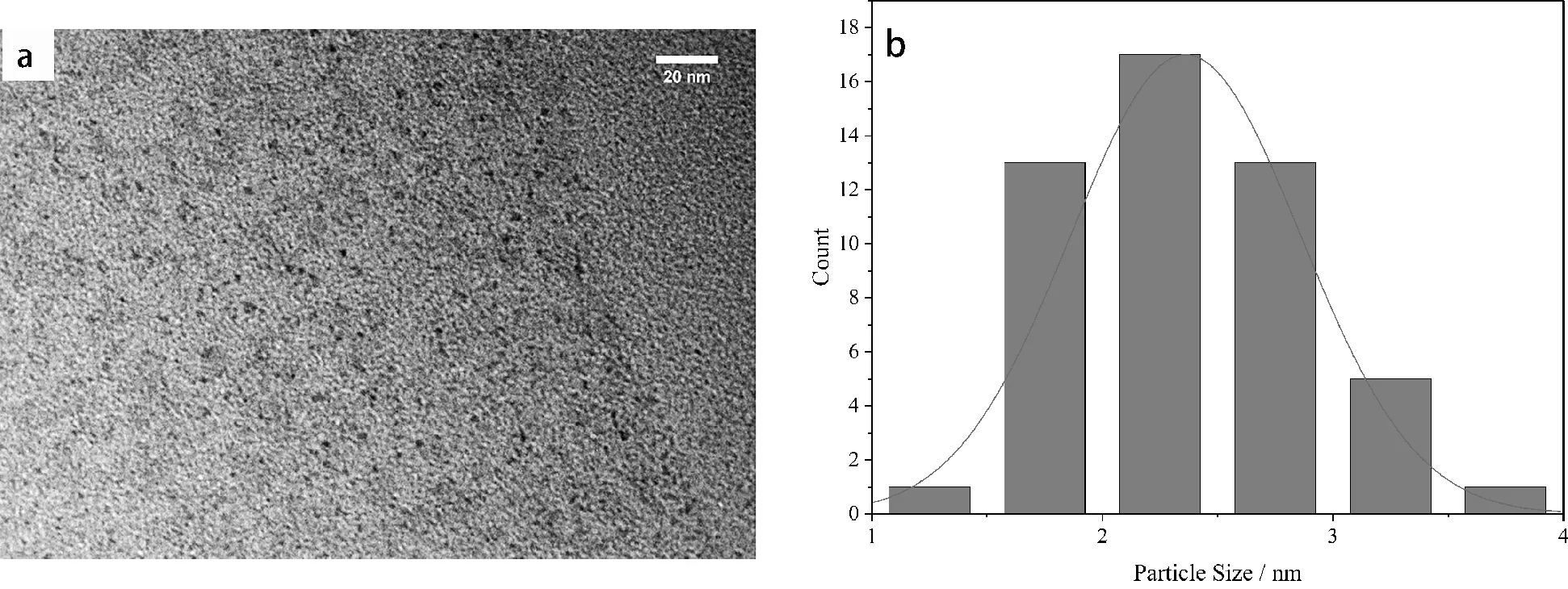
图2 CQDs及CQDs/TNTAs的TEM图(a)及颗粒尺寸分布(b)Fig.2 TEM (a)and particle size distribution (b)of CQDs
2.2 样品的晶相组成
由图3的XRD图谱可见,TNTAs在27.47°,36.08°,41.22°,54.32°和56.64°处有明显的衍射峰,与金红石相标准卡片JCPDS 21-1276中的(110)、(101)、(111)、(211)和(220)晶面相对应,在25.28°、37.80°、48.05°、62.69°处的衍射峰与二氧化钛锐钛矿晶型的标准卡片JCPDS No.21-1272中的(101)、(004)、(200)、(204)晶面相对应[15]。制备的TNTAs是金红石和锐钛矿的混晶[16]。

图3 TNTAs和CQDs/TNTAs的XRD图Fig.3 XRD patterns of TNTAs and CQDs/TNTAs
CQDs/TNTAs与TNTAs的XRD图衍射峰位置相同,峰强一致,未观测到新的衍射峰。可能是碳量子点量太少,被TNTAs的衍射峰掩盖[17]。
2.3 样品的光学性能
图4为TNTAs复合前后的吸光谱,TNTAs可见光吸收率极低,而CQDs在350 nm处有较强的吸收峰,该吸收峰对应于CQDs中-COOH官能团的n-π*跃迁[18],且CQDs对400~500 nm范围内的可见光也有一定吸收。CQDs/TNTAs在350~400 nm的紫外光及400~550 nm的可见光吸光率都有大幅上升。
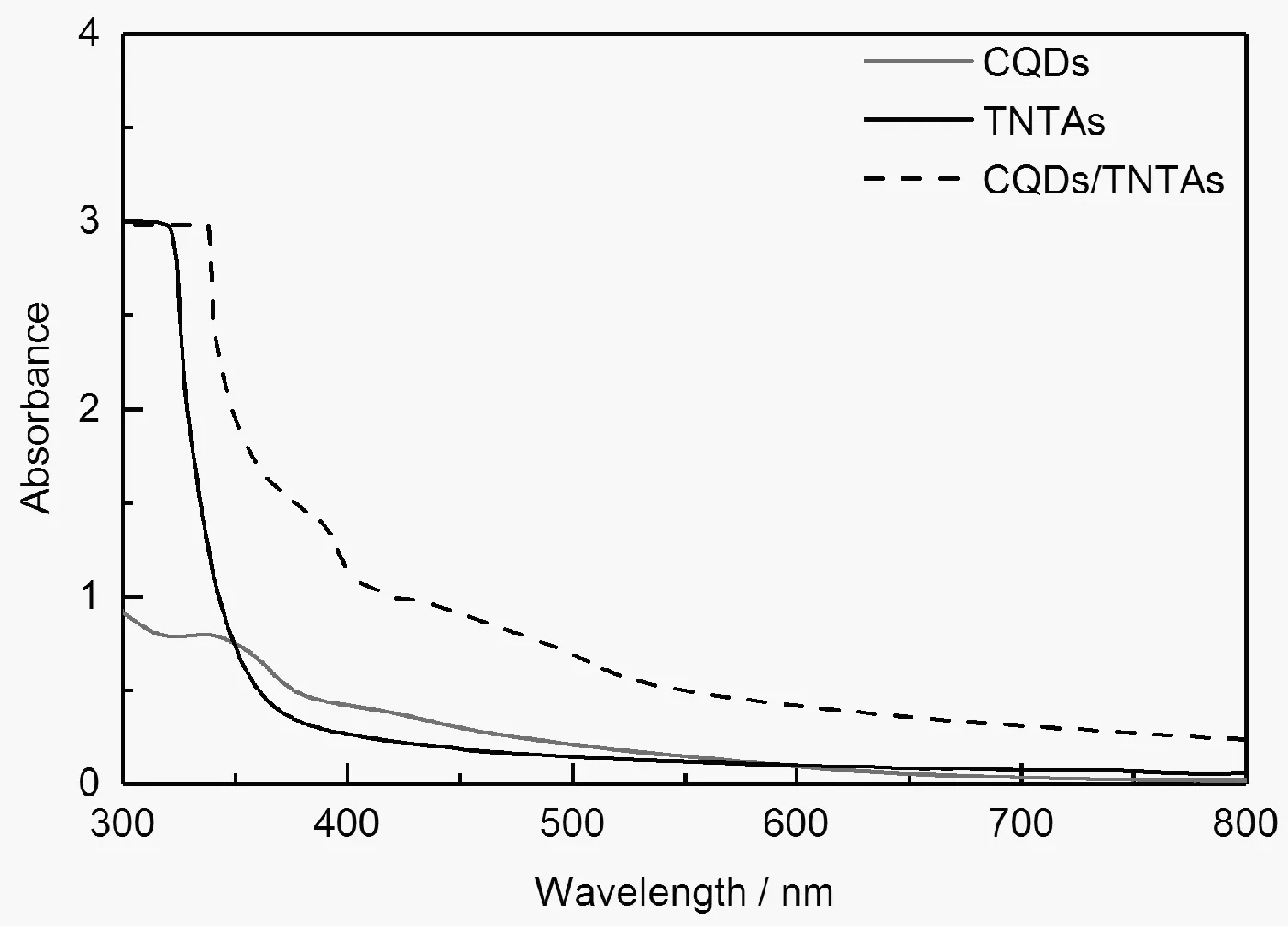
图4 TNTAs敏化前后的紫外可见吸收光谱Fig.4 UV-vis absorbence of TNTAs before and after sensitization
2.4 CQDs/TNTAs光催化降解草甘膦的性能
考察不同敏化次数的x-CQDs/TNTAs(x表示敏化次数)与TNTAs光催化性能如图5所示。
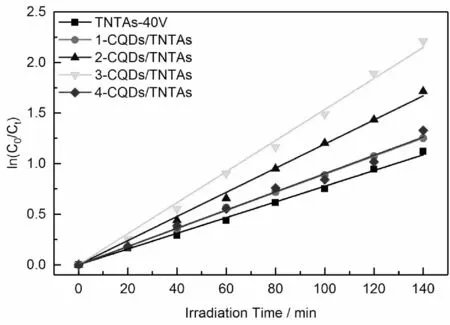
图5 TNTAs和CQDs/TNTAs光催化性Fig.5 Photocatalytic degradation of glyphosate by TNTAs and CQDs/TNTAs
图5可知,经过1次CQDs敏化后,k值从原来的7.76×103min-1提高到8.94×103min-1,提高了15%,增加敏化次数,光催化效果先提高后下降,在敏化3次时达到最高,k值是TNTAs的1.98倍,继续增加敏化次数,光催化降解性能反而下降 。
为了进一步研究敏化前后光催化剂中的光生电荷传输性能,对3-CQDs/TNTAS进行了光电性能测试,如图6所示。
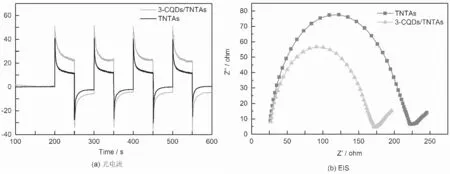
图6 TNTAs与CQDs/TNTAs的光电性能Fig.6 Photoelectric performance of TNTAs and CQDs/TNTAs
样品的瞬时光电流响应测试结果如图6 (a)所示,TNTAs与CQDS/TNATs在光照时,均可产生光电流,但敏化后的CQDS/TNATs光电流密度显著高于TNTAs。说明CQDs的敏化有助于TNTAs中光生电子的传输。而图6(b)的电化学阻抗测试结果也表明敏化后的CQDS/TNATs具有更小的电化学阻抗,说明量子点敏化抑制了光生电子-空穴对的复合。
CQDS敏化后,由于CQDs的导带位置比TNTAs更负,量子点价带激发的电子转移到TNTAs的导带上,光生电子-空穴对的分离得以促进,而且CQDs敏化有效地抑制了光生电子-空穴对的复合,其光电传输如图7所示,CQDs与TNTAs形成异质结,有助于TNTAs中光生电子的传输,并有效抑制光生电子-空穴对的复合,提高了TNTAs的光催化活性。结合图4分析可知,在TNTAs上复合CQDs后,有效地延伸了二氧化钛纳米管阵列对可见光的吸收,提高了光催化剂对光的利用率[19-20]。
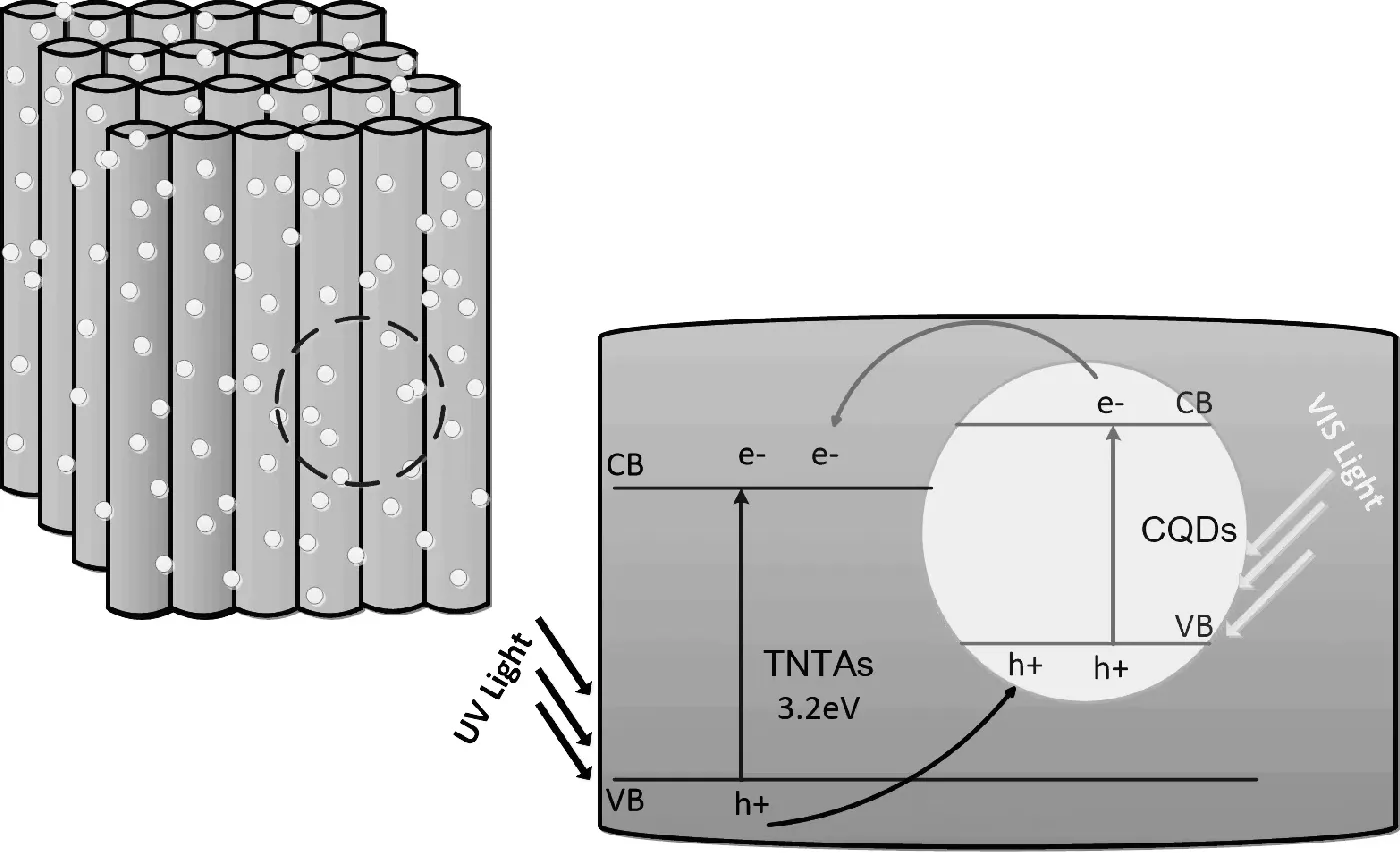
图7 CQDs/TNTAs的的光生电荷传输示意图Fig.7 Photogenerated charge transfer diagram of CQDs/TNTAs
3 结 论
通过对TNTAs进行CQDs敏化制备了CQDs/TNTAs复合光催化材料,并对其进行了光催化降解草甘膦的研究。结果表明TNTAs由于具有独特的轴向列管形状,是良好的光催化降解草甘膦材料,将TNTAs与CQDs复合后,光催化降解效率得以提高,敏化次数为3次时,光催化降解效果是复合前的1.98倍。通过碳量子点敏化可显著提高二氧化钛纳米管阵列的光催化降解草甘膦活性,本研究对二氧化钛光催化剂的应用于农药废水处理方面有一定促进作用。
