血管性帕金森综合征与帕金森病的临床特征及脑白质高信号差异性研究
2023-09-28陈柏希王婉仪詹翠京高玉元聂坤张玉虎王丽娟
陈柏希,王婉仪,詹翠京,高玉元,聂坤,张玉虎,王丽娟
目的 研究血管性帕金森综合征(vascular parkinsonism,VP)与帕金森病(Parkinson’s disease,PD)临床特征及脑白质高信号(white matter hyperintensities,WMH)的差异,为研究VP的发病机制提供一定的依据与思路。
方法 根据临床实际,健康受试者人数以1∶2的比例匹配,回顾性筛选符合入排标准的VP患者和年龄、性别、受教育程度与其相匹配的PD患者、健康志愿者,健康志愿者作为健康对照(healthy control,HC)组。收集一般临床资料及生化指标,评估患者临床症状,采集头颅MRI参数并对3组受试者的资料进行统计分析。
结果 本研究纳入26例VP患者、26例PD患者及13例HC,与PD组相比,VP组的整体认知、精神状态更差:HAMA得分(P=0.025)更高,MMSE得分(P=0.001)、MoCA得分(P=0.008)更低;血管危险因素更多:有高血压病史(P=0.012)和卒中病史(P<0.001)的患者比例更高;运动相关脑区白质受损更严重:WMH总分(P<0.001)、深部白质高信号(deep white matter hyperintensities,DWMH)总分(P=0.001)、脑室旁周围白质高信号(periventricular hyperintensities,PVH)总分(P=0.002)、运动相关脑区PVH评分[额角帽状白质高信号评分(P=0.002)、侧脑室带状白质高信号评分(P=0.018)]、运动相关脑区DWMH评分[额叶深部白质高信号评分(P<0.001)、顶叶深部白质高信号评分(P=0.007)]、基底节白质高信号评分(P=0.002)、壳核白质高信号评分(P=0.029)更高,上述差异均具有统计学意义(P<0.05)。
结论 高血压病史、卒中病史和运动相关脑区白质损伤在VP发病机制中可能有重要作用。
血管性帕金森综合征(vascular parkinsonism,VP)是一种主要由脑小血管损伤引起的帕金森综合征,常伴有血管危险因素[1],曾被称为动脉硬化性帕金森综合征和下半身帕金森综合征[2]。指南指出,VP的临床表现分为运动症状和非运动症状,运动症状主要表现为对称的双下肢运动障碍,非运动症状主要表现为认知障碍[2-3]。目前VP尚缺乏公认的临床诊断标准,临床特征尚不明确,诊断上易与帕金森病(Parkinson′s disease,PD)混淆。对称的双下肢运动障碍、锥体束征和影像学发现血管缺血性改变为VP与PD的重要鉴别点[2,4-5]。
脑白质高信号(white matter hyperintensities,WMH)是脑小血管病变的重要影像学标志,在T2加权MRI上表现为散在的高信号,是常见结构神经学影像,其分布能反映脑白质损伤的严重程度。在PD和VP患者中,脑白质损伤不仅会导致PD患者运动障碍和认知障碍[6],还与VP患者的认知障碍和疾病严重程度密切相关[7]。目前VP的发病机制主要为血管损伤[2],PD的发病机制主要为黑质多巴胺能神经元进行性退变和路易小体形成[8],尚不明确不同的发病机制是否会导致两者WMH分布出现差异,仍需进一步的研究。本研究以VP、PD患者及健康受试者为研究对象,对3组的临床资料、生化指标及WMH进行差异性分析。
1 对象与方法
1.1 研究对象 根据临床实际,健康受试者人数以1∶2的比例匹配,回顾性筛选2019年1—12月就诊于南方医科大学附属广东省人民医院的符合入排标准的VP患者和年龄、性别、受教育程度与其相匹配的PD患者、健康志愿者,健康志愿者作为健康对照(healthy control,HC)组。
VP纳入标准:①年龄18~85岁;②符合《中国血管性帕金森综合征诊断与治疗专家共识》定义的VP诊断标准[3];③由2名主治医师或以上职称的神经科医师独立诊断;④一般临床资料、生化指标、神经心理认知评估量表及MRI数据齐全;⑤患者依从性好,对本研究内容知情,自愿参加本研究,并签署知情同意书。
PD纳入标准:①年龄18~85岁;②符合《中国帕金森病的诊断标准(2016版)》中PD的诊断标准[5];③由2名主治医师或以上职称的神经科医师独立诊断;④一般临床资料、生化指标、神经心理认知评估量表及MRI数据齐全;⑤患者依从性好,对本研究内容知情,自愿参加本研究,并签署知情同意书。
VP和PD排除标准:①其他病因引起的帕金森综合征,如多系统萎缩、正常颅内压性脑积水等疾病;②认知障碍、语言障碍及MRI检查禁忌证等导致无法配合检查;③有头部外伤和脑部手术病史(如脑深部核团摧毁术、脑深部电刺激术);④有自杀倾向及严重精神分裂等精神病性症状;⑤有其他严重器质性疾病。
HC排除标准:①已存在语言功能障碍或构音障碍;②有卒中或其他神经系统疾病病史;③有严重内科疾病及视听障碍;④存在精神障碍或焦虑抑郁状态;⑤存在MRI检查禁忌证。
本研究获得南方医科大学附属广东省人民医院伦理委员会批准(伦理审查编号:KY-Q-2021-143-01)。所有受试者或其法定监护人均签署知情同意书。
1.2 研究方法
1.2.1 一般临床资料收集 根据患者住院信息收集所有受试者的人口学资料,包括年龄、性别、文化程度、既往史、病程等,以及实验室检查[游离三碘甲状腺原氨酸(free triiodothyronine,FT3)、游离甲状腺素(free thyroxin,FT4)、促甲状腺激素(thyroidstimulating hormone,TSH)、叶酸、维生素B12、尿酸、Hcy、TC、TG、HDL-C、LDL-C和糖化血红蛋白]结果。
1.2.2 临床症状评估 由2名神经科主治医师使用MMSE和MoCA评估受试者的整体认知功能,使用HAMA和HAMD评估受试者精神状态,使用国际运动障碍协会(Movement Disorder Society,MDS)修订的统一帕金森病评定量表的第三部分(unified Parkinson's disease rating scale-Ⅲ,UPDRS-Ⅲ)和Hoehn-Yahr(H&Y)分期评估受试者运动症状严重程度及分期,所有受试者均在关期进行测评。
1.2.3 影像学资料采集 所有受试者均使用GE 3.0T(Signal Excite Ⅱ HD)超导型磁共振扫描仪或GE 1.5T(Signal Infinity Twin Speed,Milwaukee WI)超导型磁共振扫描仪进行头颅MRI扫描,并由同一名影像科技师进行操作。序列为横断面的T1WI和T2WI、矢状位的T2WI和T2FLAIR序列。
1.2.4 脑白质高信号评分 由2名影像学专家使用Scheltens半定量视觉评级量表对受试者MRI显示的脑室旁周围白质高信号(periventricular hyperintensities,PVH)、深部白质高信号(deep white matter hyperintensities,DWMH)、基底节白质高信号和幕下白质高信号这4个视觉评分区域进行评分,分值越高代表脑白质损伤越严重[9]。
PVH:包括额叶帽状白质高信号、枕叶帽状白质高信号和侧脑室带状白质高信号,每个区域0~2分,各部位总分范围0~6分。
DWMH:包括额叶、顶叶、枕叶、颞叶4个评分区域,每个区域0~6分,各部位总分范围0~24分。
基底节白质高信号:包括尾状核、豆状核、丘脑、苍白球及内囊5个评分区域,每个区域0~6分,各部位总分范围0~30分。
幕下白质高信号:包括小脑、中脑、脑桥和延髓4个评分区域,每个区域0~6分,各部位总分范围0~24分。
1.3 统计学方法 采用SPSS 25.0软件对数据进行统计分析。符合正态分布的计量资料以表示,组间比较使用单因素方差分析;不符合正态分布的计量资料以M(P25~P75)表示,组间比较采用秩和检验,根据正态性检验结果,事后两两比较使用LSD检验或Tamhane检验。计数资料以率和频数表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 3组临床特征与生化指标比较 共26例VP患者、26例PD患者及13例HC完成临床症状评估、生化指标检查和MRI检查,3组受试者的年龄、性别、受教育年限、糖尿病病史、高脂血症病史、冠心病病史、饮酒史、家族史差异均无统计学意义(表1)。与PD组相比,VP组HAMA评分更高,有高血压病史、卒中病史、吸烟史者更多,MMSE评分、MoCA评分更低,差异具有统计学意义;两组病程、UPDRS-Ⅲ、H&Y分期和生化指标差异无统计学意义(表1、表2)。与HC组相比,VP组Hcy和FT4水平更高,叶酸、TC、TG、HDL-C和LDL-C水平更低,HAMA和HAMD评分更高,MMSE和MoCA评分更低,差异具有统计学意义(表1、表2)。

表1 VP组与PD组、HC组一般临床资料与临床症状比较Table 1 Comparison of general clinical data and clinical symptoms among VP group,PD group and HC group
2.2 3组不同脑区白质高信号评分比较 与PD组相比,VP组DWMH总分、PVH总分、WMH总分以及额角帽状白质高信号、侧脑室带状白质高信号、额叶深部白质高信号、顶叶深部白质高信号、基底节白质高信号、壳核白质高信号评分更高,差异具有统计学意义(表3)。与HC组相比,VP组DWMH总分、PVH总分、WMH总分以及额角帽状白质高信号、枕角帽状白质高信号、侧脑室带状白质高信号、额叶深部白质高信号、顶叶深部白质高信号、基底节白质高信号、尾状核白质高信号、壳核白质高信号及脑桥白质高信号评分更高,差异具有统计学意义(表3)。VP组、PD组、HC组3组受试者典型顶叶、额叶白质高信号MRI见图1,典型侧脑室、基底节区白质高信号MRI见图2。

图1 3组受试者典型顶叶、额叶白质高信号MRIFigure 1 White matter hyperintensities MRI of typical parietal lobe and frontal lobe of three groups subjects
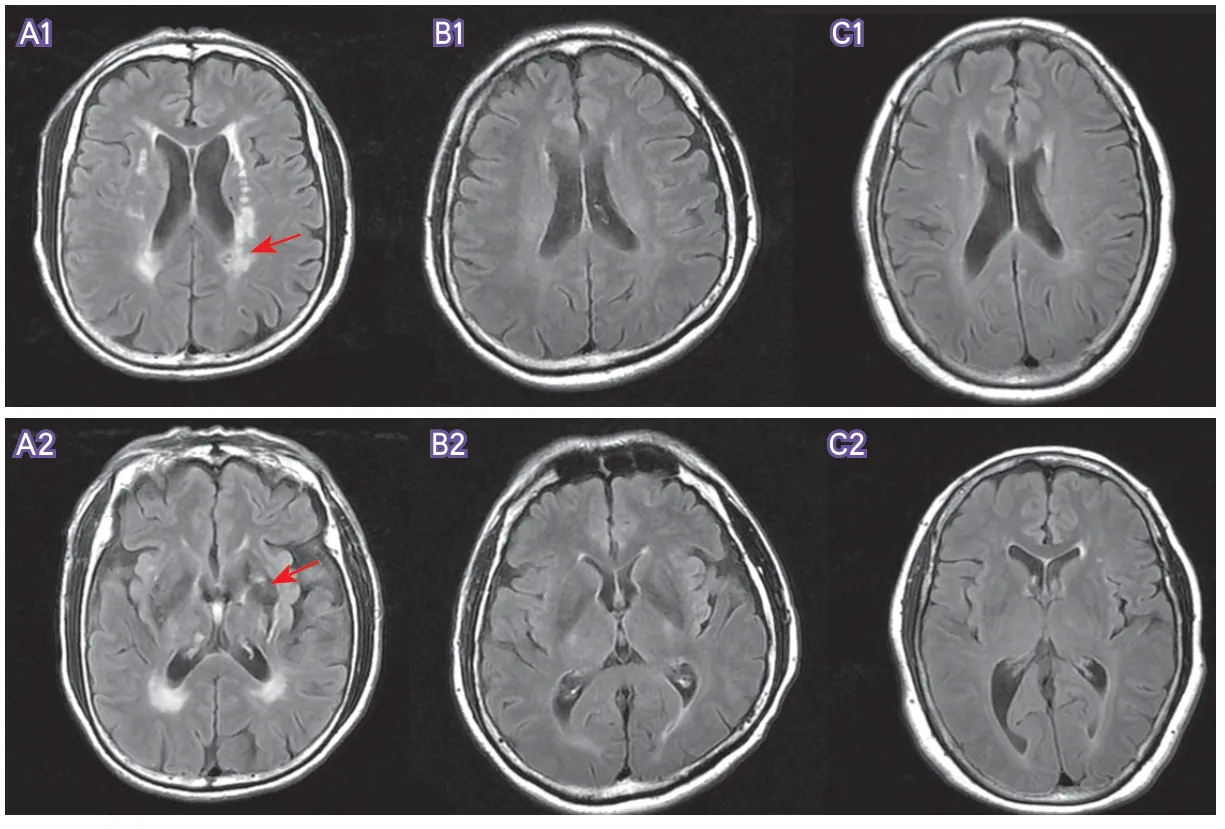
图2 3组受试者典型侧脑室、基底节区白质高信号MRIFigure 2 White matter hyperintensities MRI of typical lateral ventricle and basal ganglia of three groups subjects

表3 VP组与PD组、HC组不同脑区白质高信号评分比较Table 3 Comparison of white matter hyperintensities in different brain regions of VP group,PD group and HC group 单位:分
3 讨论
VP是一种继发性帕金森综合征,目前对其认识尚不足,血管危险因素和白质损伤在VP中比在PD中更为常见[10-11]。本研究发现VP组与PD组血管危险因素及WMH差异存在统计学意义。
本研究通过对比生化指标发现VP组Hcy水平较HC组增高,有研究认为Hcy可能是VP的危险因素,且可能与VP的认知功能障碍相关[12]。Hcy水平过高可损伤血管内皮细胞,在高血压、脑血管病及神经退行性疾病的进展中有重要作用[13-16]。本研究发现VP组有高血压病史、卒中病史的患者比例也较HC组和PD组高,而Fitzgerald等[17]通过对比VP组与PD组的既往史发现VP组只有高血压病史比PD组更常见。VP的起病与卒中的密切关联常被认为是VP的重要支持标准,较常见的血管危险因素与原发疾病还会导致其认知障碍较PD更早出现,本研究中VP组的MoCA评分、MMSE评分均较PD组、HC组低,与既往研究一致[18],其机制可能是皮质-纹状体通路的破坏或神经传导通路脱髓鞘改变[19]。
血管危险因素与白质损伤关系密切,高血压是导致白质损伤的重要危险因素,神经血管炎症可能在其中发挥重要作用[20]。VP常有广泛的白质损伤[11],本研究中,VP的DWMH总分、WMH总分、PVH总分、运动相关脑区PVH评分(额角帽状白质高信号评分、侧脑室带状白质高信号评分)、运动相关脑区DWMH评分(额叶深部白质高信号评分、顶叶深部白质高信号评分)、基底节白质高信号评分和壳核白质高信号评分均较PD高,与既往研究一致[7,19]。WMH在临床上与多种疾病相关,可能反映血管缺血缺氧改变,也可能反映淀粉样蛋白在血管的沉积[1]。白质损伤可能因少突胶质细胞减少导致纤维连接中断[2],继而影响纹状体多巴胺转运体的功能从而导致运动障碍[21-22]。PVH与姿势控制动态平衡相关[23],其可能破坏发自皮质下多巴胺能和胆碱能的投射纤维导致相应的运动障碍[22]。PVH和DWMH被认为是连续的病理过程[24]。额叶深部白质的损害会引起皮质-皮质下通路的中断,从而导致步态、平衡障碍,有研究发现额叶纤维束可能与VP患者双下肢运动障碍密切相关[4],额叶DWMH与轴向运动密切相关[25],额叶神经纤维束的损伤可能通过影响非多巴胺能运动通路或突触后黑质纹状体通路在轴向运动损伤中起重要作用[26]。顶叶是感觉-运动网络的一部分,其中额叶-丘脑-顶叶网络参与运动的控制,其结构损伤会产生轻偏瘫、姿势异常、肌张力障碍和不自主运动等运动障碍[27-29]。基底节的基底节-丘脑-大脑皮质回路参与运动的发起,额叶脑桥束、皮质脊髓束和皮质脑桥束等参与运动的协调,壳核处有感觉运动纤维连接[30],其结构损伤会导致纹状体多巴胺转运体功能障碍,继而产生帕金森综合征症状[31]。
4 结论
尽管VP的发病机制目前尚不明确,本研究结合研究结果与既往文献推测高血压病史、卒中病史和运动相关脑区白质损伤可能在VP的发病中起重要作用,不同脑区受损有不同的运动特点,为VP发病机制的研究和诊治提供一定的依据。本研究缺点在于样本量较少,且为横断面研究,也未根据VP临床亚型进一步分组,对疾病进展的观察有限,未来需要收集更多的样本量,进行更详细的分组和更长时间的随访来分析其临床特征与脑白质的关系。
利益冲突所有作者均声明不存在利益冲突。
