25G玻璃体切除联合DEX治疗PDR继发玻璃体积血伴DME
2023-09-27焦晓玲张俊凇
焦晓玲,张俊凇,王 霞,陈 伟,张 悦
目的:评价25G玻璃体切除(PPV)联合地塞米松玻璃体内植入剂(DEX)治疗增殖性糖尿病视网膜病变(PDR)继发玻璃体积血伴糖尿病性黄斑水肿(DME)的临床效果。
方法:前瞻性临床病例研究。选取2020-07/2022-01天津市眼科医院收治的PDR继发玻璃体积血伴DME的患者40例40眼,所有患者均行玻璃体切除和白内障超声乳化手术,随机分为PPV组(20眼)和PPV+DEX组(20眼)。比较两组患者术前,术后1、3、6mo最佳矫正视力(BCVA)、眼压及黄斑中心凹厚度(CMT)。
结果:所有患者均完成术后6mo随访。术后1、3、6mo PPV+DEX组患者BCVA均优于PPV组(P<0.05)。术后1mo,PPV+DEX组CMT低于PPV组(P<0.05)。随访6mo,PPV组术后出现视网膜新生血管或CMT消退小于5%者8眼行补充抗VEGF治疗,PPV+DEX组仅有1眼(P<0.05)。
结论:玻璃体切除手术联合应用地塞米松植入剂可以产生协同效应,为PDR继发玻璃体积血伴DME的患者提供更优的治疗效果。
•KEYWORDS:diabetic macular edema(DME); vitreous hemorrhage; Dexamethasone intravitreal implants(DEX); pars plana vitrectomy
0 引言
众所周知,糖尿病的患病率在逐年提高,我国已经成为全球拥有糖尿病患者最多的一个国家[1]。作为糖尿病的主要并发症,糖尿病视网膜病变近年来也呈爆发式增长。增殖性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)是一种致盲性眼病,现已成为我国导致劳动力丧失的最主要的眼病[2]。无法自行吸收的玻璃体积血、纤维增生膜和牵拉性视网膜脱离是PDR的临床表现,也是行玻璃体切除手术(pars plana vitrectomy,PPV)的主要指征。PDR继发玻璃体积血的患者常伴有糖尿病性黄斑水肿(diabetic macular edema,DME),DME会影响玻璃体积血清除后患者视力的恢复。炎症在DME的发病机制起主要作用:炎性细胞激活后释放炎性因子,增加血管通透性,破坏了血-视网膜屏障,导致DME[3-4]。地塞米松玻璃体内植入剂(dexamethasone intravitreal implant,DEX)是一种可生物降解材料,可以释放地塞米松长达3~6mo,可以用于玻璃体切除术后抗炎并治疗DME[5,6]。本研究观察因PDR继发玻璃体积血伴DME在我院行玻璃体切除手术的患者,探讨玻璃体切除联合地塞米松植入物的临床疗效。
1 对象和方法
1.1对象前瞻性临床病例研究。选取2020-07/2022-01天津市眼科医院收治的PDR继发玻璃体积血伴DME的患者40例40眼。纳入标准:(1)玻璃体积血时间1~3mo;(2)伴发白内障,晶状体核Ⅱ级以上;(3)最佳矫正视力(best corrected visual acuity,BCVA)为0.01~0.5,眼压正常,眼底彩色超声提示玻璃体积血,光学相干断层扫描提示黄斑中心凹厚度(central macular thickness, CMT)大于300μm;(4)所有患者均完成6mo随访。排除标准:(1)既往行眼内手术、激光或者眼内注药治疗;(2)青光眼、虹膜新生血管、牵拉性视网膜脱离或者有其他可能会干扰到疗效观察的特殊情况。本研究通过天津市眼科医院医学伦理委员会审批,遵循《赫尔辛基宣言》,所有患者术前均签署知情同意书。
1.2方法所有患者均行PPV联合白内障超声乳化手术。手术由同一位经验丰富的医师操作,所有患者术前行左氧氟沙星滴眼液滴术眼,术前5d玻璃体腔内注射抗血管内皮生长因子(VEGF)药物(康柏西普)0.05mL[7]。于角膜缘切口行白内障超声乳化手术,晶状体摘除后前房内注入少量黏弹剂,再经睫状体平坦部常规切口行三通道25G玻璃体切除术,清除玻璃体积血,使用玻切头切除纤维血管膜,眼内电凝活动的出血点,完成全视网膜激光光凝,将人工晶状体植入囊袋内,行气-液交换,注入消毒空气。手术结束时PPV+DEX组将0.7mg地塞米松植入物注入玻璃体腔。术毕结膜囊内涂左氧氟沙星滴眼液和妥布霉素地塞米松眼膏。检查术前,术后1、3、6mo患者BCVA(采用国际标准Snellen视力表记录视力结果,统计分析时再转换为LogMAR视力)、眼压及CMT。在术后6mo随访中,如患者出现视网膜新生血管或CMT消退小于5%时再次行玻璃体腔内注射康柏西普0.05mL。

2 结果
2.1两组患者术前一般资料比较本研究共纳入患者40例40眼,其中男21例,女19例,年龄38~72岁,糖尿病病程2~15a。随机分为PPV组(20眼)和PPV+DEX组(20眼),两组患者术前的性别、平均年龄、病程、晶状体核的分级比较差异均无统计学意义(P>0.05,表1)。

表1 两组患者术前的一般资料
2.2两组患者手术前后BCVA比较两组患者手术前后BCVA时间和组别比较差异均有统计学意义,但交互效应比较差异无统计学意义(F时间=58.087,P时间<0.001;F组别=7.392,P组别=0.007;F时间×组别=0.569,P时间×组别=0.636)。术前两组患者BCVA比较差异无统计学意义(P>0.05),术后1、3、6mo PPV+DEX组BCVA优于PPV组,差异均有统计学意义(P<0.05),各组患者术后不同时间BCVA均较术前改善,差异均有统计学意义(P<0.05),见表2。

表2 两组患者手术前后BCVA比较
2.3两组患者手术前后CMT比较两组患者手术前后CMT时间和组别比较差异均有统计学意义,但交互效应比较差异无统计学意义(F时间=34.728,P时间<0.001;F组别=5.822,P组别=0.017;F时间×组别=1.166,P时间×组别=0.325)。术前两组患者CMT比较差异无统计学意义(P>0.05),术后1mo PPV+DEX组CMT较PPV组降低,差异有统计学意义(P<0.05),术后3、6mo两组患者CMT比较差异均无统计学意义(P>0.05),各组内进一步两两比较见表3。

表3 两组患者手术前后CMT比较
2.4两组患者手术前后眼压比较两组患者手术前后眼压时间和组别比较差异均有统计学意义,但交互效应比较差异无统计学意义(F时间=3.518,P时间=0.017;F组别=27.252,P组别<0.001;F时间×组别=2.637,P时间×组别=0.052)。术前两组患者眼压比较差异无统计学意义(P>0.05),术后1、3、6mo PPV+DEX组眼压高于PPV组,差异均有统计学意义(P<0.05),各组内进一步两两比较见表4。
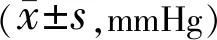
表4 两组患者手术前后眼压比较
2.5两组患者术后补充康柏西普治疗情况随访6mo,PPV组术后补充康柏西普治疗8眼,其中5眼在术后1mo行玻璃体腔注射康柏西普,其中3眼在术后3mo再次行康柏西普治疗。PPV+DEX组仅有1眼在术后3mo行康柏西普治疗,两组患者术后补充康柏西普治疗比较差异有统计学意义(χ2=6.135,P=0.013)。
2.6两组患者术后并发症情况术后1mo,PPV+DEX组有2眼(10%)出现不同程度的眼压升高,使用盐酸卡替洛尔治疗1wk眼压控制至正常。随访6mo,所有患者术后未出现复发性玻璃体积血、视网膜脱离、爆发性脉络膜出血、眼内炎、恶性青光眼、伤口渗漏等玻璃体切除手术的常见并发症。
3 讨论
PPV是目前公认的治疗PDR继发玻璃体积血的有效方法。随着玻璃体切除技术的飞速发展,目前的研究主张在玻璃体积血早期行手术治疗,即保守治疗超过1mo后积血仍未吸收者便需要接受手术治疗,以免延误病情[8-9]。据最近的研究报道,PPV也有利于DME的治疗,可能的作用机制包括去除牵引因素,改善玻璃体腔对视网膜的供氧,以及去除各类促进血管渗漏的细胞因子和炎症介质[10-11]。本研究采用的25G微创玻璃体切割系统,无需剪开球结膜,巩膜切口小,无需缝合,创伤小,手术后PPV+DEX组和PPV组患者视力均明显提高。本研究中所有患者术后6mo内均未发生复发性玻璃体积血等常见的PPV并发症,因为术前筛查比较严格,排除了虹膜新生血管、牵拉性视网膜脱离等重度PDR的患者,也可能要归因于术前的抗VEGF治疗和术中完成的全视网膜光凝。
术前抗VEGF、PPV及行全视网膜光凝均有利于DME的治疗,但结果显示在术后1mo,PPV+DEX组的CMT较术前明显降低,而PPV组的CMT与术前相比却无显著差异。炎症在DME中作用是近年来研究的热点,尤其在难治性DME中,炎症发挥着至关重要的作用[12-13]。地塞米松等类固醇激素可以阻断VEGF和其他炎症因子的产生,抑制巨噬细胞和白细胞黏附和迁移,并加强血-视网膜屏障的紧密连接,有效地治疗DME[14]。DEX可以在6mo的时间内将地塞米松释放到玻璃体中[15],于2021-08在我国被批准用于治疗成年DME患者[2]。据最新的指南推荐,在人工晶状体(IOL)眼或PPV眼,激素可以考虑作为治疗DME的一线用药[2]。据报道[16-17],PPV联合DEX对难治性DME有很好的疗效,本研究也发现联合DEX可以更有效地减轻DME,在术后1mo,PPV+DEX组的CMT与PPV组相比有显著差异。
目前,抗VEGF药物是治疗DME的一线药物,但是其在PPV术后的眼睛中清除过快,因此需要更频繁地眼内注射,相关并发症发生率高[18]。DEX已被证明在玻璃体切除和非玻璃体切除的眼睛中具有相似的药代动力学特征,与传统的抗VEGF药物比较,拥有更长效、更稳定的抗炎效果,同时减少了眼内频繁注药的不良反应[18-19]。本研究中,比较两组患者术后补充治疗情况,PPV+DEX组明显要少于PPV组。证实PPV联合DEX可以长期有效消退DME,减少眼内注药次数,可以降低频繁的眼内注射导致的眼部并发症,更降低了因抗VEGF治疗引发心脑血管意外的风险[20]。本研究发现在术后3、6mo,因为补充康柏西普治疗,PPV组的CMT平均值显著减低,与PPV+DEX组比较无差异。但是在这两个随访时间点,两组的BCVA比较仍有明显的差异,两组之间CMT与BCVA的变化出现了不平行,值得进一步的研究与探讨。
糖尿病患者的白内障患病率高且进展快,此外玻璃体切除手术也会加速白内障的进程[21],对伴发白内障的PDR患者,本研究选择PPV联合白内障超声乳化手术。联合手术的优点是手术过程中眼底视野更加的清晰,而且白内障的摘除也为术后视力的观察减少了干扰项。DEX的副作用主要是眼压升高和加速白内障的进程[22]。本研究中,患者都顺利联合实施了白内障超声乳化及人工晶状体植入术,因此无需担心DEX对晶状体的影响。但对DEX可能诱导的眼压升高仍需谨慎对待,术后要定期监测眼压。在本研究中,DEX确实导致PPV+DEX组术后眼压平均值明显高于PPV组,并且术后1mo的眼压平均值与其他时间点相比有显著差异。
总之,本研究发现PPV联合DEX能够产生协同效应,可为PDR继发玻璃体积血伴DME的患者提供更优的治疗效果。但研究依然有一些局限性:(1)随访时间短,虽然大多数术后并发症可能会6mo内出现,但其他PDR和PPV相关并发症可能在更长的随访时间里出现;(2)本研究的患者筛查比较严格,导致样本量偏小,甚至可能会出现选择偏倚,日后有必要进行更大规模的研究以进一步论证研究结果。
