lncRNA H19经BMPs/TGF-β途径对骨质疏松老龄大鼠脂肪干细胞成骨分化的影响
2023-09-26黄长智林久灶黄聿峰黄兆曦柯铭锋陈挺霖
黄长智 林久灶 黄聿峰 黄兆曦 柯铭锋 陈挺霖
(宁德师范学院附属宁德市医院骨科,福建 宁德 352000)
骨质疏松是指以骨小梁减少、骨质改变及骨脆性增加为表现的疾病,多发于老年人群,随着我国人口老龄化的加剧,老年骨质疏松的发病率逐渐升高,报道称〔1〕,因骨质疏松所致的骨折和骨缺损是目前急需解决的问题。研究发现〔2,3〕,脂肪干细胞与骨髓间充质干细胞类似,均具有多向分化潜能,其可作为种子细胞用于骨质疏松的治疗。长链非编码RNA(lncRNA)属于一类非编码RNA,其参与多种生物进程,如干细胞分化、细胞增殖及包括骨质疏松在内的多种疾病的发生进展,研究认为〔4〕,在成骨分化过程中,lncRNA具有促进或抑制干细胞成骨分化的作用。lncRNA H19属于lncRNA成员,其位于11号染色体上,研究显示〔5〕,其对干细胞成骨分化具有正向促进作用。张传志等〔6〕在其研究中认为,lncRNA H19参与骨质疏松的发生和进展。本研究为了更好地促进骨质疏松老龄大鼠脂肪干细胞成骨分化,做lncRNA H19转染处理,分析转染lncRNA H19对脂肪干细胞成骨分化的影响。
1 材料与方法
1.1材料 研究动物:选取18~20月龄老龄大鼠10只,购自广州国家实验室〔动物许可证号SYXK(粤)2022-0285〕,体质量为500~700 g,均常规分笼饲适应喂养7 d,自由进食、饮水,室温控制在21~25 ℃,相对湿度控制在45%~50%,光暗交替周期为12 h。操作均符合动物实验伦理要求。主要试剂及仪器:维甲酸(深圳振强生物技术有限公司);lncRNA H19 siRNA慢病毒载体、空载体(上海吉玛);茜素红染色液、碱性磷酸酶(ALP)活性检测试剂盒(北京伊塔生物科技有限公司);骨形态发生蛋白(BMP)-2、转化生长因子(TGF)-β、Smad1、Smad2抗体(深圳海思安生物技术有限公司)。流式细胞仪(贝克曼库尔特);倒置显微镜(美国BD)。
1.2骨质疏松模型构建 10只大鼠中5只作为空白组,正常喂养,另外5只每日使用70 mg/kg灌胃构建骨质疏松模型,14 d后观察大鼠骨密度、股骨近端组织病理变化。
1.3骨质疏松老龄大鼠脂肪干细胞分离、培养 将骨质疏松大鼠处死后,沿腹股沟处切开皮肤,暴露皮下脂肪,去除筋膜组织后,取脂肪组织,将其剪碎后常规培养,接种于培养瓶内,在DMEM培养液内脂肪原代干细胞,待细胞长满至培养瓶底75%~80%时使用酶消化法行1∶3传代,传至第三代备用。使用流式细胞仪测定第3代脂肪干细胞免疫表型。
1.4lncRNA H19转染及转染效率鉴定 将所制备的脂肪干细胞分为3组,即不做任何处理仅做细胞常规培养的对照组、转染lncRNA H19空载体的空载组、转染lncRNA H19 siRNA慢病毒载体的H19 siRNA组。48 h后做后续指标观察。
使用实时荧光定量PCR法测定lncRNA H19转染效率,提取并测定细胞RNA纯度,反转录获得cDNA,以cDNA为模板,做PCR扩增,扩增体系:0.4 μl lncRNA H19上游引物、0.4 μl lncRNA H19下游引物、1 μl cDNA模板、10 μl SYB Green,加蒸馏水至20 μl。扩增条件:94 ℃预变性1 min、55 ℃ 1 min、72 ℃ 1 min,72 ℃延伸5 min,40个循环,采用2-ΔΔCt方法计算lncRNA H19表达量。lncRNA H19上游引物:5′-GCCTGAGTCTCTCCGTATGG-3′,下游:5′-GAAGGAAGGTGCGTTGAACA-3′;内参β-actin上游引物:5′-TCTCTGGTCCTGGGTCTTGT-3′,下游:5′-ATGGCTTGTCAAGGCAGTTTC-3′。
1.5脂肪干细胞成骨分化能力测定 以5×104个/孔的密度将细胞接种于96孔板上,固定后磷酸盐缓冲液(PBS)清洗,加入2%茜素红1 ml,避光30 min后对细胞矿化结节形成情况进行观察,结节越多成骨能力越强。
1.6脂肪干细胞ALP染色和活性测定 以5×104个/孔的密度将细胞接种于96孔板上,24 h后使用40 g/L多聚甲醛固定,培养皿底部使用One-StepTMNBT/BCIP溶液完全覆盖后在室温、避光环境下孵育1 h,使用倒置显微镜观察细胞ALP染色情况,同时使用ALP试剂盒测定ALP活性。
1.7成骨基因测定 使用实时荧光定量PCR法测定成骨基因RUNX2、OPN、OCN表达量,方法同1.4。RUNX2上游引物:5′-CAATGACCCCTTCATTGACC-3′,下游:5′-GGCAGCTTCCCAGGGGTAA-3′;OPN上游引物:5′-CACCGAGACAGGATCAGAGG-3′,下游:5′-CTTTGGGACACAAGCCCGTGC-3′;OPN上游引物:5′-ACTTGCAGCGAGGTAGTGAAGA-3′,下游:5′-AACTCGTCAAGGTCCGGATTG-3′。
1.8BMPs/TGF-β信号通路蛋白测定 将脂肪干细胞裂解后提取蛋白,二喹啉甲酸(BCA)测定蛋白浓度,之后经蛋白与缓冲液以4∶1的比例混合均匀后煮沸使其变性,加脱脂奶粉,置于聚偏氟乙烯膜上,加1∶2 000稀释的一抗(BMP-2、TGF-β、Smad1、Smad2),孵育过夜。第2天使用Tris-HCl缓冲盐溶液清洗,加入二抗,增强化学发光法显影,定影,获得目标蛋白表达量。
1.9统计学分析 采用SPSS26.0软件进行方差分析、t检验。
2 结 果
2.1骨质疏松模型验证 骨质疏松组骨密度较空白组明显降低(P<0.05)。见表1。HE染色显示,空白组骨组织形态完整,骨小梁排列整齐,结构饱满,骨质疏松组骨小梁数量减少,排列不齐,断裂,间隙增宽。见图1。说明骨质疏松模型建立成功。

图1 两组股骨近端骨组织病理(HE染色,×200)
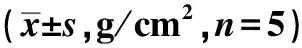
表1 空白组、骨质疏松组骨密度比较
2.2骨质疏松老龄大鼠脂肪干细胞培养、鉴定 镜下观察显示,骨质疏松老龄大鼠第三代脂肪干细胞多为长梭形、多角形,见图2。脂肪干细胞表面抗原CD73、CD90等阳性标志物表达较高,分别为99.80%、100.00%,CD34、CD45等阴性标志物表达较低,分别为0.23%、0.80%,提示所培养的细胞为脂肪来源干细胞。

图2 第三代脂肪干细胞镜下形态
2.3lncRNA H19转染效率鉴定 H19 siRNA组lncRNA H19表达量明显低于对照组、空载组(P<0.05),对照组、空载组比较无显著差异(P>0.05)。见表2。

表2 lncRNA H19转染效率及lncRNA H19对脂肪干细胞ALP活性的影响
2.4lncRNA H19对脂肪干细胞ALP活性的影响 H19 siRNA组ALP活性明显高于对照组、空载组(P<0.05)。见表2、图3。

图3 各组ALP活性(NBT/BCIP染色,×100)
2.5lncRNA H19对脂肪干细胞成骨分化能力的影响 H19 siRNA组矿化结节较多,颜色为深红,对照组、空载组仅有少量矿化结节,说明H19 siRNA组成骨分化能力较对照组、空白组增强。见图4。

图4 3组脂肪干细胞成骨分化能力(茜素红染色,×100)
2.6lncRNA H19对脂肪干细胞成骨基因的影响 H19 siRNA组成骨基因RUNX2、OPN、OCN表达量明显高于对照组、空载组(P<0.05)。见表3。

表3 lncRNA H19对脂肪干细胞成骨相关基因的影响
2.7lncRNA H19对脂肪干细胞BMPs/TGF-β信号通路蛋白表达的影响 H19 siRNA组BMPs/TGF-β信号通路蛋白BMP-2、TGF-β、Smad1、Smad2表达量均明显高于对照组、空载组(P<0.05)。见表4、图5。

图5 3组BMPs/TGF-β信号通路蛋白表达

表4 lncRNA H19对脂肪干细胞BMPs/TGF-β信号通路蛋白表达的影响
3 讨 论
骨质疏松发病率随着年龄的增加而增加,究其原因可能与随着年龄的增长,人体骨骼中骨质改变导致骨密度降低有关,而此病的发生本质为成骨和破骨细胞失衡〔7〕。近年来随着临床上对干细胞的逐渐研究发现〔8,9〕,干细胞具有较强的成骨分化作用,在移植后可抑制成骨和破骨细胞失衡,促进两者平衡,进而增加骨密度,在骨质疏松的治疗中具有较高的价值。有报道显示〔10,11〕,骨质疏松的发生涉及多个机制,lncRNA属长链非编RNA,主要分布于细胞核、细胞质内,其结构和来源与微小RNA类似,均是由RNA聚合酶Ⅱ转录所得,通常情况下,lncRNA在RNA水平上可经调节相关靶基因的表达而发挥作用。lncRNA H19具有促进肿瘤发生进展、细胞分化、胚胎生长的作用〔12,13〕。研究发现〔14〕,在骨质疏松发生过程中lncRNA H19可经影响成骨/破骨细胞、骨髓间充质干细胞参与骨代谢过程,其在骨质疏松中表达降低。Li等〔15〕在其报道中认为,在骨质疏松中lncRNA H19上调可促进炎症因子的过度表达,抑制成骨细胞增殖。
目前有关lncRNA H19的研究主要以对干细胞成骨分化和成脂分化为主,在骨质疏松中其可经作用于微小RNA-532-3p/沉默信息调节因子1信号通路诱导骨髓间质干细胞成骨分化〔16〕。一项研究发现,lncRNA H19可经调控成骨相关蛋白BMP-2的表达而增强干细胞成骨分化能力〔17〕。Zhong等〔18〕报道显示,lncRNA H19通过调控miR-140-5p和BMP-2/FGF9促进人牙髓干细胞成牙本质细胞分化。上述报道均证实,lncRNA H19具有促进干细胞成骨分化的作用,但有关lncRNA H19对骨质疏松来源脂肪干细胞成骨分化的报道较少,本研究结果说明,lncRNA H19具有促骨质疏松来源脂肪干细胞成骨分化的作用。
ALP在成骨诱导过程中最先反应,在成骨分化开始时ALP活性增加,随着成骨分化能力的增强,其活性逐渐增加,其活性高低与成骨分化能力正相关〔19,20〕。RUNX2可影响骨/成骨细胞分化、成骨基因表达和骨形成,临床上多根据其水平评估成骨能力〔21,22〕。OPN、OCN分别均由骨质细胞产生,参与骨吸收、骨改变,两者水平可直接反映出骨形成状态〔23〕。本研究结果说明,lncRNA H19具有促进脂肪干细胞成骨分化的能力。
本研究结果说明,BMPs/TGF-β可能是lncRNA H19促进脂肪干细胞成骨分化的作用途径。研究表明,BMPs/TGF-β信号通路中BMP-2、TGF-β为信号传递分子,其中BMP-2属于一种酸性糖蛋白,其主要来源于骨相关结缔组织和软骨组织,可促新骨形成〔24,25〕。TGF-β主要来源于骨基质,其参与机体骨代谢稳定和骨架维护〔26〕。研究发现〔27,28〕,TGF-β在发挥作用的过程中作用于特定配体的受体复合物Smads发挥作用,在上述作用下,Smads被激活,进而影响下游靶基因转录,增加ALP活性,促进成骨分化。另外BMPs/TGF-β信号通路分子BMP-2、TGF-β经共同作用于四聚体受体复合体,可同时向典型和非典型的Smads传递信号,进而影响成骨细胞分化、骨形成和骨稳态〔29〕。本研究发现,lncRNA H19在骨质疏松中可能经BMPs/TGF-β途径促进脂肪干细胞成骨分化。
虽然本研究认为lncRNA H19可能经BMPs/TGF-β途径促进RUNX2、OPN、OCN等成骨基因表达而发挥促骨质疏松老龄大鼠脂肪干细胞成骨分化的作用,但本研究并未进一步分析lncRNA H19与BMP-2、TGF-β的靶向关系,且目前临床上有关此类的研究较少,因此还需后续研究进一步深入探讨。
