麦麸主要组分的分离与成分分析
2023-09-22刘海棠
刘 盛, 刘海棠
(中国轻工业造纸与生物质精炼重点实验室, 天津市制浆造纸重点实验室,天津科技大学轻工科学与工程学院, 天津 300457)
麦麸是小麦加工的副产品,富含纤维素、半纤维素、木质素及蛋白质和酚类等丰富的物质[1]。 与小麦相比,麦麸的纤维素含量较高,既可以添加到食品中给人补充营养, 还可将其作为原料进行进一步开发及利用[2]。 我国麦麸的年产量高达0.26 亿t,主要应用于食品、药品、饲料的原料和酿酒等方面[3]。 然而,麦麸在造纸方面的应用研究并未深入。 本文对麦麸的纤维素、半纤维素、木质素进行分离并对主要组分的含量与结构进行分析, 同时也对麦麸是否能作为造纸原料进行了讨论。
1 实验
1.1 原料与试剂
实验所用麦麸的产地为皖北地区, 由于未经过特殊处理,麸皮呈现不规则大小及形状,经过高速多功能粉碎机处理后过40 目筛,置于烘箱, 于45 ℃烘干6 h 以上,保存于干燥器内。
过氧化氢,分析纯,天津市风船化学试剂科技有限公司;醋酸,分析纯,福晨(天津)化学试剂有限公司;浓硫酸,分析纯,天津市化学试剂供销公司;氢氧化钠,分析纯,天津市津东天正精细化学试剂厂;无水甲醇、无水乙醇,分析纯,天津国药集团;去离子水,实验室自制。
1.2 实验设备
TU-181OPC 型紫外-可见分光光度计, 北京普析通用仪器有限责任公司;650 型傅里叶红外光谱仪, 天津港东科技发展股份有限公司;769YP-15A型粉末压片机, 青岛华青集团有限公司;800Y 型高速多功能粉碎机, 永康市铂欧五金制品有限公司;DSX-24L-I 型手提式高压蒸汽灭菌器,上海申安医疗器械厂;JSM-IT300LV 型扫描式电子显微镜,日本电子株式会社;HHS-21-4 型数显恒温水浴锅,上海博讯实业有限公司医疗设备厂;SB-5200 型超声波清洗机, 宁波新艺生物科技股份有限公司;OSB-2100 型油浴锅,上海爱朗仪器有限公司;SHB-III 型循环水式多用真空泵,天津科诺仪器设备有限公司;BAO-150A 型精密鼓风干燥箱、VOS-60A 型真空干燥箱,施都凯仪器设备(上海)有限公司;AR2140 型分析天平,梅特勒-托利多仪器(上海)有限公司;ICS-5000 型离子色谱仪,谱质分析检测技术(上海)有限公司。
1.3 实验方法
1.3.1 麦麸纤维素、半纤维素的提取[4]
取一定量经过预处理后的麦麸(每次约取25 g),经蒸馏水润洗3 次后挤干水。
按料液比(g∶mL)1∶10~13 加入250 mL 4%的稀硫酸溶液,利用pH 指示剂,保证加入稀硫酸后的料液pH 维持在1.5,于90 ℃水浴锅中浸渍1.5~2.0 h。
随后趁热过滤,用热水多次洗涤滤渣,用pH 试纸检测,直至滤渣显中性。
按料液比(g∶mL)1∶10~12 加入250 mL 0.5 mol/L的NaOH 溶液,常温浸提2.5 h 后过滤。
滤液用醋酸调节pH 至6~7,用料液3 倍体积的无水乙醇沉淀,离心收集沉淀,放入烘箱中干燥,研磨粉碎获得半纤维素。
滤渣用水洗至中性,常温下用5%的H2O2漂白,经烘箱干燥、粉碎、过筛后获得水不溶性纤维素。
研磨处理提取出的纤维素、半纤维素,置于密封袋中保存备用。
1.3.2 木质素的提取[5]
称取0.3 g 麦麸预处理样品于100 mL 三角瓶中,加入3 mL 72%的浓硫酸,放入超声波清洗机中反应至样品与硫酸充分混合,后置于摇床上,在室温25 ℃、150 r/min 条件下反应1 h。
加入84 mL 去离子水,在121 ℃的手提式高温灭菌锅中恒温反应1 h。
静止冷却后,用G4 砂芯漏斗过滤样品酸解液,酸不溶木质素用滤纸过滤分离, 过滤后将滤纸和沉淀物于60 ℃烘箱中烘干并称量。
收集离心后的上清液,于6 h 内在波长205 nm 下测定溶液的吸光度,并以3%的稀硫酸溶液作参比。
1.4 表征和测定方法
1.4.1 扫描电镜(SEM)分析
使用扫描电子显微镜对纤维素、半纤维素、木质素进行观察。 将干燥后的样品均匀粘附于样品台的导电胶上,用洗耳球轻轻吹去浮样,根据所制样品的性质进行适当次数的喷金,随后调节参数,用SEM观察样品形貌并拍摄电镜图。
1.4.2 原料中化学组分的测定
样品组分分析依据NREL 报道的两步酸解法[6]进行,具体方法如下:
(1)称取15 g 烘干原料,记录其质量记为m1。将原料分为3 份,用滤纸包裹后放入索氏抽提器内,加入无水乙醇没过样包, 抽提至浸泡样包的溶液呈现无色。将样品包取出,置于表面皿上风干。继续加热使圆底烧瓶内的液体蒸发至30 mL 左右,将其转移至已烘干至质量恒定的称量瓶内, 用水浴锅加热蒸发,然后放入烘箱中烘干6 h 以上,取出称量瓶后称量瓶内剩余样品质量,记为m2。
(2)准确称取经乙醇抽提过的样品0.3 g,质量记为m3, 将样品放入150 mL 三角瓶, 加入3 mL 72%的浓硫酸,在真空清洗机中反应1 h。
(3)反应结束后,补加84 mL 蒸馏水,密封后置于高压蒸汽灭菌锅中,于121 ℃下反应60 min。 反应结束后,用G4 砂芯漏斗过滤样品酸解液,同时用蒸馏水洗涤滤渣至pH 中性, 最后将含有滤渣的漏斗置于105 ℃烘箱中烘干至质量恒定, 称量滤渣质量,记为m4。
(4)在波长205 nm 下测定经G4 砂芯漏斗过滤的二次酸解样品溶液的吸光度, 并以3%的硫酸溶液作参比。 各成分含量的计算方法如下:
式中:w1、w2、w3、w4、w5分别为乙醇抽出物、 纤维素、半纤维素、 酸溶木质素、 酸不溶木质素的质量分数,%;C1、C2、C3分别为离子色谱中葡萄糖、木糖、阿拉伯糖的标准浓度,g/L;A 为紫外吸收值;D 为样品稀释倍数;K 为酸溶木质素的吸收系数, 取110;V为试样体积,87 mL;
1.4.3 用傅里叶红外色谱(FTIR)法判断纤维素、半纤维素结构[7]
采用傅里叶变换红外光谱仪对纤维素、 半纤维素样品进行红外光谱分析。 将待测样品和KBr 以质量比1∶100 的比例混合后,用研钵充分研磨,采用压片机压片后,用于检测。扫描范围4000~400 cm-1,分辨率4 cm-1,扫描次数32 次,环境大气为空气。
1.4.4 用离子色谱仪分析纤维素、 半纤维素的糖分含量[8]
采用离子色谱仪对纤维素、 半纤维素样品进行检测分析。 分别称取0.3 g 纤维素、0.3 g 半纤维素,加入100 mL 三角瓶中, 加入3 mL 72%的浓硫酸,放入超声波清洗机中充分反应,后置于摇床上,在室温25 ℃、150 r/min 条件下反应1 h, 然后加入84 mL 去离子水,用两层保鲜薄膜封住锥形瓶口,再使用三层牛皮纸进行加固, 并在121 ℃手提式高温灭菌锅中保温反应1 h。 结束后取出锥形瓶于室温中冷却。 后将样品溶液用活化后的Na/HRP 纯化柱(10 mL 无水甲醇洗涤,15 mL 超纯水清洗) 过滤掉溶液中的有机大分子, 将上清液注入活化处理后的Na/HRP 纯化柱并舍弃前4 mL, 收集后面的样品过水系微孔滤膜(0.22 μm)备用。
2 结果与讨论
2.1 形貌分析
2.1.1 实验材料的外观分析
生麦麸表面光滑,呈片状,颜色为褐黄色,质地较为松软(图1(a))。 图1(b)、图1(c)分别为经碱液浸提法提取出的纤维素、 半纤维素。 纤维素由于受过氧化氢漂白后呈白色,略泛黄,刚提取出的纤维素质地柔软,经研磨和粉碎机处理后为细小片状颗粒;而半纤维素经乙醇沉降后颜色呈深褐色, 干燥后的研磨操作比纤维素容易, 呈小颗粒粉末状。 木质素的颜色与半纤维素相近,由于采用硫酸提取,均呈深褐色(图1(d))。

图1 生麦麸、纤维素、半纤维素、木质素的实物图
2.1.2 纤维素的扫描电镜分析
图2(a)为放大180 倍的纤维素,由于未研磨完全,呈现出较大的块状,截断面有明显褶皱凸起,整体表面比较规整光滑。当放大1800 倍时(图2(b)),其表面凸出物十分清晰,呈不规则状分布,难以观察出单根纤维的分布走向。 纤维素呈现疏松状态,可能是因为在润胀过程中分子间的氢键被削弱, 释放出部分羟基,使纤维素内部表面积增加,导致链的固定排列遭到破坏[9]。 经过酸碱处理后,半纤维素及果胶等大部分杂质与油脂质被去除, 后经过H2O2漂白,纤维素中的羟基形成氧化物自由基,破坏了纤维素分子中的氢键, 从而降低了纤维素分子间的相互作用。 纤维素呈现片层结构,有较大的表面积,表面相对光滑, 可为吸附其他物质提供更多的空间。当纤维素放大5000 倍和10 000 倍时,如图2(c),2(d)所示,由于纤维素分子链具有细长的线状结构,这些线状结构相互交织,形成一种网状结构,网状结构具有一定的稳定性,如果将其作为造纸原料,有利于提高纸张的强度性能[10]。

图2 纤维素的扫描电镜图
2.1.3 半纤维素的扫描电镜分析
图3(a)为放大1800 倍的半纤维素整体图,可以看表面存在大量不规则颗粒碎渣球,放大5000 倍后能明显看出, 半纤维素比纤维素的表面更粗糙(图3(b))。 分离出的半纤维素经过干燥结晶析出后,不再和纤维素一样具有线状结构,而是整齐、紧密地形成结晶体整体,且出现较大球状颗粒团(如图3(c))。

图3 半纤维素的扫描电镜图
2.1.4 木质素的扫描电镜分析
图4(a)为放大200 倍的木质素,可以看出整体形貌与纤维素、半纤维素有很大差异,中央有大块条状物。 在图4(b)中可明显观察出不规则形状,左侧木质素显示为螺旋分布,右侧木质素则为粗条状,可能是由于研磨不充分导致。图4(c)与图4(d)分别为放大1800 倍和5000 倍的木质素, 扫描电镜图很好地展示了木质素分子链相互交织形成的网状结构。根据文献可知, 木质素的空间结构在有利于其在吸附方面应用。

图4 木质素的扫描电镜图
2.2 化学组分含量分析
一般而言,不同材料的纤维素(30%~50%)、半纤维素(15%~35%)和木质素(10%~25%)的含量存在差异。 根据文献, 不同处理阶段麦麸的化学组成含量不同,见表1。 根据1.3.2 方法计算得出本实验中麦麸的组分含量见表2。

表1 不同处理阶段麦麸的化学组成[11]%
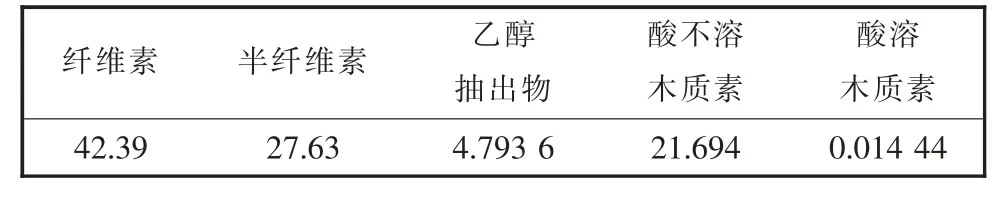
表2 本实验中麦麸的化学组成%
为了能确切地了解麦麸是否能够作为造纸原料,将其与文献中作为造纸原料的大豆秸秆、红松、麦草的成分含量进行对比,见表3。

表3 大豆秸秆、 红松、 麦草的化学成分[12]%
通过表2 与表3 对比可以得出: 麦麸中的纤维素含量虽不及红松高, 但与大豆秸秆的纤维素含量相近,甚至比麦草的纤维素含量略高,证明了麦麸可能是一种潜在的纤维素来源;仅从化学成分上看,麦麸是比较合适的制浆造纸原料。 导致表1 与表2 化学成分含量数据差异的原因可是纤维素来源和提取工艺条件差异以及实验可能出现的误差。
2.3 纤维素、半纤维素的FTIR 分析
由图5 所示纤维素、 半纤维素的FTIR 谱图可以看出:在3400 cm-1处,纤维素及半纤维素均有较宽而强的吸收峰,说明有含氢官能团的存在,该吸收峰是由于O—H 的伸缩振动产生。 在2900 cm-1处,纤维素、半纤维素均存在吸收峰,为C—H 的非对称伸缩振动。 在1626 cm-1处,纤维素、半纤维素均有O=C 的非常强的吸收峰。

图5 纤维素、半纤维素的FTIR 谱图
在半纤维素特征峰中,1045 cm-1处出现的吸收峰是由糖苷键中的吡喃糖C—O—C 基团振动产生;环振动以及C-1 基团的出现会在910 cm-1处产生吸收峰, 在半纤维素中是由于β-糖苷键振动而产生的;803 cm-1处的特征峰是苯环对位取代振动所产生的。
在纤维素特征峰中,1730 cm-1处出现一个小的吸收峰, 说明有非对称葡萄糖醛酸的伸缩振动。1620 cm-1处的吸收峰为纤维素中残留水的吸收峰。纤维素与半纤维素均在1045 cm-1处出现特征峰,但相比于半纤维素,纤维素的峰强度更大,该峰由糖苷键中吡喃糖C—O—C 基团的振动产生[13]。
2.4 纤维素、半纤维素的糖分分析
根据表4 的不同单糖标准曲线方程[14],由通过离子色谱仪测得的数据计算可得纤维素、 半纤维素糖组分的含量占比见表5。 由表5 可知,纤维素中含量最高为葡萄糖,其次为木糖,其含量远高于阿拉伯糖及半乳糖;半纤维素中含量最高为木糖。

表4 不同单糖的标准曲线
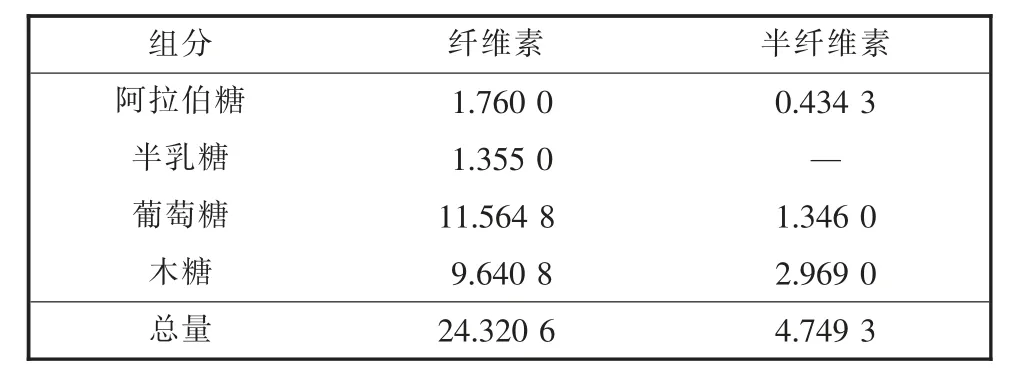
表5 纤维素、 半纤维素中的糖含量%
3 结论
本文采用碱液浸提法从麦麸中提取纤维素、半纤维素及木质素三种原料, 依据两步酸解法提取麦麸中的组分, 利用扫描电镜观察麦麸组分的形貌特征;同时,对麦麸中的各个组分含量进行测定,并与秸秆等原材料进行比较。
电镜分析表明:纤维素呈现片层结构,有较大的表面积,表面相对光滑,空间性良好,可以提高纤维之间的结合强度; 半纤维素比纤维素表面更粗糙。分离出的半纤维素经过结晶析出后, 不再具有纤维素单根纤维的结构特点,而是整齐、紧密地形成结晶体整体, 且有较大球状颗粒团。 木质素的空间结构在有利于其在吸附方面应用。
麦麸中的纤维素含量与秸秆中的纤维素含量相近, 从化学组成方面看, 麦麸有作为造纸原料的可能。麦麸中纤维素和半纤维素两组分均由阿拉伯糖、木糖、半乳糖及葡萄糖组成;纤维素中含糖量最高为葡萄糖,其次为木糖,其含量远高于阿拉伯糖及半乳糖;半纤维素中含量最高为木糖。
