3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺类化合物的合成及其抗肿瘤活性
2023-09-22张轩赫裴天运桑旭杰陈宇亮丁雯佳杨珍珍马良秀
张轩赫, 裴天运,2, 桑旭杰, 陈宇亮, 丁雯佳, 杨珍珍*, 徐 峰, 马良秀
(1. 台州职业技术学院,浙江 台州 318000; 2. 常州大学,江苏 常州 213164; 3. 天台宜生生化科技有限公司,浙江 台州 317200)
1,2,4,5-四嗪是一类重要的富含氮元素的杂环化合物,在农药[1]、染料[2]、炸药[3]和液晶[4]等领域具有广泛的应用。近年来发现一些二氢-1,2,4,5-四嗪类化合物具有潜在的抗肿瘤活性,其中HU等[5]发现1,4-二氢-1,2,4,5-四嗪类化合物对小鼠白血病细胞P-388、人实体瘤细胞肝癌BEL-7402和乳腺癌MCF-7等癌细胞株具有较好的抗肿瘤活性;RAO等[6]发现1,2-二氢-1,2,4,5-四嗪类化合物对P-388和A-549具有较强的抗癌能力。但至今外界对1,6-二氢-1,2,4,5-四嗪类化合物的抗肿瘤活性研究依旧较少。
本课题组前期研究中发现,三唑并四嗪类化合物(属于1,6-二氢-1,2,4,5-四嗪的一类)具有较强的抗肿瘤活性[7-12]。6-烷氨基-[1,2,4]三唑[4,3-b][1,2,4,5]四嗪类化合物对MCF-7、 Bewo和HL-60细胞株具有较强的抑制作用(如化合物TZXU-1~3: IC50=1.09~2.24 μmol/L)[7-8]; 6-烷氧基-[1,2,4]三唑[4,3-b][1,2,4,5]四嗪类化合物对A549, Bewo和MCF-7细胞株显示具有较强的抗肿瘤活性(如化合物TZXU-4的IC50分别为21.68, 20.72和2.81 μmol/L)[9];((4-([1,2,4]三唑[4,3-b][1,2,4,5]四嗪-6-基)哌嗪-1-基)甲基)苯甲酰肼类化合物对A549、 Bewo、 Hela和HepG2细胞株显示较强的抑制活性(如化合物TZXU-5的IC50分别为8.39, 5.21, 19.11和2.37 μmol/L)[10]; 3-烷基(芳基)-[1,2,4]三唑[4,3-b][1,2,4,5]四嗪类化合物对MCF-7, Bewo和HL-60细胞株显示较强的抗肿瘤活性(如化合物TZXU-6的IC50分别为21.68, 20.72和2.81 μmol/L)[11]; 3-双环硫基-6-(3,5-二甲基-1H-吡唑-1-基)[1,2,4]三唑[4,3-b][1,2,4,5]四嗪类化合物对HT-29具有较好抗肿瘤活性(TZXU-7的IC50为12.69 μmol/L)[12]。6-吗啉基-[1,2,4]三唑[4,3-b][1,2,4,5]四嗪(TZXU-1)通过对ICR小鼠的体内实验表明其对S180肿瘤细胞具有较好的抑制效果,抑制率达到62.99%。近期,本课题组将化合物TZXU-5中的芳酰胺结构与1,6-二氢-1,2,4,5-四嗪环结合,构建一类N-芳基-3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺类化合物(图1),并对其进行抗肿瘤活性的测试。
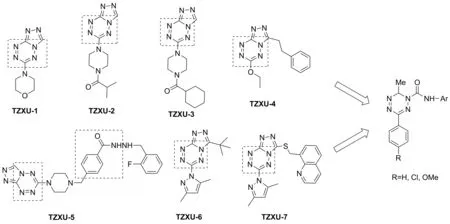
图1 部分活性较好的1,6-二氢-1,2,4,5-四嗪化合物
以3-芳基-6-甲基-1,2,4,5-四嗪为起始原料,在硼氢化钠的作用下还原得到3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪,再与芳基异氰酸酯反应得到目标化合物。其相应工艺路线见图2。
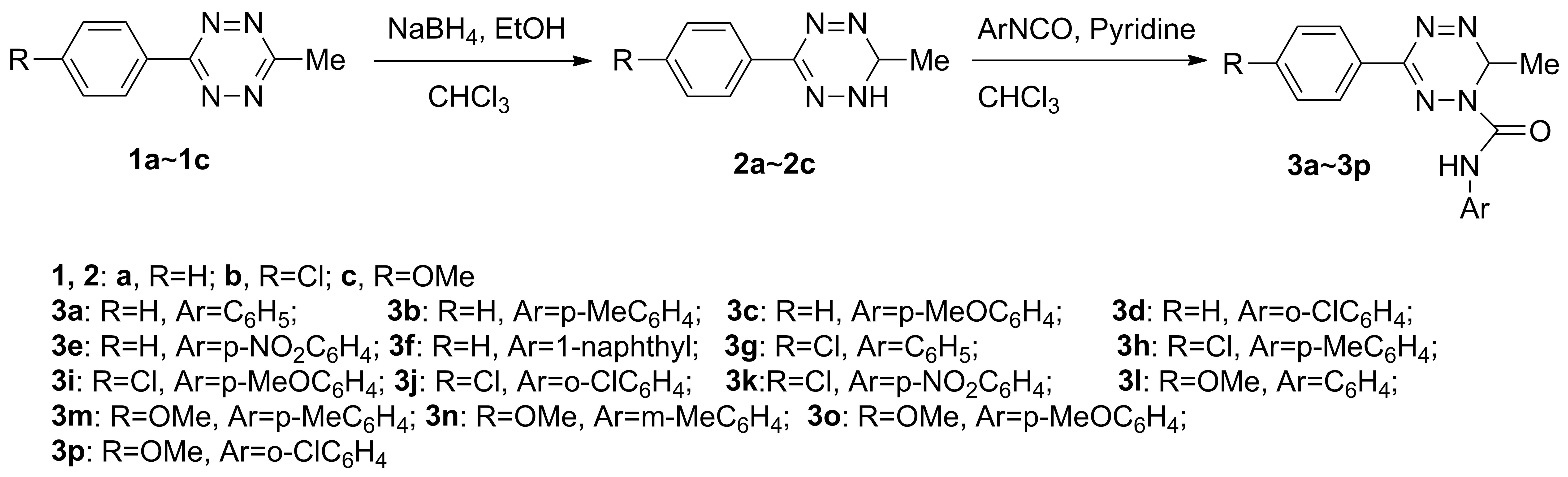
图2 目标化合物的合成路线
1 实验部分
1.1 仪器与试剂
XRC-1型显微熔点仪测定仪(温度计未经校正);Nicolex FI-IR-170型红外光谱仪(KBr压片);Brucker AC400型核磁共振仪(DMSO-d6或CDCl3为溶剂,TMS为内标);Agilent 1260 Ion Trap LC-MS 500型质谱仪;Agilent 6210 TOF LC/MS型高分辨质谱仪;Thermo-Finnigan Flash EA1112型元素分析测定仪。所用试剂均为分析纯。
1.2 合成
(1) 3-芳基-6-甲基-1,2,4,5-四嗪(1)的合成
化合物1根据文献[13-17]方法合成。
3-苯基-6-甲基-1,2,4,5-四嗪(1a): m.p.74~76 ℃(74.5~76 ℃[15]); IRν: 3050(Ar-H), 2926(CH2), 1402, 1361(C=N), 1088 cm-1; MS(m/z, %): 172(M+, 12), 103(100), 76(16); 3-对氯苯基-6-甲基-1,2,4,5-四嗪(1b): m.p.142~144 ℃(143~145 ℃[17]); IRν: 3049(Ar-H), 2980(CH2), 1405, 1364(C=N), 1093 cm-1; MS(m/z, %): 206(M+, 15), 136(100), 102(25), 75(10); 3-对甲氧基苯基-6-甲基-1,2,4,5-四嗪(1c): m.p.103~105 ℃(103~106 ℃[17]); IRν: 3056(Ar-H), 2985(CH2), 1401, 1360(C=N), 1088 cm-1; MS(m/z, %): 202(M+, 35), 133(100), 103(24), 89(28), 63(7)。
(2) 3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪(2)
在250 mL三口瓶中加入3-芳基-6-甲基-1,2,4,5-四嗪20 mmol,乙醇80 mL和氯仿40 mL,搅拌使其溶解。室温下将配置的硼氢化钠-乙醇-水混合物[将NaBH4(0.38 g, 10 mmol)溶于乙醇15 mL和水5 mL的混合物]慢慢滴加到反应瓶中,反应液颜色由深红变为橙黄后,停止滴加,继续搅拌30 min。向反应液中加入饱和氯化铵水溶液100 mL,搅拌后分层,提取有机层(下层),水层用氯仿萃取(3×50 mL),合并有机相,用MgSO4干燥。除去干燥剂,减压抽除溶剂得到橙黄色粗品,用二氯甲烷-正己烷重结晶得到精品。
3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪(2a): 橙黄色固体,收率25.1%, m.p.107~108 ℃(Lit[14]106.5~108 ℃); IRν: 3444 s(N—H), 2900 m(C—H), 1650 m(C=N), 1395 s(ring) cm-1;1H NMR(CDCl3)δ: 7.95(d,J=9.6 Hz, 2H), 7.39~7.46(m, 2H, ArH), 7.38(t,J=7.2 Hz, 1H), 2.42(q,J=6.0 Hz, 1H), 2.04(d,J=6.2 Hz, 3H); MS(m/z, %); 146(M-28, 2.58), 131(3.52), 104(100), 91(1.30), 77(19.83), 42(9.49)。
3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪(2b): 橙黄色固体,收率20.4%, m.p.120~122℃; IRν: 3441 s(N—H), 2938 m(C—H), 1634 m(C=N), 1394 s(ring), 711 m(C—Cl) cm-1;1H NMR(CDCl3)δ: 7.88(m,J=8.4 Hz, 2H), 7.25(m,J=8.4 Hz, 2H), 2.40(q,J=6.0 Hz, 1H), 2.04(d,J=6.0 Hz, 3H); MS(m/z, %); 180(M-28, 4.42), 165(4.55), 138(100), 111(10.02), 102(18.29), 75(9.42), 42(9.93); Anal. Calcd for C9H9ClN4: C 51.81, H 4.35, N 26.85, found C 52.00, H 4.40, N 27.10。
3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪(2c): 橙黄色固体, 收率24.9%, m.p.105~107 ℃; IRν: 3457 s(N—H), 2934 m(C—H), 1611 m(C=N), 1392 s(ring) cm-1;1H NMR(CDCl3)δ: 7.87(m,J=9.2 Hz, 2H), 6.96(m,J=9.2 Hz, 2H), 3.84(s, 3H), 2.32(q,J=6.0 Hz, 1H), 2.04(d,J=6.0 Hz, 3H); MS(m/z, %), 176(M-28, 13.56), 161(8.64), 133(100.00), 119(6.78), 103(15.82), 90(16.32), 77(5.71), 42(3.82); Anal. Calcd for C10H12N4O: C 58.81, H 5.92, N 27.43, found C 58.95, H 5.60, N 27.20。
(3)N-芳基-3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3a~3p)合成
在50 mL三口瓶中加入化合物21.0 mmol,干燥氯仿10 mL和吡啶(82 mg, 1.0 mmol),磁力搅拌,室温下滴加芳基异氰酸酯1.0 mmol的氯仿10 mL溶液,反应液颜色由橙黄迅速变为橘红色。滴加完毕后,继续搅拌30 min,用TCL法检测反应终点(二氯甲烷)。反应结束后,反应液用水洗涤(2×10 mL)。减压抽取溶剂,得到的粗品用硅胶GF254(2 mm)薄板层析提纯(洗脱剂:二氯甲烷 ∶石油醚=1 ∶1,V∶V),得到纯品。
14-苯基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3a): 橘黄色固体,收率74.6%, m.p.96~98 ℃; IRν: 3307 s(N—H), 2924 w(C—H), 1683 s(C=O), 1536 s(C=O—N), 1443 s(ring) cm-1;1H NMR(CDCl3)δ: 8.63(s, 1H), 8.15~8.17(m, 2H, ArH), 7.51~7.55(m, 3H, ArH), 7.28~7.40(m, 5H, ArH), 6.91(q,J=6.4 Hz, 1H), 1.08(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 150.3, 148.8, 139.0, 135.2, 131.2, 129.1(2C), 128.7(2C), 128.0, 124.6(2C), 121.3(2C), 61.8, 9.4; HR-MS(APCI)m/z: Calcd for C16H16N5O{[M+H]+}294.1354; found 294.1305; Anal. Calcd for C16H15N5O: C 65.52, H 5.15, N 23.88, found C 65.43, H 5.31, N 24.02。
N-对甲基苯基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3b): 橘黄色固体,收率78.2%, m.p.115~117 ℃; IRν: 3320 s(N—H), 2922 w(C—H), 1686 s(C=O), 1526 s((C=O)—N), 1382 s(ring) cm-1;1H NMR(CDCl3)δ: 8.57(s, 1H), 8.16~8.18(m, 2H, ArH), 7.54~7.57(m, 3H, ArH), 7.41(d,J=8.4 Hz, 2H), 7.17(d,J=8.4 Hz, 2H), 6.92(q,J=6.4 Hz, 1H), 2.34(s, 3H), 1.09(d,J=6.4 Hz 3H);13C NMR(CDCl3)δ: 150.1, 149.0, 136.8, 135.9, 134.9, 131.3, 129.2(2C), 128.5(2C), 124.5(2C), 121.2(2C), 61.7, 21.5, 9.4; HR-MS(APCI)m/z: Calcd for C17H18N5O {[M+H]+}308.1511, found 308.1550; Anal. Calcd for C17H17N5O: C 66.43, H 5.58, N 22.79, found C 66.70, H 5.56, N 23.12。
N-对甲氧基苯基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3c): 橘黄色固体,收率76.0%, m.p.135~137 ℃; IRν: 3305 s(N—H), 2921 w(C—H), 1683 s(C=O), 1538 s((C=O)—N), 1378 s(ring) cm-1;1H NMR(CDCl3)δ: 8.49(s, 1H), 8.14~8.16(m, 2H, ArH), 7.53~7.54(m, 3H, ArH), 7.42(d,J=9.2 Hz, 2H), 6.89(d,J=9.2 Hz, 2H), 6.87(q,J=6.4 Hz, 1H), 3.81(s, 3H), 1.07(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 155.6, 150.2, 148.5, 135.2, 132.5, 131.3, 129.2(2C), 124.8(2C), 120.2(2C), 115.3(2C), 61.7, 55.9, 9.4; HR-MS(APCI)m/z: Calcd for C17H18N5O2{[M+H]+}324.1455, found 324.1434。
N-邻氯苯基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3d): 橘黄色固体,收率78.8%, m.p.108~110 ℃; IRν: 3362 s(N—H), 2929 w(C—H), 1715 s(C=O), 1528 s(C=O—N), 1378 s(ring) cm-1;1H NMR(CDCl3)δ: 9.44(s, 1H), 8.30(d,J=8.0 Hz, 1H), 8.17~8.19(m, 2H, ArH), 7.53~7.57(m, 3H, ArH), 7.40(d,J=8.0 Hz, 1H), 7.31(t,J=8.0 Hz, 1H), 7.06(t,J=8.0 Hz, 1H), 6.88(q,J=6.4 Hz, 1H), 1.11(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 150.1, 148.4, 135.6, 135.1, 131.2, 130.7, 130.5, 129.3(2C), 128.5, 126.3, 124.7(2C), 121.8, 61.7, 9.4; HR-MS(APCI)m/z: Calcd for C16H15ClN5O{[M+H]+}328.0965, found 328.0983。
N-对硝基苯基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3e): 橘黄色固体,收率61.3%, m.p.153~155 ℃; IRν: 3397 s(N—H), 2981 w(C—H), 1692 s(C=O), 1540 s((C=O)—N), 1387 s(ring) cm-1;1H NMR(CDCl3)δ: 8.97(s, 1H), 8.24(d,J=9.2 Hz, 2H), 8.15~8.18(m, 2H, ArH), 7.72(d,J=9.2 Hz, 2H), 7.56~7.57(m, 3H, ArH), 6.89(q,J=6.4 Hz, 1H), 1.11(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 150.3, 148.6, 138.6, 137.7, 135.0, 131.1, 129.1(2C), 124.7(2C), 121.6(2C), 118.6(2C), 61.8, 9.4; HR-MS(APCI)m/z: Calcd for C16H15N6O3{[M+H]+} 339.1200, found 339.1217。
N-1-萘基-3-苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3f): 橘黄色固体,收率65.1%, m.p.117~118 ℃; IRν: 3398 s(N—H), 3056, 2981 w(C—H), 1679 s(C=O), 1537 s((C=O)—N), 1497, 1379 s(ring), 1191, 767, 565 cm-1;1H NMR(CDCl3)δ: 9.15(s, 1H), 8.24(d,J=8.0 Hz, 2H), 7.99(d,J=8.0 Hz, 1H), 7.86~7.91(m, 3H, ArH), 7.73(d,J=8.0 Hz, 1H), 7.46~7.60(m, 5H, ArH), 6.98(q,J=6.5 Hz, 1H), 1.14(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 150.2, 148.3, 138.6, 135.2, 133.8, 131.3, 129.1(2C), 128.6, 127.6, 126.0, 125.0, 124.7, 124.5(2C), 121.0, 119.1, 106.8, 61.8, 9.4; HR-MS(APCI)m/z: Calcd for C20H18N5O{[M+H]+}344.1511, found 344.1493。
N-苯基-3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3g): 橘黄色固体,收率96.6%, m.p.131~133 ℃; IRν: 3295 s(N—H), 2983 w(C—H), 1692 s(C=O), 1540 s((C=O)—N), 1384 s(ring), 689 m(C—Cl) cm-1;1H NMR(CDCl3)δ: 8.58(s, 1H), 8.09(d,J=8.4 Hz, 2H), 7.52(d,J=8.0 Hz, 4H), 7.37(t,J=7.8 Hz, 2H), 7.15(t,J=7.2 Hz, 1H), 6.92(q,J=6.4 Hz, 1H), 1.08(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 150.1, 148.5, 139.0, 136.8, 130.6, 129.4(2C), 129.0(2C), 128.7(2C), 128.0, 121.3(2C), 61.9, 9.4; HR-MS(APCI)m/z: Calcd for C16H15N5OCl{[M+H]+} 328.0959, found 328.0957。
N-对甲基苯基-3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3h): 橘黄色固体,收率87.8%, m.p.149~151 ℃; IRν: 3296 s(N—H), 2980 w(C—H), 1704 s(C=O), 1529 s((C=O)—N), 1385 s(ring), 720 m(C—Cl) cm-1;1H NMR(CDCl3)δ: 8.52(s, 1H), 8.09(d,J=8.4 Hz, 2H), 7.51(d,J=8.4 Hz, 2H), 7.43(d,J=8.8 Hz, 2H), 7.16(d,J=8.8 Hz, 2H), 6.91(q,J=6.4 Hz, 1H), 2.34(s, 3H), 1.07(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 150.2, 148.6, 136.8, 136.6, 135.9, 130.6, 129.9(2C), 129.1(2C), 128.5(2C), 121.2(2C), 61.8, 21.5, 9.4; HR-MS(APCI)m/z: Calcd for C17H17N5OCl{[M+H]+} 342.1116, found 342.1107。
N-对甲氧基苯基-3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3i): 橘黄色固体,收率83.6%, m.p.140~142 ℃; IRν: 3318 s(N—H), 2982 w(C—H), 1699 s(C=O), 1538 s((C=O)—N), 1415 s(ring), 736 m(C—Cl) cm-1;1H NMR(CDCl3)δ: 8.46(s, 1H), 8.08(d,J=8.8Hz, 2H), 7.51(d,J=8.8 Hz, 2H), 7.41(d,J=9.2 Hz, 2H), 6.90(d,J=9.2 Hz, 2H), 6.90(q,J=6.4 Hz, 1H), 3.81(s, 3H), 1.06(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 155.2, 150.4, 148.5, 136.7, 132.5, 130.3, 129.8(2C), 129.0(2C), 120.3(2C), 115.4(2C), 61.9, 55.8, 9.4; HR-MS(APCI)m/z: Calcd for C17H17N5O2Cl{[M+H]+} 358.1065; found 358.1083。
N-邻氯苯基-3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3j): 橘黄色固体,收率80.2%, m.p.136~138 ℃; IRν: 3347 s(N—H), 2989 w(C—H), 1711 s(C=O), 1533 s((C=O)—N), 1382 s(ring), 731 m(C—Cl) cm-1;1H NMR(CDCl3)δ: 9.40(s, 1H), 8.29(d,J=8.0 Hz, 1H), 8.11(d,J=8.4 Hz, 2H), 7.53(d,J=8.4 Hz, 2H), 7.42(d,J=8.0 Hz, 1H), 7.32(t,J=7.8 Hz, 1H), 7.07(t,J=7.8 Hz, 1H), 6.89(q,J=6.4 Hz, 1H), 1.11(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 150.2, 148.8, 136.2, 135.3, 130.5, 130.0, 129.8, 129.6(2C), 129.0(2C), 128.5, 126.3, 121.8, 61.8, 9.4; HR-MS(APCI)m/z: Calcd for C16H14N5OCl2{[M+H]+} 362.0569, found 362.0562。
N-对硝基苯基-3-对氯苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3k): 橘黄色固体,收率74.8%, m.p.154~156 ℃; IRν: 3397 s(N—H), 2981 w(C—H), 1742 m(C=O), 1539 s((C=O)—N), 1384 s(ring), 1336 s(Ar-NO2) cm-1;1H NMR(CDCl3)δ: 8.92(s, 1H), 8.25(d,J=8.8 Hz, 2H), 8.20(d,J=8.4 Hz, 2H), 8.10(d,J=8.4 Hz, 2H), 7.73(d,J=8.8 Hz, 2H), 6.90(q,J=6.4 Hz, 1H), 1.11(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 150.3, 148.6, 138.6, 137.7, 136.7, 130.8, 129.5(2C), 128.9(2C), 121.6(2C), 118.8(2C), 61.8, 9.4; HR-MS(APCI)m/z: Calcd for C16H14N6O3Cl{[M+H]+} 373.0810, found 373.0797。
N-苯基-3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3l): 橘黄色固体,收率60.5%, m.p.103~105 ℃; IRν: 3356 s(N—H), 2923 w(C—H), 1706 s(C=O), 1509 s((C=O)—N), 1385 m(ring) cm-1;1H NMR(CDCl3)δ: 8.62(s, 1H), 8.12(d,J=8.8 Hz, 2H), 7.82(d,J=8.0 Hz, 2H), 7.37(t,J=7.8 Hz, 2H), 7.14(t,J=7.2 Hz, 1H), 7.07(d,J=8.8 Hz, 2H), 6.90(q,J=6.4 Hz, 1H), 3.92(s, 3H), 1.08(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 162.1, 150.4, 149.1, 139.1, 130(2C), 128.7(2C), 128.1, 124.3, 121.2(2C), 114.5(2C), 61.7, 55.6, 9.6; HR-MS(APCI)m/z: Calcd for C17H18N5O2{[M+H]+} 324.1455, found 324.1462。
N-对甲基苯基-3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3m): 橘黄色固体,收率41.4%, m.p.117~119 ℃; IRν: 3270 s(N—H), 2921 w(C—H), 1674 s(C=O), 1514 s((C=O)—N), 1387 m(ring) cm-1;1H NMR(CDCl3)δ: 8.54(s, 1H), 8.10(d,J=8.8 Hz, 2H), 7.40(d,J=8.0 Hz, 2H), 7.16(d,J=8.0 Hz, 2H), 7.06(d,J=8.8 Hz, 2H), 6.87(q,J=6.4 Hz, 1H), 3.89(s, 3H), 2.33(s, 3H), 1.06(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 162.0, 150.5, 149.2, 136.8, 135.7, 130.1(2C), 128.5(2C), 124.3, 121.2(2C), 114.5(2C), 61.7, 55.5, 21.6, 9.6; HR-MS(APCI)m/z: Calcd for C18H20N5O2{[M+H]+}338.1611, found 338.1647。
N-间甲基苯基-3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3n): 橘黄色固体,收率65.3%, m.p.120~122 ℃; IRν: 3374 s(N—H), 2924 w(C—H), 1708 s(C=O), 1516 s((C=O)—N), 1388 m(ring), 1245, 1201, 1027, 838, 814 cm-1;1H NMR(CDCl3)δ: 8.63(s, 1H), 8.10(d,J=8.8 Hz, 2H), 7.93(d,J=8.4 Hz, 1H), 7.20~7.52(m, 2H, ArH), 7.06(t,J=9.2 Hz, 3H), 6.88(q,J=6.5 Hz, 1H), 3.90(s, 3H), 2.33(s, 3H), 1.08(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 162.2, 150.3, 149.1, 139.0, 138.0, 130.2(2C), 129.4, 127.7, 124.3, 120.4, 116.9, 114.4(2C), 61.8, 55.6, 21.5, 9.6; HR-MS(APCI)m/z: Calcd for C18H20N5O2{[M+H]+}338.1617, found 338.1618。
N-对甲氧基苯基-3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3o: 橘黄色固体,收率42.3%, m.p.124~126 ℃; IRν: 3374 s(N—H), 2960 w(C—H), 1708 s(C=O), 1516 s((C=O)—N), 1388 m(ring) cm-1;1H NMR(CDCl3)δ: 8.49(s, 1H), 8.11(d,J=8.8 Hz, 2H), 7.43(d,J=9.2 Hz, 2H), 7.07(d,J=8.8 Hz, 2H), 6.90(d,J=9.2 Hz, 2H), 6.88(q,J=5.6 Hz, 1H), 3.91(s, 3H), 3.82(s, 3H), 1.07(d,J=6.4 Hz, 3H);13C NMR(CDCl3)δ: 162.1, 155.2, 150.3, 149.2, 132.5, 130.1(2C), 124.3, 120.3(2C), 115.4(2C), 114.4(2C), 61.8, 55.8, 55.6, 9.6; HR-MS(APCI)m/z: Calcd for C18H20N5O3{[M+H]+}354.1561; found 354.1571。
N-邻氯苯基-3-对甲氧基苯基-6-甲基-1,6-二氢-1,2,4,5-四嗪-1(6H)-甲酰胺(3p): 橘黄色固体,收率62.3%, m.p.108~110 ℃; IRν: 3378 s(N—H), 2962 w(C—H), 1711 s(C=O), 1518 s((C=O)—N), 1382 m(ring) cm-1;1H NMR(CDCl3)δ: 9.43(s, 1H), 8.32(d,J=8.0 Hz, 1H), 8.15(d,J=8.8 Hz, 2H), 7.41(d,J=8.0 Hz, 1H), 7.32(t,J=7.6 Hz, 1H), 7.07(d,J=8.8 Hz, 2H), 7.06(t,J=8.4 Hz, 1H), 6.87(q,J=6.4 Hz, 1H), 3.92(s, 3H), 1.11(d,J=6.8 Hz, 3H);13C NMR(CDCl3)δ: 162.1, 150.4, 149.3, 135.3, 130.2(2C), 130.0, 129.8, 128.6, 126.3, 124.3, 121.8, 114.3(2C), 61.8, 55.5, 9.6; HR-MS(APCI)m/z: Calcd for C17H16ClN5O2{[M+H]+}358.1071, found 338.1057。
2 结果与讨论
2.1 工艺优化
化合物2的合成过程中,缓慢滴加硼氢化钠乙醇水溶液,保持反应在室温下进行。结果表明:
滴加速度过快会导致副产物增多,收率降低。合成目标产物3时,以合成3a为候选实验,其他条件不变的情况下,分别采用氢氧化钠、碳酸钾、三乙胺和吡啶作为催化剂进行筛选,发现采用氢氧化钠时碱性过强,会对四嗪环进行分解而造成收率过低(20%),但碳酸钾(53%)和三乙胺(62%)的收率均低于吡啶(75%),因此采用吡啶作为催化剂。
2.2 抗肿瘤活性研究
将化合物3进行体外抗肿瘤活性检测。测试方法采用四氮唑盐还原法(MTT法),选用体外人肺癌细胞株A549、人白血病细胞株HL-60、人宫颈癌细胞Hela和人乳腺癌细胞株MCF-7测试,作用时间为72 h,测试结果如表1所示。从表1中可以发现,顺铂对A549、 HL-60、 A549、 MCF-7和Hela的细胞有很好的抑制作用,其IC50分别为3.70 μmol/L、 30.19 μmol/L、 0.97 μmol/L和12.96 μmol/L。相对于顺铂对上述肿瘤细胞的抑制作用,本文中大部分化合物具有一定的肿瘤细胞抑制作用,其中部分化合物对肿瘤细胞具有更强的抑制作用,如3j对HL-60的抑制作用(31.46 μmol/L)接近于顺铂(30.19 μg/mL)。从表1中可以发现,1-位取代基中的芳基取代基为吸电子取代基时,化合物的活性明显提高,而为给电子基时,活性明显降低;同时,取代基是间位取代时的活性好于邻位或对位取代;6-位芳基取代基为吸电子基时的活性好于给电子基。
本文以3-芳基-6-甲基-1,2,4,5-四嗪为起始原料,在硼氢化钠的作用下还原得到3-芳基-6-甲基-1,6-二氢-1,2,4,5-四嗪,再与芳基异氰酸酯反应得到目标化合物。对合成的化合物进行肿瘤细胞株人白血病细胞株HL-60、人肺癌A549、人乳腺癌MCF-7和人子宫颈癌细胞株Hela体外抗肿瘤活性测试。结果表明:目标化合物对上述肿瘤细胞具有一定的抑制活性,其中化合物3j对HL-60癌细胞株具有接近于顺铂的抗肿瘤活性,值得进一步研究。
