N2等离子体活化增强镍铁-甘油酸微球的析氧性能
2023-09-19史静怡遇鑫遥
史静怡,严 萍,遇鑫遥,
(1.安徽大学 物质科学与信息技术研究院,安徽 合肥 230601;2.安徽大学 材料科学与工程学院,安徽 合肥 230601)
随着人类环保意识的日益增强和对清洁能源需求的不断增加,开发可替代的新能源转换和存储体系势在必行。析氧反应(Oxygen evolution reaction,OER)是电解水制氢、金属-空气电池、CO2还原等新能源器件中一个重要的反应[1-3]。然而,析氧反应涉及4个质子/电子的反应,反应动力学缓慢,制约了这些新能源器件的效率,需要电催化剂来提升反应动力学[4]。目前,商用的析氧反应电催化剂主要是IrO2和RuO2,可以有效加速析氧反应动力学,但这些材料的稀缺性和昂贵价格阻碍了其广泛应用[5]。因此,急需开发高效、低成本的非贵金属基析氧反应催化剂来取代贵金属基催化剂[6]。过渡金属基催化剂具有价格低廉、活性高等特点,是研究最为广泛的析氧反应催化剂,有望取代贵金属基催化剂[7]。
金属-甘油酸是一类由金属离子与甘油分子反应而形成的配位化合物,它具有纳米结构易于合成、组分可调等特点[8]。但金属-甘油酸配位化合物的导电性较差且缺乏析氧反应活性位点,导致其析氧反应性能较差。因此,它通常被用作模板合成金属氧化物、磷化物、硫化物等用于催化析氧反应[9]。Zhao等[10]以钴镍-甘油酸微球为模板,将其在300 ℃煅烧2 h合成了空心钴镍氧化物微球,其Tafel斜率为57 mV/dec、在电流密度为10 mA/cm2时的过电位为310 mV。Jia等[11]以镍-甘油酸微球为模板,通过铁离子刻蚀和后续气相磷化法(磷化氢为磷源、磷化温度为300 ℃、磷化时间为2 h)制备了镍铁混合金属氧磷化物空心球,获得了较低的Tafel斜率(59 mV/dec)和过电位(253 mV,电流密度为10 mA/cm2时)。Dai等[12]以钴-甘油酸微球为前驱体,采用部分硫化/磷化策略在320 ℃下合成了单磷硫化钴材料(Co0.9S0.58P0.42),该Co0.9S0.58P0.42催化剂获得的过电位为266 mV、Tafel斜率为48 mV/dec。尽管采用金属-甘油酸配位化合物为模板制备高效过渡金属基析氧反应催化剂取得了一些进展,但这些催化剂合成存在一些问题,包括合成温度较高、反应时间长、使用有毒磷源和硫源等。因此,仍然缺乏一种低温、高效和环境友好的方式来活化金属-甘油酸,从而有效提升其析氧反应性能。
近期,有结合水热和N2等离子体活化提升催化剂的析氧反应活性的少量报道[13-14]。Wang等[13]首先采用水热法合成了块状CoFe插层双氢氧化物,随后使用N2等离子体处理,获得了具有N掺杂、富含缺陷的超薄CoFe插层双氢氧化物纳米片,电流密度为10 mA/cm2时的过电位由324 mV减小到281 mV;Liu等[14]采用N2等离子体活化水热合成的氢氧化钴,得到的过电位为266 mV (电流密度为20 mA/cm2时)、Tafel斜率为85 mV/dec。由此可见,N2等离子体活化能够显著提升催化剂的析氧反应活性,但是利用N2等离子体活化提升金属-甘油酸的析氧反应活性却鲜有报道。
本研究采用N2等离子体活化镍铁-甘油酸实心微球,在低温、环境友好的条件下将其快速转化为由镍单质、氮化镍和少量铁物种组成的复合中空微球。由于其结构和组分上的优势,该中空微球展现了增强的析氧反应性能,包括突出的活性和较好的稳定性。
1 实验部分
1.1 原料和试剂
六水合硝酸镍,分析纯,上海阿拉丁生化科技股份有限公司产品;九水合硫酸铁、异丙醇、甘油、乙醇、硫酸,均为分析纯,国药集团化学试剂有限公司产品;氢氧化钾(95%),上海麦克林生化科技有限公司产品;萘酚溶液(质量分数5%),美国杜邦公司产品;去离子水(电阻率18 MΩ·cm),实验室自制;碳布,苏州晟尔诺科技有限公司产品;泡沫镍(厚度2 mm),昆山市广嘉源电子材料公司产品。
1.2 催化剂的制备
镍-甘油酸微球(Ni-Gly)的制备:将7.5 mL甘油和52.5 mL异丙醇加入到100 mL聚四氟乙烯内胆中,搅拌均匀后将0.4 mmol六水合硝酸镍溶解到上述混合溶液中,充分搅拌后加入1 mL蒸馏水继续搅拌10 min。将聚四氟乙烯内胆转移到不锈钢高压釜中,并放置在烘箱中于200 ℃持续反应12 h。反应结束后将沉淀物取出,使用乙醇洗涤、离心分离3次以上,然后置于烘箱中于60 ℃下烘干,最终得到Ni-Gly样品。
镍铁-甘油酸微球(NiFe-Gly)的制备:将7.5 mL甘油和52.5 mL异丙醇加入到100 mL聚四氟乙烯内胆中,将六水合硝酸镍与九水合硫酸铁按照3种投料摩尔比(9.5/0.5、9/1和8.5/1.5)分别溶解到上述混合溶液中,充分搅拌后加入1 mL蒸馏水继续搅拌10 min。将聚四氟乙烯内胆转移到不锈钢高压釜中,并放置在烘箱中于200 ℃持续反应12 h。反应结束后将沉淀物取出,使用乙醇洗涤、离心分离3次以上,然后置于烘箱中于60 ℃下烘干,最终得到不同Ni/Fe比的NiFe-Gly样品。将六水合硝酸镍与九水合硫酸铁3种投料摩尔比为9.5/0.5、9/1和8.5/1.5所制得的样品分别命名为NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5。
Ni-Gly和NiFe-Gly等离子体活化样品的制备:将得到的Ni-Gly或NiFe-Gly粉末均匀平铺在石英板上,放入等离子体增强化学气相沉积装置(合肥科晶材料技术有限公司产品,OTF-1200X-50-4CLV-PE型)中,将装置抽至真空。随后通入N2并调整气压为60 Pa,射频等离子体功率设置为400 W,反应时间设置为 5 min,获得的活化后样品分别记为P-Ni-Gly和P-NiFe-Gly。在等离子体活化过程中,不对装置进行加热。
等离子体工艺参量包括射频功率和活化时间对析氧反应性能的影响实验:射频功率分别为100、200、300和400 W,活化时间为5 min条件下,获得的催化剂样品分别命名为P-NiFe-Gly-100W、P-NiFe-Gly-200W、P-NiFe-Gly-300W和P-NiFe-Gly-400W。在射频功率为400 W时,改变活化时间分别为1、5和15 min条件下,获得的催化剂样品分别命名为P-NiFe-Gly-1min、P-NiFe-Gly-5min和P-NiFe-Gly-15min。
1.3 催化剂的结构表征
采用场发射扫描电子显微镜(SEM,日本Hitachi公司产品,S4800型)和与其配套的X射线能谱分析仪(EDS,德国Zeiss公司产品,Sigma 500型)测定催化剂样品的表面形貌和元素含量。采用透射电子显微镜(TEM,日本JEOL公司产品,JEM-2100F型)观察材料的微观内部结构。采用X射线衍射仪(XRD,日本Rigaku公司产品,D2phaser型)表征材料的晶体结构。采用X射线光电子能谱仪(XPS,美国Thermo Scientific公司产品,ESCALAB250xi型)测定元素的种类和价态。采用多通道光纤光谱仪(上海复享光学股份有限公司产品,PG2000型)记录等离子体的发射光谱。采用拉曼光谱仪(Raman,美国BWTEK公司产品)收集不同电位下的拉曼光谱。
1.4 催化剂的析氧反应性能表征
所有电化学性能均在1 mol/L KOH中采用三电极体系进行测试(对电极为碳棒电极、参比电极为Hg/HgO电极),所使用的电化学工作站来自于上海辰华仪器有限公司,型号为CHI760E。根据能特斯方程,所有测试的电位转换为相对可逆氢电极(Reversible hydrogen electrode,RHE)所对应的电位(E)尺度。具体电位计算由以下公式得出:ERHE=EHg/HgO+0.059×pH+0.098(pH=14)。其中,ERHE为相对于RHE的电位,V;EHg/HgO为相对于Hg/HgO电极的电位,V;pH值为电解液的pH值;0.059为比例系数;0.098为Hg/HgO电极的标准电极电位,V。负载催化剂的旋转圆盘电极(面积为0.0706 cm2)用作工作电极,转速设置为1600 r/min。为制备工作电极,将5.0 mg催化剂分散到由270 μL乙醇、200 μL蒸馏水和30 μL质量分数为5%的萘酚溶液组成的混合溶液中,超声30 min后形成催化剂浆料。然后,将2.5 μL催化剂浆料滴到旋转圆盘电极表面,并于25 ℃下干燥。在测试前,采用循环伏安法(Cyclic voltammetry,CV),以扫描速率50 mV/s在ERHE为1.17~1.67 V区间内对工作电极进行活化直至CV稳定。在线性扫描伏安法(Linear sweep voltammetry,LSV)测试中,扫描速率为5 mV/s,采用iR补偿对极化曲线进行校正。在频率范围0.1~105Hz和电位1.65 V下测量电极的电化学阻抗谱(EIS),振幅为5 mV。通过Tafel方程η=blg|j|+a,将析氧极化曲线进行对数拟合即可得到Tafel斜率。采用双层电容法(Double layer capacitance,Cdl)估算电化学活性面积(Electrochemical active surface area,SECSA)。在ERHE为1.2~1.3 V区间内,在不同扫描速率下获得一系列CV曲线,以在ERHE=1.25 V时的阳极和阴极电流密度的差值为y轴、扫描速率为x轴,所拟合直线的斜率即为Cdl。在稳定性测试中,将配制好催化剂浆料涂覆在泡沫镍上,催化剂载量为15 mg/cm2。采用恒电位法测试稳定性,ERHE保持在1.477 V。稳定性测试前后进行LSV测试,扫描速率为5 mV/s。在原位拉曼光谱测试中,将催化剂浆料涂覆到泡沫镍表面(2 cm×3 cm),进行干燥和压实处理,截取面积为2 cm×0.2 cm的泡沫镍作为工作电极。采用LSV测试手段以扫描速率0.5 mV/s从开路电位扫至ERHE=1.6 V,测试过程中将激光点(波长为785 nm)对准泡沫镍,在此期间实时记录拉曼光谱。
2 结果与讨论
2.1 Ni-Gly和NiFe-Gly的表征
图1(a)为Ni-Gly、NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5的XRD谱图。由图1(a)可知,Ni-Gly、NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5中均出现了金属-甘油酸对应的特征衍射峰(10.25°、34.8°和60.9°)[15-16]。NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5的衍射峰中没有出现Fe元素的相关化合物。从EDS图谱(见图1(b))可以看出,NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5均由Ni、Fe、C、O 4种元素构成,Ni/Fe摩尔比分别为14.7、11.1和5.89,表明Fe被成功引入。

ERHE—Potential of reversible hydrogen electrode;j—Current density图1 Ni-Gly、NiFe-Gly-9.5/0.5、NiFe-Gly-9/1和NiFe-Gly-8.5/1.5的组分表征和析氧反应性能Fig.1 Compositional characterization and oxygen evolution reaction performance of Ni-Gly,NiFe-Gly-9.5/0.5,NiFe-Gly-9/1 and NiFe-Gly-8.5/1.5(a)XRD patterns;(b)EDS spectra;(c)LSV curves at a scan rate of 5 mV/s in 1 mol/L KOH;(d)Tafel plots
图1(c)为LSV曲线。由图1(c)可以看出,Ni-Gly的析氧反应活性较差。但当引入Fe元素后,析氧反应活性得到大幅度提高,Ni/Fe摩尔比为11.10的NiFe-Gly表现出最佳的析氧反应活性。在电流密度为10 mA/cm2时,NiFe-Gly的过电位仅为302 mV。这与文献[17]中报道的在Ni基催化剂中引入Fe能够增强析氧反应活性的结论是一致的。同时,Fe的引入也能够显著提升析氧反应的反应动力学,如图1(d)所示。经过计算,Ni-Gly、NiFe-Gly-9.5/0.5、NiFe-Gly-9/1、NiFe-Gly-8.5/1.5的Tafel斜率分别为119、52.8、51、53.6 mV/dec。可见,NiFe-Gly的Tafel斜率远低于Ni-Gly的Tafel斜率。
2.2 P-Ni-Gly和P-NiFe-Gly的结构表征
为进一步提升析氧反应活性,采用N2等离子体对Ni-Gly和NiFe-Gly进行活化,在射频功率为400 W、活化时间为5 min、N2气压为60 Pa时活化后样品分别记为P-Ni-Gly和P-NiFe-Gly。其结构表征结果如图2所示。由图2(a)可见,经过5 min的N2等离子体活化,金属-甘油酸的衍射峰几乎全部消失。相比于Ni-Gly和NiFe-Gly,P-Ni-Gly和P-NiFe-Gly中均出现了Ni3N和Ni单质的衍射峰。Ni3N和Ni单质的产生可以归因于N2等离子体的氮化作用和还原作用[18]。由于Fe的含量较低,导致Fe相关化合物的衍射峰较弱,其中在2θ为19.8°和34.8°处出现的衍射峰可能为Fe3O4。由图2(b)的SEM照片可见,NiFe-Gly呈现均匀的微球状。由图2(c)和图2(d)的TEM照片可见,NiFe-Gly是实心球。从图2(e)的EDS图谱可以看出,经过N2等离子体活化后,Ni/Fe摩尔比(11.10)没有发生较大的变化,且存在N元素的信号,说明N元素被成功地引入到P-NiFe-Gly中。P-NiFe-Gly很好地保持了NiFe-Gly的球形(见图2(f))。N2等离子体活化后,NiFe-Gly的内部出现了空腔(见图2(g)和图2(h))。等离子体中含有大量的高活性电子和含氮物种。其中,电子具有高还原活性,能够将Ni离子还原为Ni单质;而含氮物种能够与Ni离子反应形成氮化镍。因此推测,等离子体首先与NiFe-Gly表面发生反应,生成Ni单质和Ni3N薄层,使等离子体很难穿过这一薄层与内部的NiFe-Gly发生进一步反应,这使内部NiFe-Gly中的Ni离子会扩散到外部与等离子体发生反应,继续形成Ni单质和Ni3N,内部Ni离子的扩散导致空腔的形成。

图2 P-Ni-Gly、NiFe-Gly和P-NiFe-Gly的结构表征结果Fig.2 Structural characterization results of P-Ni-Gly,NiFe-Gly and P-NiFe-Gly(a)XRD patterns of P-Ni-Gly and P-NiFe-Gly;(b)SEM image of NiFe-Gly;(c),(d)TEM images of NiFe-Gly;(e)EDS spectrum;(f)SEM image of P-NiFe-Gly;(g),(h)TEM images of P-NiFe-Gly
为进一步探究等离子体活化前后NiFe-Gly的化学组成和元素价态的变化,进行了XPS分析,结果见图3。由图3(a)可知,NiFe-Gly和P-NiFe-Gly均存在Ni、Fe、C和O 4种元素。与NiFe-Gly不同的是,P-NiFe-Gly中出现了N元素的信号,说明N被成功引入。由Ni 2p XPS谱图(见图3(b))可知,NiFe-Gly在855.8和873.5 eV处的峰可以归因于Ni2+,而857.3和875.3 eV处的峰可以被指认为Ni3+[17]。经过N2等离子体活化后,P-NiFe-Gly中仍然存在Ni2+和Ni3+,但在853.0/870.1 eV和854.3/870.9 eV分别出现了Ni0和Ni—N键的峰[19],进一步证实了Ni单质和Ni3N的产生。位于862.2和880.3 eV处的峰为卫星峰(Satellite)。由Fe 2p XPS谱图(见图3(c))可知,NiFe-Gly和P-NiFe-Gly均在712.3/723.8 eV和714.9/726.9 eV分别出现Fe2+和Fe3+[20]。但P-NiFe-Gly中Fe2+/Fe3+所占面积的比(1.47)高于NiFe-Gly中Fe2+/Fe3+面积比(1.37),说明N2等离子体将部分Fe3+还原为Fe2+。由图3(d)可见,NiFe-Gly的C 1s XPS谱图中C=O(288.7 eV)、C—O(286.3 eV)和C—C (284.8 eV)键是金属-甘油酸的典型特征[9]。在等离子体活化后,仍然可以看到C相关化学键的存在,但峰强明显减弱,说明P-NiFe-Gly中还存在少部分金属-甘油酸。相对应的,在O 1s的XPS谱图(见图3(e))中,NiFe-Gly和P-NiFe-Gly均可以看到金属-甘油酸中的C—O(532.6 eV)和C=O(530.7 eV)键[14-15]。531.3 eV处对应的峰为金属—OH(M—OH)键或金属—O—C(M—O—C)键[21]。P-NiFe-Gly在530.1 eV处出现了金属—O(M—O)键[22]。在P-NiFe-Gly的N 1s XPS谱图(见图3(f))中,出现了Ni—N键对应的峰,进一步说明了Ni3N的生成。在397.8 eV处出现的N—O键是由于Ni3N接触空气被氧化造成的[23]。综上结构分析可见,实心的NiFe-Gly微球经过N2等离子体活化后变为空心结构的P-NiFe-Gly微球,P-NiFe-Gly主要由Ni3N和Ni单质构成,并含有少量的Fe物种和未经转化的NiFe-Gly。

sat.—Satellite图3 NiFe-Gly和P-NiFe-Gly的XPS谱图Fig.3 XPS spectra of NiFe-Gly and P-NiFe-Gly(a)Survey spectrum;(b)Ni;(c)Fe;(d)C;(e)O;(f)N
为明晰P-NiFe-Gly中新物种产生的原因,在射频功率400 W、压力60 Pa条件下进行了N2等离子体的发射光谱(Optical emission spectroscopy,OES)测试,结果如图4所示。由图4可知,OES谱图中位于280~490 nm和500~750 nm的信号代表离子化的N2分子[24],具有很强的氮化作用导致形成氮化镍[18,13]。此外,N2等离子体中存在大量高能电子,具有较强的还原作用[25],会将NiFe-Gly中的部分Ni2+和Fe3+分别还原为Ni0和Fe2+。
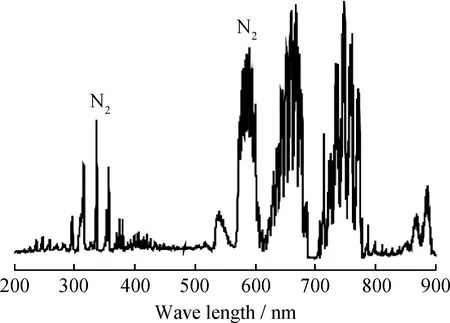
图4 N2等离子体的发射光谱(OES)谱图Fig.4 Optical emission spectroscopy (OES) spectra of N2 plasma
2.3 P-Ni-Gly和P-NiFe-Gly的析氧反应性能评价
在最优等离子体参数(射频功率400 W、N2压力60 Pa、活化时间5 min)条件下活化获得的P-Ni-Gly和P-NiFe-Gly的LSV曲线如图5(a)所示。由图5(a)可以观察到,N2等离子体对Ni-Gly和NiFe-Gly均有活化增强作用。且P-NiFe-Gly的活性明显优于P-Ni-Gly,进一步说明了Fe对析氧反应活性的增强作用。P-NiFe-Gly只需要230 mV的过电位就可驱动电流密度达到10 mA/cm2,远低于NiFe-Gly(300 mV)和P-Ni-Gly(350 mV)达到相同电流密度所需的过电位。与此同时,经过计算后,P-Ni-Gly的Tafel斜率为85.4 mV/dec,P-NiFe-Gly的Tafel斜率为32.1 mV/dec。因此,P-NiFe-Gly具有最小的Tafel斜率(如图5(b)所示),表明该材料具有加速的析氧反应动力学[25-26]。此外,P-NiFe-GIy的析氧反应活性也优于文献报道的大部分金属-甘油酸及其衍生物(见表1)。为进一步明晰等离子体活化增强析氧反应活性的原因,进行了电化学阻抗和电化学活性面积测试。由图5(c)的Nyquist图表明,Ni-Gly和NiFe-Gly经N2等离子体活化后电化学阻抗有所减小,电荷转移动力学明显提升[27]。P-NiFe-Gly展现了最小的阻抗,这可能是由于等离子体活化产生的Ni3N和Ni单质具有较高的导电性,中空结构使得材料的内部与外部都可以很好地与电解液接触,薄的壳层可以缩短电荷的传输路径。采用电容法评价了催化剂的SECSA。一般情况下,催化剂的SECSA与Cdl成正比[28]。NiFe-Gly和P-NiFe-Gly的Cdl分别为0.8775和14.12 F/cm2,表明P-NiFe-Gly暴露了更多的催化活性位点,其表面反应物和中间体在析氧反应过程中能够有效地吸附/转移[29]。评价析氧反应催化剂的另外一个重要的参数是稳定性。P-NiFe-Gly不仅具有增强的析氧反应活性,而且具有较好的稳定性(见图5(g)),在持续催化析氧反应达40 h后活性并无衰减(见图5(h))。
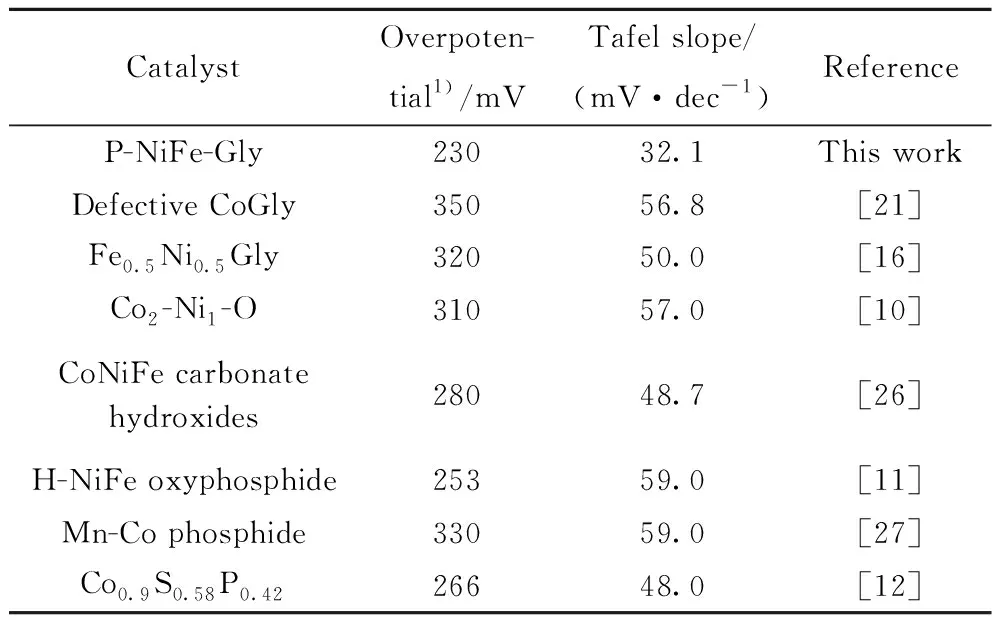
表1 P-NiFe-Gly与文献报道的析氧反应催化剂的活性比较Table 1 Comparison of activity between P-NiFe-Gly and the reported oxygen evolution reaction catalysts
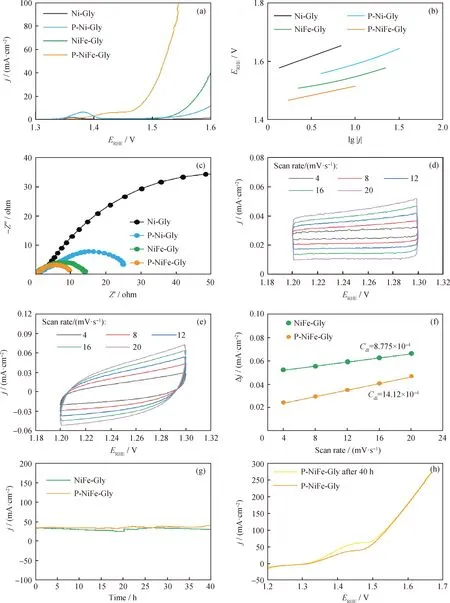
ERHE—Potential of reversible hydrogen electrode;j—Current density;Δj—Current density differences;Z′—Real part value,Z″—Imaginary part value图5 Ni-Gly、P-Ni-Gly、NiFe-Gly和P-NiFe-Gly的电化学表征Fig.5 Electrochemical characterization of Ni-Gly,P-Ni-Gly,NiFe-Gly,and P-NiFe-Gly(a)LSV curves at a scan rate of 5 mV/s in 1 mol/L KOH;(b)Tafel plots;(c)Nyquist plots obtained at an overpotential of 417 mV;(d)CV curves of NiFe-Gly at scan rates from 4 mV/s to 20 mV/s;(e)CV curves of P-NiFe-Gly at scan rates from 4 mV/s to 20 mV/s;(f)Δj vs. scan rate;(g)Stability test of NiFe-Gly and P-NiFe-Gly at a constant overpotential of 247 mV in 1 mol/L KOH;(h)LSV curves of P-NiFe-Gly before and after 40 h of long term stability test at a scan rate of 5 mV/s in 1 mol/L KOH
考察不同等离子体参数(射频功率和活化时间)对NiFe-Gly活性增强的影响,结果见图6。由图6(a)可知,当活化时间固定为5 min时,镍铁-甘油酸的析氧反应活性随着射频功率的增大而增强,射频功率为400 W时获得的P-NiFe-Gly-400 W具有最佳的活性。由于所使用等离子体设备的最大工作功率为400 W,因此进一步延长和缩短活化时间,结果如图6 (b)所示。由图6(b)可以看出:当活化时间从1 min延长到5 min时,析氧反应活性增强;但当进一步延长活化时间至15 min时,析氧反应活性降低。因此,确定最佳的等离子体射频功率为400 W、活化时间为5 min。
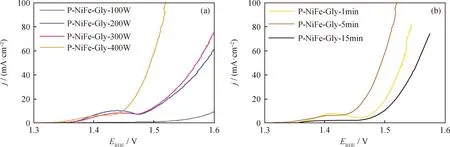
ERHE—Potential of reversible hydrogen electrode;j—Current density图6 射频功率和活化时间对P-NiFe-Gly活性的影响Fig.6 Effect of radio frequency power and activation time on the activity of P-NiFe-Gly(a)LSV curves of samples obtained at plasma power of 100 W,200 W,300 W,and 400 W at a scan rate of 5 mV/s in 1 mol/L KOH. The activation time and gas pressure is 5 min and 60 Pa,respectively;(b)LSV curves of samples obtained at the activation time of 1 min,5 min,and 15 min at a scan rate of 5 mV/s in 1 mol/L KOH. The plasma power and gas pressure is 400 W and 60 Pa,respectively
2.4 电化学原位拉曼分析
采用电化学原位拉曼光谱观测NiFe-Gly和P-NiFe-Gly的析氧反应过程,记录从开路电位到ERHE=1.6 V的连续拉曼光谱。排除泡沫镍对拉曼信号的贡献后的拉曼光谱图如图7(a)所示。由图7(a)可以看出,无论对于P-NiFe-Gly还是NiFe-Gly,在开路电位时,均没有明显的拉曼信号。当ERHE增加到1.2 V时,P-NiFe-Gly在443 cm-1出现了1个峰,对应于Ni—OH的振动[19],表明P-NiFe-Gly表面转化为Ni(OH)2;随着电位进一步增加到1.5 V,在461和532 cm-1出现了2个明显的峰,分别对应于NiOOH的Eg(δ(Ni-O))和A1g(υ(Ni-O))[30],表明表面产生的Ni(OH)2进一步氧化为NiOOH;而NiFe-Gly在ERHE为1.5 V时并未产生NiOOH。这可能是由于等离子体活化产生的Ni3N和Ni单质增强了导电性,有助于电子的传递,进而有助于Ni(OH)2的转变。此外,有研究报道,Fe基化合物能够促进NiOOH的生成[17],因此P-NiFe-Gly中的含Fe物种也有可能促进NiOOH的产生。镍基催化剂表面原位产生的NiOOH通常被认为是析氧反应的真正活性位点[28]。因P-NiFe-Gly能够更快速地产生NiOOH,所以相比于NiFe-Gly展现出更加优异的析氧反应活性。
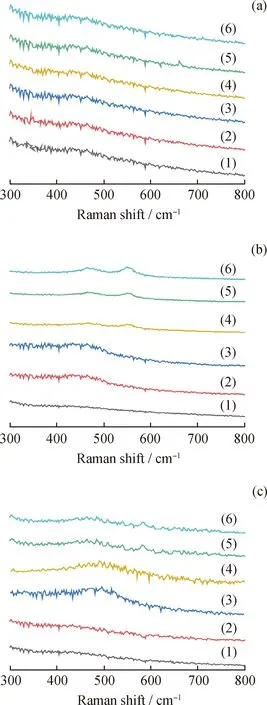
ERHE/V:(1)0;(2)1.2;(3)1.4;(4)1.5;(5)1.53;(6)1.6图7 不同电位下的原位拉曼光谱图Fig.7 In-situ Raman spectra at various potentials(a)Ni-foam;(b)P-NiFe-Gly;(c)NiFe-Gly
基于上述分析,等离子体活化后的NiFe-Gly具有增强的析氧反应活性主要源于以下3方面原因:①由于等离子体的氮化和还原作用,P-NiFe-Gly中产生了Ni3N和Ni单质,增强了电催化剂的导电性,有助于电子的转移;②P-NiFe-Gly中存在含铁物种,有助于促进活性物种NiOOH的快速生成,进而增强析氧反应活性;③P-NiFe-Gly的中空结构增大了电化学活性面积,使催化剂暴露更多的活性位点,同时缩短了电荷和电子传输路径。
3 结 论
(1)利用N2等离子体活化技术,在低温和环境友好的条件下成功将镍铁-甘油酸实心微球快速转化为由Ni单质、Ni3N和含铁物种构成的复合中空微球,获得了增强的析氧反应活性。
(2)通过对Fe离子含量(Ni/Fe摩尔比为14.7、11.1和5.89)和等离子体活化参数的优化,获得的P-NiFe-Gly在电流密度为10 mA/cm2下的过电位仅为230 mV、Tafel斜率仅为32.1 mV/dec。
(3)P-NiFe-Gly还具有较佳的稳定性,可以持续稳定催化析氧反应达到40 h。
(4)通过电化学原位拉曼分析揭示了等离子体活化后析氧反应活性的增强主要源于P-NiFe-Gly表面NiOOH的快速产生。
