等离子体增强Ni基催化剂制备及其催化正戊烷重整性能
2023-09-19周为莉章旭明徐顺秒吴祖良朱祖超
周为莉,章旭明,徐顺秒,吴祖良,任 燕,朱祖超
(1.中国科学技术大学 国家同步辐射实验室,安徽 合肥 230029;2.浙江理工大学 浙江省流体传输技术研究重点实验室,浙江 杭州 310018;3.浙江理工大学 绍兴柯桥研究院,浙江 绍兴 312000;4.杭州佰斯维环境科技有限公司,浙江 杭州 310018;5.常州大学 环境科学与工程学院,江苏 常州 213164;6.浙江中泰环保股份有限公司,浙江 衢州 324000)
中国经济水平不断提高,能源需求持续快速增长,其中对化石燃料的大量需求,不仅影响中国能源安全[1],也会对生态环境造成影响。如机动车燃料燃烧将排放大量的环境有害物质颗粒物(PM)、CO2和NOx,不仅污染大气环境[2-5],而且机动车尾气低空排放的特性会对人体造成伤害[6]。尽管已开发用于减少NOx排放的后处理技术,仍无法避免PM、CO2在大气中的大量积聚,继而导致系列环境问题。因此基于国家能源安全和节能减排考虑,中国现阶段迫切需要清洁能源[7-8]。
含氧燃料可作为石油替代燃料,既可以单独使用(如甲醇新能源汽车),也可与汽油或柴油等混合使用,不仅可减少汽车工业对石油的依赖,还能获得优良的发动机燃烧性能,同时也可极大减少尾气排放。如在汽油中混入乙醇燃料,不仅能够有效降低HC和CO的排放,还可提升发动机动力性,改善燃油经济性[9]。CO2作为温室气体严重危害大气环境,但其所含的O可作为产生含氧燃料的O源,且其解离产物相对简单,有利于机理的研究。此外,以H2作为机动车驱动的能源也能有效减少尾气污染,具有很好的发展经济性,但其易燃易爆且难以储存令其实用性饱受争议[10-12]。针对这个问题,对汽油或柴油等液态化石燃料进行原位车载重整制取H2和含氧燃料是一种十分有前景的方法[13-17]。
目前发展较为成熟的是热催化技术,但其反应条件较为苛刻,一般需要高温[18],不仅不利于车载装置的安全,而且达到目标温度所需时间较长[19]。此外,催化剂常因高温烧结而失活,无疑增加了成本,降低了经济性。而非热平衡等离子体(Non-thermal plasma,NTP)技术可以为车载装置的安全高效提供保障,因为NTP中包含大量高能电子,可以在常温常压下快速通过碰撞解离开启反应[20-22]。但单独NTP技术存在转化率低、选择性低、能量效率不高的问题,而催化剂的引入是一种有效的解决方式。燃料重整中最常见的是Ni基催化剂,因其催化活性仅次于贵金属催化剂,且价格低廉[23]。常见制备Ni基催化剂的方法是浸渍-烘干-焙烧后高温还原,该方法制备的催化剂很容易因为积炭、烧结而失活。而借助NTP技术可有效改善这种情况。Jin等[24]利用H2等离子体制备Ni/γ-Al2O3催化剂并应用于CH4-CO2重整反应,实验结果显示输入功率越高,活性物质还原程度、催化活性和稳定性越高,较之传统高温还原催化剂,经过等离子体处理的催化剂的活性物质Ni的粒径更小,活性位点更多,催化剂碱性更弱,这些都令其拥有更好的催化活性和抗积炭性能。Wang等[25]利用大气压介质阻挡放电(Dielectric barrier discharge,DBD)在350 ℃下采用Ar等离子体对催化剂处理3 h,得到的催化剂用于CH4-CO2一步催化重整产生液态燃料和高价值化学产品,对液相产物分布有较好的调控作用。Peng等[23]采用H2/Ar气氛的DBD以不同顺序制备了一系列浸渍法制备的Ni/La2Zr2O7烧绿石催化剂并用于CH4干重整,实验结果发现,与未经DBD处理的催化剂相比,经过DBD处理的催化剂均显示出更高的活性和抗结焦能力;结合TGA-DSC和SEM表征发现,经过等离子体处理的样品上的积炭情况都得到了显著的抑制,抗积炭性能明显增强。
笔者采用自主设计的温-压双控同轴DBD反应器,首先利用NTP改性Ni基催化剂,并对催化剂在等离子体辅助汽油模拟物C5H12和温室气体CO2重整反应中对反应物活化和产物生成的影响进行评价,分析了等离子体改性的作用。然后通过改变反应参数(能量密度、背景温度和压力),阐明电子引发化学和热化学的相对贡献,最后通过改变原料气CO2浓度对等离子体协同催化C5H12-CO2重整的产物生成机理做了进一步探索与分析。
1 实验部分
1.1 原料和试剂
氧化铝小球,工业级,购于大连海鑫化工有限公司;硝酸镍、正戊烷、无水乙醇,均为分析纯,购于上海凌峰化学试剂有限公司;二氧化碳、氮气、氩气,纯度均高于99.99%,购于南京今工特种气体厂;氢气,纯度高于99.999%,自福立氢气发生器自制;去离子水,实验室自制。
1.2 催化剂的制备
将氧化铝小球用无水乙醇和去离子水超声洗涤,在120 ℃烘箱中干燥10 h,然后在马弗炉中600 ℃焙烧4 h后装入样品瓶备用。采用等体积浸渍法制备负载型Ni基催化剂。称取0.49 g的硝酸镍(Ni(NO3)2·6H2O)溶解于去离子水中,加入1 g的氧化铝小球,在25 ℃下转速为100 r/min振荡2 h,然后静置老化12 h,然后在烘箱中110 ℃干燥10 h。最后再置于马弗炉中以500 ℃焙烧5 h,得到负载型Ni基催化剂Ni/Al2O3,编号为IC。使用前将IC在H2/Ar氛围下500 ℃处理1 h后的催化剂编号为ICH;在温度25 ℃、压力0.1 MPa、能量密度6 kJ/L和H2/Ar(体积比1/4,总体积流量100 mL/min)混合气的条件下,将IC利用等离子体进行处理,得到的催化剂记为ICP。
1.3 催化剂的表征
采用荷兰帕纳科公司生产的X-Pert-MPD型X射线衍射仪(XRD)对催化剂样品进行晶相结构表征。采用美国麦克公司生产的Micromeritics TriStar Ⅱ 3020型化学吸附仪对催化剂样品进行孔结构表征,利用BET方程计算所测试样品的比表面积,根据N2吸附容量估算孔体积。采用天津先权工贸发展有限公司生产的Tp-5080型化学吸附仪对催化剂样品进行H2-TPR和CO2-TPD表征,首先用He在300 ℃下吹扫1 h后降温至50 ℃,然后将载气/参比气切换为H2(体积分数10%)/Ar或CO2,并在室温下吹扫1 h,然后以升温速率10 ℃/min升到800 ℃。采用美国FEI公司生产的FEI TECNAI G2 F20透射电子显微镜(TEM)对催化剂样品进行形貌表征。采用美国梅特勒-托利多公司生产的Mettler TGA/DSC3+型热分析系统对催化剂样品进行热重(TG)表征,在N2气氛下进行试验,从25 ℃以升温速率10 ℃/min升温至800 ℃。
1.4 实验装置及分析方法
等离子体协同催化C5H12-CO2重整反应装置见图1。DBD反应器使用内径为14.4 mm的石英管作为介质材料,外部缠裹长度为50 mm的不锈钢网作为低压极,作为高压电极的金属棒同心同轴安置于石英管的内部。高压交流电源(CTP-2000K型,南京苏曼等离子体科技有限公司产品)电压范围是0~20 kV,频率为4~10 kHz。利用分压比为1000∶1的高压探头测量电压,利用电流探头测量反应器中电流,相应电学参数通过数字示波器显示。

MFC—Mass flow controller;GC—Gas chromatography;GC-MS—Gas chromatography-mass spectrometry图1 等离子体协同催化C5H12-CO2重整反应装置Fig.1 Schematic of experimental system for plasma-catalytic reforming of C5H12-CO2
催化剂的等离子体处理与评价在同一套反应器内进行。实验气体为C5H12、CO2和N2按体积比1∶5∶4的混合气体,总体积流量为200 mL/min。催化剂填充于等离子体放电区域。
冷阱串联进DBD反应器下游用于收集液相产物。气相产物利用气相色谱仪(GC,SP-3420,北京北分瑞利分析仪器有限责任公司,配备FID检测器)进行在线分析,液相产物采用气相色谱-质谱联用仪(GC-MS,7890A-5975C,安捷伦科技有限公司生产)进行分析测定。采用外接H2检测仪(APES-TH2S-S,深圳市安帕尔科技有限公司生产)对产生的H2进行测定。
能量密度(Energy density,Ed,kJ/L)用来表示电源供给的能量,计算式如式(1)所示。
(1)
式中:qflow为反应气体的总体积流量,mL/min;Pdis为放电功率,W。
等离子体协同催化C5H12-CO2重整反应以C5H12转化率(x1,%)、CO2转化率(x2,%)和产物碳氢化合物CxHy选择性(sCxHy,%)、H2选择性(sH2,%)、CO选择性(sCO,%)和含氧化合物Oz选择性(sOz,%)为评价指标,计算式见式(2)~式(6)。
(2)
(3)
(4)
(5)

(6)
式中:n1 or 2,in为进入反应器的C5H12或CO2物质的量,mol;n1 or 2,out为反应器出口C5H12或CO2物质的量,mol;nCxHy为生成的CxHy物质的量,mol;nH2为生成的H2物质的量,mol;nCO为生成的CO物质的量,mol;nOz为生成的含氧产物物质的量,mol;ΔnCO2为转化CO2物质的量,mol;sCxHy为产物CxHy的选择性,%;sH2为产物中H2的选择性,%;sCO为产物中CO的选择性,%;sOz为产物中含氧化合物的选择性,%;a为产物中烃类产物的含碳数。
2 结果与讨论
2.1 等离子体处理对催化剂性能的影响
图2为催化剂ICH和ICP的XRD图谱。由图2可以看出,2种催化剂均有2θ为32.7°、45.8°和66.9°的Al2O3衍射峰,2θ为37.3°、43.2°和62.8°的NiO特征峰,2θ为43.1°和45.2°的Ni特征峰以及2θ为75.2°和79.1°的NiAl2O4特征峰。Al2O3特征峰的峰宽和强度无明显差异,说明等离子体处理并未明显改变载体的体相结构,这主要是因为Al2O3具有较好的机械强度和稳定性。对于NiO和NiAl2O4特征峰,催化剂ICP的峰强更低,可能是等离子体处理减小了NiO和NiAl2O4粒径,使得分散更加均匀。

图2 ICH和ICP催化剂样品的XRD图谱Fig.2 XRD patterns of catalysts ICH and ICP
表1给出了ICH和ICP催化剂样品的N2吸附-脱附测试结果。由表1可知,与ICH相比,ICP比表面积更大,这可能是因为等离子体处理使得活性物种颗粒尺寸减小。值得注意的是,2种催化剂的比表面积都小于载体的比表面积(167 m2/g),这可能是负载金属后,催化剂表面活性物种占据了部分表面,也有可能是Al2O3经过处理后部分孔道坍塌,从而比表面积减小。此外,不论是否经过等离子体处理,2种催化剂的孔体积值相近,可能是因为Al2O3拥有良好的机械强度和热稳定性,故而结构稳定,不容易发生改变。

表1 ICH和ICP催化剂样品的比表面积和孔体积Table 1 Specific surface area and pore volume of catalysts ICH and ICP
图3为ICH和ICP催化剂样品的H2-TPR图谱。从图3可知,ICH存在位于250 ℃附近的低温脱附峰和位于500 ℃附近的中温脱附峰[26]。而对于ICP,只能在500 ℃左右观测到1个很强的H2消耗峰,说明ICP的金属和载体相互作用更强,也就是说等离子体处理可以增强金属与载体的相互作用,这可能是该催化剂活性更高的原因之一。

图3 ICH和ICP催化剂样品的H2-TPR图谱Fig.3 H2-TPR profiles of catalysts ICH and ICP
催化剂的碱性可能对其在重整反应中的活性也有一定影响,利用CO2-TPD表征催化剂的碱性。图4为ICH和ICP催化剂样品的CO2-TPD图谱。从图4可知,ICH和ICP都存在230 ℃附近的低温脱附峰和420 ℃附近的中温脱附峰,说明它们都拥有2个碱性中心。且脱附峰的位置和面积并无显著区别,说明等离子体处理对催化剂的碱性无显著影响。
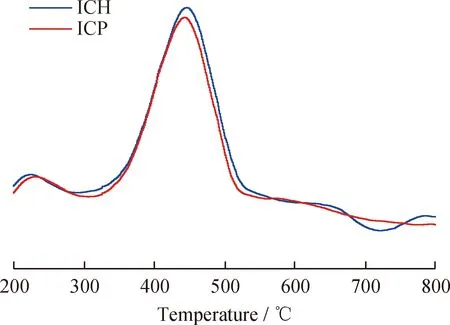
图4 ICH和ICP催化剂样品的CO2-TPD图谱Fig.4 CO2-TPD profiles of catalysts ICH and CIP
反应前后ICH和ICP催化剂样品的TEM照片见图5。由图5可知,ICH中颗粒团聚且粒径较大,约12 nm;而ICP中颗粒明显更加分散且粒径更小,约为5.6 nm。说明等离子体处理可减小活性物种粒径且提高其分散度,使得更多活性物种向催化剂外表面迁移,催化活性位点增多,因此催化活性更好,这与催化剂评价结果一致。经过评价反应后,ICH明显烧结团聚,而ICP的活性物种仍保持较好的分散性,粒径也并未增加,因此可以推断,等离子体处理提高了催化剂的抗烧结性能,催化活性位点也更多的保留下来,因而催化稳定性和活性更高[27]。

图5 反应前后ICH和ICP催化剂样品的TEM照片Fig.5 TEM images of ICH and ICP catalyst samples before and after reaction(a)ICH before reaction;(b)ICP before reaction;(c)ICH after reaction;(d)ICP after reaction
积炭是导致催化剂失活的主要原因,借助TG表征来分析ICH和ICP催化剂经过32 h反应后的积炭情况,结果见图6。根据文献[28-29]可知,Ni基催化剂积炭的质量损失在200~500 ℃范围内进行计算。由图6可知,反应后ICP的积炭率(2.8%)低于ICH(6.0%),即经过等离子体处理后催化剂抗积炭性能更好,这可能与催化剂ICP表面活性物种的粒径较小有关,积炭一般需要在较大的Ni晶粒上生成[30],这与之前表征结果一致。以上结果表明,等离子体处理可减小催化剂表面活性物种的粒径,从而减少反应中积炭的产生。
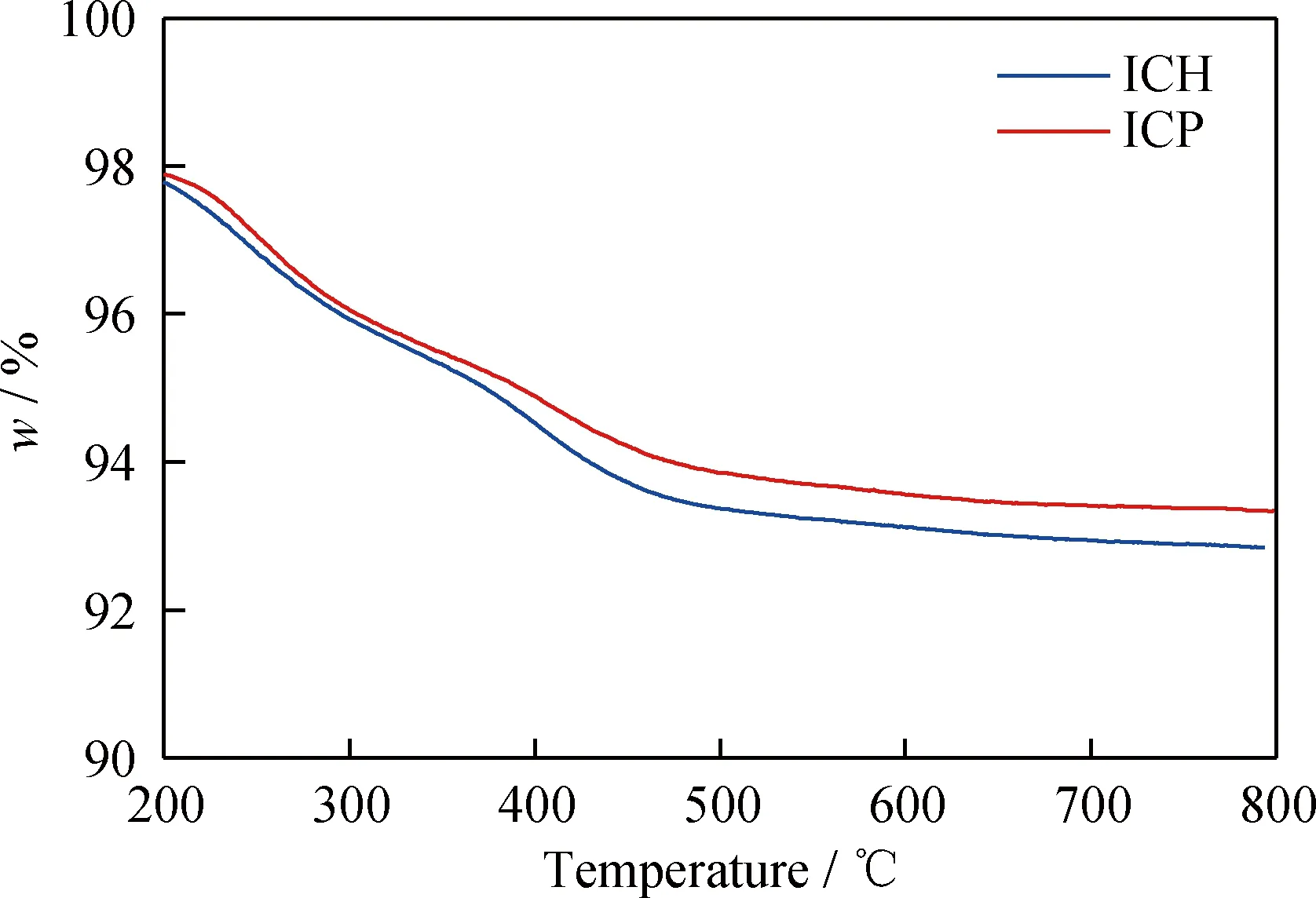
图6 ICH和ICP催化剂样品的经过32 h反应后的热重曲线Fig.6 TG curves of ICH and ICP catalyst samples after 32 h reaction
2.2 等离子体催化C5H12-CO2重整反应性能
2.2.1 催化剂处理方法对重整反应性能的影响
不加催化剂及加入经不同方法处理的催化剂于温度25 ℃、压力0.1 MPa、能量密度3.6 kJ/L和电源频率5 kHz条件下等离子体催化C5H12-CO2重整反应的反应性能见图7。从图7可知,加入催化剂后的反应物转化率和产物总选择性提高。加入1 g的ICP后,C5H12的转化率从15.3%增加到24.3%,CO2的转化率从0.8%提高到1.2%,气相产物选择性均上升,且H2的增加多于CO,因此合成气比例高于加入ICH的情况。加入ICP后,含氧化合物的选择性从2.34%增加至7.12%。这是因为加入催化剂后,催化剂的碱中心会吸附气相中的CO2参与反应而产生更多的CO,故而CO选择性都有所提高;而分解产生的O和OH自由基会与C5H12反应,在进一步提高C5H12转化率的同时产生更多的C5H11、C5-nH11-2m等物质,继而发生重组反应产生烷烃及含氧化合物[31]。ICP的活性物种粒径更小,分散性更好,且金属与载体的相互作用更强,这些都促进了反应物的转化。
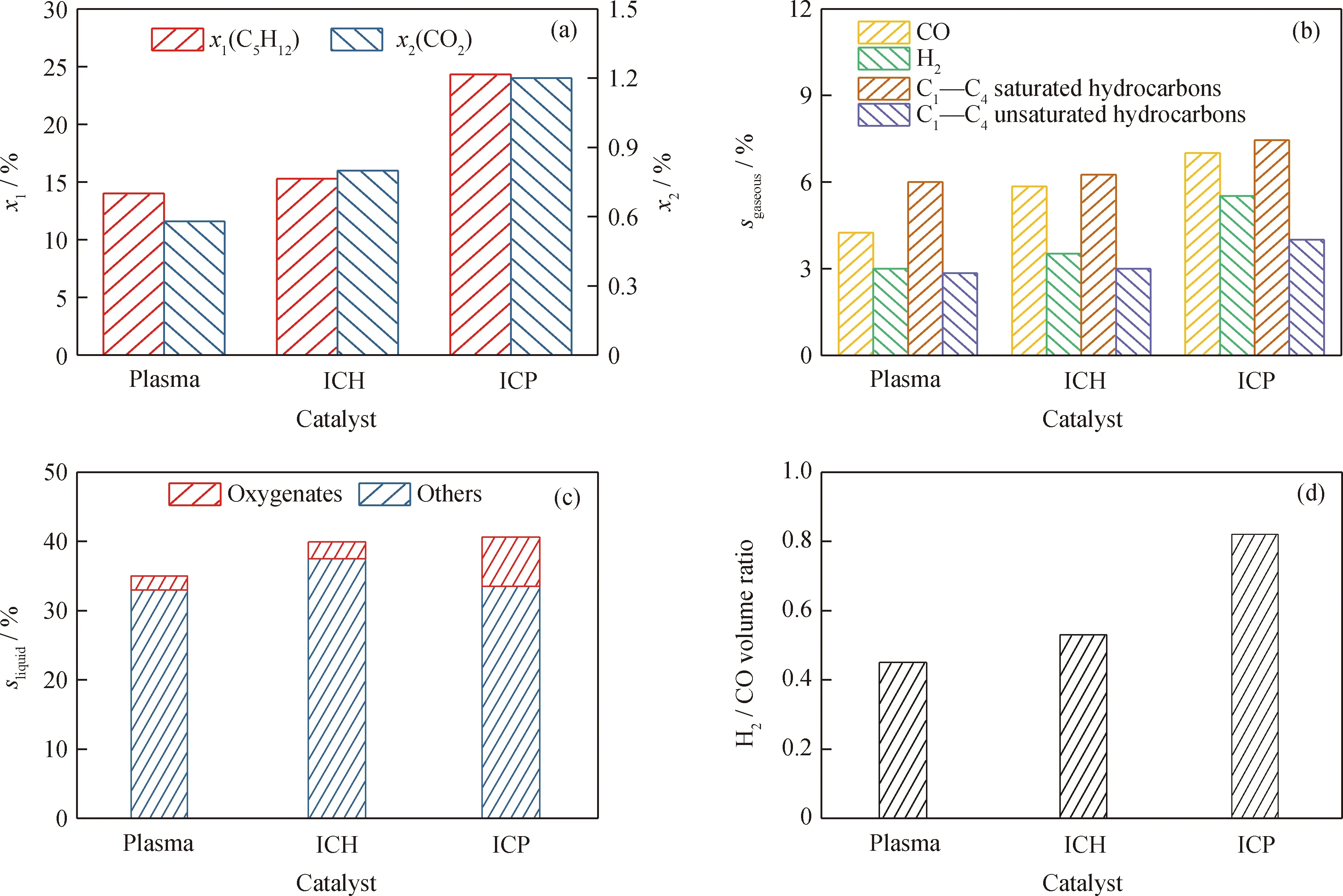
图7 经过不同方法处理的催化剂样品催化C5H12-CO2重整反应性能Fig.7 The performance of catalysts with different treatments in the reforming of C5H12 and CO2(a)Reactant conversion;(b)Selectivity of gaseous product;(c)Selectivity of liquid product;(d)SyngasConditions:m(Catalyst)=1 g;T=25 ℃;p=0.1 MPa;f=5 kHz;Ed=3.6 kJ/L;qflow=200 mL/min
2.2.2 反应体系放电特性
在等离子体辅助C5H12-CO2重整反应中添加催化剂后,体系放电特性将会发生变化。有无添加催化剂ICP时反应体系的电压和电流随时间的变化情况见图8。从图8可知,高于起始电晕电压时,每段施加电压的周期内都可观测到数量很多的电流脉冲,这些电流短脉冲与放电间隙内的放电细丝相对应,当将适量的催化剂填充于放电空间后,在不改变放电形式的情况下,电流脉冲的强度明显增强,说明适量催化剂的添加不仅不会改变放电模式,还可促进丝状微放电[32]。

图8 有无催化剂ICP时反应体系的电压和电流随时间的变化Fig.8 Changes in voltage and current of the reaction system with and without catalyst ICP over time (a)Without catalyst ICP;(b)With catalyst ICPConditions:m (Catalyst)=1 g;T=25 ℃;p=0.1 MPa;f=5 kHz;Ed=3.6 kJ/L;qflow=200 mL/min
此外,开启等离子体会伴随局部加热,即电子引发化学和热化学并存,所以有必要阐明两者对反应性能的相对贡献。温度会影响DBD的放电特性[33],因此对所有填充催化剂ICP的实验温度进行研究。利用电荷-电压李萨如(Q-ULissajous)图对反应系统的放电特性进行表征,结果见图9。由图9可知,Lissajous面积随温度升高而增加。而当温度提升至250 ℃时,Lissajous图形变得平滑且面积明显增加;当进一步提高温度至300 ℃时,Lissajous图形完全丧失其典型的DBD特征[34]。根据以上结果可知,300 ℃时放电模式发生改变[35]。

图9 不同背景温度下填充催化剂ICP反应系统的电荷-电压李萨如图Fig.9 Typical Q-U Lissajous diagrams of the reaction system packed with catalyst ICP at various temperatures T/℃:(a)30,100,200,250;(b)300Conditions:m(Catalyst)=1 g;p=0.1 MPa;Ed=3.6 kJ/L;qflow=200 mL/min
2.2.3 能量密度对重整反应性能的影响
在温度25 ℃、压力0.1 MPa的条件下,填充1 g催化剂ICP,考察能量密度对重整反应性能的影响,结果见图10。由图10可知,当能量密度从1.2 kJ/L增加到3.6 kJ/L,反应物C5H12和CO2的转化率分别从10.75%和0.60%提高至24.28%和1.20%,说明反应物转化主要受到给定温度和约化电场强度(E/N)时的电子密度控制的,这是因为电子碰撞解离反应速率与电子密度呈正相关[34]。而产物选择性几乎不随能量密度而改变,这表明反应路径不受其影响。K型热电偶测量得到反应器后端实际温度变化低于30 ℃,即实验温度未明显改变,因此反应物转化率改变的唯一解释是电子密度即电子引发化学发生了改变,这与单独等离子体的结果一致[31]。

图10 能量密度对C5H12-CO2重整反应性能的影响Fig.10 Effect of energy density on the performance of catalyst ICP in the reforming of C5H12 and CO2(a)Reactant conversion (x1 and x2);(b)Product selectivity (s)Conditions:m(Catalyst)=1 g;T=25 ℃;p=0.1 MPa;f=5 kHz;qflow=200 mL/min
2.2.4 背景温度对重整反应性能的影响
在压力0.1 MPa、能量密度3.6 kJ/L和电源频率5 kHz的条件下,填充1 g催化剂ICP,考察背景温度对重整反应性能的影响,结果见图11。由图11可以看出,在不开启等离子体时,当温度低于150 ℃时,反应物不会分解,这与热力学计算模拟相符合[32];而当温度进一步升高,反应物转化率随之提高,这可能是由于催化剂开始起催化作用。而当开启等离子体时,反应物即使在较低的温度也发生转化,且反应物转化率随温度提高而提高;但当温度达到250 ℃时,反应物转化率都有所降低,这可归因于放电模式的转变。值得注意的是,与单独等离子体相比[31],加入催化剂后转化率下降幅度减小,这可能是由于温度升高,催化剂与等离子体的协同作用增强。

图11 背景温度对C5H12-CO2重整反应性能的影响Fig.11 Effect of background temperature on the performance of catalyst ICP in the reforming of C5H12 and CO2(a)C5H12 conversion (x1);(b)CO2 conversion (x2);(c)Product selectivity (s)Conditions:m(Catalyst)=1 g;p=0.1 MPa;Ed=3.6 kJ/L;f=5 kHz;qflow=200 mL/min
2.2.5 约化电场强度的影响
不同温度下反应性能差异可能是由于平均电子能量改变,也有可能是因为热化学增强[36],所以需要阐明在不同温度和压力下E/N的作用。在能量密度3.6 kJ/L和电源频率5 kHz的条件下,填充1 g催化剂ICP,考察E/N对重整反应性能的影响,结果见图12。分别通过固定温度调节压力和固定压力调节温度来调节E/N。由于较高的E/N提供了较高的平均电子能量,所以反应物转化率随E/N增加而增加。然而在相近的E/N值,通过固定压力改变温度的反应物转化率值略高于通过固定温度改变压力的情况,这表明,在实验条件范围内,反应物转化主要受电子引发化学影响。产物选择性随E/N增加而单调变化。但相近的E/N值,通过固定压力改变温度的产物选择性的改变都明显大于固定温度改变压力的情况,这表明背景温度在产物生成方面的贡献更大。因此,在固定压力时提高温度,E/N对产物选择性的影响归因于反应温度的提高,而不单纯是E/N的增加,也就是说背景温度即热化学主要控制后续的反应路径。

图12 约化电场强度(E/N)对C5H12-CO2重整反应性能的影响Fig.12 Effect of reduced field intensity (E/N)on the performance of catalyst ICP in the reforming of C5H12 and CO2(a)Reactant conversion (x1 and x2);(b)Product selectivity (s)Conditions:m(Catalyst)=1 g;Ed=3.6 kJ/L;f=5 kHz;qflow=200 mL/min
2.3 等离子体协同催化重整机理分析
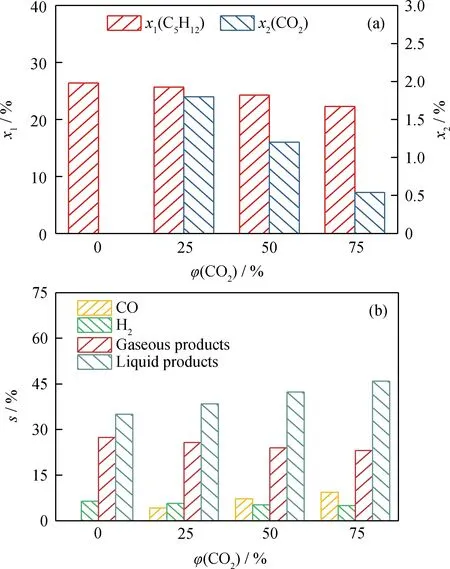
电子引发反应开启等离子体催化反应,产物生成主要受热化学影响,但自由基、离子等的种类、浓度等是产物生成的先决条件,因此需要研究不同自由基种类、浓度对产物生成的影响。首先对等离子体协同催化时的C5H12的转化进行说明,根据本课题组之前的实验结果可知,C5H12的激发能量可估算为3.5 eV,该数值低于DBD中电子能量,故可将C5H12碰撞分解[34],产生如C5H11,H,CnH2m+1(0 表2 C5H12-CO2-N2-ICP重整反应过程重要反应Table 2 Important reactions related to C5H12-CO2-N2-ICP reforming 在温度25 ℃、压力0.1 MPa、能量密度3.6 kJ/L和电源频率5 kHz的条件下,填充1 g催化剂ICP,改变CO2体积分数对等离子体协同催化重整反应的影响见图13。从图13可以看到,随着CO2含量的增加,反应物转化率下降,气相产物中除CO外,选择性均下降,而液相产物选择性整体上升。说明不同CO2含量不仅对反应物转化产生影响,还能对产物分布进行调控。产物分布主要受制于中间产物的重组反应,H2主要产自H自由基重组反应(R1~R3),HC则来自CnHm、C5-nH11-2m和C5H11的重组(R17~R19)。由于C—C键能小于C—H键能,因此产生的H自由基较少,这可能是H2选择性不高的原因。此外随着CO2含量提高,气相产物选择性(除CO)下降。引入更多的CO2,将会增加O自由基的数量,进而通过(R7)、(R8)和(R16)反应提高OH自由基的含量,促进反应(R17~R19)的发生,因而产生更多的长链碳氢化合物及液相产物。 图13 不同CO2体积分数对催化C5H12-CO2重整反应性能的影响Fig.13 Effect of CO2 volume fractions on the performance of catalyst ICP in the reforming of C5H12 and CO2(a)Reactant conversion (x1 and x2);(b)Product selectivity (s)Conditions:m(Catalyst)=1 g;T=25 ℃;p=0.1 MPa;Ed=3.6 kJ/L;f=5 kHz;qflow=200 mL/min 图14为不同CO2体积分数下液相产物的GC-MS图谱。从图14可知,提高CO2含量,液相产物生成量整体呈现上升趋势,含氧产物浓度显著增加,这印证了CO2解离反应产生额外的O自由基的假设(R6),而O自由基也会通过一系列后续反应产生更多的OH自由基,短链烷基与含氧基团继续反应(R20~R21),最终形成含氧化合物,因此含氧产物生成量会随CO2含量增加而增加。 图14 不同CO2体积分数下的液相产物GC-MS图谱Fig.14 GC-MS spectrum of liquid phase products under different CO2 volume fractions conditions:m(Catalyst)=1 g;T=25 ℃;p=0.1 MPa; Ed=3.6 kJ/L;f=5 kHz;qflow=200 mL/min (1)采用DBD反应器改性催化剂Ni/Al2O3,对其在等离子体协同催化C5H12-CO2重整中的性能进行研究。实验发现,较之空管反应,填充催化剂提高了反应物转化率和产物总选择性,这是因为催化剂的存在使得吸附到催化剂表面的CO2参与反应,产生更多的含氧自由基与C5H12反应,在提高C5H12转化率的同时也促进了含氧化合物的产生。而较之加入催化剂ICH,加入催化剂ICP后,反应物转化率和气相产物选择性均提高,含氧产物显著增加。这是因为经等离子体处理后,催化剂比表面积增加,粒径减小,活性物种分散度提高,且金属与载体相互作用更强,抗积炭性能更好,因而反应活性更高。 (2)通过改变能量密度的结果可知,反应起始于电子引发化学。催化剂的填充可有效减缓由于温度提高导致放电特性改变而引起的反应物转化率的下降,这可归因于催化剂在高温下的催化活性。而产物的选择性不受背景温度提高而导致的放电特性转变的影响,说明热化学影响产物分布。通过改变约化场强验证了反应物的转化开始于电子引发化学反应,而热化学对反应物的转化也会产生一定的影响。此外,进一步提高原料气中CO2体积分数可以得到更多的含氧化合物,说明原料气的改变也会影响产物的生成。本研究工作为车载重整器的开发提供了基础数据,等离子体改性催化剂及其反应性能将是后续研究重点。

3 结 论
