孕足月低位水囊引产联合静滴缩宫素对产妇血清WBC、CRP 水平的影响
2023-09-16孙星星王晓娜姚景
孙星星,王晓娜,姚景
江苏大学附属武进医院(徐州医科大学武进临床学院)妇产科,江苏 常州 213017
目前不少产妇因母体或胎儿因素,妊娠晚期需要人工辅助终止妊娠。对足月妊娠产妇,通过及时、有效的引产,能够降低各类合并症发生率、并发症对产妇及胎儿的不利影响,有助于胎儿尽快脱离宫内环境,对改善妊娠结局有明显价值[1-2]。在引产治疗中需要促进宫颈扩张,诱发宫缩,以加快胎儿娩出进程,而引产成功率与宫颈成熟度有着密切关联[3]。静滴缩宫素为常规促宫颈成熟方案,但因个体差异,不少患者对缩宫素不敏感,且可能造成子宫不协调、强直性收缩,甚至可造成子宫破裂、羊水栓塞等[4-5]。低位水囊引产目前在临床中已经有了一定应用,既往多用于中期妊娠引产,该方案主要利用无菌硅胶球囊对子宫下段、宫颈进行机械性压迫,进而可促进宫颈成熟[6]。相关研究指出,对足月妊娠引产产妇,在静滴缩宫素的基础上,通过联合水囊干预,能进一步提高经阴道分娩率,改善妊娠结局[7-8]。基于此,本研究便利选取2020 年2 月—2023 年2 月江苏大学附属武进医院(徐州医科大学武进临床学院)收治的孕足月产妇96 例,通过随机对照,进一步探讨低位水囊联合静滴缩宫素方案的价值,现报道如下。
1 资料与方法
1.1 一般资料
便利选择本院收治的孕足月妊娠产妇96 例为研究对象,随机将其分为两组。对照组48 例,年龄21~35 岁,平均(27.96±2.25)岁;孕周38~42 周,平均(39.76±0.85)周;经产妇16 例,初产妇32 例。观察组48 例,年龄20~34 岁,平均(28.10±2.31)岁;孕周38~42 周,平均(39.82±0.89)周;经产妇17 例,初产妇31 例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会批准。
1.2 纳入与排除标准
纳入标准:①孕38~42 周;②单胎头位且胎膜未破;③宫颈Bishop 评分≤6 分;④骨产道、软产道正常;⑤患者及家属知情同意。排除标准:①双胎、多胎或巨大儿者;②既往剖宫产或子宫手术史者;③胎位不正或前置胎盘者;④生殖系统炎症者;⑤合并妊娠期糖尿病、高血压等者;⑥缩宫素、水囊引产禁忌证者;⑦依从性极差者。
1.3 方法
对照组常规静滴缩宫素治疗,首日使用缩宫素(国药准字H34020473,规格:0.5 mL∶2.5 单位)2.5 U配比氯化钠注射液500 mL 静滴,8 滴/min,期间密切监控宫缩,每20 min 调整1 次滴速,宫缩频率强度控制在每10 min 2~3 次,持续30~40 s,但最大滴速不超过40 滴/min。可用药2 d,如仍未临产,提示引产失败。注意滴注缩宫素期间,持续进行胎心监护,并定期观察,每日总剂量控制≤5 U。
观察组则采用低位水囊引产,促宫颈成熟后,适时静滴缩宫素。采用爱佑AY-K-1 型一次性球囊宫颈扩张器(苏械注准20172661101)进行单球囊扩张宫颈。取膀胱截石位,常规阴道、外阴消毒,充分暴露宫颈,并向宫颈置入球囊,经过宫颈管后,向球囊注入120 mL 0.9%氯化钠溶液。充盈球囊后,略向外轻拉,使宫颈球囊贴紧宫颈内口,以胶布固定在产妇大腿内侧。如无临产,可在12 h 后取出,以人工破膜加缩宫素引产。水囊引产仅放置1 次,不可触碰阴道壁,且放置后每4 h 监测1 次,并注意复查血象,分析是否感染。
1.4 观察指标
①两组分娩方式及宫颈成熟情况比较。分娩方式包括经阴道分娩、剖宫产。促宫颈成熟判定标准:显效为治疗24 h,Bishop 评分增加>3 分;或24 h内顺利分泌;有效为治疗24 h,Bishop 评分增加1~2分;无效为Bishop 评分未见明显改变。总有效率=显效率+有效率。②两组分娩情况比较。统计两组引产至临产时间、产程情况与产后2 h 出血量。产程情况包括第一、第二产程及总产程。③两组炎症反应比较。于分娩前后采集产妇空腹静脉血,检测白细胞计数(white blood cell count, WBC)、C 反应蛋白(C-reactive protein, CRP)水平。④两组并发症发生率比较。比较两组贫血、产褥感染、尿潴留、胎儿宫内窘迫总发生率。
1.5 统计方法
采用SPSS 21.0 统计学软件分析数据。符合正态分布的计量资料用()表示,采用t检验;计数资料用例数(n)和率表示,采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组产妇分娩方式及宫颈成熟情况比较
观察组经阴道分娩率、促宫颈成熟总有效率优于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组产妇分娩方式及宫颈成熟情况比较
2.2 两组产妇分娩情况比较
观察组引产至临产时间、第一产程、第二产程、总产程、产后2 h 出血量优于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组产妇分娩情况比较()
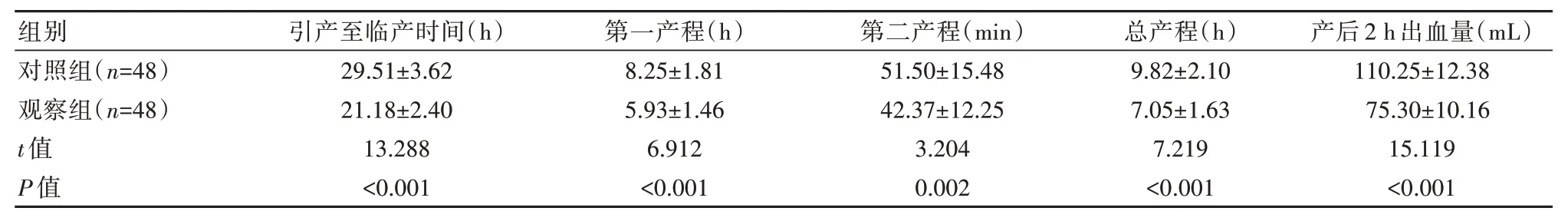
表2 两组产妇分娩情况比较()
?
2.3 两组产妇炎症反应比较
分娩前,两组WBC、CRP 水平比较,差异无统计学意义(P>0.05);分娩后,两组WBC、CRP 水平均升高,但观察组低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组产妇炎症反应比较()

表3 两组产妇炎症反应比较()
注:与同组分娩前比较,*P<0.05。
?
2.4 两组产妇并发症发生率比较
观察组并发症发生率低于对照组,差异有统计学意义(P<0.05)。见表4。

表4 两组产妇并发症发生率比较
3 讨论
引产即在分娩自然发动之前,通过人工方法有效促进子宫收缩以及宫颈成熟,进而终止妊娠。通常因孕妇、胎儿原因需要及时终止妊娠,且无引产禁忌,医生则需要及时引产,而引产治疗中,宫颈成熟度对分娩启动有着至关重要的影响,宫颈成熟度越高,产妇引产的成功的概率也就越高[9-10]。而在常规引产中,临床多采用静脉滴注缩宫素的方式。缩宫素可对子宫平滑肌受体产生选择性刺激,兴奋子宫平滑肌,提高子宫收缩强度、频次,进而加快宫颈成熟,推进产程。但宫颈中缩宫素受体较少,故药物起效缓慢,且部分孕妇用药后容易出现不规律宫缩,甚至可发生宫颈水肿、痉挛[11]。另外,缩宫素可增加血药升高、脉搏加快等的风险,产妇容易疲倦,而子宫血管收缩也会影响血供,进而剖宫产率会明显增加。
低位水囊治疗能够通过机械性刺激,加快宫颈成熟,促进子宫收缩。其主要可对子宫下段以及子宫颈产生机械性压迫,能够刺激子宫,使其产生节律性收缩,并能提高子宫容受度。向宫颈内口置入球囊,可促进宫颈软化以及扩张,注入生理盐水,扩张水囊,则能增加宫腔内的压力,在产妇适应后,通过自然活动,水囊内液体以及胎儿本身的重力可加强宫颈刺激,诱发反射性宫缩[12-13]。水囊也有着良好的变形能力,能够嵌入宫颈管,对宫颈管产生机械性扩张作用,且置入位置可促进胎膜剥离,蜕膜变性,有助于产生局灶性坏死,增加前列腺素水平,进而引发宫缩。宫颈内水囊也能够通过反馈性刺激,加快垂体后叶素、内源性的缩宫素的合成、释放,可诱发宫缩,促进产程顺利推进,可提高引产成功率。也能促进宫颈肌层的拉升,加快环氧化酶-2、基质金属蛋白-8 等的分泌,而该类生化介质也有助于促进宫颈成熟。将低位水囊与缩宫素联合应用,能提高子宫收缩力,加快收缩频率,并有助于宫颈成熟,故而可获得更好的引产效果[14]。经阴道进入宫腔引产,可能会破坏产妇正常的防御能力,增加产后感染的风险,进而影响产妇分娩后的康复。而引产中胎膜早破、产后出血量大等因素,也会增加感染风险。采用低位水囊干预,因水囊弹性、张力、可塑性较好,能维持相对封闭的环境,并可预防胎膜早破,也能进一步促进子宫收缩,降低产后出血风险,故而有利于减轻产妇产后炎症反应。
本次研究中,观察组阴道分娩率(91.67%)、促宫颈成熟有效率(97.92%),高于对照组(72.92%、81.25%)(P<0.05),可见该方案能提高阴道分娩率,可促进宫颈成熟。徐香梅[15]研究中,观察组宫颈成熟有效率(96.15%)、阴道分娩率(78.85%),均高于参照组(P<0.05),也说明低位水囊干预能促进宫颈成熟,提高阴道分娩率。本研究结果显示,观察组引产至临产时间(21.18±2.40)h、第一产程(5.93±1.46)h、第二产程(42.37±12.25)min、总产程(7.05±1.63)h、产后2 h 出血量(75.30±10.16)mL,均优于对照组(P<0.05),说明联合低位水囊干预能推进产程,减少产后出血量。王海礁等[16]研究中,低位水囊干预组引产至临产时间(19.2±8.7)h、总产程(6.7±1.8)h、产后2 h 出血量(210.3±50.6)mL,均优于常规组(P<0.05),与本次研究基本一致。本研究结果显示,观察组分娩后WBC(9.62±1.65)×109/L、CRP(5.72±1.35)mg/L,均低于对照组(P<0.05),可见低位水囊干预能减轻术后炎症反应。廖媛[17]研究中,观察组在联合低位水囊引产后,WBC(9.43±1.79)×109/L、CRP(5.65±1.83)mg/L,均低于缩宫素组(P<0.05),佐证了其对减轻炎症反应的作用。本次观察组并发症率明显低于对照组(4.17% vs 16.67%)(P<0.05),则提示低位水囊干预能降低并发症风险。康清华等[18]研究中,低位水囊干预组并发症率为3.70%,较缩宫素组的16.98%明显更低(P<0.05),也可见低位水囊干预能降低并发症发生率。
综上所述,对孕足月产妇采用低位水囊引产联合静滴缩宫素方案能促进宫颈成熟,可提高自然分娩率,能推进产程,降低产后出血量,可减轻产后炎症反应,并能降低并发症风险,值得推广。
