乳化剂和共乳化剂组成对亚麻籽油纳米乳液氧化稳定性的影响
2023-09-13田奕彤李银汇冯思敏
田奕彤,李银汇,冯思敏
(浙江工业大学食品科学与工程学院,浙江 杭州 310014)
亚麻籽油富含ω-3多不饱和脂肪酸,特别是α-亚麻酸。亚麻籽油可通过细胞-细胞相互作用、细胞信号等预防和治疗糖尿病、心血管疾病、神经系统性疾病等[1]。因此,亚麻籽油的研究受到越来越多的关注。然而,ω-3多不饱和脂肪酸非常容易氧化产生脂质氢过氧化物。亚麻籽油的高氧化敏感性极大地限制了其在食品工业中的应用[2]。通过将亚麻籽油包封在不同形式的包封系统中,可以有效提高其生物利用度,减少其难闻的气味[3]。
选择适合的乳化剂和共乳化剂对于包埋体系的建立至关重要[4],因为它们会影响乳液包埋率和物化特性[5]。乳化剂的性质通常包括乳化性、成膜性、溶解性、黏度及抗氧化性等,但任何一种乳化剂都不能同时具有这些良好的性质,因此需要对多种乳化剂和共乳化剂进行复配使用。研究表明,变性淀粉和蛋白质具有较优的乳化性和成膜性,可用于制备纳米乳液,包封多不饱和脂肪酸[6],从而提高不饱和脂肪酸的氧化稳定性。然而另外一部分研究表明,纳米乳液的高通透性和小颗粒效应,反而会加速被包埋脂质的氧化。乳液的氧化稳定性与其界面属性、油滴分散特性和乳化剂的选择休戚相关[7]。最新研究表明,天然蛋白可以作为共乳化剂吸附在乳液界面表面,形成一层保护层,从而提高乳液的氧化稳定性[8]。例如,与单壁材料相比,大豆分离蛋白(soy protein isolate,SPI)-壳聚糖复合壁材料显著提高了藻类油微胶囊的包埋率和氧化稳定性[9]。
辛烯基琥珀酸淀粉酯(sodium starch octenyl succinate,SSOS)是一种常见的酯化变性淀粉,具有两亲性,常被当作乳化、增稠剂使用。其乳化剂机理与小分子乳化剂不同,乳液的稳定性主要受空间位阻影响,通过空间位阻防止分散液滴的聚结以保持乳状液的稳定[10]。SSOS虽具有乳化能力强、包埋效率高的特点,但制备的乳液氧化稳定性不够理想,需要与其他物质复配来降低氧气的渗透性[6]。SPI也具有两亲性,可吸附在油滴表面保持稳定[11],在水溶液中SPI可以形成含有亲水外层和疏水中心的球状结构[12],其疏水性中心富含疏水性氨基酸残基,具有与疏水性物质结合的潜在能力,在食品工业中被广泛应用于稳定纳米乳液中。将SPI加入SSOS溶液后,SPI可以和SSOS相互作用,形成聚合物层,可阻隔氧气通过空间位阻提高乳液氧化稳定性。
本研究旨在探索SSOS和SPI作为乳化剂和共乳化剂包埋亚麻籽油,并对纳米乳液的最佳工艺进行探究,讨论乳化剂组成对亚麻籽油氧化稳定性的影响规律。通过离心稳定常数测定、场发射扫描电子显微镜(field emission scanning electron microscopy,FESEM)、差示扫描量热(differential scanning calorimetry,DSC)法、傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)分析和乳液加速氧化分析等物理化学方法,比较不同共乳化剂比率对纳米乳液粒径、包埋率和氧化稳定性的影响。
1 材料与方法
1.1 材料与试剂
亚麻籽油 江苏知了生物科技有限公司。
SPI 山东嘉华保健品股份有限公司;1,1,3,3-四乙氧基丙烷(97%)上海阿拉丁生化科技股份有限公司;硫代巴比妥酸(生化试剂)中国医药(集团)上海化学试剂公司;SSOS(取代度≤0.02)杭州瑞霖化工有限公司。其他化学品均为分析纯。
1.2 仪器与设备
FS-1200pv超声波处理器 上海生析超声仪器有限公司;85-1磁力搅拌仪器 杭州大卫科教仪器有限公司;Omni动态光散射粒径分析仪 美国Brookhaven科技有限公司;OCA50AP接触角测定仪 德国Dataphysics仪器股份有限公司;BTP-3XL冷冻干燥仪 美国Spectronics公司;T18DS25高速剪切机 德国IKA公司;AF-103AS制冰机 杭州福力德机电器材经营服务部;DHG-9140A电热鼓风干燥箱 上海一恒科学仪器有限公司;Nicolet iS50傅里叶变换红外光谱仪 美国赛默飞世尔公司;RE-2000A真空旋转蒸发仪 上海研承仪器有限公司;HWCL-3集热式恒温磁力搅拌浴 郑州长城科工贸有限公司;ME204E电子天平 美国Mettler Toledo公司;TU-1900紫外-可见分光光度计 北京普析通用仪器有限责任公司;TGL-16台式高速冷冻离心机 湖南湘仪实验室仪器开发有限公司;Q20差示扫描量热仪 美国TA仪器公司;SU8010冷场发射扫描电子显微镜 日本日立建机株式会社;FS-1200 pv超声处理器 上海生析超声仪器有限公司。
1.3 方法
1.3.1 纳米乳液的制备
SSOS的质量分数为1.25%,溶液于45 ℃水浴中搅拌4 h,冷却后静置过夜。根据一定的芯壁质量比(2∶1、1∶1.5、1∶3、1∶5)称取亚麻籽油,搅拌时将亚麻籽油(3、1、0.5、0.3 g)滴入120 mL乳化剂相中。纳米乳液采用超声处理器,超声功率为400~1000 W,处理时间为10~25 min,连续或1、4、8 s脉冲模式,超声操作均在冰浴条件下完成。对于不含SPI共乳化剂的纳米乳液(NS为SPI∶SSOS=0∶1,m/m),将1.5 g SSOS加入120 mL水中,作为乳化剂相。对于高SPI共乳化剂含量的纳米乳液(HS为SPI∶SSOS=2∶1,m/m),1 g SPI和0.5 g SSOS加入120 mL水中作为乳化剂相,对于低SPI共乳化剂含量的纳米乳液(LS为SPI∶SSOS=1∶2,m/m),120 mL水中加入0.5 g SPI和1 g SSOS作为乳化剂相。采用叠氮化钠(0.02 g/100 mL)作为抗菌剂。将每组纳米乳液转移到一个玻璃瓶中,在室温(25 ℃)下放置,通过记录第1、12、24 小时,第7、45天的乳液分层确定其贮存稳定性。在制备过程中,所有容器均使用铝箔包裹,进行避光处理,以此避免亚麻籽油的损失。
1.3.2 离心稳定性常数(Ke)
采用离心光谱法[13]测定。用移液管吸取刚制备好的乳液0.5 mL,用去离子水稀释100 倍,在4000 r/min条件下离心15 min,用注射器在底部取样,用紫外分光光度计分别对该样品和离心前的稀释样品于500 nm波长处测定吸光度(A500nm),每个样品设置3 个平行组。稳定性用Ke表示,Ke按式(1)计算:
式中:A0为离心前乳液的吸光度;A为离心后乳液的吸光度。
1.3.3 包埋率
将1.3.1节中制得的乳液进行冷冻干燥处理,制成粉末状,具体过程如下:取200 mL乳液样品,倒入培养皿中,高度不超过培养皿高度的一半,将培养皿用保鲜膜封好,在-80 ℃的冰箱中冷冻数小时,至完全冻结。冷冻结束后,将培养皿取出并放入冷冻干燥机中,扎好适量小孔后干燥。
将25 mL己烷与1 g冻干粉末混匀,并振荡30 s,然后5000 r/min离心10 min,上清液通过滤纸过滤,并将粉末残余物用己烷冲洗2 次。然后将滤液置于60 ℃的旋转蒸发器中15 min,然后在105 ℃下干燥无溶剂的萃取物,直至恒质量,剩余物即为未包埋的亚麻籽油,称量其质量,则包埋率为剩余物质量与1 g冻干粉中含有的总亚麻籽油质量的比值。包埋率按式(2)计算:
式中:TO为纳米乳液制备过程中添加的亚麻籽油的质量/g;SO为未封装的亚麻籽油的质量/g。
1.3.4 纳米乳液的表征
1.3.4.1 乳液粒径测定
吸取适量纳米乳液溶液,利用动态光散射粒径分析仪在DLS Particle Sizing Measurement模式下测定乳液粒径和分散度,入射角度为90°,光子相关器选择常规,温度为25 ℃,平衡时间为10 min,单次测定时间为2~3 min,溶剂选项为水。重复测定3 次。
1.3.4.2 Zeta电位测定
吸取适量纳米乳液溶液,利用动态光散射粒径分析仪在PALS Zeta Potential Measurement模式下测定乳液Zeta电位,重复测定3 次,结合粒径和电位数据,选择最佳原料添加比及超声制备工艺。
1.3.4.3 FESEM分析
使用FESEM表征混合乳化剂制备的纳米乳液中颗粒形态。在FESEM载物盘上固定单晶硅片,吸取适量纳米乳液滴在硅片上,自然风干后喷金处理,放入电镜观察室进行观察。
1.3.4.4 DSC分析
采用Q20 DSC仪,在铝制坩埚中称取约5~10 mg样品,利用冲压池对其进行密封,放入量热池。设定升温程序后,进行测定。操作参数:升温范围为25~250 ℃;升温速率为10 ℃/min;氮气流量为50 mL/min。
1.3.4.5 FTIR
利用KBr压片法对试样的官能团进行表征。取干燥的溴化钾和质量为溴化钾百分之一的固体待测样品于玛瑙钵中混合均匀,充分磨细,压成薄片(直径13 mm,厚度约1 mm的透明玻片)。若待测样为液体,则取少量溴化钾研磨并压成薄片后,在表面均匀滴上1 滴待测样品进行测定。光谱范围选择4000~600 cm-1,分辨率选择4 cm-1下扫描32 次。
1.3.4.6 混合乳化剂空气-水界面接触角特性
空气-水界面的接触角在OCA50AF接触角计数据物理仪器上测定,评价乳化剂和共乳化剂混合材料的两亲性。取适量的SSOS和SPI,溶解于水中,干燥后,将适量的样品压入晶片中,黏附在载玻片上。然后通过电注射系统滴下3 μm的水滴,用CDD相机拍摄接触角图像。每个样品在几个不同的位置平均重复测定10 次。
1.3.5 乳液加速氧化分析
采用Schaal烘箱法加速氧化实验进行乳液加速氧化分析,在加速氧化贮存条件下测试不同亚麻籽油纳米乳液(记为NS、HS、LS)的氧化稳定性,并与散装油进行对比。其中,散装油样品的制备按最佳芯壁比称取油的质量,加入到100 mL去离子水中并搅拌均匀,超声处理后静置。分别取100 mL纳米乳液(NS、HS、LS)以及散装油样品,放入密封的深色瓶中6 d,并在通风烘箱中于65 ℃温育,根据Arrhenius经验公式,烘箱法的1 d相当于常温条件下贮藏1 个月[14]。在温育0、1、3 d和6 d后取样(其中散装油样品振动混匀超声后取样),并测定氧化参数,所有实验一式3 份进行[15]。
1.3.5.1 过氧化值(peroxide value,PV)的测定
根据Fioramonti等[16]的方法进行测定。取乳液样品或亚麻籽油样品300 μL,与1.5 mL异辛烷-异丙醇溶液(3∶2,V/V)混合,得到最终体积为1.80 mL。将混合物涡旋3 次,每次持续10 s,并3400×g离心5 min。取200 μL离心后的上层有机相加入到2.8 mL氯仿-甲醇(7∶3,V/V)溶液中,接着加入15 μL硫氰酸铵溶液(3.94 mol/L)和15 μL Fe2+溶液(0.072 mol/L,1.5 mL 144 mol/L FeSO4和1.5 mL 0.132 mol/L BaCl2溶液在0.4 mol/L盐酸中混合后的上清液中得到),涡旋振荡4 s并在室温下避光静置20 min,然后使用紫外分光光度计在500 nm波长处测定样品的吸光度。用Fe3+标准曲线确定脂质氢过氧化物浓度。PV表示为每千克样品中过氧化物的毫克当量,按式(3)计算:
式中:AS为样品的吸光度;ASB为空白样的吸光度;ARB为空白试剂的吸光度;m为从校准曲线获得的斜率;m0为亚麻籽油的质量/g;55.84为铁的相对原子质量;2为过氧化物值所必需的分裂因子;4.5相当于与异辛烷有机相相关的稀释因子的倒数(0.9/0.2)。
1.3.5.2 硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值的测定
参考Fioramonti等[16]的方法进行修改测定。将0.1 mL乳液与0.9 mL水和2 mL TBA试剂(15 g三氯乙酸+375 mg硫代巴比妥酸+1.76 mL浓盐酸+82.9 mL去离子水,50 ℃保持30 min,冷却10 min)在试管中混合,并置于沸水浴中15 min。将管冷却至室温10 min,然后离心(12000 r/min,15 min),收集上清液,用紫外-可见分光光度计测定波长532 nm处的吸光度。根据1,1,3,3-四乙氧基丙烷制成的标准曲线测定样品中丙二醛的含量。
1.4 数据处理
2 结果与分析
2.1 不同制备条件对SSOS包封纳米乳液表征的影响
如图1所示,随着超声功率的增大,纳米乳液的Ke值在400~800 W之间有下降趋势,但数值变化不大,当超声功率800 W以上时,Ke值显著增大(图1A)。这是由于乳液颗粒的大小与输入的能量有关。在较高的超声能量下处理纳米乳液可以更有效地分解液滴。然而,超声处理的持续增加会导致乳液聚集加速,这被称为“过度处理”[17]。图1B显示,Ke值随着SSOS的增加而减小。然而,在食品工业中并不推荐使用高比例的表面活性剂。以1∶1.5芯壁比制备的纳米乳液在保存45 d后没有明显的分层(如乳液静置图所示),图1C显示随着加工时间的延长,Ke值变化很小。同时脉冲模式对Ke值的影响很小(图1D)。因此,超声制备纳米乳液的最佳条件为超声功率600 W、芯壁比1∶1.5、脉冲模式8 s、加工时间20 min。
2.2 共乳化剂SPI对纳米乳液表征的影响
如表1所示,随着SPI的比例从0%增加到33.3%,平均粒径从(218.1±3.9)nm显著增加到(244.0±3.0)nm,Zeta 电位从(-38.2±0.3)mV 显著降低到(-67.2±3.0)mV。当Zeta电位的绝对值大于30 mV时,认为系统相对稳定;绝对值越大,系统就越稳定[17]。随着在pH 7环境加入SPI,此时SPI和SSOS均带负电荷,两者通过两亲性吸附在油水界面,而高静电排斥力可以防止乳液滴之间的聚集[18-19]。
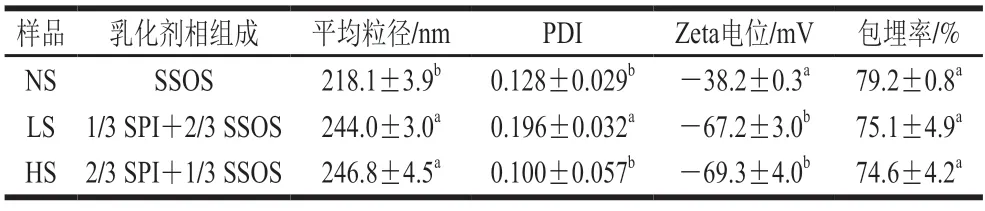
表1 共乳化剂SPI对纳米乳液的参数影响Table 1 Effect of SPI as co-emulsifier of properties of nanoemulsion
SPI和SSOS结合形成的界面导致了较大的粒径。然而,当SPI从1/3(LS)增加到2/3(HS)时,平均粒径和Zeta电位没有显著变化。这是因为芯壁比控制在1∶1.5。随着SPI比例的增加,PDI首先从0.128±0.029增加到0.196±0.032,然后显著下降到0.100±0.057。SPI与SSOS之间的静电斥力导致了PDI的增加。随着更多的SPI吸附在纳米乳液界面,可能会形成致密的蛋白层,然后与SSOS达到平衡。PDI为多分散性指数,PDI越小,纳米乳液的粒径分布越窄、越集中。PDI小于0.20,说明纳米乳液的粒径分布相对集中[20]。表1还显示,3 个样本的包埋率均在(74.6±4.2)%~(79.2±0.8)%左右,无显著性差异。与扁豆蛋白(最高包埋率为62.8%)[21]或乳清分离蛋白、海藻酸钠和麦芽糊精组合[22](最高包埋率为63.70%)纳米乳液相比,包埋率相对较高。结果表明,以SSOS为乳化剂SPI为共乳化剂的纳米乳液能较好地包埋亚麻籽油。
2.3 纳米乳液冻干粉末的性质表征
如图2A所示,三者的宏观外观没有明显差异,均呈现乳白色。3 种纳米乳液的扫描电镜分析如图2B所示,纳米乳液的粒径约为250 nm,而NS的粒径略小于LS、HS。此外,LS(图2B2)和HS(图2B3)之间的粒径没有显著差异,这也与表1结果一致。
2.4 DSC分析
如图3所示,SSOS曲线显示出2 个主要的吸收峰,峰值温度(Tp)分别为148.91 ℃(峰1)和178.59 ℃(峰2)(表2)。峰值1可能是SSOS中水分蒸发形成的脱水峰值[23]。峰的脱水温度高于100 ℃,这是由于SSOS分子与水分子之间的氢键等结合力造成。峰2为SSOS的熔化吸热峰。在NS样品中,只观察到熔化的吸热峰(Tp=154.73 ℃)。NS样品的焓值(25.09 J/g)低于SSOS样品的焓值(33.90 J/g)(表2)。在HS和LS样品中,特征峰分别改变为124.21 ℃和142.05 ℃,焓值分别降低到23.54 J/g和25.57 J/g。SPI和SSOS都有明显的主吸收峰,但是在HS和LS样品中,两者的特征峰被完全抑制(图3),这说明乳液的包埋效果良好[24]。纳米颗粒具有良好的热力学稳定性,升温过程对颗粒的破坏性较小。
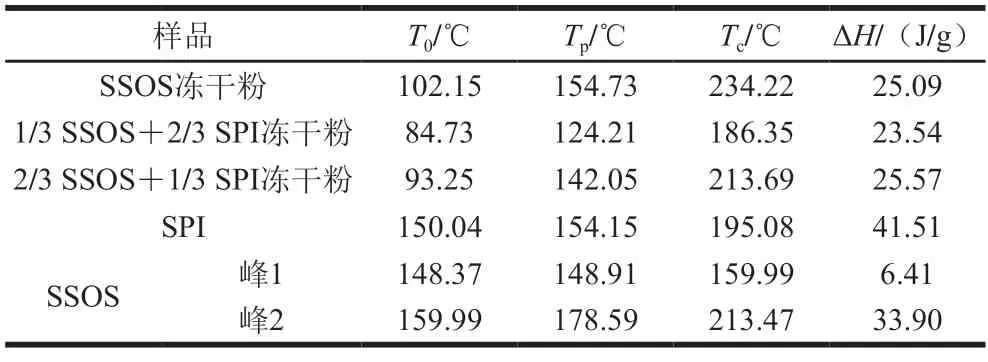
表2 DSC测定的热力学参数Table 2 Thermodynamic parameters determined by DSC
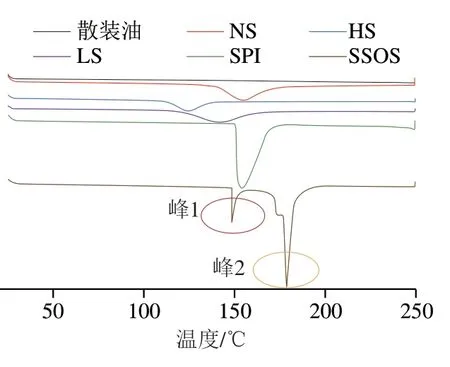
图3 DSC分析Fig.3 DSC analysis
2.5 FTIR分析
如图4所示,在3000~3700 cm-1处的宽衍射峰与羟基有关[25]。对应水分子羟基基团的对称和反对称伸缩振动峰,说明通过冷冻干燥制备的粉体中残留有水分子(或羟基基团),而亚麻籽油在3000 cm-1以上没有明显的吸收峰,这是典型的脂肪酸酯结构。1024 cm-1处为SSOS的特征峰,其透过率的响应值符合3 种粉体中所含SSOS比例的增减规律。SPI在1657 cm-1和1535 cm-1处吸收峰与酰胺和酰胺II有关,这是蛋白质的特征峰[26]。与SPI相比,纳米颗粒的酰胺和酰胺II(1650、1547 cm-1)的振动强度略有变化,表明SSOS、SPI和亚麻籽油之间存在相互作用。3009 cm-1吸收峰与亚麻籽油的双键有关[27],1750 cm-1处为酯基存在的证明[28],此处亚麻籽油的吸收峰最大,其余3 个样品的响应值均小于亚麻籽油的峰,说明乳液的包埋效果良好;3010 cm-1处和710 cm-1处的吸收峰与双键有关,特别是710 cm-1处可以观察到3 种粉末样品吸收峰明显小于亚麻籽油的吸收峰,说明乳液的包埋效果良好。
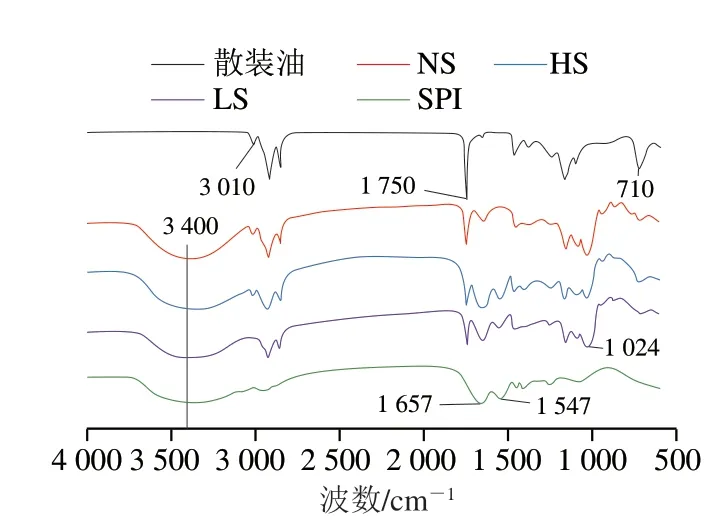
图4 FTIR分析Fig.4 FTIR analysis
2.6 纳米乳液的氧化稳定性
脂质氧化会影响产品的保质期,损害产品的质量。氧化反应一旦发生,它就会产生自由基并在链式反应中传播[29]。为了研究亚麻籽油在纳米乳液中的氧化稳定性,本研究分别用PV和TBARS值表征初级和次级氧化产物的生成量。
从图5A可以看出,NS和HS的初始氧化状态的PV((0.29±0.04)mg/kg和(0.12±0.01)mg/kg)明显高于散装油样品。据推测,是因为超声处理过程中发生了氧浸润,并促进了脂质氧化。超声乳化的作用机制是空化机制,空化过程中产生的空化泡崩溃时会产生局部高温和高压,这可能会加速体系的氧化反应,从而导致纳米乳液的PV更高。如图5A所示,NS的PV波动最剧烈,在加速氧化过程的第3天达到峰值((7.72±0.47)mg/kg),远高于散装油样品的PV((1.68±0.03)mg/kg)。说明单一乳化剂的纳米乳液反而促进了氧化,油乳液中脂质氧化通常比散装油更早、更快,因为界面区域促进了油与氧气的接触。在纳米乳液中单位界面面积较大,增加了油相对水相中溶解氧的可及性,从而促进了氧化[30]。在加速氧化过程中,HS的PV明显低于散装油(第1~3天)。LS的PV((1.30±0.03)mg/kg)在第1天显著低于散装油((1.99±0.05)mg/kg),但在第3天无显著差异。这些现象表明,SSOS作为单一乳化剂可以促进纳米乳液的氧化,而SPI作为共乳化剂的加入可以剂量依赖性地增加纳米乳液的氧化稳定性。除HS外,其他纳米乳液的PV随氧化时间的延长而先增加然后减小。PV的降低可能是由于初级氧化产物(氢过氧化物)的不稳定性和进一步的氧化[16]形成次级氧化产物造成。随着共乳化剂SPI的加入,氧化作用的减少可能归因于防止亚麻籽油获取氧自由基。在油水界面添加了SPI后,乳液的PV和TBARS值均有明显下降,推测为SPI和SSOS产生了某种相互作用并形成了复合界面。单一乳化剂时,纳米乳液由于比表面积较大,增加了亚麻油与油水界面氧气接触的机会,促进了氧化。而加入SPI后,SPI通过氢键等非共价键作用力与SSOS形成共聚物水化膜,降低了氧气透过性,抑制了亚麻油与水的接触,从而减缓氧化[31];此外聚合物层降低了油-水界面处的界面张力,从而抑制液滴聚集,防止亚麻籽油渗出乳液体系,起到稳定乳液的作用。
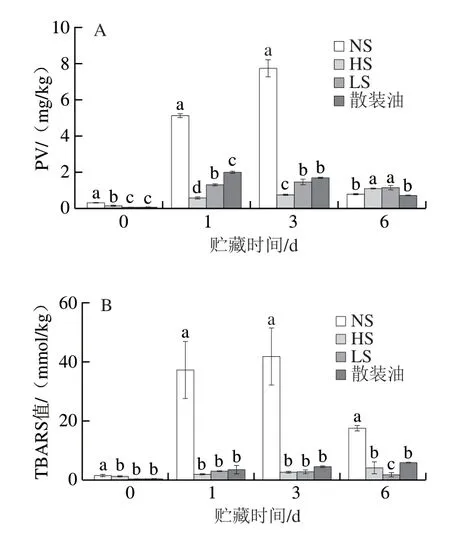
图5 不同共乳化剂比率对PV(A)和TBARS值(B)的影响Fig.5 Effects of co-emulsifier concentration on PV (A) and TBARS values (B)
与PV相似,NS和LS的TBARS值随着氧化时间的延长而先增加,然后减小(图5B)。而HS组和散装油组的TBARS值则不断增加。NS的TBARS值波动最为明显,在第3天达到峰值((41.84±9.62)mmol/kg),远高于同一天的散装油样品((4.43±0.41)mmol/kg)。这也表明,用SSOS封装的纳米乳液具有促进氧化的作用。在次级氧化产物的生成阶段,HS和LS的TBARS值均低于NS。HS((4.03±2.08)mmol/kg)和LS((2.98±0.24)mmol/kg)的最高TBARS值均低于散装油的最高TBARS值((5.70±0.14)mmol/kg)。TBARS的结果表明,加入SPI可以减缓氧化速率,这与PV的结果一致。
2.7 混合乳化剂在气-水界面接触角
研究确定了不同比率乳化剂和共乳化剂在气-水界面上的接触角。SSOS接触角在70.30°~71.59°之间(图6A),而SPI接触角在92.6°~94.8°之间(图6B),表明SPI的疏水性优于SSOS,两者均可作为乳液稳定剂。通过改变SSOS与SPI的比值,可以调整混合乳化剂的接触角。随着SPI的增加,混合乳化剂的接触角分别从70°~72°增加到79.7°~80.0°和83.8°~86.4°。随着SPI的加入,SPI通过氢键等非共价键作用力吸附在SSOS表面形成水化膜,随着混合乳化剂的疏水性增加,有效阻止了氧自由基从水相环境向乳液内部的传质递送[32],从而防止了氧自由基与亚麻籽油的接触,从而大大提高了油的氧化稳定性。
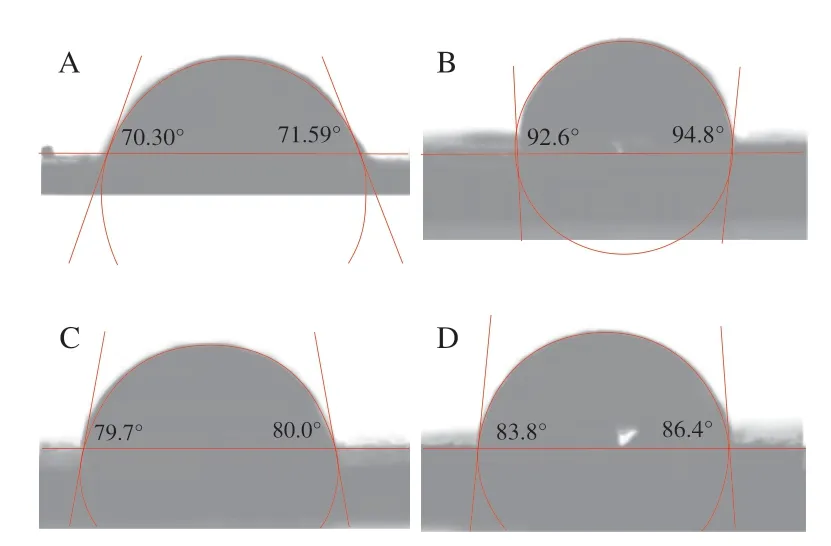
图6 静态水接触角Fig.6 Static water contact angle
3 结论
以SSOS为乳化剂,SPI为共乳化剂,采用超声乳化法制备了亚麻籽油纳米乳液。超声功率、芯壁比、处理时间对纳米乳液的分布都有影响,最佳条件为超声功率600 W、芯壁比1∶1.5、脉冲模式8 s、处理时间20 min。扫描电镜、DSC和FTIR分析结果表明,亚麻籽油包埋效果良好。随着SPI的加入,纳米乳液的氧化稳定性大大提高。这是因为随着SPI的加入,混合乳化剂的疏水性增加,防止了亚麻籽油接触氧自由基,从而提高了亚麻籽油在纳米乳液中的氧化稳定性。本研究为提高亚麻籽油的水溶性和氧化稳定性提供了一条新的途径。延长了亚麻籽油货架期,促进亚麻籽油工业化开发和其他应用领域拓展。
