改良部分性脾动脉栓塞术治疗经颈静脉肝内门体分流术后肝性脑病的临床研究
2023-09-09黄祥忠
高 峰, 黄祥忠
(东南大学医学院附属江阴医院 介入科, 江苏 江阴, 214400)
肝性脑病(HE)是经颈静脉肝内门体分流(TIPS)的常见并发症之一[1-2], 增加了患者死亡风险[3], 导致住院时间延长及治疗费用增加[4]。门体分流引起血氨升高是造成TIPS术后HE的重要原因[5]。部分性脾动脉栓塞术(PSE)可以减少脾静脉入门静脉血流量,门体分流道血流量自然也随之下降,进而起到限流作用。但传统PSE选择颗粒栓塞剂,栓塞后往往脾梗死明显,术后症状较严重。本研究采用不良反应较轻的改良部分性PSE(MPSE)治疗TIPS术后HE患者,初步结果满意,现报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2021年1月—2022年2月东南大学医学院附属江阴医院采用MPSE治疗的10例TIPS术后HE患者的临床资料,男6例,女4例,年龄47~78岁,中位年龄65岁。肝硬化病因为慢性乙型肝炎7例,药物性1例,血吸虫性1例,不明原因1例。HE分级采用West Haven分级标准,其中1级4例,2级1例, 3级4例, 4级1例。患者一般情况见表1。患者入组均接受TIPS手术,符合《肝硬化肝性脑病诊疗指南》[6]中HE的诊断标准。排除疾病终末期和脾动脉栓塞后发生脾脓肿的高危脓毒血症患者和严重肝、肾功能损害患者。本研究获得医院医学伦理委员会批准,所有患者治疗前签署知情同意书。

表1 患者一般情况比较
1.2 治疗方法
常规消毒铺巾,局部麻醉,采用改良Seldinger法穿刺股动脉,置入5F导管鞘(泰尔茂,日本),经鞘管送入5F RH导管(埃普特,中国),插管至腹腔动脉造影,了解脾动脉走形特征。进一步将导管超选至脾动脉造影,了解脾脏大小及血管解剖。10例患者均进一步使用2.4F微导管(波科,美国)超选择至脾动脉一级分支以减少并发症,栓塞材料选择Interlock可解脱带纤毛弹簧圈或联合微弹簧圈(波科,美国),采用脾动脉分支血管直径比值法计算脾脏栓塞体积[7], 即脾脏栓塞体积百分比(%)=SA1b直径/(SA1a直径+SA1b直径) ×100%, 其中SA1a、SA1b为脾动脉一级分支血管且SA1b为栓塞靶血管,栓塞范围应控制在30%~40%, 栓塞终点为减慢血流为宜。
1.3 观察指标
通过比较MPSE治疗前及治疗后3、6个月的多普勒超声,从门静脉主干血流速度、分流道血流速度,多方面评价MPSE对TIPS术后发生HE的患者血流动力学影响; 通过比较MPSE治疗前及治疗后3、6个月肝功能变化情况,评价MPSE对TIPS术后发生HE患者肝功能的影响; 记录术后1周HE症状,术后3、6个月 HE发作情况; 观察术后并发症发生情况,包括腹痛、发热、脾脓肿、肺部感染等。
1.4 统计学分析

2 结 果
2.1 手术情况
10例患者均成功完成MPSE, 造影提示脾肿大,脾动脉明显增粗、扭曲。2例患者仅使用Interlock可解脱带纤毛弹簧圈,8例联合微弹簧圈进行栓塞。栓塞脾动脉一级分支包括上极分支(1例)、中极分支(3例)、下极分支(6例),栓塞终点均为血流减慢,栓塞部分血供减少。
2.2 术后不良反应发生情况
术后1周HE症状消失9例,1例患者West Haven分级由3级降至1级,经药物治疗后疾病得到控制,但患者术后6个月内仍发作HE 2次,MPSE术前CT提示门静脉主干、门静脉右支、肠系膜上静脉、脾静脉广泛血栓形成,且门静脉主干明显增粗。术后仅1例患者出现左侧腹部轻度隐痛,使用塞来昔布镇痛,症状逐渐消失,患者均未出现发热、脾脓肿、肺部感染等并发症,随访6个月均未出现脾梗死,8例患者出现了不同程度的栓塞部位脾脏萎缩。
2.3 术前与术后肝功能、门静脉血流及分流道血流比较
MPSE术后3、6个月,患者ALT、AST、TBIL及ALB水平与术前比较,差异均无统计学意义(P>0.05); MPSE术后3、6个月,门静脉主干血流速度与术前比较,差异无统计学意义(P>0.05); MPSE术后3、6个月,分流道血流速度与术前比较,差异均有统计学意义(P<0.05)。见表2。
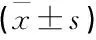
表2 MPSE术前与术后3、6个月肝功能指标及门静脉主干、分流道血流比较
3 讨 论
近年来,TIPS已成为食管胃静脉曲张破裂出血、顽固性腹腔积液等门静脉高压并发症的重要治疗方法[8-9], 主要通过在体静脉与门静脉之间置入支架达到“分流”的作用,从而有效降低门静脉压力,避免再次出血或积液复现等,同时栓塞曲张的胃食管静脉,达到内镜下套扎、硬化剂注射或外科断流术的效果。肝移植目前仍是治疗门静脉高压并发症的首选方法,随着技术的不断进步, TIPS不仅延长了非肝移植患者的生存时间,也大大降低了相关并发症发生率[10-11], 然而, TIPS术后HE仍有很高的发生率[12], 严重制约了TIPS术的临床应用,影响了患者的预后及生存质量。
氨代谢紊乱是门体分流性HE重要的发病机制,氨通过门静脉进入肝脏,健康的肝脏通过对氨进行处理避免其进入体循环, TIPS术后部分氨经分流道直接进入体循环,导致血氨升高,游离的氨可以通过血脑屏障导致脑功能障碍,引起HE[13]。另外,门静脉是肝脏的主要供血来源,门体分流后,肝内门静脉血流量减少,进而损伤肝功能,肝脏对氨的处理能力随之下降,导致血氨升高[5]。针对TIPS术后HE的保守治疗主要包括饮食控制和药物治疗,但这些措施并不能从根源上解决因TIPS术导致的HE。研究[14-15]表明,门静脉左支主要收集来自脾静脉的血液,血氨浓度较门静脉右支低, TIPS术中穿刺门静脉左支进行分流,术后发生HE风险更低。但此类研究报道偏少,仍需多中心大样本的研究进一步证实。分流道限流[16-19]可以控制HE的发生,主要采用在分流道中置入支架的方法减小分流道直径,但是操作费用昂贵,而且支架刺激所致的内膜增生或血栓形成可能引起分流道的闭塞。有研究[20]采用弹簧圈和可脱球囊永久性闭塞分流道,可从根源上控制TIPS术后发生HE, 但是可导致食管胃底静脉曲张、顽固性腹腔积液等门脉高压并发症的再次发生,严重者甚至危及患者生命。
传统PSE主要应用于脾功能亢进的治疗,通常选用明胶海绵、聚乙烯醇等颗粒栓塞脾动脉下极分支,这种颗粒栓塞可导致栓塞脾脏实质发生彻底坏死,从而有效缓解脾功能亢进。虽然栓塞脾动脉下极分支可减少该术式的术后并发症,但术后发热、腹痛的发生率仍较高,且症状持续时间较长,严重者术后会出现脾脓肿、自发性细菌性腹膜炎等严重并发症[21]。MPSE则选择弹簧圈栓塞脾动脉主干或分支,通过减少脾脏血供导致脾脏萎缩变小,进而缓解脾功能亢进,很少导致脾脏实质性坏死,大大减少腹痛、发热、脾脓肿等并发症。但栓塞脾动脉主干后脾动脉远端可能因胃动脉吻合供血再次出现脾肿大及盗血,影响远期疗效,且无法再次行脾动脉栓塞。因此,本研究主要采用弹簧圈栓塞脾动脉分支,不仅提高了手术的可重复性,而且术后不良反应轻。
PSE后脾静脉回流门静脉血流量降低,致门静脉压力下降,进一步导致TIPS分流量降低,减少了经分流道进入体循环氨的量,降低血氨水平,从而解决因分流量过大导致的HE。本研究显示, MPSE可降低分流道血流速度,说明具有一定的限流作用。但是仍有1例患者术后HE未能得到控制,分流道血流速度没有明显降低,该患者因门静脉系统多发血栓形成行TIPS术, CT检查提示门静脉主干明显增粗, TIPS术中分流前门静脉压力31.6 mmHg, 分流后27.9 mmHg, 因此患者HE未能改善与门静脉压力过高有关。脾脏的淤血肿大是肝硬化门脉高压常见并发症, TIPS术患者多存在肝硬化,增粗的脾动脉和肝动脉“竞争”血流,导致肝动脉灌注不良,进一步损害肝功能。本研究结果显示, MPSE并未有效改善肝功能,可能与研究样本量小、仅行脾动脉分支栓塞和术前肝功能仅轻度异常有关。因此,该研究所采取的术式并不能通过改善肝功能控制TIPS术后HE。
综上所述, MPSE可有效控制因TIPS术所致的HE, 分流道限流作用是主要因素,但本研究入组病例较少,期望后续研究能够纳入多中心样本,为临床进一步推广提供有力证据。
