老年患者桥小脑角区脑膜瘤的MRI影像诊断与分析*
2023-08-26宋晨吴燕焦凯剑吴磊
宋晨 ,吴燕,焦凯剑,吴磊
(1.锦州医科大学,辽宁 锦州 121000;2.湖北医药学院附属太和医院 医学影像中心,湖北 十堰 442000)
桥小脑角区脑膜瘤(cerebellopontine angle meningioma,CPAM)是桥小脑角区好发的肿瘤之一,约占桥小脑角区肿瘤的5%~15%[1]。由于解剖位置特殊,生长较缓慢,症状常出现较晚且不明显,且当病灶体积较大时可向内听道生长[2],与其他肿瘤鉴别困难。为提高对老年患者的CPAM病灶磁共振成像特征的认识,本文对34 例经手术病理证实为CPAM 的60 岁以上患者的MRI 影像表现进行回顾性分析,探讨该年龄段的CPAM 的MRI 影像特征及鉴别诊断要点,以提高其诊断正确率。
1 资料与方法
1.1 一般资料
回顾性收集2015 年6 月至2022 年7 月湖北医药学院附属太和医院收治的60 岁以上的桥小脑角区脑膜瘤患者的资料,共34 例,所有患者均已行手术切除并病理确诊。其中男9 例,占26.5%;女25 例,占73.5%。年龄60~87 岁,平均66.37岁。临床表现为头痛、头晕者15 例,颜面部疼痛9 例,单侧听力下降6 例,体检发现4 例。
1.2 检查方法
采用GE Discovery MR750 3.0T 超导磁共振机进行颅脑MRI 检查。磁共振扫描采用头颅线圈先进行轴位及矢状位T1WI、轴位和冠状位T2WI、轴位T2Flair 扫描,然后行增强轴位、冠状位和矢状位T1WI 以及3D Bravo 序列增强扫描。增强扫描使用高压注射器以2.5 mL/s 流率注射0.1 mmol/kg 对比剂Gd-DTPA。
1.3 图像分析
图像纳入标准:完成MR 平扫及增强的各序列扫描,图像质量能够满足诊断需要。排除标准:图像因强化效果差或各种伪影影响诊断的。扫描范围未能包含肿瘤全部的。
由本院影像中心两名副高职称的医师对患者的所有图像进行独立的观察和分析,包括肿瘤的位置、大小、形态、强化特征及与周围组织解剖关系等,如意见不同则由上级主任医师仲裁。
2 结果
2.1 影像表现
肿瘤数量:34 例病变均为单侧单发肿物,其中左侧16 例、右侧18 例。
肿瘤位置:位于内听道前区(Ⅰ型)9 例,占26.5%;位于内听道开口区部分或完全覆盖内听道(Ⅱ型)18 例,占52.9%,其中部分覆盖内听道口7 例(Ⅱa 型),完全覆盖内听道口(Ⅱb 型)11例,Ⅱb 型中肿瘤伸入内听道内8 例,未伸入3例,所有伸入内听道的病例中均未出现内听道扩大;位于内听道后部区域(Ⅲ型)7 例,占20.6%。见表1、表2。
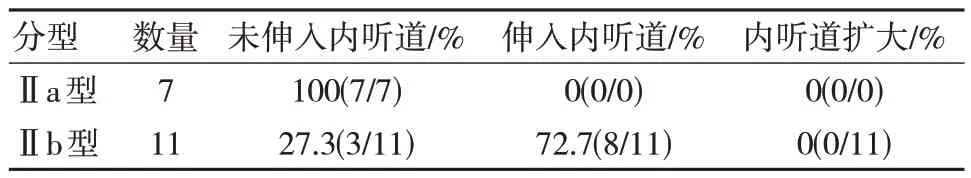
表2 Ⅱ型脑膜瘤与内听道关系
肿瘤大小:肿块最大横截面的最小范围约1.6 cm×0.9 cm,最大范围约5.1 cm×2.1 cm,平均面积约7.5 cm2;其中8 例伸入内听道的肿瘤,伸入深度约0.4~0.8 cm,平均伸入0.6 cm。
肿瘤的形态及信号特征:肿块均宽基底附着于桥小脑角区的硬脑膜,其中32 例形态较规整,呈类圆形或半圆形,占总数的94.1%;2 例肿块形态不规则,呈分叶状,占5.9%;未见呈哑铃形状的肿块。肿瘤大多以实性成分为主,占88.2%(30例),磁共振T1WI 呈等或稍低信号、T2WI 呈等或稍高信号,少部分T2WI 呈稍低信号,T2Flair 呈等或稍高信号。4 例肿块信号不均匀呈囊实性,占11.8%,T2WI 和T2Flair 表现为混杂信号。增强后26 例明显均匀强化,占76.5%;余8 例强化不均匀,占23.5%,其中4 例囊实性病灶呈显著的不均匀强化,其囊性成分不强化。在所有病例中,出现脑膜尾征21 例,占61.8%。见图1、图2。
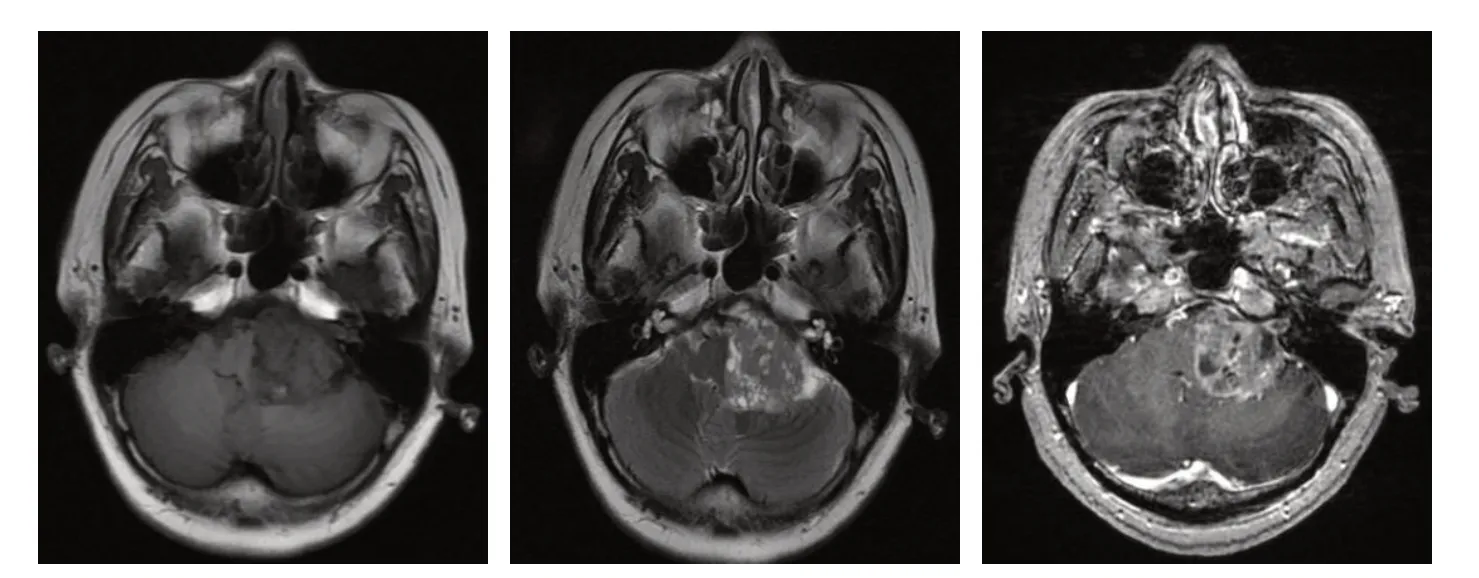
图1 左侧桥小脑角区脑膜瘤(Ⅱb 型)
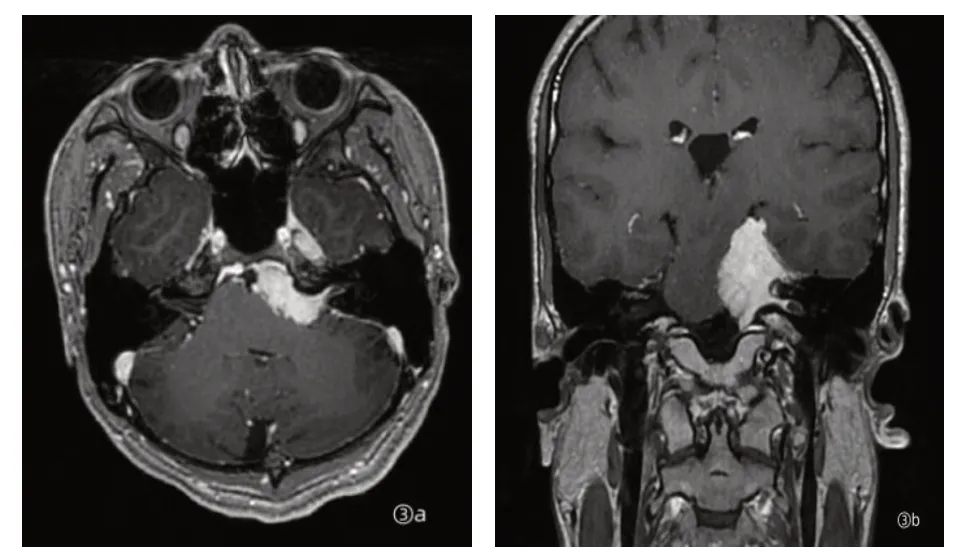
图2 增强后左侧桥小脑角区脑膜瘤(Ⅱb 型)
周边其它征象:三叉神经受挤压向外上方移位4 例,均为Ⅰ型CPAM。灶周水肿8 例,邻近小脑及脑干可见明显受压。所有肿块均导致患侧桥小脑角池扩大,而所有位于内听道后区的Ⅲ型CPAM 均未出现颈静脉孔的扩大。
2.2 病理类型
所有病理确诊的脑膜瘤中世界卫生组织(WHO)Ⅰ级共32 例,Ⅱ级2 例;病理分型中上皮型11 例、过渡型6 例、分泌型5 例、纤维型5例、透明细胞型2 例,血管型2 例,砂砾体型2例、微囊型1 例。
3 讨论
脑膜瘤多起源于蛛网膜帽状细胞[3]。CPAM 多位于颞骨岩部内听道口周围,好发中老年女性,本研究女性患者25 例,约占73.5%。本研究入组的是60 岁以上的老年人,平均年龄66.37 岁,肿瘤生长时间较长,所以瘤体多较大,平均最大截面积约7.5 cm2,大于全年龄段的平均值[2],且压迫周围神经及组织出现症状的病例较多,无临床症状而被体检发现的较少。较大病灶累及面听神经时患者可出现听力下降、颜面部疼痛等临床表现,当肿瘤累及三叉神经时可表现为面瘫,未侵犯周围组织时,则仅为头痛或无症状。WHO 中枢神经系统肿瘤分类将脑膜瘤分为3 级共15 种亚型,而大部分(约90%)的脑膜瘤为低级别的WHO Ⅰ级[4]。
CPAM 影像特征与其他部位的脑膜瘤相似,肿块常宽基底、形态规整,本研究中94.1% 的CPAM 呈较光整的形态。CPAM 在MRI 平扫T1WI为等或稍低信号,T2WI 等或稍高信号、少数呈稍低信号,这与颅内神经鞘瘤不同,出现混杂信号的囊变、坏死区的概率也大大低于同部位的神经鞘瘤[5]。增强扫描多为明显均匀强化,少数囊实性病灶则呈不均匀强化。均匀强化是由于脑膜瘤的肿瘤细胞排列紧密,较少囊变坏死,而脑膜瘤常血供丰富,且不存在血脑屏障,决定了其明显强化的特征[6]。病理分型的不同也可导致病灶在MRI 中信号特征不同[7],WHO Ⅱ级脑膜瘤出现分叶征和囊变的概率较Ⅰ级稍高,而约一半的纤维型脑膜瘤T2WI 信号与其他类型相反,可呈较低信号。脑膜尾征是诊断脑膜瘤的重要依据之一,但不是决定性证据,在本研究中有61.8%的病例出现,其病理基础可能是肿瘤浸润硬脑膜及脑膜瘤富血管反应共同作用的结果[8]。CPAM 可导致同侧桥小脑角池不同程度的扩张,较大者还可压迫脑干和小脑组织,但因为是脑外肿瘤,所以引起邻近脑组织水肿并不多见[9]。本研究入组患者年龄较大,肿瘤也较大,但也只有8 例出现灶周水肿。
CPAM 的诊断应按照肿瘤与内听道口的相对位置分型并分析,本研究参考已有文献[10]并根据影像表现和手术情况创新性地将其分为Ⅰ型、Ⅱa型、Ⅱb 型和Ⅲ型,其中内听道区的Ⅱa 和Ⅱb 型病变的发生概率最大。
位于内听道前区的Ⅰ型CPAM 主要需与三叉神经鞘瘤鉴别。颅内的神经鞘瘤除T2WI 信号较高、易囊变外,三叉神经鞘瘤通常是哑铃状形态。虽然有研究[10]提示少量的内听道前型脑膜瘤也可呈哑铃状,但本研究未发现此种改变。另外,脑膜瘤多推移三叉神经,而三叉神经瘤多包埋三叉神经,本研究中Ⅰ型CPAM 有4 例三叉神经受压向外上方移位,未发现三叉神经被包埋。Ⅱ型CPAM 主要需与听神经鞘瘤鉴别[11]。除前述的T2WI 信号高低和囊变概率来区分外,肿瘤对内听道的侵犯是最重要的鉴别征象。听神经鞘瘤常起源于听神经内听道段前庭神经支的神经鞘膜[12],肿瘤在内听道内生长,除微型听神经瘤外,长大的肿块极易引起内听道的扩大[13]并通过内听道开口进入桥小脑角区。而Ⅱb 型的CPAM 从桥小脑角区向内听道内生长并填充,伸入范围较小,引起内听道扩大的可能性较小。本研究中Ⅱb 型肿瘤组织伸入内听道内8 例,较其它全年龄组文献比例高[10],伸入深度平均为0.6 cm,却没有1 例出现内听道扩大。而且,CPAM 伸入内听道的肿瘤组织有时呈细条状强化(图2),与面听神经分界清楚,而听神经鞘瘤通常表现为面神经及听神经束增粗并被包埋,与肿瘤主体无明确分界[14]。Ⅱa 型CPAM 仅部分覆盖内听道开口,肿瘤组织不会伸入内听道,鉴别容易。Ⅲ型CPAM 受小脑幕阻挡,以向下方生长为主,需与颈静脉孔区的神经鞘瘤、颈静脉球瘤和颅底的软骨肉瘤相鉴别[15]。颈静脉孔区神经鞘瘤影像特征同其他部位神经鞘瘤;颈静脉球瘤在MRI 上呈特征性的“胡椒盐征”;软骨肉瘤是起源于颅底的骨源性肿瘤,中央可见多发的钙化和骨化;这些征象都与脑膜瘤容易鉴别。另外,Ⅲ型CPAM 极少引起颈静脉孔扩大,本研究结果也是如此,而其他三种肿瘤均会导致颈静脉孔或蝶骨等骨质的破坏。
综上所述,CPAM 的诊断应按照肿瘤与内听道口的相对位置分型并综合各序列MRI 影像特征全面分析。老年患者的CPAM 肿瘤往往较大,更易侵入内听道,但一般不会引起内听道扩大,内听道是否扩大和周围神经是否被包埋是鉴别CPAM和神经鞘膜起源肿瘤的关键。
