低温等离子体净化去除甲苯综合实验设计
2023-08-22刘洪博黄志勇
刘洪博,黄志勇
(北京理工大学珠海学院材料与环境学院,广东珠海 519088)
0 引 言
全球气候变暖形势严峻,温室气体排放越来越受到全球关注。挥发性有机物(VOCs)一直是PM 2.5等颗粒物和O3产生的主要前体物之一[1-3]。对VOCs采取有效的控制与处理措施也成为改善我国空气质量,实现碳中和目标的一项刻不容缓的工作[4]。
目前VOCs的治理技术主要从源头减排,过程控制及末端治理3 个方面展开。但就目前技术水平来看,仅靠源头和过程控制两个阶段并不能完全实现VOCs 减排目标,因此末端治理是VOCs 污染控制中必不可少的阶段。根据VOCs 的治理原理,可以将VOCs的末端治理技术具体分为回收技术和分解技术[5]。对于VOCs 的处理技术目前有光催化法、吸附法、冷凝法、生物处理技术和低温等离子体技术(Non-Thermal Plasma,NTP)等[6-8]。单一的等离子体技术仍存在较明显的短板,比如转化率较低、副产物较多、产物种类不可控等,制约了该技术进一步的工业化应用。因此,国内外学者利用NTP 技术与催化技术协同,研究了NTP协同催化技术对VOCs 进行降解。目前,用于等离子体催化体系的催化剂分为贵金属催化剂和过渡金属催化剂两大类。其中,贵金属催化剂较高的成本及较弱的抗水抗硫性限制了其进一步工业化应用。相比于贵金属催化剂,过渡金属催化剂虽然活性较低,但其储量大且价格低廉,且具有氧化还原能力强,热稳定好及抗毒能力优异等优势,具有更好的应用前景,已成为VOCs氧化领域的研究重点之一[9-10]。
本实验结合目前VOCs 净化去除的研究热点,将教师近年的科研成果转化为环境工程的综合设计实验。实验以采用Zn/Mg/Al金属氧化物粉末为催化剂原料,进行结构表征和造粒加工,在低温等离子体辅助下,以甲苯模拟VOCs进行净化去除实验,并探讨低温等离子体实验条件对甲苯净化去除效果的影响。通过低温等离子体辅助净化去除甲苯实验的操作及对实验结果的分析讨论,可以掌握研究型综合实验对大气污染物净化处理的一般方法和检测手段,提升创新能力和科研思维[11]。
1 实验部分
1.1 材料与试剂
Zn/Mg/Al金属氧化物催化剂粉末,自制;甲苯(C6H5CH3),分析纯,上海麦克林生化科技有限公司;高纯干燥空气,珠海伟名气体有限公司;去离子水。
1.2 仪器
压片机;SHIMADZU LabX XRD-6100 型X 射线衍射仪,岛津公司;低温等离子体装置(介电阻挡放电(DBD)反应器、交流电源、调压器、示波器),南京苏曼等离子科技有限公司;MultiRAE Lite PGM6208 VOC 气体检测仪,华瑞科学仪器有限公司;DZB-718 便携式多参数分析仪,上海雷磁有限公司;HWS-12 恒温水浴锅,上海一恒科学仪器有限公司。
1.3 金属氧化物催化剂的制备及表征
将自制的金属氧化物粉末,用压片机压片,敲碎后过筛,获得粒径为178~425 μm的催化剂颗粒。利用X 射线粉末衍射仪,Cu 靶,光源波长λ = 0.154 06 nm,工作电压和电流分别为40 kV和30 mA,扫描速度3 °/min,扫描范围10°~75°。
1.4 净化去除甲苯的性能测试
1.4.1 测试装置
低温等离子体处理甲苯的实验装置示意如图1 所示。该装置流程由三部分组成,分别是配气系统、介质阻挡放电反应器和气体组分分析系统。实验采用鼓泡法作为甲苯的释放源,为维持实验期间甲苯释放稳定性,将释放源置于30 ℃恒温循环水浴器中,将其与干空气在缓冲瓶内混合后,进入DBD低温等离子体反应器进行处理。处理系统采用干空气瓶进气,通过转子流量计控制进入甲苯发生器的进气流量与空气进气流量,以调节模拟含甲苯废气的所需要浓度和流量。同时在尾气排放管道连接VOC 气体测仪以在线监测尾气中甲苯的浓度。

图1 低温等离子体处理甲苯的实验装置示意
1.4.2 测试方法
采用上述低温等离子体实验装置处理含甲苯废气时,先往甲苯鼓泡瓶中注入50 mL甲苯液体,然后打开干空气瓶阀门,通过转子流量计来控制进气流量,在DBD 工作电源未开启时采用VOC 监测仪测定甲苯的进气浓度。打开等离子体发生器并调节稳压器的工作电压至所需实验值,待低温等离子体放电稳定放电后,开始计时,一定时间后进行相关指标的测定分析。其中,甲苯采用在线分析法;尾气用去离子水吸收,并对吸收液进行测定。
1.4.3 测定指标与分析方法
(1)尾气中甲苯气体浓度的测定。反应器尾气中的甲苯浓度采用VOC气体检测仪检测,处理装置对甲苯的转化率[7]:
式中,Cin和Cout分别为DBD 反应器进、出口甲苯的浓度(mg/L)。
(2)能量密度的测定。能量密度(Energy Density,SIE)定义为输入功率与通入反应器的气体流量的比值,由下式计算[7]:
式中:Q为气体流量(L/s);P为电源放电反应器的输入功率(由输入反应器的电压和电流计算,W):
式中:Ui和Ii分别为输入的电压和电流;θ 为扫描范围,2θ =45°[7]。
(3)pH和电导率的测定。吸收液pH 值和电导率由便携式多参数分析仪测定。
2 测试结果与讨论
2.1 催化剂的结构
图2 所示为Zn/Mg/Al金属氧化物催化剂的XRD谱图,由图可知,Zn/Mg/Al复合金属氧化物呈现金属氧化物ZnO的衍射峰,未检测到氧化镁和氧化铝的物相,说明Zn/Mg/Al的晶体结构由ZnO和高度分散的无定形MgO和Al2O3构成的,这与文献[12]中报道一致。

图2 Zn/Mg/Al金属氧化物催化剂的XRD谱图
2.2 甲苯初始浓度的影响
图3 所示为不同甲苯初始浓度和η 的关系图,由图可知,当甲苯初始浓度低于0.74 mg/L时,其η可达到100 %,随着甲苯初始浓度的不断增大,η是不断减小的;当甲苯初始浓度为2.22 mg/L时,其η依然保持在99 %以上;继续增大甲苯的浓度,η开始不断下降,当甲苯初始浓度为3.33 mg/L 时,η 降低至94.6 %。由此本文选择甲苯初始浓度为2.22 mg/L作为研究的初始浓度条件。
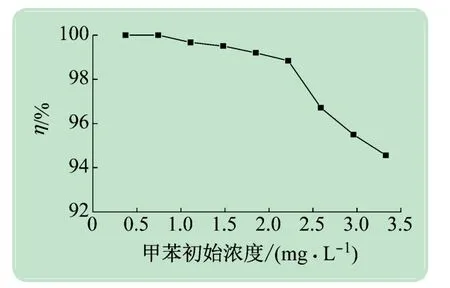
图3 不同甲苯初始浓度与η的关系
2.3 空速的影响
图4 所示为不同空速和η的关系图,由图可知,随着空速的增大,η 逐渐下降,当空速为12 000 h-1时(本文所指空速为单位时间单位体积催化剂处理的气体量,简化为h-1),η 达到最大值99.7 %;当空速达到24 000 h-1时,η依然保持在99 %以上;当空速增加至72 000 h-1时,η 变为93.6 %,较低空速有所下降。这是由于随着空速的增大,气体流速会增大,导致停留时间变短,平均反应效率变低,从而导致η 降低[13]。因此,本文选择甲苯的空速为24 000 h-1作为研究的流量。
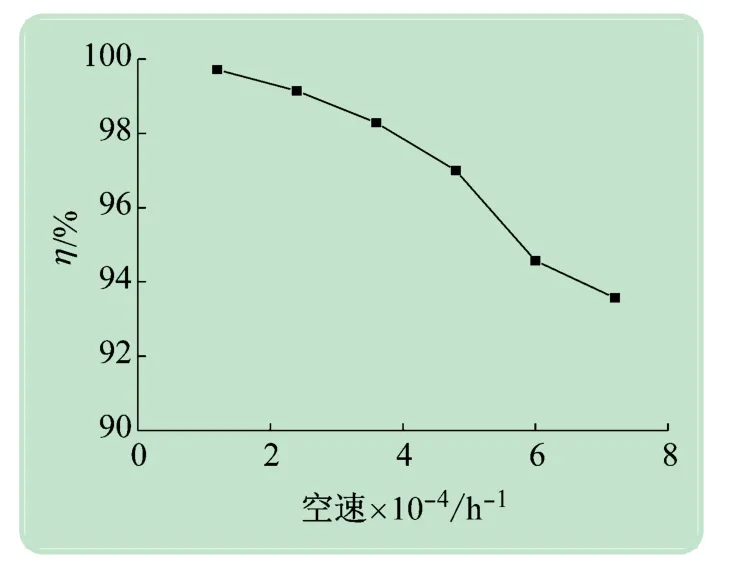
图4 不同空速与η的关系
2.4 反应时间的影响
图5 所示为不同反应时间和η 的关系图,由图可知,随着反应时间的延长,η 是不断增大的,当反应时间低于30 min 时,η 随着反应时间的延长急剧增大;在反应时间为30 min 时,η 达到96.3%;继续延长反应时间,η 变化缓慢,当反应时间为60 min 时,η 为99.1%;再继续增加反应时间,η不再发生变化。考虑到实验时间问题,本文选择30 min为反应时间的研究条件。

图5 不同反应时间与η的关系
2.5 能量密度的影响
图6 所示为不同SIE 和η 的关系曲线图,由图可知,SIE对η 有很大影响,η 随SIE 的增加而增加,当SIE低于1.5 kJ/L 时,η 较低;继续增大SIE,则η 随SIE的增加而迅速增加;当SIE 为2.19 kJ/L 时,η 达到90 %;当SIE为2.93 kJ/L时,其最大值为99.9 %。由此,本文选择SIE在2.19 kJ/L以上。
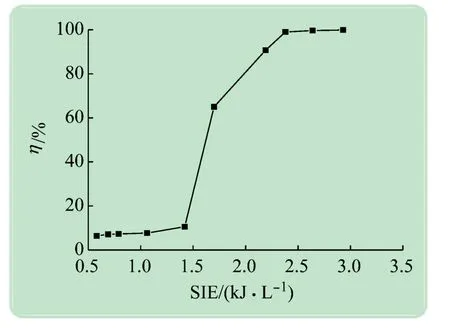
图6 SIE与η的关系曲线
2.6 催化剂的影响
本实验还对催化剂协同低温等离子体与单一低温等离子体去除甲苯效果进行了对比。如表1 所列为相同SIE下,不同催化条件下η的数据表。由表1 可见,当SIE同为2.19 kJ/L 的情况下,有催化剂协同的低温等离子体的η要远远高于单一的低温等离子体。由此可见,催化等离子体协同作用下,表现出更好的甲苯净化去除性能。

表1 不同催化条件下甲苯转化率的数据表
同时,还对比了相同η 条件下,所需SIE 的情况。如表2 所列为相同η 下,不同催化条件下所需的SIE和单位能量下甲苯的处理量的数据表,由表2 可见,在η相同条件下,催化剂协同低温等离子体更节能,即单位能耗下甲苯处理量由15.3 %提高到20.6 %,提高了34.6 %。因此,Zn/Mg/Al 金属氧化物催化剂协同低温等离子体的效果优于单一低温等离子体,这与文献[14]中报道一致。
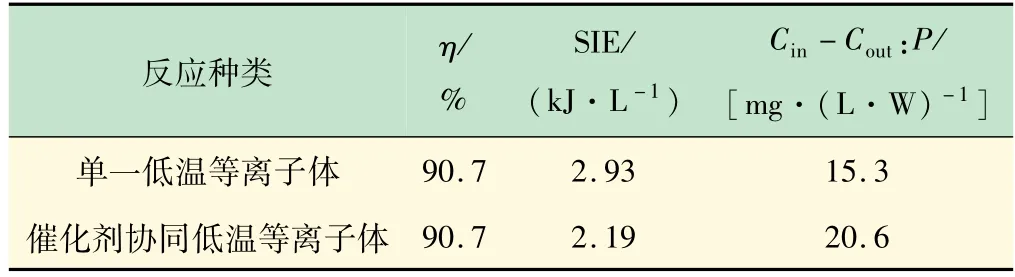
表2 不同催化条件下SIE和单位能耗下甲苯的处理量数据表
2.7 吸收效果的评价
图7 所示为反应时间与吸收液的pH值及电导率的关系曲线,由图可知,随着反应时间的延长,吸收液的pH值是不断减小的,而电导率是不断增大的,这表明吸收液的酸性不断增强,且溶液中离子的浓度不断增大。这可能是由于随着反应时间的延长,甲苯分解得到的离子浓度不断增大,进而使吸收液酸性和电导率提高。

图7 反应时间与吸收液的pH值及电导率的关系曲线
图8 所示为初始浓度和吸收液的pH值及电导率的关系曲线,由图可知,随着甲苯初始浓度的增大,吸收液的pH 值和电导率呈现一定波动。但总体呈现pH不断变小,而电导率不断增大的趋势。这表明,随着处理甲苯浓度的增大,吸收液中的离子的含量也是不断增大的。
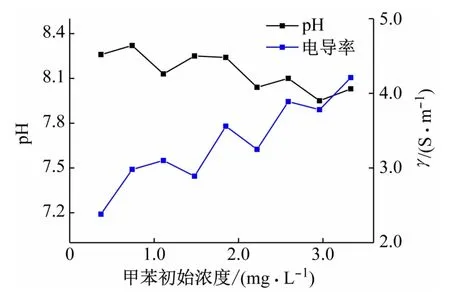
图8 甲苯初始浓度与吸收液的pH值及γ的关系曲线
2.8 低温等离子体净化去除甲苯机理
图9 所示为催化剂协同低温等离子体去除甲苯的机理示意图,由图可知,甲苯分子在与等离子体放电区域内的高能电子发生碰撞后被破坏,分子中甲基上的C—H 键、苯环中的C—H 键以及苯环与甲基之间的C—C 键依次断裂,进而得到甲基、甲苯基、苯基、苄基等自由基。随着SIE增加,这些自由基和从晶格氧中释放出来的和吸附在催化剂表面的OH·、O3和O·等活性物种相结合,并被进一步裂解成小分子有机化合物,最后转化为水和碳氧化物[15]。
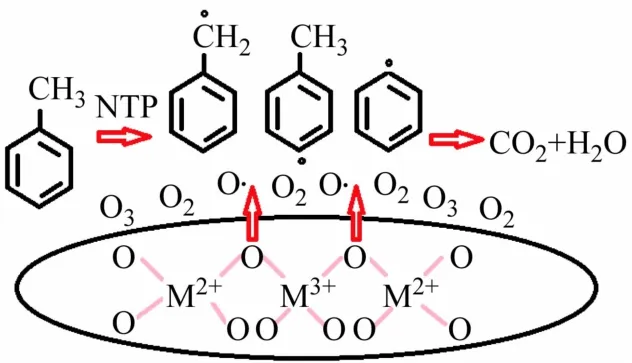
图9 催化剂协同低温等离子体去除甲苯的机理示意
3 结 语
本研究型综合实验采用自制金属氧化物催化剂,协同低温等离子体技术,用于净化去除VOCs 中的甲苯,探究了甲苯的初始浓度、气体流量、反应时间和能量密度等条件对甲苯净化去除效果的影响,并对催化机理进行了初步探讨。研究表明:甲苯初始浓度为2.22 mg·L-1,空速为24 000 h-1,反应时间为30min,SIE大于2.19 kJ·L-1时,具有较好的甲苯转化率;相比于单一低温等离子体,金属氧化物催化剂协同低温等离子体去除甲苯具有更好的催化性能;此外,吸收液的pH值和电导率结果表明增大反应时间有利于甲苯的降解。
本实验是将教师的科研成果转化成本科生研究型综合设计实验,可以用于环境工程及相关专业的综合实验教学,实验设置为8 学时,采用循环小组式,每组3~5 人。此外,可针对该研究型综合实验的开展,加深了对大气污染控制工程理论知识的理解,融合了低温等离子体学科前沿技术,提高了科研探究和解决问题的实际动手能力。同时,小组实验也提升了团队合作精神。
