内侧突出技术对成人发育性髋关节发育不良患者全髋关节置换术后髋关节外展肌力恢复的影响*
2023-08-21曾晓霜陈俊文黄梁坤周建林邓爽孙飞方洪松彭昊
曾晓霜# 陈俊文# 黄梁坤 周建林 邓爽 孙飞 方洪松* 彭昊*
成人发育性髋关节发育不良(developmental dysplasia of the hip, DDH)患者由于髋臼及股骨近端发育异常,导致髋关节对位不良,随病情进展常合并关节囊挛缩、髋关节周围肌肉萎缩、假臼形成,最终合并髋关节炎导致患者跛行、髋关节疼痛及活动受限等,严重影响着患者的生活质量[1]。由于DDH患者髋关节发育的异常,DDH患者合并髋关节炎行全髋关节置换术(total hip arthroplasty, THA)对关节外科医生而言是一个巨大的挑战。
DDH 患者行THA 时,由于关节囊挛缩、假臼形成、患肢短缩等问题,为最大程度恢复患者的髋关节功能、保证假体稳定及避免术后并发症的发生,各国学者提出了许多重建技术,如高位髋关节旋转中心、髋关节软组织平衡、自体植骨增强、内侧突出技术及转子下截骨等。和传统髋关节置换手术相比,严重的解剖畸形使髋臼重建成为DDH 患者行THA 的最大挑战之一。对髋臼形态和骨缺损的透彻了解是髋臼重建技术的基础[2],研究发现髋臼位置重建的技术中采用内侧突起技术结合THA 治疗DDH 较其他技术相比,手术时间短、技术要求低,易于提高臼杯覆盖率,促进髋臼窝重建,达到良好的髋关节生物力学,能减小髋关节负重区应力,降低假体磨损量,延长假体使用寿命等优点[3-6]。
下肢肌力在髋、膝关节稳定中起着重要作用[7]。外展肌功能障碍是THA术后关节不稳的高危因素之一,最终可能导致假体脱位甚至松动等严重后果[8]。患者因髋关节骨关节炎行THA 术后患肢髋关节外展肌力降低15% ~31%[9-10],这提示THA 术后患者髋关节外展肌力恢复程度存在差异。术后患者髋关节外展肌力的恢复受多种因素影响。如手术入路的选择、软组织平衡技术及髋关节旋转中心的位置等。DDH 患者由于髋臼发育浅甚至假臼的形成,为了在真臼中重建旋转中心及维持假体稳定,常应用内侧突出技术。内移的髋关节旋转中心改变了髋关节生物力学特征,这是否会影响术后髋关节外展肌力的恢复不得而知。因此,笔者开展了一项回顾性研究,分析应用内侧突出技术行THA术是否会对患者术后外展肌力产生影响。
1 资料与方法
1.1 纳入与排除标准
纳入标准:诊断为DDH、股骨颈骨折、股骨头坏死及髋关节骨性关节炎单侧病变患者。排除标准:①股骨头垂直移位小于10 mm;②对侧髋关节异常;③患有运动、神经系统疾病导致下肢功能障碍。
1.2 一般资料
收集2012年1月至2021年12月于武汉大学人民医院由于DDH、股骨颈骨折、类风湿性髋关节炎、股骨头坏死及髋关节骨性关节炎,初次行单侧髋关节置换患者共116例,根据诊断不同将患者分为DDH 组(52 例,临床诊断为先天性髋关节发育不良的患者)及非DDH 组(64 例,临床诊断为股骨颈骨折、股骨头坏死及髋关节骨性关节炎的患者)。DDH 组:男20 例,女32 例,年龄33 ~ 65(50.5±8.35)岁;Crowe Ⅰ型24 例,Crowe Ⅱ型19 例,Crowe Ⅲ型9 例。非DDH 组:男28 例,女36 例,年龄34 ~ 87(63.1±15.95)岁(见表1)。本研究经医院伦理委员会批准(WDRY2022-K206),患者均签署知情同意书。
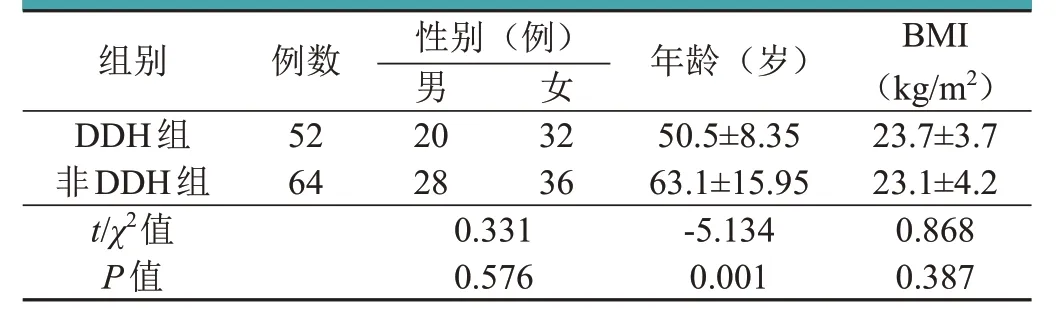
表1 两组患者一般资料的比较
1.3 手术方法
所有手术均由同一组手术医生完成,假体均采用生物型假体(美国Zimmer公司)。全身麻醉或腰硬联合麻醉成功后,患者采用健侧卧位,以固定支架固定骨盆。采用改良后外侧入路,髋关节屈曲45°,沿股骨轴线,以大转子顶点为中心,做长8 ~ 10 cm 切口,依次切开皮肤、皮下组织、钝性分离臀大肌、切开外旋肌群及关节囊并保护梨状肌、臀中肌止点。脱出并截下股骨头,清除骨赘、盂唇及增生软组织,充分松解髋关节并暴露髋臼。根据术前规划及术中闭孔、坐骨和耻骨以及泪滴等解剖提示定位DDH组真臼后(非DDH组原髋臼即是真臼),以大约45°的外展和15°的前倾角度进行髋臼磨锉。髋臼磨锉时评估深度及内移距离,可先用小号髋臼锉磨锉髋臼,逐号扩大加深,传统髋臼磨锉后的髋臼腔深度不足以允许髋臼组件的稳定所需的压配和固定,可使用内侧突出技术来加深髋臼腔。磨锉时髋臼内侧壁骨皮质通常保持完整,如髋臼覆盖不够(覆盖率小于50%),可适当增加磨锉制造髋臼内侧骨皮质缺损,缺损直径控制在15 mm 以内,若内侧壁缺损过大(缺损直径超过20 mm),则可能导致不稳定的髋臼重建,甚至有髋臼假体突入盆腔的危险。收集髋臼磨锉产生的骨碎片,并通过在海绵中压缩碎片来去除脂肪,然后将处理好的碎片放入内侧缺损中,以便日后成骨。再以合适外展角、前倾角打入试模后,术中透视,评估深度及内移距离,在骨盆正位X 线上,臼杯内侧缘到达或超过Kӧhler线,假体位于真臼中,且覆盖大于50%。取出试模,安装相应髋臼假体,以2 枚螺钉固定髋臼假体并安装聚乙烯内衬。显露股骨侧,调整合适前倾角后开槽,沿股骨髓腔中心,植入髓腔锉,按照型号大小,依次磨锉股骨髓腔至合适大小,将髓腔锉留置髓腔内,安装球头试模,复位髋关节。测试关节活动范围、下肢长度及关节稳定性,满意后安装股骨假体柄及球头,采用可吸收线缝合修补关节囊及部分外旋肌止点。留置引流管,按照解剖结构逐层缝合至皮肤。
1.4 术后处理
所有患者术后使用抗生素48 h,术后24 h 后常规抗凝28 d。术后24 h 后拔除引流管,所有患者麻醉作用消失后在康复科医生指导下进行股四头肌等长收缩及踝关节、跖趾关节活动,踝泵锻炼等,术后2 d开始鼓励患者在助行器辅助下下地活动,1 个月后步态平稳可考虑改用单拐或手杖辅助行走。术后2个月后正常行走。
1.5 观察指标
在术前,术后1、4、24及48周进行临床数据采集。采用Harris 髋关节评分系统对患者髋关节功能进行评价,康复科医生采用手持握力器仰卧位等距收缩测量外展肌力,并双侧对比计算外展肌力矩比(hip abductor muscle moment ratio, HAMMR)。回顾分析骨盆正位平片,采用Crowe分型标准对评价DDH患者分型,测量股骨头水平旋转中心距、股骨头垂直旋转中心距、股骨头垂直移位并计算旋转中心内移距离(见图1)。记录髋关节脱位、神经损伤、髋关节感染、假体松动及假体周围骨折等并发症的发生。
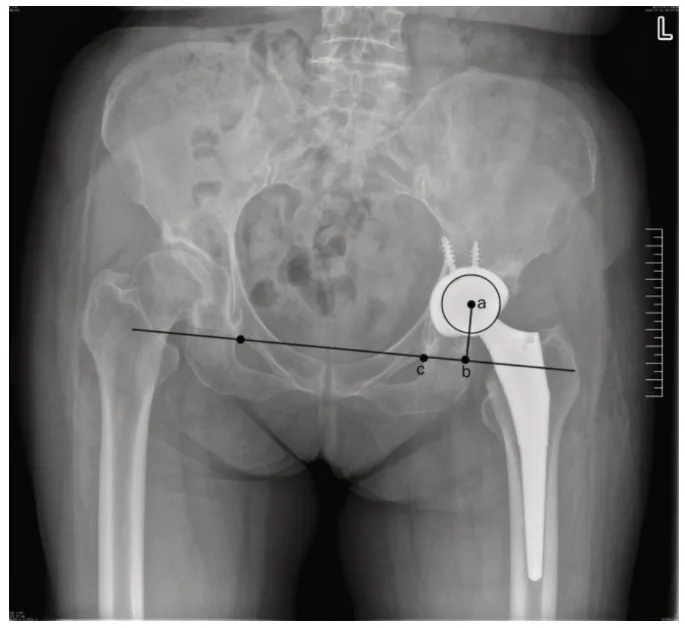
图1 髋关节旋转中心的测量:ab为股骨头垂直旋转中心距;bc为股骨头水平旋转中心距
1.6 统计学方法
采用SPSS 21.0软件对数据进行统计学分析。计量资料采用均数±标准差表示,髋关节功能评分、外展肌力矩比采用配对t检验,DDH组与非DDH组间HAMMR比较采用独立样本t检验,P<0.05为差异有统计学意义。旋转中心内移距离与外展肌力矩比采用线性回归分析,置信区间为95%。
2 结果
共116例患者获得随访,其中DDH组52例,非DDH组64例,时间12 ~ 18个月,平均随访时间14.3个月,所有患者截至末次随访时间,术后均无髋关节脱位、神经损伤、髋关节感染、假体松动及假体周围骨折等并发症的发生。
离子液体是由离子组成的有机盐化合物,在室温下多为流动状态的液体,对纤维素等聚合物具有良好的溶解性能。在纤维素向5-HMF的催化转化过程中,离子液体被广泛采用[12]。
2.1 DDH组患者术后临床效果
DDH组52例患者髋关节Harris评分从术前(39.6±7.9)分改善至术后12 个月(85.1±6.2)分,术前术后比较差异具有统计学意义(P<0.05)。髋关节旋转中心内移距离平均(15.5±6.0) mm,其中Crowe Ⅰ型24 例,Crowe Ⅱ型19 例,Crowe Ⅲ型9 例,各分型Harris 评分及旋转中心内移距离如表2所示。应用内侧突出技术可显著改善DDH患者髋关节功能。
表2 DDH组术后Harris评分及旋转中心内移距离的变化(±s)

表2 DDH组术后Harris评分及旋转中心内移距离的变化(±s)
Crowe分型n Harris评分(分)术前40.2±7.6 38.6±6.2 40.3±11.9ⅠⅡⅢ24 19 9术后85.5±6.9 86.3±4.8 81.8±6.4 t值-20.316-25.769-14.369 P值<0.001<0.001<0.001旋转中心内移距离(mm)10.8±2.2 17.4±3.9 24.4±3.8
2.2 两组术后HAMMR 变化及旋转中心内移距离对HAMMR的相关性分析
DDH组患者术后6个月及12个月HAMMR分别为(85.3±7.4)%及(93.9±3.6)%,较术前显著改善(P<0.05)。且在术后12 个月时,HAMMR 恢复至(93.9±3.6)%,提示患侧外展肌力恢复接近对侧水平(见表3)。
表3 两组间术后HAMMR对比(±s,%)

表3 两组间术后HAMMR对比(±s,%)
注:*表示与术前比较,差异有统计学意义(P<0.05);#表示与术前比较,差异无统计学意义(P>0.05)。
术前72.0±9.5-时间DDH组非DDH组t值P值术后1个月71.4±9.1#74.3±6.1-2.058 0.042术后6个月85.4±7.4*86.1±6.8-0.566 0.572术后12个月93.9±3.6*94.8±4.1-1.263 0.209
通过皮尔逊相关性分析,DDH组中旋转中心内移距离与HAMMR无明显相关性(r=-0.061,P=0.665>0.05)。在内移旋转中心平均距离不超过24.4 mm 时,对术后髋关节外展肌力的恢复无明显影响。
对DDH 组与非DDH 组间HAMMR 进行独立样本t检验发现,在术后6、12 个月HAMMR 均无明显差异(P>0.05)。应用内侧突出技术内移髋关节旋转中心,在术后6、12 个月时DDH 组对术后外展肌力的恢复较非DDH组无明显差异(见表3)。
典型病例1:患者,男,34 岁,左髋DDH(Crowe Ⅲ型),血友病性骨关节炎,入院Harris评分37分。术前骨盆正位提示股骨头变形,关节间隙严重狭窄,股骨头上移半脱位,应用内侧突出技术行全髋关节置换术。术后双下肢等长,无跛行,活动无撞击,术后12个月Harris评分82分(见图2)。

图2 A. 术前骨盆正位片提示左股骨头坏死变形并向上脱位,真臼发育差;B. 术后12个月髋关节旋转中心内移距离21.2 mm,假体无松动,HAMMR恢复至94%,提示患侧外展肌力恢复接近对侧水平
典型病例2:患者,女,76岁,左侧股骨头坏死、关节间隙狭窄,应用内侧突出技术行全髋关节置换术(见图3)。
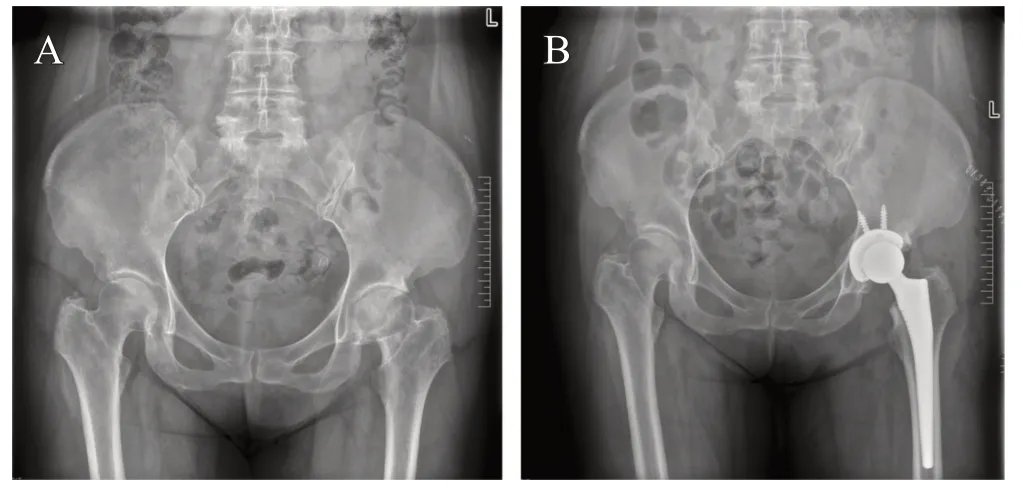
图3 A. 术前骨盆正位片提示左侧股骨头坏死,关节间隙狭窄;B. 术后12个月X线片示髋关节旋转中心内移距离10.2 mm,假体无松动,HAMMR恢复至94%,提示患侧外展肌力恢复接近对侧水平

图4 A. 术前骨盆正位片提示左股骨头坏死,双侧髋臼骨质增生;B. 术后12个月X线片示髋关节旋转中心内移距离16.0 mm,假体无松动,HAMMR恢复至98%,提示患侧外展肌力恢复接近对侧水平
3 讨论
理想状态下,在解剖位置重建髋关节旋转中心可以使髋关节活动达到最理想的生物力学状态。DDH患者由于髋臼发育不良,采用常规策略重建髋臼难以保证髋臼假体稳定,于是常采用高位髋关节旋转中心及内侧突出技术,髋关节旋转中心的内移及上移无疑改变了髋关节生物力学状态。其中髋关节旋转中心的上移会影响髋关节外展肌力效率及增加关节内应力,影响髋关节功能及假体使用寿命[11-13]。另外通过计算机模型分析,髋关节旋转中心内移可能会减少髋关节活动度及增加髋关节撞击的风险[14]。而在本研究中,患者术后髋关节Harris 评分明显改善,且旋转中心内移距离与HAMMR无明显相关性。
研究发现,下肢肌力通常在术后6 ~ 24 个月基本恢复[15-17]。影响术后肌力恢复的因素通常包括年龄、BMI 及假体位置等[12,18],年龄、BMI 与外展肌力恢复呈负相关。值得一提的是有研究发现[19],通过调整股骨偏心距可以改变外展肌力臂,从而改善外展肌力。Terrier 等[20]通过有限元分析发现,在应用内侧突出技术内移髋关节旋转中心时,对外展肌力臂有不同程度改善,尽管这种相关性差异较大,主要与患者股骨假体前倾及股骨偏心距等因素相关。笔者认为,在内移髋关节旋转中心的同时,代偿性地增大股骨偏心距,保持阔筋膜张力的同时,增大外展肌力矩。
外展肌群包括臀中肌、臀小肌及阔筋膜张肌肉,可确保行走时骨盆稳定,并驱动髋关节内外旋及外展[21]。外展肌群在维持髋关节稳定中起着关键作用,外展肌群功能障碍是THA术后关节不稳的高危因素之一[8]。在美国,THA术后关节不稳是导致人工关节翻修的最主要原因,占比22.5%[22]。这充分说明了外展肌群功能恢复对于THA 术后患者的重要性。首先,应避免直接损伤外展肌群及其止点。其次,外展肌群受臀上神经支配,手术操作应避免臀上神经损伤。最后,出现外展肌群损伤导致功能障碍后及时修复外展肌群,其技术主要包括直接缝合修补[23]、同种异体跟腱移植物修补[24-25]、臀大肌转位[26-28]、股外侧肌转位[29]等。
目前,已有研究证实运用内侧突出技术,内移髋关节旋转中心能增加臀中肌的动力臂,改善臀中肌功能,有效增加髋臼覆盖面积,实现发育不良髋关节的假体稳定性,从生物力学的角度来讲为了降低髋关节的负荷,髋关节旋转中心应尽可能放在内下侧,即真臼的所在位置来减轻负荷[6]。本研究中,旋转中心最大内移距离是24.4 mm,笔者发现旋转中心在此有限内移距离内,外展肌力的恢复未见明显相关性,这说明应用内侧突出技术有限内移髋关节旋转中心对术后外展肌力的恢复无明显影响。
本研究中也存在局限性。首先,笔者采用手持握力器仰卧位等距收缩测量外展肌力,并计算外展肌力矩比,其优势在于操作简单[30],相比等速肌力测定可能存在误差。其次,纳入样本均由同一组手术医生完成,限制了样本量。同时为了排除股骨头垂直移位对外展肌力的影响,本研究未纳入Crowe Ⅳ型病例,这类患者旋转中心内移距离通常更大,更大的髋关节旋转中心内移对外展肌力的恢复是否会产生影响,值得进一步观察。
综上,DDH 患者行THA 术应用内侧突出技术,在有限范围(内移距离不超过24.4 mm)内移旋转中心时,对术后髋关节外展肌力的恢复无明显影响,术后髋关节功能及外展肌力得到明显改善。
