加味逍遥散联合甲巯咪唑片对Graves病气滞痰凝证患者的临床疗效
2023-08-14段姗姗,王永恒,彭书旺,胡维
段姗姗,王永恒,彭书旺,胡维







〔摘要〕 目的 观察加味逍遥散联合甲巯咪唑片治疗Graves病气滞痰凝证患者的临床疗效。方法 选取2020年6月至2022年6月湖南中医药大学第一附属医院门诊及病房的80例患者随机分为对照组和观察组,每组40例,对照组在基础治疗的基础上给予甲巯咪唑片,观察组在对照组基础上加用加味逍遥散,4周为1个疗程,连续治疗3个疗程。观察两组患者治疗前后临床疗效、中医证候积分、临床症状评分、甲状腺体积大小、甲状腺上动脉收缩期峰值血流速度(peak systolic velocity of the superior thyroid artery, STA-PSV)、简易生活质量量表(36-item short form, SF-36)评分变化,检测血清中促甲状腺激素(thyroid stimulating hormone, TSH)、游离三碘甲状腺原氨酸(free triiodothyronine, FT3)、游离甲状腺素(free thyroxine, FT4)、促甲状腺液素受体抗体(thyrotropin receptor antibody, TRAb)以及甲状腺过氧化物酶自身抗体(thyroid peroxidase autoantibody, TPOAb)水平变化,同时评估两组患者治疗方案的安全性。结果 观察组总有效率为87.18%(34/39),对照组总有效率为68.42%(26/38),观察组总有效率高于对照组(P<0.05)。治疗后两组患者中医证候积分、临床症状评分、甲状腺体积、STA-PSV及血清FT3、FT4、TRAb、TPOAb含量均较治疗前降低(P<0.01),且观察组低于对照组(P<0.01)。治疗后两组患者SF-36评分、血清TSH含量均较治疗前升高(P<0.01),且观察组高于对照组(P<0.01)。在治疗期间,两组患者均未发生明显不良反应,且患者的肝肾功能、血常规、心肌酶、心率、脉搏、血压等安全性指标均未见异常。结論 加味逍遥散联合甲巯咪唑片对Graves病气滞痰凝证患者的临床疗效以及安全性良好,其作用机制可能与调节免疫、改善甲状腺激素及相关抗体水平有关。
〔关键词〕 加味逍遥散;甲巯咪唑片;甲状腺功能亢进症;Graves病;气滞痰凝证
〔中图分类号〕R285.6 〔文献标志码〕B 〔文章编号〕doi:10.3969/j.issn.1674-070X.2023.07.021
Clinical efficacy of Jiawei Xiaoyao Powder combined with Methimazole Tablet in treating Graves disease of qi stagnation with phlegm
retention pattern
DUAN Shanshan, WANG Yongheng, PENG Shuwang, HU Wei*
The First Hospital of Hunan University of Chinese Medicine, Changsha, Hunan 410007, China
〔Abstract〕 Objective To observe the clinical efficacy of Jiawei Xiaoyao Powder (JWXYP) combined with Methimazole Tablet in treating Graves disease of qi stagnation with phlegm retention pattern. Methods From June 2020 to June 2022, 80 outpatients and wards of the First Affiliated Hospital of Hunan University of Chinese Medicine were randomly divided into the control group and the observation group, with 40 cases in each group. Control group was given Methimazole Tablet based on conventional treatment, while observation group was treated with JWXYP based on the treatment of control group, 4 weeks as a course of treatment, for 3 continuous courses. Then the changes in clinical efficacy, TCM pattern score, clinical symptom score, thyroid volume, peak systolic velocity of the superior thyroid artery (STA-PSV), and score of 36-item short form (SF-36) before and after treatment were observed. Meanwhile, the level changes of thyroid stimulating hormone (TSH), free triiodothyronine (FT3), free thyroxine (FT4), thyrotropin receptor antibody (TRAb), and thyroid peroxidase autoantibody (TPOAb) in serum was determined. At the same time, the safety of both regimens was evaluated. Results The total effective rate was 87.18% (34/39) in observation group, which was higher than that in control group with 68.42% (26/38) (P<0.05). After treatment, the TCM pattern score, clinical symptom score, thyroid volume, STA-PSV, and the content of FT3, FT4, TRAb, and TPOAb in serum in both groups were lower than those before treatment (P<0.01), and those in observation group were lower than those in control group (P<0.01). After treatment, the SF-36 score and serum TSH content in both groups were higher than those before treatment (P<0.01), and those in observation group were higher than those in control group (P<0.01). During the treatment, no obvious adverse reactions occurred in the two groups, and there were no abnormalities in liver and kidney function, blood routine, myocardial enzymes, heart rate, pulse, blood pressure, and other safety indicators. Conclusion JWXYP combined with Methimazole Tablet has high clinical efficacy and safety in treating Graves disease of qi stagnation with phlegm retention pattern, and its mechanism of action may be related to regulating immunity as well as improving the levels of thyroid hormone and related antibodies.
〔Keywords〕 Jiawei Xiaoyao Powder; Methimazole Tablet; hyperthyroidism; Graves disease; qi stagnation with phlegm retention pattern
甲状腺功能亢进症是一种由于多種病因引起甲状腺功能紊乱而出现一系列全身异常表现的内分泌系统疾病,临床上常表现为代谢亢进以及神经、消化、循环等多个系统兴奋性增高,其中格雷夫斯(Graves)病是最常见的类型[1],占甲状腺功能亢进症的80%~85%,中青年女性多见[2],发病率在中国约2%[3]。目前临床上针对Graves 病,西医常予以口服抗甲状腺药物、手术切除、放射性131I等治疗手段,但疗效相对有限,且存在不良反应、易复发、手术后遗症等问题,不仅增加了患者的经济负担,同时也影响患者的生活质量。
中医学将Graves病归属于“瘿病”“瘿气”等范畴。中医药治疗“瘿病”具有悠久的历史,中西医结合治疗Graves病具有广阔的应用前景。本病的产生与情志密切相关,病位主要在肝脾,与心相关,病机为情志不畅,肝失疏泄,肝郁气滞。气滞则津停血瘀,或是肝郁犯脾,脾失健运,津液失布,聚湿成痰,痰气交阻,气血运行不畅,气滞、血瘀、痰凝壅滞于颈前而发病,辨证分型主要包括气滞痰凝证、脾肾阳虚证、阴虚火旺证,其中以气滞痰凝证最为常见,故治疗上应标本兼顾,常以行气疏肝、健脾化痰之逍遥散为主方,配以半夏厚朴汤行气化痰,组成加味逍遥散治之,随证加减,临床上取得了较好疗效。因此,本研究考察加味逍遥散联合甲巯咪唑片对Graves病气滞痰凝证患者的临床疗效及其可能的作用机制,现报道如下。
1 资料与方法
1.1 一般资料
选取2020年6月至2022年6月湖南中医药大学第一附属医院门诊及病房治疗的Graves病气滞痰凝证患者80例。采用随机数字表法分为对照组和观察组,每组40例,剔除或脱落共3例,其中对照组2例,观察组1例,最终分别纳入38、39例,两组患者性别、年龄、病程、体质量指数(body mass index, BMI)等一般资料比较,差异无统计学意义(P>0.05),具有可比性,详见表1。研究经湖南中医药大学第一附属医院伦理审查委员会批准(HN-LL-LW-2020-011)。
1.2 诊断标准
1.2.1 西医 甲状腺功能亢进症诊断参照《甲状腺功能亢进症基层诊疗指南(2019)》[4]的诊断标准。(1)临床表现:代谢亢进及多个系统兴奋性增高等;(2)体征:甲状腺弥漫性肿大、心率增快、汗多手抖、焦虑紧张、易激动等;(3)辅助检查:血清甲状腺激素水平增高,促甲状腺激素降低,甲状腺B超检查显示甲状腺弥漫性增生而无明显结节等。
Graves病诊断标准参照《甲状腺功能亢进症基层诊疗指南(2019)》[4]的诊断标准:(1)符合临床甲状腺功能亢进症的诊断;(2)甲状腺弥漫性肿大;(3)可伴有胫前黏液性水肿;(4)可伴有眼球突出或其他浸润性眼症;(5)促甲状腺激素受体抗体(thy?鄄rotropin receptor antibody, TRAb)、甲状腺过氧化物酶自身抗体(thyroid peroxidase autoantibody, TPOAb)阳性。以上诊断中1~2项为必备条件,3~5项为辅助条件。
1.2.2 中医 参照《中医内科学》[5]“瘿病”及《证候类中药新药临床研究技术指导原则》[6],主症包括:(1)颈部肿胀,喉中有堵塞感;(2)情志抑郁,心烦易怒;(3)胸闷不舒,胁肋胀痛;(4)眼胀眼突,心慌手抖。次症包括:(1)心悸失眠;(2)倦怠乏力;(3)恶心痰多;(4)气短懒言;(5)善叹息;(6)食欲亢进;(7)形体消瘦;(8)大便溏薄或便后不爽。舌脉:舌苔薄白腻,脉弦滑或弦细,满足主症中4项并至少满足次症中2项,同时符合舌脉,即可诊断为气滞痰凝证。
1.3 纳入标准
(1)满足“1.2”项下诊断标准;(2)年龄18~70岁;(3)神志清楚,生命体征稳定;(4)可进行正常的沟通交流;(5)患者及其家属了解本研究,自愿签署知情同意书。
1.4 排除标准
(1)合并精神方面疾病病史(精神分裂症、抑郁症、狂躁症、强迫症等);(2)合并严重心、脑、肝、肾、血液系统疾病或恶性肿瘤;(3)1个月内参与其他药物临床试验;(4)备孕、妊娠或哺乳期女性;(5)内分泌功能严重紊乱,目前使用糖皮质激素及细胞毒性药物治疗者;(6)抗甲状腺药物治疗无效或甲状腺压迫邻近器官需手术者;(7)对研究药物过敏、不耐受或出现严重不良反应者。
1.5 剔除、脱落标准
(1)依从性差,未规律服药或违背本研究方案;(2)治疗期间出现过敏、不耐受或严重不良反应;(3)自愿退出本研究;(4)基础疾病进行性加重。
1.6 治疗方法
两组患者入院后完善相关检查,如肝肾功能、血常规、心肌酶、甲状腺激素水平及甲状腺肿大情况,同时监测患者心率、脉搏、血压等基本生命体征。
基础治疗:嘱患者避免剧烈运动,保持心情舒畅,清淡饮食,摄入含碘量少的食物,补充高蛋白及维生素。对照组患者在基础治疗条件下,口服甲巯咪唑片(德国默克公司,生产批号:H20120405),初始剂量30 mg,每日1次,可根据患者甲状腺功能整体情况调整药量至15 mg,每日1次,病情控制后维持药量为5 mg,每日1次,4周为1个疗程,连续治疗3个疗程。
观察组患者在对照组基础上服用加味逍遥散,组方药材:白芍20 g,当归、茯苓、白术、柴胡各15 g,半夏、厚朴、紫苏叶各10 g,随证加减,均购自湖南中医药大学第一附属医院中药房,质量均符合2020年版《中华人民共和国药典》[7]规定,由湖南中医药大学第一附属医院中药房代煎,先武火后文火熬制成200 mL药液,等体积分装为2袋,每袋100 mL,每日早晚餐后30 min各温服1次,每次100 mL,4周为1个疗程,连续治疗3个疗程。
1.7 观察指标
1.7.1 中医证候积分 治疗前后各评估1次,以中医诊断标准为基础,即Graves病属中医“瘿病”范畴,主症包括:颈部肿胀、情志抑郁、胸胁胀满、眼突手抖4项;次症包括:心悸失眠、倦怠乏力、恶心痰多、气短懒言、善叹息、食欲亢进、形体消瘦、大便溏薄或便后不爽8项。根据患者出现相应症状的病情程度,主症、次症均设定为4个等级,分别为无、轻、中、重,前者分别对应为0、2、4、6分,后者分别对应0、1、2、3分,中医证候积分=主症积分+次症积分,总分0~48分,分数越高,表示气滞痰凝证程度越高[8]。
1.7.2 甲状腺功能 治疗前后分别取患者清晨空腹时静脉血于肝素抗凝管内,3 500 r·min-1离心5 min(离心半径10 cm),分离血浆,取上层血清。采用全自动分析仪测定血清中促甲状腺激素(thyroid stim?鄄ulating hormone, TSH)、游离三碘甲状腺原氨酸(free triiodothyronine, FT3)、游离甲状腺素(free thyroxine, FT4)含量。
1.7.3 甲状腺相关抗体水平 治疗前后分别取患者清晨空腹时静脉血于肝素抗凝管内,3 500 r·min-1离心 5 min(离心半径10 cm),分离血浆,取上层血清。采用ELISA法测定血清中TRAb、TPOAb含量。人TRAb的ELISA试剂盒购自上海古朵生物科技有限公司,批号GD-S0996;人TPOAb的ELISA试剂盒购自上海帛科生物技术有限公司,批号BK-E9066。按试剂盒说明书操作进行。
1.7.4 甲状腺体积及甲状腺上动脉收缩期峰值血流速度(peak systolic velocity of the superior thyroid artery, STA-PSV)变化 采用我院彩超室GELOGIQ E9 CDFI诊断仪,探头型号为ML6-15,嘱患者仰卧位,充分暴露颈部,显示甲状腺及周边组织结构,测量治疗前后甲状腺体积及STA-PSV变化。
1.7.5 临床症状评分 参考《实用临床中医内科学》[9]对瘿病的诊断标准,评价Graves病患者治疗前后甲状腺肿大、怕热多汗、心慌手抖、形体消瘦、眼胀眼突、胫前黏液性水肿等临床症状程度,每项症状依据严重程度依次分为无、轻度、中度、重度,分别计为0、1、2、3分,得分越低則表明临床症状越轻,得分越高则表明临床症状越重。
1.7.6 生活质量量表评分 采用简易生活质量量表(36-item short form, SF-36)评分[10],综合评估治疗前后Graves病患者日常生活质量。SF-36又称健康状况调查问卷,涉及生理功能、健康状况、社会功能及精神健康等方面,包括8个分量表,共36个条目,根据各条目不同的权重,计算分量表中各条目积分之和,得到分量表的粗积分,将粗积分转换为0~100的标准分,得分越低表明日常生活质量越差,得分越高则表明日常生活质量越好。
1.7.7 安全性评价 通过观察两组患者在治疗期间不良反应的发生情况,以及检测患者治疗前后的肝肾功能、血常规、心肌酶、心率、脉搏、血压等安全性指标的变化情况,以评价两组患者治疗方案的安全性。
1.8 疗效评价
参照《证候类中药新药临床研究技术指导原则》[6]。(1)痊愈:患者临床症状及相关阳性体征基本消失,较治疗前缓解90%以上,即90%<有效指数≤100%;(2)显效:心烦易怒,胸闷不舒,胁肋胀痛,颈部肿胀,喉中有堵塞感,眼胀眼突,心慌手抖等气滞痰凝证症状有显著的缓解,较治疗前缓解75%以上,即75%<有效指数≤90%;(3)有效:患者临床症状及相关阳性体征有一定的缓解,较治疗前缓解50%以上,但仍影响生活,即50%<有效指数≤75%;(4)无效:患者临床症状及相关阳性体征无任何改善或加重,即有效指数≤50%。有效指数=(治疗前积分-治疗后积分)/治疗前积分×100%。治疗总有效率=(痊愈+显效+好转)/总例数×100%。
1.9 统计学分析
采用SPSS 25.0软件进行处理,计数资料以百分率表示,组间比较采用卡方检验;符合正态分布的计量资料以“x±s”表示,组内比较采用配对样本t检验,组间比较采用独立样本t检验,组间比较采用Mann Whitney U秩和检验;等级资料(疗效评价)组间比较采用非参数检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者临床疗效比较
两组患者治疗后,观察组的总有效率87.18%,高于对照组总有效率68.42%,差异有统计学意义(P<0.05)。详见表2。
2.2 两组患者中医证候积分比较
治疗前,两组患者中医证候积分差异无统计学意义(P>0.05)。治疗后,两组患者中医证候积分均降低(P<0.01),且观察组低于对照组(P<0.01)。详见表3。
2.3 两组患者甲状腺功能比较
治疗前,两组患者血清的 TSH、FT3、FT4水平差异无统计学意义(P>0.05)。治疗后,两组患者血清的FT3、FT4水平均降低(P<0.01),且观察组低于对照组(P<0.01);两组患者血清的TSH水平均升高(P<0.01),且观察组高于对照组(P<0.01)。详见表4。
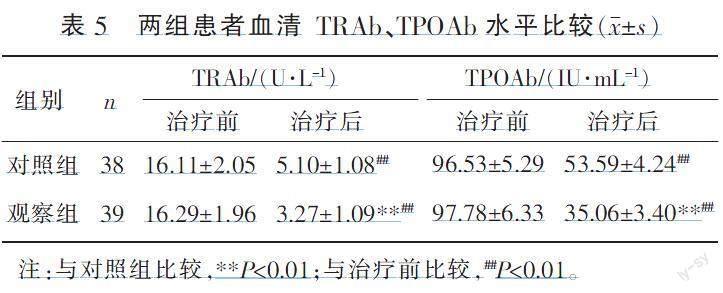
2.4 两组患者甲状腺相关抗体水平比较
治疗前,两组患者血清TRAb、TPOAb 水平差异无统计学意义(P>0.05)。治疗后,两组患者血清的TRAb、TPOAb水平均降低(P<0.01),且观察组低于对照组(P<0.01)。详见表5。
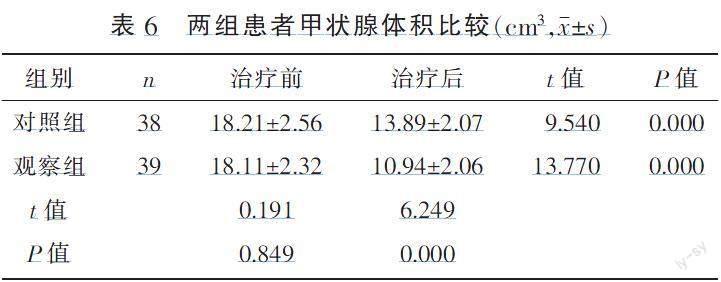
2.5 两组患者甲状腺体积变化
治疗前,两组患者甲状腺体积比较,差异无统计学意义(P>0.05)。治疗后,两组患者甲状腺体积均减小(P<0.01),且观察组小于对照组(P<0.01)。详见表6。
2.6 两组患者STA-PSV变化
治疗前,两组患者STA-PSV差异无统计学意义(P>0.05)。治疗后,两组患者STA-PSV均降低(P<0.01),且观察组低于对照组(P<0.01)。详见表7。
2.7 两组患者临床症状评分比较
治疗前,两组患者甲状腺肿大、怕热多汗、形体消瘦、心慌手抖、眼胀眼突以及胫前黏液性水肿评分差异均无统计学意义(P>0.05)。治疗后,两组患者甲状腺肿大、怕热多汗、形体消瘦、心慌手抖、眼胀眼突、胫前黏液性水肿评分均降低(P<0.01),且观察组低于对照组(P<0.01)。详见表8。
2.8 两组患者SF-36量表评分比较
治疗前,两组患者SF-36评分差异无统计学意义(P>0.05)。治疗后,两组患者SF-36评分均升高(P<0.01),且观察组高于对照组(P<0.01)。详见表9。
2.9 安全性评价
在治疗期间,两组患者均未发生明显不良反应,同时患者的肝肾功能、血常规、心肌酶、心率、脉搏、血压等安全性指标均未见异常。
3 讨论
甲状腺功能亢进症是临床上常见的内分泌系统疾病,因血清中甲状腺激素过量而导致机体出现一系列的临床症状,病变可累及全身多器官、多系统,其中,Graves 病是甲状腺功能亢进症最常见的类型,占80%~85%[2]。《欧洲甲状腺协会:Graves病管理指南(2018版)》[2]表明,Graves病与自身免疫密切相关,甲状腺抗原特异性T细胞通过浸润到表达促甲状腺激素受体(thyrotropin receptor, TSH-R)的组织中,刺激B淋巴细胞分泌刺激性TRAb,与TSH-R结合,导致甲状腺激素紊乱。《中成药辅助治疗甲状腺功能亢进症(Graves病)临床应用指南(2021年)》[11]指出,口服抗甲状腺药物、手术切除、放射性131I是目前临床上治疗Graves病常用的手段,但存在不良反应大、易复发等问题,限制了临床疗效。
中醫学将Graves病归属于“瘿病”范畴。《济生方·瘿瘤论治》言:“夫瘿瘤者,多由喜怒不节,忧思过度,而成斯疾焉。”[12]认为本病与情志有关,情志不畅,肝郁气滞,气滞则津停血瘀,或是肝郁犯脾,脾失健运,津液失布,聚湿成痰,痰气交阻,气血运行不畅,气滞、血瘀、痰凝壅滞于颈前而发病[13]。病久肝阳上亢可见眼突目赤,郁热熏蒸可见怕热多汗,肝郁犯胃可见大便溏薄,耗伤心阴可见心悸失眠,肝肾阴虚、肝风内动可见手足颤动[14]。可见,本病的基本病机为肝气郁结,气滞痰凝,治疗上应标本兼顾,当以行气疏肝,健脾化痰为总治则。加味逍遥散由白芍、当归、茯苓、白术、柴胡、半夏、厚朴、紫苏叶组成。方中柴胡疏肝解郁;白芍养血敛阴,柔肝缓急;白术、茯苓益气健脾,化痰祛湿;当归养血和血;半夏化痰散结,降逆和胃;厚朴燥湿化痰,下气除满;紫苏叶芳香行气疏肝,助厚朴以行气宽胸、宣通郁结。诸药合用,共奏行气疏肝、健脾化痰之功。基于“瘿者由忧恚气结所生”理论,本研究采用具有行气疏肝、健脾化痰的加味逍遥散联合甲巯咪唑片的中西医结合诊疗方案,将有望进一步提高临床疗效,为中医药现代化提供新思路。
TSH是由腺垂体分泌的一种糖蛋白类激素,能够促进甲状腺激素的释放以及T4、T3的合成[15],同时也能促进甲状腺上皮细胞增生,使腺体增大[16]。TSH的分泌受下丘脑分泌的促甲状腺激素释放激素的调节,又受到血清T3、T4的反馈性调节,共同组成下丘脑-腺垂体-甲状腺轴[17-18]。TRAb包括甲状腺兴奋性抗体和甲状腺受体阻断性抗体,二者可与TSH-R上不同靶点结合,发挥不同的效应[19-20]。研究表明[21-22],TPOAb属于自身抑制性抗体,与Graves病高度相关,甲状腺病变后,滤泡细胞结构破坏,甲状腺过氧化物酶可向外周血液溢漏,刺激机体产生TPOAb,破坏甲状腺细胞。SF-36评分量表是目前国际上最常用的慢性病日常生活质量评估工具之一,可用来评价Graves病患者日常生活质量[10]。本研究结果显示,加味逍遥散联合甲巯咪唑片干预后,Graves病患者临床疗效、临床症状评分、中医证候积分、SF-36积分、甲状腺体积改善程度均优于单用甲巯咪唑片,同时可降低患者血清中FT3、FT4、TRAb、TPOAb含量以及STA-PSV,所有患者均未发生明显不良反应,且患者的肝肾功能、血常规、心肌酶等安全性指标均未见异常,说明加味逍遥散与甲巯咪唑片联合使用后,能够有效改善患者症状,提高生活质量,且安全性良好,其作用机制可能与调节免疫、改善甲状腺激素及相关抗体水平有关,仍有待进一步研究。
综上所述,加味逍遥散与甲巯咪唑片有协同作用,可为相关中西医结合治疗提供新方案,但由于样本量较少,观察时间较短,有待进行长期、大样本的研究,以明确其作用的具体机制。
参考文献
[1] ROSS D S, BURCH H B, COOPER D S, et al. 2016 American thyroid association guidelines for diagnosis and management of hyperthyroidism and other causes of thyrotoxicosis[J]. Thyroid: Official Journal of the American Thyroid Association, 2016, 26(10): 1343-1421.
[2] KAHALY G J, BARTALENA L, HEGED?譈S L, et al. 2018 European thyroid association guideline for the management of Graves' hyperthyroidism[J]. European Thyroid Journal, 2018, 7(4): 167-186.
[3] FRANKLYN J A, BOELAERT K. Thyrotoxicosis[J]. The Lancet, 2012, 379(9821): 1155-1166.
[4] 孙江芳. 甲状腺功能亢进症基层诊疗指南(2019年)[J]. 中华全科医师杂志, 2021, 18(16): 1118-1128.
[5] 张伯礼, 吴勉华. 中医内科学: 新世纪第四版[M]. 北京: 中国中医药出版社, 2017: 372-378.
[6] 黄 蓓. 《证候类中药新药临床研究技术指导原则》发布[J]. 中医药管理杂志, 2018, 26(21): 107.
[7] 国家药典委员会. 中华人民共和国药典: 一部[M]. 北京: 中国医药科技出版社, 2020: 155-168.
[8] 杨甲禄. 新药(中药)治疗老年病临床研究指导原则[J]. 中国医药学报, 1989, 4(3): 72-74.
[9] 徐 秋, 王尚臣, 怀 珺, 等. 实用临床中医内科学[M]. 天津: 天津科学技术出版社, 2011: 281-284.
[10] T RRING O, WATT T, SJ LIN G, et al. Impaired quality of life after radioiodine therapy compared to antithyroid drugs or surgical treatment for Graves' hyperthyroidism: A long-term follow-up with the thyroid-related patient-reported outcome questionnaire and 36-item short form health status survey[J]. Thyroid: Official Journal of the American Thyroid Association, 2019, 29(3): 322-331.
[11] 《中成藥治疗优势病种临床应用指南》标准化项目组. 中成药辅助治疗甲状腺功能亢进症(Graves病)临床应用指南(2021年)[J]. 中国中西医结合杂志, 2022, 42(9): 1029-1039.
[12] 赵一璟, 相萍萍, 刘克冕, 等. 泻火消瘿方联合甲巯咪唑片治疗毒性弥漫性甲状腺肿心肝火旺证30例临床观察[J]. 中医杂志, 2017, 58(14): 1209-1213.
[13] 段姗姗, 王永恒, 彭书旺, 等. 基于网络药理学探讨加味逍遥散治疗气滞痰阻型桥本氏甲状腺炎的作用机制[J]. 药物评价研究, 2020, 43(9): 1771-1779.
[14] 张晓军. 柴胡疏肝散加味联合甲巯咪唑片治疗甲状腺功能亢进症疗效观察[J]. 现代中西医结合杂志, 2017, 26(30): 3396-3399.
[15] KOPP P. The TSH receptor and its role in thyroid disease[J]. Cellular and Molecular Life Sciences, 2001, 58(9): 1301-1322.
[16] BABI LEKO M, GUNJA A I, PLEI N, et al. Environmental factors affecting thyroid-stimulating hormone and thyroid hormone levels[J]. International Journal of Molecular Sciences, 2021, 22(12): 6521.
[17] ORTIGA-CARVALHO T M, CHIAMOLERA M I, PAZOS-MOURA C C, et al. Hypothalamus-pituitary-thyroid axis[J]. Comprehensive Physiology, 2016, 6(3): 1387-1428.
[18] FELDT-RASMUSSEN U, EFFRAIMIDIS G, KLOSE M. The hypothalamus-pituitary-thyroid (HPT)-axis and its role in physiology and pathophysiology of other hypothalamus-pituitary functions[J]. Molecular and Cellular Endocrinology, 2021, 525: 111173.
[19] EHLERS M, SCHOTT M, ALLELEIN S. Graves' disease in clinical perspective[J]. Frontiers in Bioscience, 2019, 24(1): 35-47.
[20] L?譫PEZ ORTEGA J M, MART?魱NEZ P S, ACEVEDO-LE?譫N D, et al. Anti-TSH receptor antibodies (TRAb): Comparison of two third generation automated immunoassays broadly used in clinical laboratories and results interpretation[J]. PLoS One, 2022, 17(7): e0270890.
[21] ZHOU Z, LIU L X, JIN M H, et al. Relationships between the serum TPOAb and TGAb antibody distributions and water iodine concentrations, thyroid hormones and thyroid diseases: A cross-sectional study of 2503 adults in China[J]. The British Journal of Nutrition, 2022: 1-11.
[22] BENSE OR I M, JANOVSKY C C P S, GOULART A C, et al. Incidence of TPOAb over a 4-year follow-up period: Results from the Brazilian Longitudinal Study of Adult Health (ELSA-Brasil)[J]. Archives of Endocrinology and Metabolism, 2021, 65(6): 832-840.
(本文编辑 周 旦)
