立足平衡,聚焦转化
2023-08-11谢叶归
谢叶归
(长沙市东雅中学)
转化率及平衡转化率一直是高考的热门考点,试题往往以真实的化工生产为背景,在真实的情境中考查学生的“理解与辨析、归纳与论证”能力,凸显化学学科的社会价值。教育部曾印发《关于做好2022年普通高校招生工作的通知》,进一步深化高校考试招生改革。《通知》要求,稳妥推进高考综合改革,引导减少死记硬背和“机械刷题”现象。笔者对近四年高考试题及2023年浙江省1月真题中有关化学反应平衡试题的命题特点进行了对比分析,总结解答此类问题的策略,避免“题海战术”,以期对师生的高考复习备考有所帮助。
一、近四年高考真题分析
笔者对近四年全国卷及新高考卷(2019~2022)中化学反应原理题进行分析总结,发现考题特征如下:
(1)此类试题大多以真实的工业生产作为载体,体现了真实情境下的项目式教学,试题的陌生程度增大,引导考生提升综合素质。
(2)近四年的高考真题中共出现转化率/化学平衡转化率考点大约29次,近期的2023年浙江省1月份高考试题就出现了3次,转化率/化学平衡转化率年年考,化学平衡图像重点考,变化的是素材,不变的是原理。
(3)试题往往结合化学图像来考查转化率及平衡转化率,试题综合性较大,对考生处理信息的能力提出了较高的要求。
二、解题策略
(一)区分好“转化率”与“平衡转化率”
某一物质的转化率等于该物质在反应中已转化的量与该物质起始总量的比值;某一反应物的平衡转化率α等于该物质在反应达平衡时已转化的量与该物质起始总量的比值。
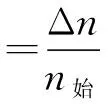
在实际的工业生产中,实际转化率并非平衡转化率。工业生产应该统筹考虑反应限度和反应速率的问题,以实现限定时间内的产量最大。其中,转化率-温度图像能真实地反映化工生产过程,在调控温度时,往往选择以催化剂的活性最高时的温度为最佳温度,此时化学反应速率最大,可实现一段时间内的产量最大化。即转化率可分为非平衡转化率与平衡转化率,非平衡转化率与化学反应速率快慢有关,平衡转化率与化学反应限度有关。
(二)影响“转化率”与“平衡转化率”的因素


表1 反应物不止一种aA(g)+bB(g)cC(g)+dD(g) ΔH<0

表2 反应物只有一种aA(g)bB(g)+cC(g) ΔH<0
(三)催化剂活性、温度对转化率影响的异同
在实际化工生产中,往往采取升温及加入催化剂的方法来提高化学反应速率,从而提高生产效能。从前面分析可知,催化剂不能使平衡发生移动,不能改变化学平衡转化率,但可提高非平衡转化率。对于放热反应,转化率-温度图像往往呈现为“先升后降”,如何正确突破这类图像问题成为高考备考中的难点。

表3

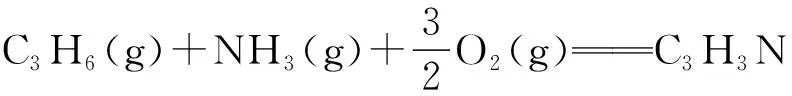

回答下列问题:
如图1为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,有人认为丙烯腈的产率不是对应温度下的平衡产率,其理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(填标号)。
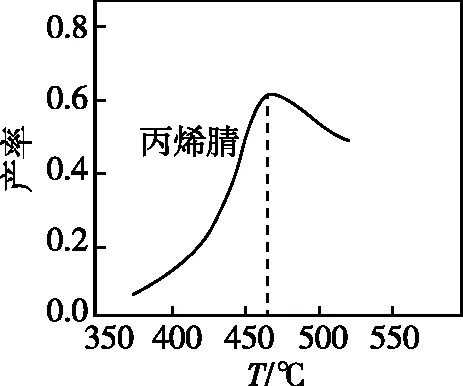
图1
A.催化剂活性降低
B.平衡常数变大
C.副反应增多
D.反应的活化能增大
【答案】该反应为放热反应,平衡产率应随温度升高而降低;AC
三、真题赏析
【例1】(2019年江苏卷,15题)(不定项)在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图2中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
( )
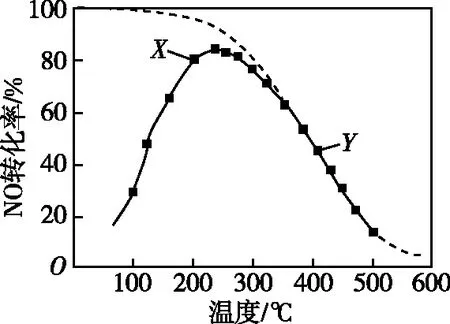
图2
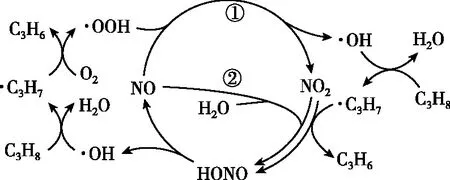
图3

B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×10-4mol·L-1,NO平衡转化率为50%,则平衡常数K>2 000
【答案】BD

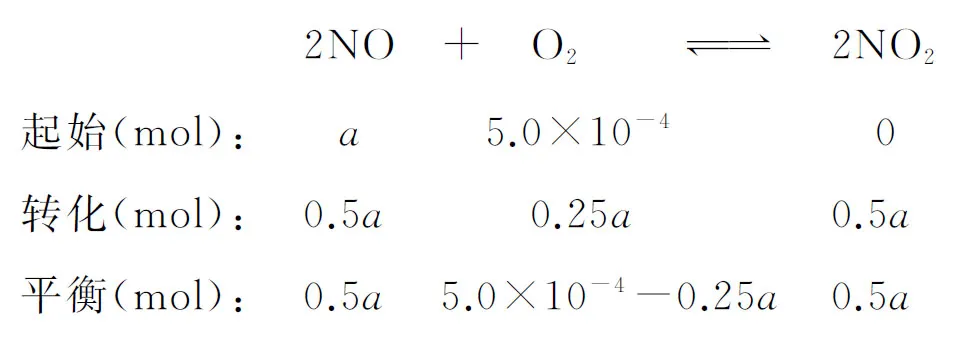

【试题巧解】实线表示催化反应相同时间,不同温度下NO转化为NO2的转化率,虚线表示相同条件下NO的平衡转化率随温度的变化,由解题策略(二)可知,延长反应时间可提高NO转化率,B正确。
【例2】(2022年山东卷,10题)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
( )
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C3H8的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D

【试题巧解】NO是该反应的催化剂,催化剂不改变化学平衡转化率,C正确。
【例3】(2023年1月浙江卷,19题节选)“碳达峰·碳中和”是我国社会发展重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有:

ΔH1=+247 kJ·mol-1,K1

(1)有利于提高CO2平衡转化率的条件是________。
A.低温低压 B.低温高压
C.高温低压 D.高温高压
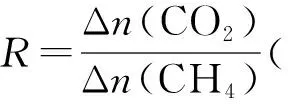
①常压下CH4和CO2按物质的量之比1∶3投料,某一时段内CH4和CO2的转化率随温度变化如图4,请在图5中画出400~1 000℃之间R的变化趋势并标明1 000℃时R值。
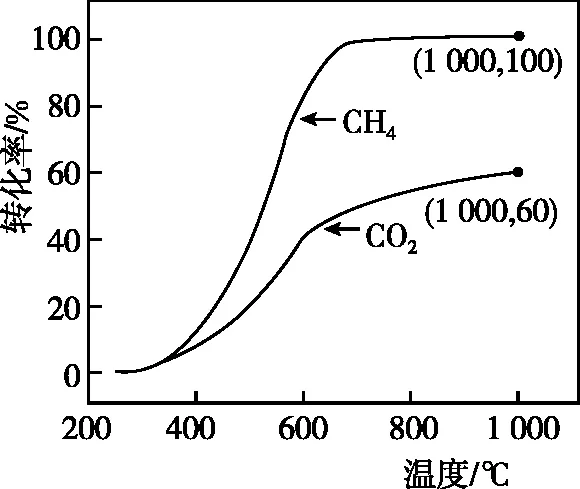
图4
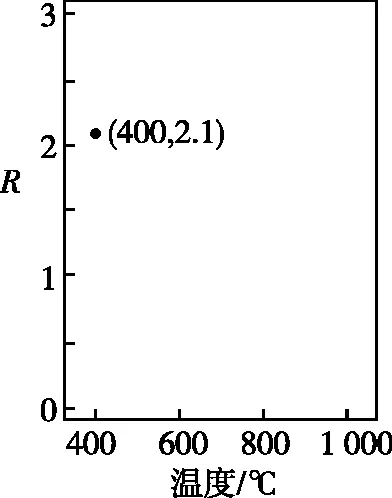
图5
②催化剂X可提高R值,另一时段内CH4转化率、R值随温度变化如表4所示:
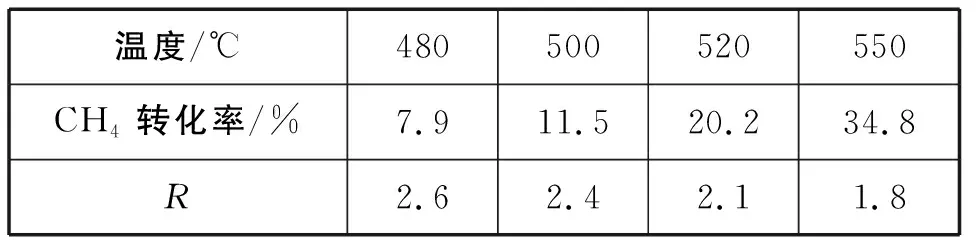
表4
下列说法不正确的是________。
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中H2O占比越高
C.温度升高,CH4转化率增加,CO2转化率降低,R值减小
D.改变催化剂提高CH4转化率,R值不一定增大
【答案】(1)C


四、原创试题赏析
【例4】将CO、O2、H2、N2混合气体在铜-铈氧化物(xCuO·yCeO2,Ce是活泼金属)催化氧化下可除去H2中少量CO,其可能机理如图6所示,CO的转化率随温度变化的曲线如图7所示。已知Ce基态原子核外电子排布式为[Xe]4f15d16s2,下列说法错误的是
( )

图6

图7
A.反应ⅰ中,Cu元素的化合价从+2变成+1,Ce元素的化合价从+4变成+3
B.图中a点所示条件下,延长反应时间能提高CO转化率
C.选择合适的催化剂可减小反应体系中氢气的损耗
D.140℃时曲线上的点为平衡点,继续升温平衡逆向移动导致CO转化率降低
【答案】D

五、总结
从近几年的高考真题可以看出,转化率与平衡转化率已成为落实“变化观念与平衡思想”学科核心素养的重要载体。试题主要以文字叙述及化学平衡图像的形式呈现,能力考查突出,情境设置新颖,试题呈现灵活。落脚点往往是考查读取图表信息的能力以及利用题目给予的新信息解决问题的能力。充分体现了高考试题的基础性和创新性,符合高考评价体系的要求。
此外,通过研究高考真题不难发现,转化率及平衡转化率的考查始终稳中求新、稳中求变,变化的是题材,不变的是基本考点,在复习备考中,做到深研真题、发掘规律、精准备考,定能事半功倍。
