华氏巨球蛋白血症合并新型冠状病毒肺炎1例*
2023-08-01曹国君吴之源
项 瑾,曹国君,陈 锟,吴之源,关 明
复旦大学附属华山医院检验科,上海 201907
淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)是一种少见的惰性成熟B细胞淋巴瘤,在非霍奇金淋巴瘤中所占比例<2%。LPL侵犯骨髓同时伴有血清单克隆性免疫球蛋白(Ig)M时诊断为WM[1]。WM好发于60岁以上老年人,临床诊断中易与IgM型多发性骨髓瘤混淆[2]。有研究报道,新型冠状病毒感染(COVID-19)流行期间,WM患者感染新型冠状病毒(SARS-CoV-2)风险增加,感染后易发生严重并发症[3]。目前国内尚未见WM合并COVID-19的病例报道。本研究报道的1例高龄女性患者以全血细胞减少为首发症状,有代谢性疾病及脑出血史,在确诊普通型COVID-19后鼻咽拭子SARS-CoV-2核酸检测结果连续40 d呈阳性。入院后通过免疫固定电泳和骨髓形态学等实验室检测确诊为WM。本报道旨在提高临床工作者对于WM的认识,并为WM患者合并COVID-19的诊治提供参考。
1 病例资料
患者,女,87岁,2022年4月30日SARS-CoV-2核酸检测结果阳性,外院治疗3周后未转阴,转至复旦大学附属华山医院宝山院区继续进行隔离观察。2022年5月27日入院时SARS-CoV-2 ORF1ab基因Ct值为32.32,N基因Ct值为29.11。入院时无发热、咳嗽、鼻塞等症状,无明显呼吸困难、气急表现,体温36.7 ℃,呼吸16次/分,脉率86次/分,血压127/66 mmHg,氧饱和度99%,生命体征平稳。患者神志不清,面色萎黄,右前臂可见点片状皮下出血灶。胸部CT可见病毒性肺炎征象。头颅CT提示右侧颞叶脑出血可能,两侧基底节区及半卵圆区缺血灶。患者红细胞计数(RBC)1.34×1012/L,白细胞计数(WBC)1.51×109/L,血红蛋白(Hb)47 g/L,血小板计数(PLT)70×109/L。血糖8.3 mmol/L;糖化血红蛋白12.57%。临床初步诊断:(1)COVID-19普通型;(2)全血细胞减少,巨幼细胞性贫血;(3)脑出血恢复期;(4)原发性高血压2级;(5)2型糖尿病。
2 实验室和影像学检查
患者2022年6月4日血清免疫固定电泳提示单克隆条带异常增强,表现为IgM-κ型,见图1。IgM 34.50 g/L,总蛋白(TP)67.9 g/L,清蛋白(Alb)29.8 g/L,白球比例0.8,β2微球蛋白7.06 mg/L,游离κ轻链(κFLC)32.50 mg/L,游离λ轻链(λFLC)32.20 mg/L,乳酸脱氢酶(LDH)155 U/L。白细胞介素(IL)-1β 12.60 pg/mL,IL-2受体>7 500.00 U/mL,IL-6 30.10 pg/mL,IL-8 44.10 pg/mL,IL-10 20.80 pg/mL,肿瘤坏死因子α 39.50 pg/mL。尿培养结果提示肺炎克雷伯菌、阴沟肠杆菌与光滑假丝酵母菌混合感染。
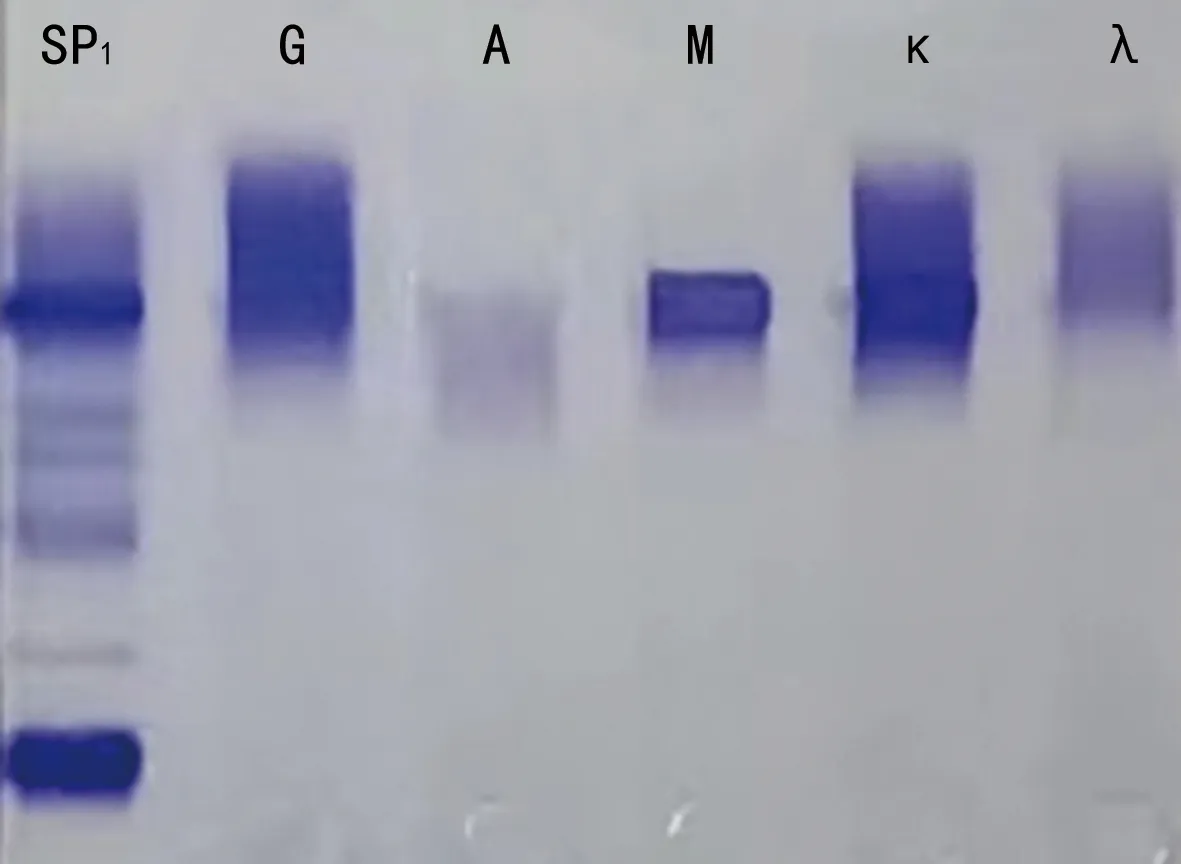
图1 患者血清免疫固定电泳结果
骨髓细胞学检查见形态较单一的异常小淋巴细胞异常增殖,以成熟型为主,淋巴样浆细胞细胞占比16%。粒系细胞比例减少,中晚幼粒细胞以上阶段细胞比例明显减少,部分成熟中性粒细胞可见颗粒增多、增粗、核分叶过多及空泡现象,红系比例明显减少。部分成熟红细胞呈缗钱状排列。还可见少量单核组织巨噬细胞,偶见噬血现象。全片见巨核细胞24只,其中颗粒型18只,4只产板型,2只裸核。成熟血小板散在或成小簇可见,片上可见簇状分布的异常小淋巴样细胞及淋巴样浆细胞。见图2。

注:A为淋巴样浆细胞呈弥漫性增生,细胞体积中等或偏小,呈圆形或类圆形,细胞质量少,色蓝,部分有空泡,细胞核呈圆形、类圆形、椭圆形或不规则形,偶见扭曲及折叠;B为成堆分布的淋巴样浆细胞,细胞体积中等,细胞质色蓝、部分有空泡;C为聚集分布的淋巴样浆细胞,核染色质较疏松,幼稚型可见核仁;D为聚集分布的淋巴样浆细胞。
患者入院后行胸部CT检查,见图3。显示双肺有散在炎症,有病毒性肺炎的可能,双侧有少许胸腔积液,双肺散在肺大泡,左肺上叶钙化灶,冠脉钙化。甲状腺两叶结节伴钙化。头颅CT扫描提示,右额颞叶梗死后;右侧脑室后角旁线状高密度影,少许出血灶可能;双侧额顶叶、基底节区、侧脑室旁缺血腔隙灶,脑萎缩;鼻旁窦炎症。四肢血管彩色多普勒超声检查提示:右侧股静脉内血栓形成,余双下肢深静脉血流尚通畅;双下肢动脉内中膜多发斑块,血流通畅。

图3 患者胸部CT检查
3 诊断和治疗
患者新型冠状病毒核酸检测结果呈阳性,具有肺部影像学表现,COVID-19普通型诊断明确[4]。患者血清中检测到单克隆性的IgM。骨髓中浆细胞样小淋巴细胞侵犯小梁间隙,诊断为WM,可与IgM型意义未明的单克隆免疫球蛋白血症、IgM型多发性骨髓瘤等鉴别。前者仅表现为血清单克隆IgM异常增生,常小于30 g/L,而且无骨髓中浆细胞浸润、其他B淋巴细胞增殖性疾病、相关器官或组织受损的证据;后者非常少见,细胞形态学为浆细胞形态,常伴溶骨性损害[1,5]。根据目前WM的预后判断系统Revised IPSSWM(rIPSSWM)[6],患者年龄87岁,大于75岁;β2微球蛋白7.06 mg/L,大于4 mg/L;LDH 155 U/L,小于250 U/L;Alb 29.8 g/L,小于35 g/L。累计4分,判为极高危组,WM 3年病死率48%,5年生存率36%,预后较差。
患者入隔离点后予以对症支持及医学观察,症状改善。予以奈马特韦/利托那韦片抗病毒、胸腺肽调节免疫及中药辅助治疗。患者Hb 47 g/L,2022年6月8日输注红细胞悬液2 U,输注后复查Hb 66 g/L,输注有效。予以维生素B12、叶酸治疗,粒细胞集落刺激因子皮下注射,WBC、PLT有所上升,较前好转,皮下出血灶较前明显减少。考虑全血细胞减少与肿瘤骨髓浸润有关,予以泽布替尼160 mg鼻饲(每日2次),血小板恢复正常,贫血较前好转。病程中发现股静脉血栓,但患者存在血小板减少,有可疑脑出血,存在抗凝禁忌未予以抗凝治疗。予以头孢哌酮舒巴坦联合多西环素治疗尿路感染,较前好转,停用抗菌药物。监测血糖,根据血糖水平调整胰岛素用量。予以沙库巴曲缬沙坦控制血压,美托洛尔控制心率。患者于2022年6月8日、6月15日连续多次新型冠状病毒核酸检测阴性,贫血状况较前改善,病情平稳。
4 讨 论
全血细胞减少本身不是一种疾病,却是一种疾病诊断的标志[7]。当机体感染SARS-CoV-2后,通过大量的细胞因子风暴和骨髓浸润作用,可引起血细胞的减少,其中主要以淋巴细胞减少为特征。在免疫力正常人群中,全血细胞减少作为COVID-19并发症的案例鲜有报道[8-9]。高龄患者机体功能整体退化,各项检测指标可能出现生理性异常。本例报道提示当这一类群体出现贫血、全血细胞减少时,不能排除血液系统疾病抑制骨髓造血可能。
WM发病率约为0.57/100 000,男性高于女性[10],作为一种惰性疾病,约25%的患者在诊断时无症状[11],极易发生漏诊和误诊,贫血是WM最常见临床表现和最主要的治疗指征[1]。世界卫生组织造血和淋巴组织肿瘤分类规定LPL的诊断包括[12]:(1)由小B淋巴细胞、浆细胞样淋巴细胞和浆细胞组成的淋巴瘤;(2)通常侵犯骨髓,也可侵犯淋巴结和脾脏;(3)不符合其他可能伴浆细胞分化的小B细胞淋巴瘤诊断标准。而将LPL浸润骨髓同时分泌单克隆性IgM者定义为WM。因此WM的诊断需要满足两大条件:(1)病理检查证实淋巴浆细胞侵犯骨髓;(2)外周血检测到单克隆IgM增高。此外,免疫表型和MYD88 L265P突变是WM诊断的重要标志,后者发生率达90%以上[5],但非特异性的诊断指标。本例报道中患者血清游离轻链结果高于正常值,免疫固定电泳结果提示IgM单克隆性增生,骨髓细胞学检查中淋巴样浆细胞弥漫性增生对于疾病的诊断与鉴别诊断起关键作用。由于WM起病隐匿,临床表现症状不具有特异性,可将血清电泳列为常规检测项目,如出现M蛋白阳性时可进一步进行骨髓穿刺观察形态学有无改变以进行鉴别诊断,必要时还可进行免疫表型和MYD88基因检测,以提高疾病诊断效率。
WM作为一种不可治愈的疾病,治疗指征在于出现症状,治疗目标在于缓解症状。当WM合并COVID-19时,需要根据原发疾病的轻重缓急、SARS-Cov-2变异株的毒性、患者的身体状况权衡抗肿瘤治疗的利弊并确定治疗时机。初诊的WM患者若临床表现为无症状则建议暂缓治疗。当合并显著临床症状时,评估结果为适合布鲁顿氏酪氨酸激酶抑制剂(BTKi)治疗的患者应优先考虑使用BTKi治疗[13]。BTK是一种非受体酪氨酸激酶,其在B淋巴细胞的发育、成熟、分化和增殖中起重要作用[14]。本例报道中,患者确诊WM后使用的泽布替尼是一种强效的BTKi。美国食品药品监督管理局于2021年8月31日批准泽布替尼用于治疗WM。相较于上一代BTKi伊布替尼,泽布替尼靶点占有率更高、选择性更强、抑制更持久,可进一步改善WM患者预后[15-16]。近期研究提出泽布替尼对于COVID-19患者的治疗价值,包括可提高患者氧饱和度、减少病毒感染症状、降低血栓和高凝状态的发生[14]。然而,用药同时需要警惕BTKi的免疫调节和抗炎反应,以及停药可能带来的潜在风险——细胞因子风暴和高黏滞将加重COVID-19后期并发症的发生[3]。CASTILLO等[17]报道,20%使用一代BTKi伊布替尼治疗的WM患者停药时出现以发热、全身疼痛、头痛、关节痛为主的“伊布替尼戒断”症状。MAYNARD等[18]报道1例接受一代BTKi伊布替尼治疗的81岁男性WM患者在确诊COVID-19后停药,继而出现呼吸困难、氧饱和度下降等症状,进入ICU使用无创通气,并且在恢复BTKi伊布替尼足剂量每日单次420 mg给药、合并使用瑞德西韦抗病毒治疗后,患者症状缓解,逐步好转,治疗19 d后恢复自主呼吸,撤除供氧设备。
综上所述,当患者合并COVID-19时,特别是高龄患者,核酸转阴时间更长,同时对于原发疾病的诊断和治疗趋于复杂化。WM发病率低,临床少见,此时血清免疫球蛋白、免疫固定电泳和骨髓形态学等多种常规实验室检测结果对其诊断与鉴别诊断有重要价值。此外,BTKi等抗肿瘤药物对于COVID-19的治疗价值同样值得更进一步的深入研究。
