EGFR 基因突变非小细胞肺癌患者临床特征及酪氨酸激酶抑制剂疗效分析*
2023-07-26杜迪,栗静,程烨,戴助
杜 迪,栗 静,程 烨,戴 助
(湖北省肿瘤医院,湖北 武汉 430079)
肺癌是全球致死人数最多的癌种,据全球最新癌症负担数据(GLOBCAN 2020)及我国国家癌症中心2020 年更新的统计数据[1-2],全球共有1 796 144 例肿瘤患者,我国有631 000 例患者死于肺癌。非小细胞肺癌(NSCLC)占肺癌患者的85%~90%,其中大多数患者确诊时即为晚期或转移性,已不适合手术切除。表皮生长因子受体(EGFR)基因突变在NSCLC 患者中最常见。其中超过85%的为第19 外显子的缺失(E19 DEL)及第21 外显子中第858 位亮氨酸由精氨酸取代(E21 L858R)[3-4],而第20 外显子插入(E20 ins)等突变较少见。其中部分患者存在多个EGFR基因位点的突变(即复合突变),或合并其他基因突变(即共突变)。酪氨酸激酶抑制剂(TKI)已成为EGFR基因敏感突变NSCLC患者的晚期一线治疗方案,其缓解率为70%~80%,中位无进展生存期(mPFS)为10~12 个月[5-6]。TKI 较一线常规含铂双药化学药物治疗(简称化疗)已显示出良好的缓解率与生存获益[7-9]。但数据主要来自Ⅲ期、随机、对照临床试验,且缺乏TKI 之间基于真实世界数据的比较。本研究旨在明确EGFR基因突变NSCLC患者的临床特征及TKI 一线治疗方案,并进一步分析突变类型、治疗方案与疗效之间的相关性。现报道如下。
1 资料与方法
1.1 一般资料
选取2020年1月至11月在湖北省肿瘤医院行EGFR基因突变检测的NSCLC 患者280 例,排除病例记录不完整患者7 例,实际纳入273 例,患者均经病理学检查确诊。统计患者的性别、年龄、吸烟史、肿瘤家族史、病理类型、肿瘤分期、肿瘤部位、淋巴结转移、远处转移等情况。TKI一线治疗患者均随访至2021年5月31日或发生疾病进展(以先发生者为准)。本研究经医院医学伦理委员会批准。
1.2 基因突变检测及疗效评价
患者标本包括手术标本、活检物和外周血。采用血清/血浆核酸纯化试剂盒提取患者DNA,以高通量测序仪进行基因测序,检测范围包括常见NSCLC 相关驱动基因改变(EGFR基因突变、ALK基因融合、HER2基因突变、BRAF基因突变、ROS1基因融合、MET基因突变、KRAS基因突变、MET基因扩增、RET基因融合)。EGFR基因常见单点突变定义为E19 DEL 和E21 L858R,少见单点突变定义为其他单点突变,复合突变定义为同一组织标本中检测出至少2 个EGFR基因突变,共突变定义为同一组织标本中检测出BRAF/KRAS/ROS1/MET/NTRK3等基因突变与EGFR基因突变同时存在。患者接受TKI 治疗前均进行影像学检查并由医师依据实体瘤疗效评价标准(RECIST,1.1 版)评估基线水平,PFS 定义为从接受TKI 一线治疗开始至肿瘤进展或死亡的时间。
1.3 统计学处理
2 结果
2.1 患者临床特征
结果见表1。患者年龄31~85岁,中位年龄63 岁。
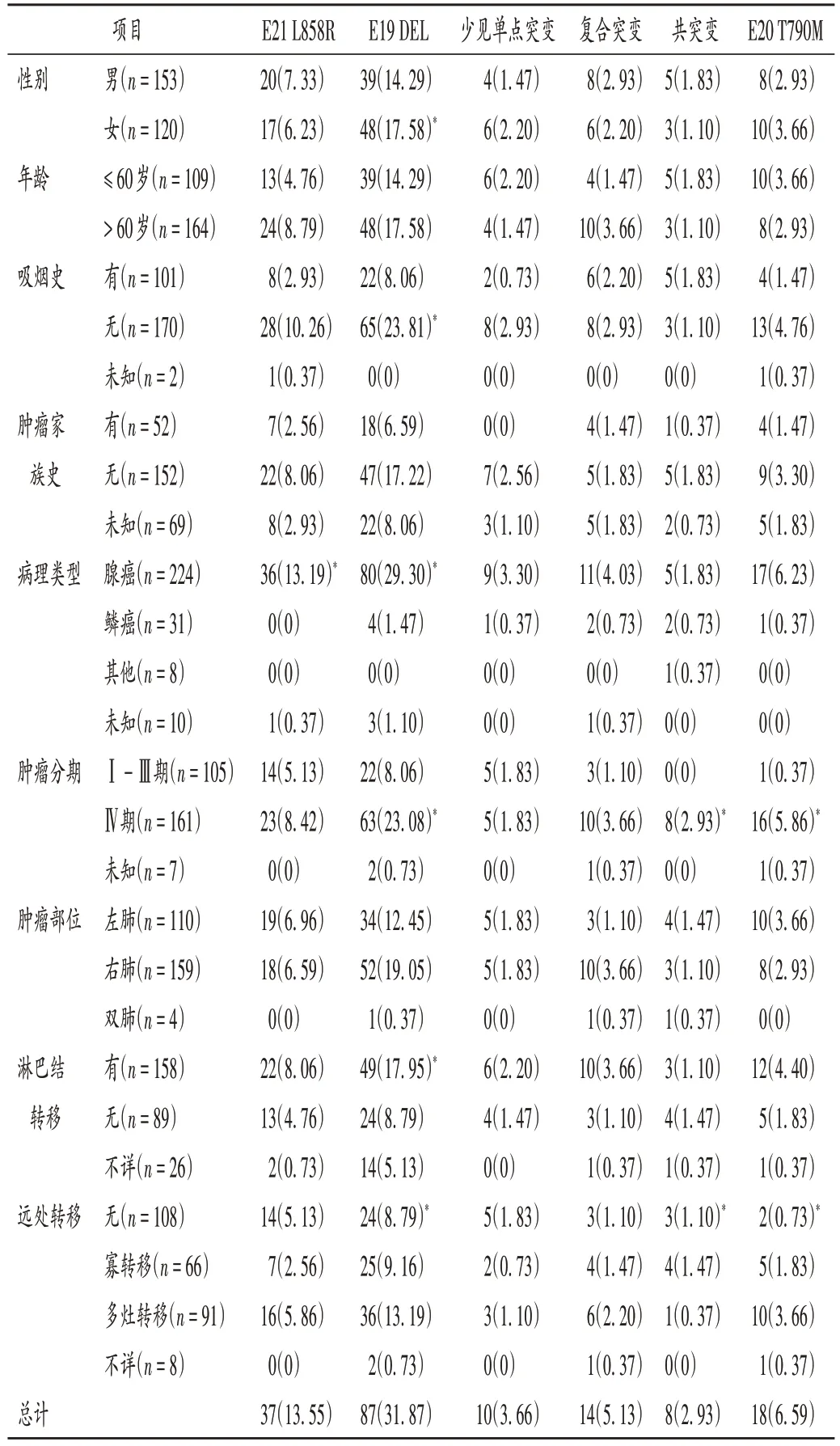
表1 纳入患者临床特征及与基因突变的相关性[例(%),n=273]Tab.1 Clinical characteristics of included patients and their correlation with gene mutations[case(%),n=273]
2.2 EGFR 突变的单因素分析
156 例(57.14%)患者检测到EGFR基因突变。单因素分析结果显示,E19 DEL 突变与女性(P=0.011)、无吸烟史(P=0.008)、腺癌(P=0.003)、肿瘤分期为Ⅳ期(P= 0.007)、淋巴结转移(P= 0.033)、存在远处转移(P= 0.035)显著相关,E21 L858R 突变与腺癌(P=0.006)显著相关;共突变与肿瘤分期为Ⅳ期(P=0.013)和存在远处转移(P= 0.029)显著相关;肿瘤分期为Ⅳ期(P=0.003)和存在远处转移(P=0.040)患者与经TKI 一线治疗后检测到的E20 T790M 突变显著相关。详见表1。EGFR突变类型及频率见表2。

表2 EGFR基因突变类型及频率[例(%),n=156]Tab.2 EGFR gene mutation types and frequencies[case(%),n=156]
2.3 PFS 单因素分析及生存分析
156 例EGFR基因突变患者中,99 例接受TKI 一线治疗,方案包括吉非替尼、埃克替尼、阿法替尼、厄洛替尼、奥希替尼。单因素分析结果显示,性别(P=0.460)、年龄(P=0.785)、吸烟史(P=0.436)、肿瘤家族史(P=0.851)、病理类型(P=0.274)、肿瘤分期(P=0.496),均与PFS无相关性(P>0.05)。99 例患者的mPFS 为8.0 个月,其中共突变患者的PFS 最短,但不同突变、不同用药患者间PFS 比较,差异无统计学意义(P> 0.05)。患者临床特征与PFS关联分析结果见表3。Kaplan-Meier 生存曲线见图1。
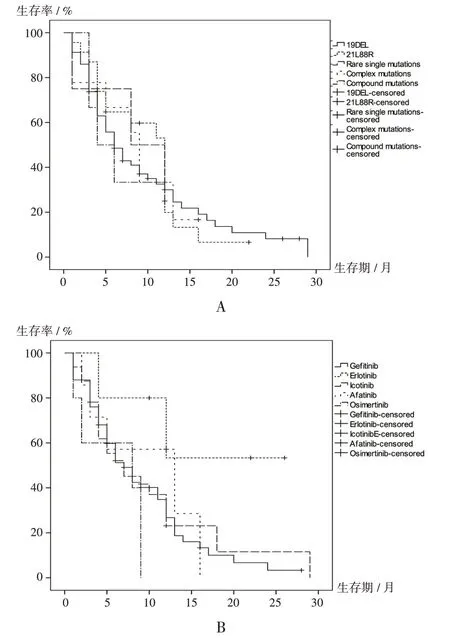
图1 Kaplan-Meier无进展生存情况分析Fig.1 Kaplan-Meier curve analysis of PFS

表3 TKI一线治疗患者临床特征与PFS的相关性(n=99)Tab.3 Correlation of clinical characteristics and PFS in patients receiving TKI first-line treatment(n=99)
3 讨论
目前,TKI 已成为晚期NSCLCEGFR基因敏感突变患者的一线治疗方案。EGFR致癌突变引起酪氨酸激酶结构域介导的信号通路被激活,TKI 通过与EGFR 酪氨酸激酶胞内结构域结合,中止EGFR 的自磷酸化,抑制下游信号通路[10],从而发挥抗肿瘤作用。如在肺癌中,TKIs 通过阻断RAS - RAF - MEK - ERK、PI3K -AKT-mTOR 和JAK-STAT3 等与细胞转移、增殖和抑制细胞凋亡相关的信号通路[11-13],致肿瘤细胞生长停滞和凋亡[14]。
本研究中首先分析了EGFR基因突变类型与临床特征的相关性,结果超半数检测到EGFR基因突变,并涵盖多种突变类型,其中共突变主要涉及KRAS/MET扩增/NTRK3融合。相关性分析结果显示,女性、无吸烟史、腺癌、存在淋巴结转移、肿瘤分期为Ⅳ期和存在远处转移患者与EGFRE19 DEL 突变存在相关性;EG⁃FRE21 L858R 突变仅与腺癌相关。肿瘤分期为Ⅳ期、存在远处转移患者发生共突变和一线TKI 治疗后E20T790M 耐药突变的风险更高。在既往的研究报道中,EGFR基因突变NSCLC 患者多见于腺癌、女性、无吸烟史、东亚人群[3,15-17]。这一结论与本次观察到的E19 DEL 突变情况一致,但E21 L858R 仅观察到与腺癌有相关性,这种差异可能与样本量较小有关。
本研究中随后对第1,2,3 代TKI 的疗效进行了分析。结果显示,不同治疗方案、不同EGFR基因型患者间PFS 均无显著差异。可见,携带EGFR基因突变的NSCLC 患者,无论是何种基因突变类型抑或接受何种治疗方案,均能从TKI 治疗中获益,这一结论与既往研究一致[18-21]。但本研究中观察到,服用第3 代TKI 奥希替尼患者的PFS与其他患者间比较无统计学差异,这一结论与FLAURA 研究相悖。这5例患者均为晚期且存在远处转移,其中2 例患者为全身多发转移,加之纳入样本量较少,结果可能存在偏倚。同时,由于TKIs 序贯治疗策略,患者在未发生进展的情况下序贯药物对一线治疗药物PFS的影响(如药物可及性、经济状况、不良反应等)导致更改治疗方案等混杂因素未纳入本研究中,致使该部分结论的临床价值有限,有待纳入更多样本数据及相关因素,进一步分析,以评估第3 代TKI 在真实世界中的疗效。因此,在一线TKI 药物选择上应纳入更多考量因素,如基础疾病和合并用药,对于既往存在心脏疾病,尤其是Q - T 间期延长的患者,应尽量避免选用奥希替尼;患者如长期服用质子泵抑制剂,则势必影响吉非替尼、厄洛替尼、达可替尼的疗效[22-25]。
综上所述,本研究报告了基于真实世界数据的NSCLC 患者的临床特征与EGFR基因突变类型的相关性,以及不同TKI 一线治疗方案的疗效差异,可为临床治疗不同EGFR基因突变NSCLC患者提供一定参考。但本研究属回顾性研究,存在局限性,且患者数据来源于单中心,样本量较小,复合突变及共突变患者的进一步疗效分析尚需更大样本量的数据支持。
