预防性延伸野放疗联合同步化疗与盆腔野放疗联合同步化疗治疗局部晚期宫颈癌的近远期疗效及安全性对比▲
2023-07-17张贤雨郝晓慧刘晓玉张志林
张贤雨 马 欢 郝晓慧 刘晓玉 原 娜 席 强 张志林
(河北北方学院附属第一医院放疗科,河北省张家口市 075000)
宫颈癌是女性生殖系统常见的恶性肿瘤之一,其患病率近年来逐年升高。早期宫颈癌症状不典型,多数患者首次确诊时已处于中晚期。在宫颈癌进展过程中,淋巴结转移是肿瘤转移扩散的主要途径,包括盆腔淋巴结转移及腹主动脉旁淋巴结(para-aortic lymph node,PALN)转移等[1]。研究显示,淋巴结转移是影响宫颈癌患者预后的独立危险因素,尤其是PALN转移的发生往往预示着不良预后[2]。同步放化疗是目前治疗局部晚期宫颈癌的标准方案,盆腔是放疗的常规外照射范围,延伸野放疗则是在盆腔野照射的基础上增加PALN引流区的照射[3]。美国国家综合癌症网络指南明确指出,对合并有PALN转移的宫颈癌患者,必须行腹主动脉旁延伸野放疗。然而,针对PALN阴性的宫颈癌患者是否需要行预防性延伸野放疗,国内外尚未形成共识[4-5]。为进一步探讨预防性延伸野放疗在无PALN转移的局部晚期宫颈癌患者中的应用价值,本研究对比预防性延伸野放疗联合同步化疗与盆腔野放疗联合同步化疗治疗局部晚期宫颈癌的近远期疗效与安全性。现报告如下。
1 资料与方法
1.1 临床资料 选择2017年1月至2018年10月河北北方学院附属第一医院收治的初次接受治疗的90例局部晚期宫颈癌患者作为研究对象。纳入标准:(1)患者经组织病理学检查确诊为宫颈癌,且国际妇产科联盟分期为ⅡB~ⅣA期。(2)经电子计算机断层扫描确诊为无PALN转移的宫颈癌,且至少伴有以下情况之一者。① 盆腔淋巴结转移数目≥2枚,② 盆腔转移淋巴结短径≥1.5 cm,③ 经妇科检查或磁共振成像确诊宫旁受累达盆壁。(3)自愿签署知情同意书。(4)首次接受治疗。(5)Karnofsky功能状态量表(Karnofsky Performance Status,KPS)评分≥70分。(6)年龄≤70岁。(7)血常规、肝肾功能正常。(8)认知功能良好,可正常沟通交流。排除标准:(1)合并其他脏器恶性肿瘤者;(2)伴有心肺肝肾等重要器官功能障碍者;(3)合并凝血功能异常者;(4)既往有宫颈或盆腔手术史者;(5)既往有放疗或化疗史者;(6)妊娠期或哺乳期妇女;(7)合并严重内科疾病者。采用随机数字表法将患者分成观察组与对照组,每组45例。观察组患者年龄41~70(55.32±8.3)岁;临床分期为ⅡB期8例,Ⅲ期15例,ⅣA期22例。对照组患者年龄43~68(54.08±9.5)岁;临床分期为ⅡB期10例,Ⅲ期16例,ⅣA期19例。两组患者的年龄、临床分期比较,差异均无统计学意义(均P>0.05),具有可比性。本研究经河北北方学院附属第一医院医学伦理委员会批准同意。
1.2 治疗方法 (1)观察组采用预防性延伸野放疗联合TP方案(紫杉醇+顺铂)同步化疗。放疗方案为延伸野照射联合腔内后装照射。① 延伸野照射(体外照射):照射区域为盆腔及PALN引流区,上界为左侧肾静脉水平,下界根据阴道累及情况决定,采用6MV-X线直线加速器(仪器为Elekta Infinity 6MV/10MV直线加速器)调强放疗,计划靶区(planning target volume,PTV)45~50.4 Gy,转移淋巴结靶区(positive lymph node,pGTVnd)54~63 Gy,5次/周。② 腔内后装照射:于体外照射第4周开始,使用Ir-192后装治疗机(仪器为山东新华XHDR18/XHDR18B/XHDR18F γ射线近距离遥控后装治疗机)进行腔内后装照射,宫旁A点(宫颈口上2 cm、宫轴线旁2 cm的位置)剂量为6 Gy/次,1次/周,共5次,腔内后装放疗当日暂停体外照射。在8周内完成放疗。③ TP方案同步化疗:于体外照射第1天开始同步进行化疗,化疗方案为紫杉醇注射液(海南新世通制药有限公司,规格为5 mL:30 mg,产品批号:20151104、20170106、20180305)175 mg/m2+注射用顺铂(锦州九泰药业有限责任公司,规格为20 mg/支,产品批号:1510216、1701063、1802154)75 mg/m2,化疗周期为21~28 d,8周共化疗1~2次。(2)对照组予以盆腔野放疗联合TP方案同步化疗。放疗方案为盆腔野照射联合腔内后装照射。盆腔野照射(体外照射):照射区域为盆腔,运用6MV-X线直线加速器(设备同观察组)调强放疗,PTV 45~50.4 Gy,5次/周。腔内后装放疗过程与方案、TP同步化疗方案同观察组。
1.3 观察指标 (1)近期疗效:于同步放化疗方案结束后4周,结合妇科查体及盆腔CT检查结果,由2位副主任及以上职称的医生按实体瘤疗效评价标准(RECIST 1.1)[6]评价患者的近期疗效。完全缓解为治疗后靶病灶全部消失;部分缓解为治疗后靶病灶最长径之和较治疗前减少≥30%;疾病进展为治疗后靶病灶最长径之和较治疗前增加≥20%,或出现1个或多个新病灶;病情稳定为介于部分缓解和疾病进展之间。客观缓解率=(完全缓解+部分缓解)例数/总例数×100%。(2)血清学肿瘤标志物水平:分别于治疗前和治疗结束后4周,采集患者空腹肘静脉血3 mL,以3 000 r/min离心10 min分离血清,通过化学发光免疫分析仪(北京科美生物技术有限公司,CHEMCLIN1500型)检测血清鳞状细胞癌相关抗原(squamous cell carcinoma associated antigen,SCCA)、癌胚抗原及糖类抗原50(carbohydrate antigen 50,CA50)水平,严格按照试剂盒说明书进行操作,试剂盒均购自北京华科泰生物技术有限公司(批号分别为:201612003、201711009,201611012、201709008,201610025、201710038)。(3)毒副反应发生情况:于同步放化疗结束后4周,按美国肿瘤放射治疗协作组分级标准[7]及美国国立癌症研究所常见毒性事件标准5.0版[8]评价受试对象放化疗毒副反应发生情况,包括骨髓抑制、消化系统毒副反应、泌尿系统毒副反应、放射性直肠炎、放射性膀胱炎等,各类型毒副反应均按严重程度分为0~Ⅳ度(除消化系统毒副反应无Ⅳ度外)。① 骨髓抑制。0度为无改变;Ⅰ度为轻微细胞过少或与该年龄段的正常细胞总数相比减少≤25%;Ⅱ度为中度细胞过少或与该年龄段的正常细胞总数相比减少>25%且≤50%;Ⅲ度为重度细胞过少或与该年龄段的正常细胞总数相比减少>50%且≤75%;Ⅳ度为骨髓细胞再生障碍持续≥2周或患者死亡。② 消化系统毒副反应(以腹胀、腹痛为例)。0度为无腹胀腹痛;Ⅰ度为无腹胀症状或轻度腹痛,仅为临床或诊断所见,无需治疗;Ⅱ度为有腹胀症状或中度腹痛,工具性日常生活活动受限;Ⅲ度为极度腹胀不适或重度疼痛,自理性日常生活活动受限;Ⅳ度不存在。③ 泌尿系统毒副反应(以血尿为例)。0度为无症状,无需治疗;Ⅰ度为有症状,需导尿或清洗膀胱,影响工具性日常生活活动;Ⅱ度为大量血尿,需输血、静脉给药或住院治疗,需择期行侵入性治疗,个人活动能力受限;Ⅲ度指症状危及生命,需紧急行侵入性治疗;Ⅳ度指造成患者死亡。④ 放射性直肠炎。0度为无变化;Ⅰ度为轻度腹泻、轻度肠痉挛、较少直肠渗液或出血;Ⅱ度为中度腹泻,中度肠痉挛,大便次数>5次/d,过多直肠渗液或间歇出血;Ⅲ度为肠梗阻或出血需手术处理;Ⅳ度为肠坏死、穿孔或窦道形成。⑤ 放射性膀胱炎。0度为无变化;Ⅰ度为膀胱上皮轻度萎缩,膀胱轻度毛细血管扩张(显微镜下血尿);Ⅱ度为中度尿频,广泛毛细血管扩张,间歇性肉眼血尿;Ⅲ度为重度尿频,排尿困难,重度广泛毛细血管扩张(常伴瘀斑),常见血尿,膀胱容量减少(<150 mL);Ⅳ度为坏死缩窄性膀胱(容量<100 mL),重度出血性膀胱炎。(4)远期疗效:以患者开始放疗为随访起点,共随访3年,以患者死亡、失访或随访截止为随访终点。比较两组患者3年总生存率、无进展生存率及PALN控制率,PALN控制率=未发生PALN转移例数/总例数×100%。
1.4 统计学分析 采用SPSS 25.0软件进行统计学分析。计量资料以(x±s)表示,组间比较采用两独立样本t检验,组内治疗前后的比较采用配对t检验;计数资料以例数(百分比)表示,组间比较采用χ2检验。以P<0.05为差异具有统计学意义。
2 结 果
2.1 两组患者近期疗效的比较 90例患者均顺利完成既定方案治疗。观察组客观缓解率为88.89%(40/45),对照组为80.00%(36/45),两组客观缓解率差异无统计学意义(χ2=1.353,P=0.245)。见表1。

表1 两组患者近期疗效的比较[n(%)]
2.2 治疗前后两组患者血清学肿瘤标志物水平的比较 治疗前,两组患者血清SCCA、癌胚抗原和CA50水平比较,差异均无统计学意义(均P>0.05);治疗后,两组患者血清SCCA、癌胚抗原和CA50水平均较治疗前降低,且观察组上述指标水平均低于对照组(均P<0.05)。见表2。
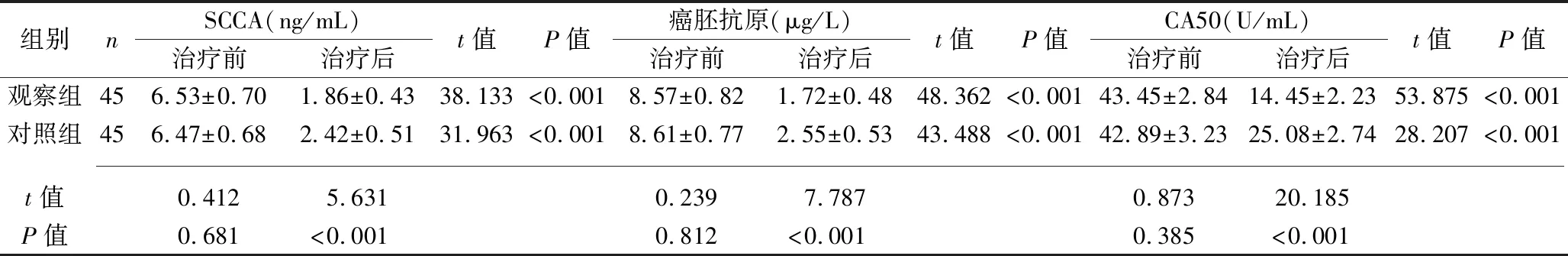
表2 治疗前后两组患者血清学肿瘤标志物水平的比较(x±s)
2.3 两组患者毒副反应发生情况的比较 两组患者在治疗结束的4周内均出现不同程度的骨髓抑制、消化系统及泌尿系统毒副反应、放射性直肠炎、放射性膀胱炎。观察组骨髓抑制发生率高于对照组(P<0.05),但两组其他毒副反应发生率比较,差异均无统计学意义(均P>0.05)。两组均无治疗相关死亡病例。见表3。

表3 两组患者毒副反应发生情况的比较[n(%)]
2.4 两组患者3年总生存率、无进展生存率及PALN控制率的比较 观察组3年无进展生存率、PALN控制率均高于对照组(均P<0.05),但两组3年总生存率差异无统计学意义(P>0.05),见表4。
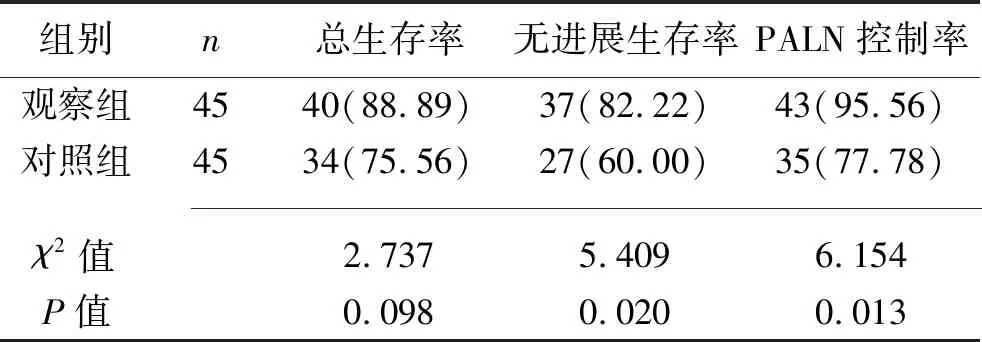
表4 两组患者3年总生存率、无进展生存率及PALN控制率的比较[n(%)]
3 讨 论
宫颈癌最常见的转移途径是淋巴结转移,且其转移具有规律性,通常沿着宫颈旁淋巴管依次转移至闭孔、髂内、髂外、骼总淋巴结,再转移至PALN,也可经骶前转移至PALN[9-10]。宫颈癌一旦发生PALN转移,短时间内即易出现远处脏器转移,预后极差。宋云红[11]研究发现,发生PALN转移的宫颈癌患者,当PALN短径≥1.5 cm时其5年生存率仅为58%,明显低于PALN短径<1.5 cm及PALN转移阴性的宫颈癌患者。研究显示,宫颈癌PALN转移率为13.1%~16.0%,且PALN转移率随着宫颈癌分期的进展而升高,是导致宫颈癌预后不良的重要危险因素[12-13]。还有研究表明,盆腔淋巴结转移情况与PALN转移密切相关,盆腔淋巴结转移个数多是PALN转移的独立危险因素[14]。常规放疗范围并不包含PALN,而发生盆腔淋巴结转移的宫颈癌可能已经出现PALN微转移,通过正电子发射计算机体层显像仪等敏感度较高的诊断方法评估淋巴结常难以完全检出微小转移淋巴结,因此宫颈癌患者经常规治疗后仍存在较高的PALN转移风险。故对于盆腔淋巴结转移阳性的宫颈癌患者,行PALN引流区在内的预防性延伸野放疗具有积极意义。
相对于常规放疗,延伸野调强放疗能进一步提升高剂量分布区和靶区的适形度,使靶区剂量分布更均匀,且延伸野放疗可减少临近组织与脏器的受照剂量,增加转移淋巴结的照射剂量。目前已有不少研究对延伸野放疗在宫颈癌中的应用价值进行了分析,但对于接受同步放化疗的患者,是否推荐行预防性延伸野放疗尚未达成共识。Lee等[15]对198例出现盆腔淋巴结转移但未出现腹膜后淋巴结转移的局部进展期宫颈癌患者的临床资料进行了回顾性分析,结果显示,虽然接受预防性延伸野放疗的宫颈癌患者肿瘤分期更晚,有髂总淋巴结转移的患者更多,但相对于仅接受盆腔野放疗的宫颈癌患者,接受预防性延伸野放疗的宫颈癌患者预后更佳。但另一项研究则显示,接受预防性延伸野放疗与接受盆腔野放疗的宫颈癌患者的10年总生存率、无进展生存率及腹膜后淋巴结转移率比较,差异并无统计学意义[16],究其原因,可能与接受盆腔野放疗和接受预防性延伸野放疗的宫颈癌患者的基线资料不平衡有关。为了平衡基线资料,有学者[17]对纳入的研究对象进行了倾向评分匹配,在纳入的280例国际妇产科联盟分期为ⅢC1期的宫颈癌患者中,选取了71对分别接受盆腔野放疗联合同步化疗与接受盆腔+PALN区调强放疗联合同步化疗的宫颈癌患者进行分析,结果显示,接受调强放疗者的5年总生存率、无进展生存率均高于接受同步化疗者(85.0%vs.61.9%;77.9%vs.53.0%)。在亚组分析中,根据髂总淋巴结阳性、盆腔淋巴结转移数目≥3枚、T3疾病3个因素将宫颈癌患者分为高危组和低危组,高危组接受调强放疗者的5年无进展生存率显著高于接受同步化疗者(84.4%vs.54.9%);低危组接受调强放疗者的5年总生存率、无进展生存率、PALN控制率均显著高于接受同步化疗者(91.1%vs.61.8%;80.3%vs.53.8%;100.0%vs.88.4%)。另外,同步化疗组与调强放疗组Ⅲ级或以上慢性毒性反应发生率分别为1.2%和5.9%,差异无统计学意义。这说明预防性延伸野放疗联合同步化疗能有效改善宫颈癌合并盆腔淋巴结转移患者的总生存率、无进展生存率及PALN控制率,且并未明显增加毒性反应。
以上相关研究主要以回顾性分析为主,本研究对比预防性延伸野放疗联合TP方案同步化疗与盆腔野放疗联合TP方案同步化疗治疗局部晚期宫颈癌的近远期疗效,结果显示,两组客观缓解率差异无统计学意义(P>0.05),提示两组近期疗效相当。对两组患者追踪随访3年后发现,观察组3年无进展生存率、PALN控制率均高于对照组(均P<0.05)。这提示,在常规盆腔野放疗基础上将照射区域延伸至PALN引流区,能有效杀灭PALN隐匿转移灶或微转移灶,减少PALN转移的发生,从而有利于延长局部晚期宫颈癌患者的生存期,改善其预后[18]。但观察组3年总生存率仅略高于对照组,差异无统计学意义(P>0.05),考虑其原因可能与本研究纳入的样本量较小有关。
肿瘤标志物是诊断及评估肿瘤恶性程度的常用指标,也可用于评估恶性肿瘤的治疗效果。宫颈癌患者的血液中存在较多异常表达的肿瘤标志物,如SCCA、癌胚抗原等[19]。其中SCCA是宫颈癌的特异性标志物,主要表达于鳞癌组织,且其表达水平与肿瘤恶性程度密切相关。癌胚抗原、CA50属于广谱肿瘤标志物,除了在宫颈癌中异常表达,在胃癌、结直肠癌、肝癌等恶性肿瘤中也异常表达。本研究结果显示,治疗后,两组血清SCCA、癌胚抗原及CA50水平均较治疗前降低,且观察组下降更明显(均P<0.05)。这提示,预防性延伸野放疗联合同步化疗相对于盆腔野放疗联合同步化疗能更有效地下调局部晚期宫颈癌患者的血清学肿瘤标志物表达水平,有助于稳定患者病情。本研究结果还显示,两组患者在治疗过程中均出现骨髓抑制、消化系统及泌尿系统毒副反应、放射性直肠炎、放射性膀胱炎,给予相应的对症治疗后均能缓解,且均未影响治疗进程,患者尚可耐受。观察组骨髓抑制发生率为77.78%,高于对照组的57.77%(P<0.05),其中观察组有12例患者出现了Ⅲ~Ⅳ级骨髓抑制,但两组的其他毒副反应发生率差异均无统计学意义(均P>0.05)。这提示,对于局部晚期宫颈癌患者,预防性延伸野放疗联合同步化疗能获得更好的远期疗效,且相对于盆腔野放疗联合同步化疗,其总体毒副反应尚能接受。但本研究样本量相对较小,且随访时间有限,后续仍有待大样本量研究、长时间随访观察验证相关结论。
综上所述,与盆腔野放疗联合同步化疗相比,预防性延伸野放疗联合同步化疗治疗局部晚期宫颈癌患者可以更好地降低血清学肿瘤标志物水平,提高PALN控制率,远期疗效好,但增加了骨髓抑制的发生风险,两种疗法的近期疗效相当。
