双线统摄,多维探究
2023-07-12缪徐
缪徐

摘 要:情境真实化、知识结构化,是《义务教育化学课程标准(2022年版)》倡导的教学理念。针对初中化学核心概念教学中知识的结构性、思维的深刻性的提高,做了相关的探索。沪教版初中化学九年级下册《溶液组成的表示》第一课时的教学,教学情境具有贯穿性,教学流程以活动线统摄,教学活动聚焦学生思维的流动。
关键词:初中化学;教学情境;认知维度;大概念;《溶液组成的表示》
* 本文系江苏省教育科学“十四五”规划课题“‘双减背景下素养式化学教学方式变革的课例研究”(编号:Ec/2021/44)的阶段性研究成果。
情境真实化、知识结构化,是《义务教育化学课程标准(2022年版)》(以下简称“新课标”)倡导的教学理念。如何提高初中化学核心概念教学中知识的结构性、思维的深刻性,实现“知识传授”到“素养提升”的转变?笔者做了相关的探索。现结合沪教版初中化学九年级下册《溶液组成的表示》第一课时的教学实例,做阐释说明。
一、 教学思路
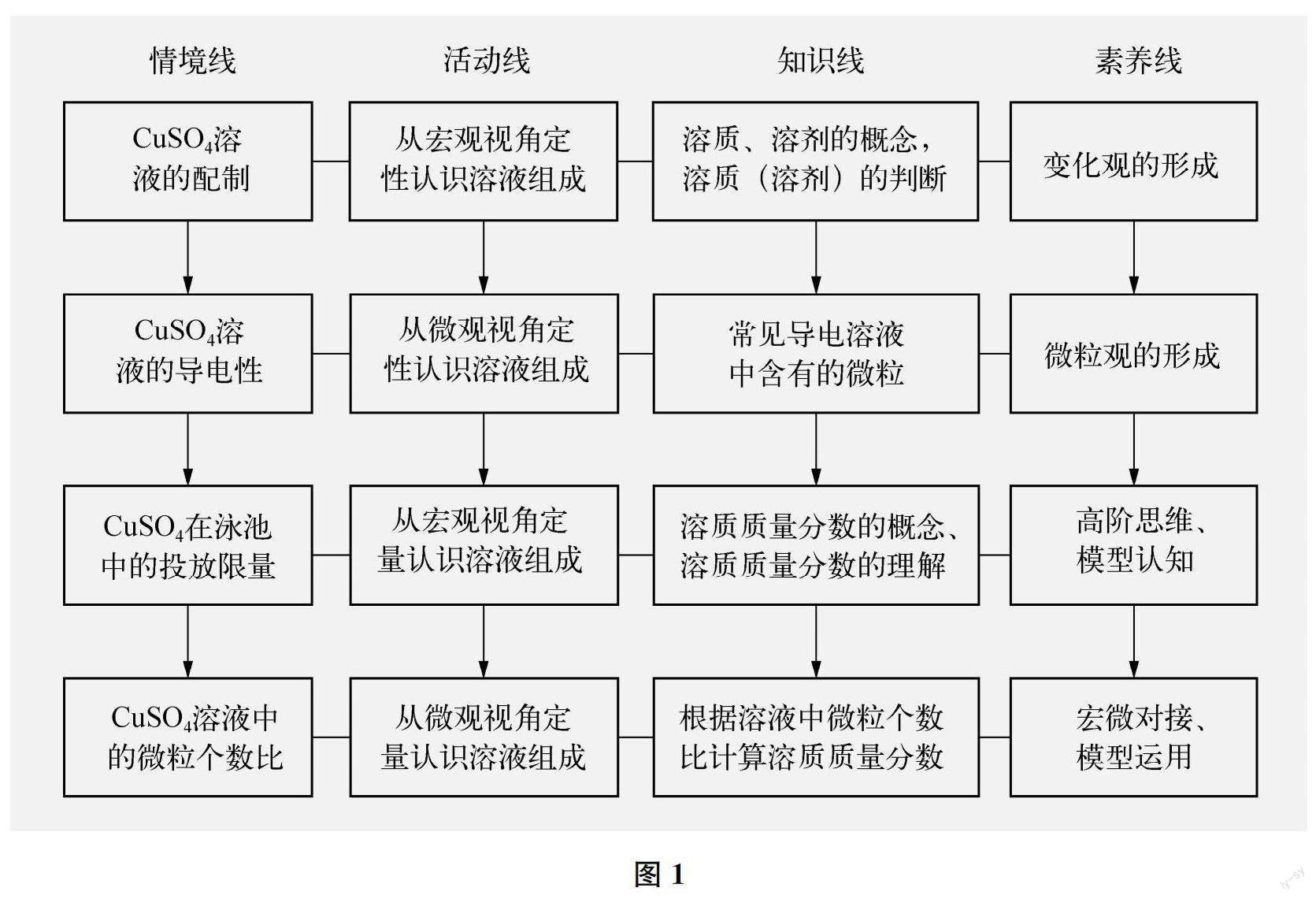
溶质、溶剂、溶质质量分数,是沪教版初中化学九年级下册《溶液组成的表示》第一课时中的3个核心概念。教学时,可以用学生较为熟悉的硫酸铜溶液创设情境线,用“多维度认识溶液组成”(溶液组成有宏观、微观两种认识视角及定性、定量两种表征形式)的大概念视角创设活动线,以此来统摄3个核心概念的教学。具体思路见下页图1。
二、 教学过程
(一) 从宏观、定性的视角认识溶液组成
师 同学们,(展示硫酸铜溶液)
这瓶蓝色溶液在前面的学习中曾出现过两次,还记得吗? (学生回顾、交流。)
师 今天,我们将以硫酸铜溶液为线索来研究新的问题——溶液组成的表示。
师 (课件呈现硫酸铜溶液配制过程的示意图)
在硫酸铜溶液的配制过程中,被溶解的物质、能溶解其他物质的物质分别是什么?
生 硫酸铜、水。
师 对照教材上溶质、溶剂的概念,说一说这两种物质的归类。
生 硫酸铜是溶质,水是溶剂。
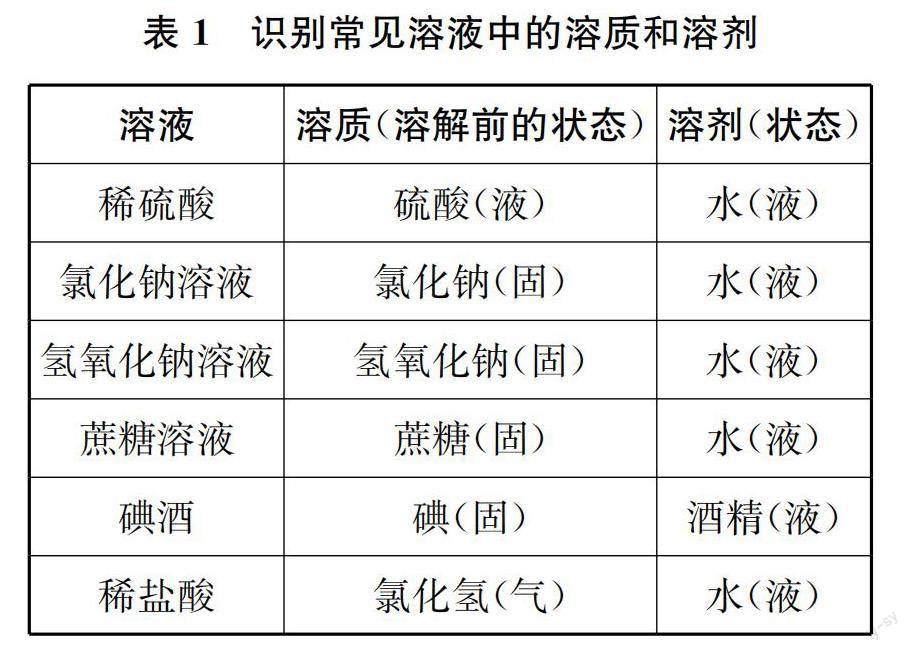
师 带着对溶质、溶剂概念的初步认识,我们来填写表格。(学生填写表格,教师巡视指导,最终得到表1。)
师 从表格中,同学们能总结出溶质、溶剂识别的一般规律吗?
生 固液相溶,固体为溶质,液体为溶剂;气液相溶,气体为溶质,液体为溶剂;液液相溶,非水液体为溶质,水为溶剂;如果两种液体都不是水,则量少的液体为溶质,量多的液体为溶剂。
师 硫酸铜溶液中的溶质是硫酸铜,如果硫酸铜溶液与氢氧化钠溶液恰好完全反应,所得溶液中的溶质是什么?
生 硫酸钠。
师 如果硫酸铜溶液和铁粉恰好完全反应,所得溶液中的溶质又是什么?
生 硫酸亚铁。
师 从宏观、定性的角度看,溶液由溶质和溶剂组成,在判断溶质、溶剂的过程中,要注意规律的运用,还要注意溶质的变化。
[设计意图:借助硫酸铜溶液的配制,引出“被溶解和能溶解”的话题,帮助学生建立溶质、溶剂的初步概念。通过常见溶液中溶质、溶剂的识别,总结识别规律,拓展学生认知宽度。通过硫酸铜溶液与氢氧化钠溶液、铁粉两个化学反应的再现,重回教学情境,提高学生认知深度。]
(二) 从微观、定性的视角认识溶液组成
师 前面的学习中曾分析过稀硫酸、氯化钠溶液、氢氧化钠溶液等导电的原因,请同学们回忆、交流。
生 稀硫酸能够导电,是因为其中含有自由移动的氢离子和硫酸根离子;氯化钠溶液能够导电,是因为其中含有自由移动的钠离子和氯离子;氢氧化钠溶液能够导电,是因为其中含有自由移动的钠离子和氢氧根离子。
师 硫酸铜溶液也能导电,原因是什么?
生 因为硫酸铜溶液中含有自由移动的铜离子和硫酸根离子。
师 从微观、定性的角度看,溶液的组成该如何描述?
生 溶液由溶质离子(分子)和溶剂分子等微粒构成。
[设计意圖:通过稀硫酸、氯化钠溶液、氢氧化钠溶液等导电原因的回忆,将溶液组成的认识思路由宏观转向微观,然后回到硫酸铜溶液导电原因的分析上。这样,既丰富了学生从微观角度认识溶液组成的素材,又保持了以硫酸铜溶液为主角所创设的教学情境的一致性。]
(三) 从宏观、定量的视角认识溶液组成
师 在溶液的实际应用中,有时仅仅知道溶液的定性组成还不够,还需要了解溶液的定量构成。让我们沿着硫酸铜溶液这条主线继续开展探究活动。(课件呈现泳池的画面)
为了消毒杀菌,通常会向泳池的水中加入一定量的硫酸铜。有关资料表明,为了减少硫酸铜这种有毒物质对人体的伤害,泳池水中硫酸铜的含量一般要控制在0.000025%-0.00005%之间。你知道这里的百分数的含义吗?
生 溶液中溶质的质量占比,也叫溶质质量分数。
师 在化学实验室里,某同学将1g硫酸铜完全溶解于19g水中,所得溶液中硫酸铜的质量分数为多少?
生 1g/1g+19g×100%=5%。
师 溶质质量分数是一个比值,它和我们先前学过的众多比值中的哪些比值在内涵上最为接近。可以从比的方向(横向还是竖向)、比的方式(局部与局部还是局部与整体)、比的结果(整数比还是小于100%的比)等几个方面去思考。
生 和赤铁矿中氧化铁的质量分数最接近——都是竖向的比,都是局部与整体的比,都是结果小于100%的比……
师 请同学们结合刚才的学习内容,对溶液的组成做一个简要的小结。
生 从宏观、定量的角度看,溶液的组成可以用溶质的质量分数来表示。
[设计意图:借助泳池中硫酸铜含量的限定范围,将溶液组成的认识视角从定性转向定量,帮助学生建立溶质质量分数的概念。通过实验室配制硫酸铜溶液的计算,让学生进一步理解概念。通过已学的各种“比”的多角度对比,促进学生加深概念理解,完善知识结构,培养高阶思维。]
(四) 从微观、定量的视角认识溶液组成
师 (指板书,见下页图2)黑板上的板书还缺一部分,同学们预测一下,此处应该写什么?没错,从微观、定量的视角去认识溶液的组成。已知硫酸铜溶液中铜离子和水分子的个数比为1∶170,求该溶液中硫酸铜的质量分数。
生 约为5%。
师 能把你解决问题的思路和大家分享一下吗?
生 由硫酸铜溶液中铜离子和水分子的个数比,求算铜离子和水分子的质量比,再算硫酸铜和水的质量比,最终得出硫酸铜溶液中溶质的质量分数。
师 显然,溶液的组成也可以用溶液中溶质微粒与溶剂微粒(通常为水分子)的个数比来表示。这种微观、定量的数值可以转化为宏观、定量的表示结果。
师 (小结)九年级开始学化学至今,我们和硫酸铜溶液打过三次交道——初遇硫酸铜,认识了质量守恒定律;二遇硫酸铜,了解了铁与其发生置换反应的性质;三遇硫酸铜,从不同的视角认识了溶液的组成。可以说,遇见一次硫酸铜,我们的眼界就开阔一次。这就是成长,这就是飞跃!
[设计意图:借助板书缺角的观察、思考,引出最后一个认识问题的角度——从微观、定量的视角认识溶液的组成。通过学生思维路线的呈现,培养学生的有序思维习惯和语言表达能力;同时,也让学生意识到认识溶液的组成有多个视角(宏观、微观;定性、定量),这些认识视角可以彼此切换,认识结果也可以相互转化。最后的结语将学习和成长相连,意在激励学生努力学习、享受学习,寻求生命飞跃。]
三、 教学反思
(一) 教学情境具有贯穿性
新課标指出,“真实、生动、直观且富有启迪性的情境,能够激发化学学习兴趣,引发学生的思考,帮助学生建构大概念和核心概念,促进学生核心素养的发展”[1]。
硫酸铜溶液先后在教材第4章、第5章的学习中出现过,是学生较为熟悉的一种溶液。用硫酸铜溶液创设的情境主线,环环相扣,一“境”到底。这种贯穿式的教学情境避免了目前大多数中学化学教学中的“脱境”(创设的情境只能用于新课导入,后面的教学脱离该情境)和“多境”(一节课创设多个教学情境)现象,提高了教学的流畅性,为本节课的教学推进提供了逻辑基础。
(二) 教学流程以活动线统摄
对于“物质的组成”这一大概念,新课标是这样解读的:初步形成基于元素和分子、原子认识物质及其变化的视角,建立认识物质的宏观和微观视角之间的关联,知道物质的性质与组成、结构有关。[2]“多维度认识溶液的组成”是“物质的组成”大概念和本课教学内容结合的产物,即“课时大概念”。
在“多维度认识溶液的组成”这一课时大概念的统摄下,“溶液的组成”的学习有四条路径:宏观、定性;微观、定性;宏观、定量;微观、定量。核心概念的学习不再是碎片化的,而是一种整体建构式的探索,这样的教学也有了单元教学的意蕴。溶质、溶剂、溶质质量分数就不再是没有逻辑的“知识拼盘”,而是组成了一个彼此关联的“学习小主题”。这个学习小主题与基于物质的视角认识气态混合物的组成、基于物质的视角认识固态混合物的组成以及基于元素的视角认识纯净物的组成等主题,共同丰富了“物质的组成”大概念的内涵。
因为有“多维度认识溶液组成”这一课时大概念的统摄,“从宏观的视角定性认识溶液组成”“从微观的视角定性认识溶液组成”“从宏观的视角定量认识溶液组成”“从微观的视角定量认识溶液组成”等4个活动,形成了一个角度有异、指向一致的活动链。这样的活动链,消除了学生碎片化的学习,催生了他们结构化的认知。
(三) 教学活动聚焦学生思维的流动
思维是课堂教学的核心,是学生发展的关键。不管课堂教学采用什么样的方式,如果抓不住学生的思维,没有学生思维的积极流动,特别是高水平的思维流动,就不可能将知识转化为能力,也不可能将知识上升为观念,更不可能促进学生核心素养的发展。[3]
在多途径认识溶液的组成的学习过程中,学生经历了多次高水平的思维流动。比如,在溶质、溶剂的概念建立后,返回硫酸铜溶液情境的过程中,教师要求学生思考氢氧化钠溶液、铁粉分别与硫酸铜溶液恰好反应后所得溶液中的溶质。这不仅打通了“物质的组成与结构”“物质的性质与应用”“物质的化学变化”等学习主题之间的知识壁垒,而且让学生学会从变化的视角辨识溶质,加深了学生对溶质内涵的理解。又如,在溶质质量分数的概念建立后,教师没有立刻让学生做题巩固,而是用一个思考题将学生的思维引向深处:溶质质量分数是一个比值,它和我们先前学过的众多比值中的哪些比值在内涵上最为接近?通过回忆和比对,建立“溶质质量分数”模型(竖比,局部对整体,小于100%的比),为下一个高水平的思维流动——用模型从微观的视角定量认识硫酸铜溶液的组成,奠定了坚实的基础。
参考文献:
[1][2] 中华人民共和国教育部.义务教育化学课程标准(2022年版)[S].北京:北京师范大学出版社,2022:44,23.
[3] 毕华林.促进核心素养发展的化学课程改革——《义务教育化学课程标准(2022年版)》的研制及其变化[J].中学化学教学参考,2022(11):9.
