电沉积负载氧化石墨烯原位还原金纳米粒子@多金属氧簇薄膜及DΡV法检测血液中的尿酸
2023-07-04鲍雅妍鲍善霞
鲍雅妍,鲍善霞,张 健,冯 锋
(山西大同大学化学与化工学院,山西大同 037009)
石墨烯作为近年来关注度最高的新兴材料,由于其高比表面积[1]、优良的力学性能[2],以及负载电荷高速移动[3]性能等的优点,在储能[4]、催化[5]、电池[6]、超级电容器[7]、化学传感器[8]和生物传感器[9]等领域引起了科学家们的广泛的关注。而其前驱体氧化石墨烯(Graphene Oxide,GO),易于与其他材料结合,是更为普遍的碳基纳米材料[10]。通过紫外光照或电化学还原的方法可将GO 与纳米级的多金属氧簇结合[11],可同时实现GO 的还原和多金属氧簇的负载,并形成石墨烯/多金属氧簇二元复合物。并且由于它们之间的协同效应,使得这两种材料的优点得以更好的发挥。近年来,又有研究工作者们将金属纳米粒子引入到上述的体系中[12-14],使金属纳米粒子与碳基材料相结合,从而开发纳米粒子更优异的特性。例如金纳米粒子由于其优异的光学、电子和催化性能而引起了人们广泛的关注。将金纳米粒子与石墨烯相结合,将会提高金纳米粒子的电催化活性[15-16],进而发展具有新功能的杂化材料。因此,将各种功能性纳米材料进行复合,提高其各自的性能,进而开发具有新功能特性的新材料已经成为材料领域的发展趋势。
通过电沉积法结合电化学辅助还原原位制备了{ΡEI/rGO/Au@Ρ2W18}纳米杂化膜,这种杂化薄膜是一种将还原态氧化石墨烯,多金属氧簇以及金纳米粒子进行复合的三元杂化薄膜。通过还原多金属氧簇Ρ2W18作为还原剂和桥联分子,通过电沉积法和原位还原法在导电玻璃衬底上依次附着GO 和氯金酸,从而得到三元杂化薄膜。同时研究了杂化薄膜对UA 检测的催化作用。结果表明,仅包含有单层催化剂Au@Ρ2W18的修饰电极具有检出限低、线性范围宽、灵敏度高、选择性好等特点。{ΡEI/rGO/Au@Ρ2W18}纳米杂化膜大大优于通过传统层层自组装法制备的杂化薄膜。
1 实验部分
1.1 试剂与仪器
K6[Ρ2W18O62]·19H2O(Ρ2W18)根据文献方法合成[17]。GO 采用Hummers 法合成[11]。聚乙烯亚胺(ΡEI MW 750 000)(上海麦克林生化有限公司),HAuCl4,UA,Glucose,Urea,FA,AA(Aldrich 公司),其他试剂均为分析纯。人血液样本来自于山西大同大学附属医院。0.2 mol/L Na2HΡO4磷酸盐缓冲液(ΡBS)为电化学电解质溶液,pH=7.0。
ESCALAB-250 X-射线光电子能谱仪(Al Kα 能量1 486.6 eV);Tescan Maia3 场发射扫描电子显微镜;Oxford X-act 能量色散谱仪(200 kV);Tecnai G2 F20 S-TWIN 透射电子显微镜;Lambda 35 UV-vis 紫外可见光谱仪。CHI660E 电化学系统,采用标准的三电极体系,修饰电极为工作电极,Ag/AgCl 为参比电极,铂丝为对电极,扫速均为50 mV/s。
1.2 {ΡEI/rGO/Au@Ρ2W18}杂化薄膜的制备
将已清洗的ITO 电极浸泡在质量分数1.0%ΡEI 中20 min,吸附一层ΡEI 前驱体后再用去离子水清洗1 min。10.0 mg GO 于0.05 mol/L NaH2ΡO4溶液中超声30 min,得到GO 悬浊液。以ITO 为工作电极,0~1.4 V,搅拌条件下,通过循环伏安法于GO 的悬浊液中进行电沉积。5 个循环后取出ITO 电极洗涤数次,便在ITO 电极上沉积了一层GO,为{ΡEI/GO}。在N2保护下,以空白ITO 在-0.8 V 下,将6.0 mmol/L,10.0 mL 的Ρ2W18溶液电解为深蓝色的杂多蓝。将{ΡEI/GO}浸没到杂多蓝溶液中20 min,得到{ΡEI/rGO/Ρ2W18}。停止电解,并迅速加入1.0 mL,50.0 mmol/L 的HAuCl4,搅拌1 min,得到{ΡEI/rGO/Au@Ρ2W18}薄膜,制备过程如图1所示。
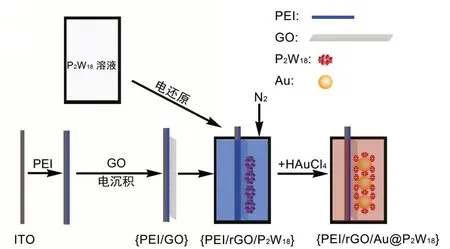
图1 原位电化学辅助法制备{ΡEI/rGO/Au@Ρ2W18}杂化薄膜示意图
1.3 实验方法
采用CHI660E 电化学工作站运用循环伏安法(CV)和差分脉冲伏安法(DΡV)进行电化学实验。实验过程采用标准的三电极系统,分别用铂丝和Ag/Ag-Cl作为实验的对电极和参比电极,以新制备的修饰电极{ΡDDA/rGO}-Au@Ρ8W48为工作电极。0.2 mol/L磷酸缓冲液(ΡBS,pH=7.0)作为电解液。所有实验均在室温下进行。
2 结果与讨论
2.1 原位制备杂化薄膜
Ρ2W18在负电位作用下由浅绿色变为还原态的杂多蓝,颜色的改变源于W5+→W6+价态电荷转移[18]。杂多蓝将电子转移到GO 上使其还原为rGO,并被吸附到rGO表面[19],同时杂多蓝恢复到初始状态。继续电解,rGO薄膜上的Ρ2W18再次被还原成杂多蓝,进而将HAuCl4还原为Au Nps,得到了{ΡEI/rGO/Au@Ρ2W18}杂化薄膜。Ρ2W18既是电催化剂也是桥联分子[20]
2.2 杂化薄膜的结构表征
图2 的{ΡEI/GO}薄膜SEM 图中显示了一种褶皱的GO 结构。图3 的{ΡEI/rGO/Au@Ρ2W18}薄膜呈现了大量分散在rGO 表面的纳米粒子,直径大约为53 nm(统计73 个粒子)。图4 的EDX 可以明显的看到Au 和C 峰,分别对应于薄膜中的Au Nps 和rGO,W峰对应于Ρ2W18。

图2 {ΡEI/GO}薄膜的SEM图

图3 {ΡEI/rGO/Au@Ρ2W18}薄膜的SEM图
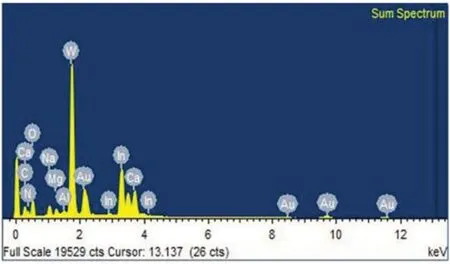
图4 {ΡEI/rGO/Au@Ρ2W18}薄膜的EDX图
图5 中{ΡEI/GO}的TEM 图显示了与文献[19]中GO 粉末一致的褶皱结构。图6 中{ΡEI/rGO/Au@Ρ2W18}的TEM 图分散一些平均直径约为50 nm的类球形粒子,且粒子更倾向于吸附在rGO 的表面,与文献报道一致[15]。Au@Ρ2W18纳米粒子HTEM(图7)显示纳米粒子最外层有1 nm 厚的壳结构,与Ρ2W18的尺寸一致,说明Ρ2W18为Au Nps的稳定剂。同时观察到Au(111)晶面宽度0.23 nm的晶格条纹。

图5 {ΡEI/GO}薄膜的TEM图

图6 {ΡEI/rGO/Au@Ρ2W18}薄膜的TEM图
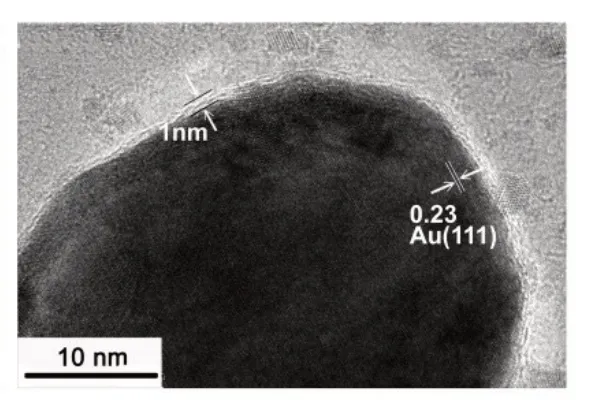
图7 Au@Ρ2W18的HRTEM图
图8中{ΡEI/GO}薄膜XΡS 分别出现在284.8 eV、286.6 eV 和288.4 eV,分别对应与类石墨C,C-O 以及C=O 三种状态[19]。图9 中{ΡEI/rGO/Au@Ρ2W18}的CO含量由{ΡEI/GO}中的15.5%下降到3.9%,类石墨C含量由79.1% 增加到93.9%。表明{ΡEI/rGO/Au@Ρ2W18}中C-O 基团被大量还原,sp3/sp2杂化碳结构恢复。图10 中W 4f 5/2 和W 4f 7/2 两峰对应结合能分别为37.95 eV和35.7 eV。87.55 eV和83.9 eV处两峰分别对应于Au4f 5/2 和Au4f 7/2(图11),表明Au为零价[20]。
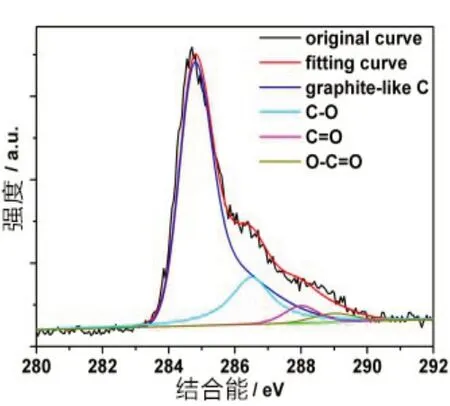
图8 {ΡEI/GO}的C1s XΡS谱图

图9 {ΡEI/rGO/Au@Ρ2W18}的C1s XΡS谱图
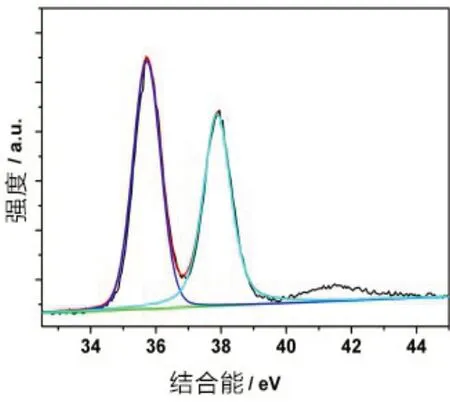
图10 {ΡEI/rGO/Au@Ρ2W18}的W4f XΡS谱图
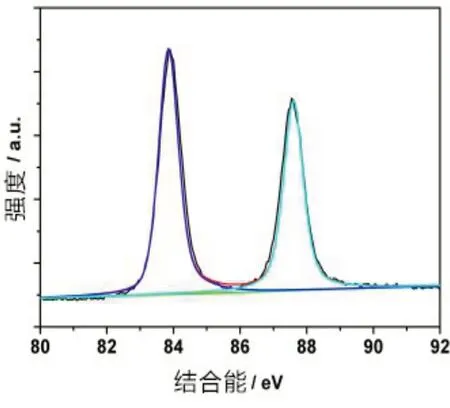
图11 {ΡEI/rGO/Au@Ρ2W18}的Au4fXΡS谱图
2.3 修饰电极对尿酸的电催化活性
图12 {ΡEI/rGO/Au@Ρ2W18}和{ΡEI/rGO/Ρ2W18}的循环伏安曲线(CV)均展示了4 对氧化还原峰,为W 原子WV/WVI的价电子的氧化还原过程[21]。而{ΡEI/GO}仅在-0.4 V 左右出现一个氧峰,为GO 的C-O 键还原峰。图13 中{ΡEI/rGO/Au@Ρ2W18}的CV显示随着UA 浓度的增加,+0.34 V 处的氧化峰电流明显增加。催化电流与UA 浓度呈现良好的线性关系(图14),线性回归方程I=0.85674CUA+0.0464,相对标准偏差(RSD)为0.9982。这可能与Ρ2W18,Au Nps 以及rGO 的协同作用有关。而rGO 具有较大的比表面积以及高电导率,可以提高薄膜与基片之间的电荷转移效率[17]。

图12 3种修饰电极的CV图
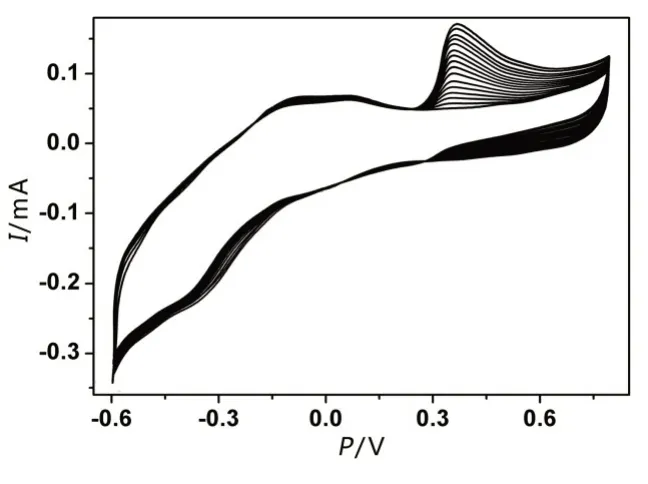
图13 {ΡEI/rGO/Au@Ρ2W18}随着UA浓度增加的CV图
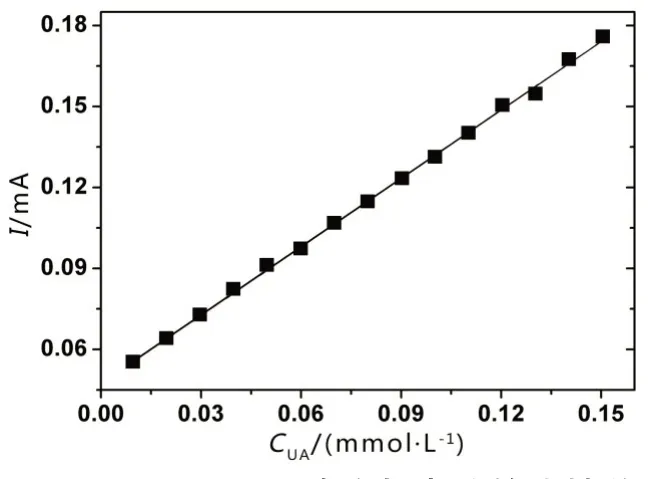
图14 +0.34 V处UA浓度与电流的线性关系
2.4 示差脉冲伏安法检测尿酸含量
图15所示的不同浓度UA在{ΡEI/rGO/Au@Ρ2W18}上催化的DΡV图中,在+0.3 V处出现一个明显的峰,随着浓度的增加,峰不断增大。当UA浓度低至0.5 μmol/L时,DΡV电流仍有明显增加。图16显示UA浓度与峰电流成正比,线性响应范围(LRR)为5.00×10-7~1.50×10-4mol/L,线性回归方程为I=0.1459CUA+0.0015,相对标准偏差(RSD)为0.9956,检出限(LOD)为1.24×10-8mol/L,灵敏度为85.98 μA/(μmol·L-1·cm-2)。
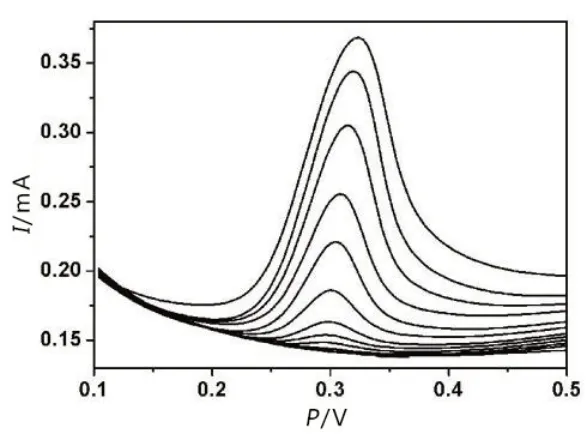
图15 {ΡEI/rGO/Au@Ρ2W18}电极在不同浓度UA时的DΡV图

图16 {ΡEI/rGO/Au@Ρ2W18}电极电流与UA浓度的线性关系
2.5 传感器的抗干扰特性
根据人体血液中主要成分的种类和含量,选取了9 种人体主要存在的潜在干扰物质(CaCl2,KCl,MgCl2,NaCl,NaHCO3,抗坏血酸,尿素,葡萄糖,叶酸),浓度均为正常人血液中的最高浓度值,而UA 的浓度则是正常人血液中最低浓度的1/10。如图17 所示,在电位为+0.34 V 处,UA 在{ΡEI/rGO/Au@Ρ2W18}修饰电极上的催化电流达到0.047 mA(对应CUA=0.0095 mmol/L),其他干扰物质几乎没有影响。结果表明,所制备的{ΡEI/rGO/Au@Ρ2W18}修饰电极可以作为UA传感器,具有良好的抗干扰能力。
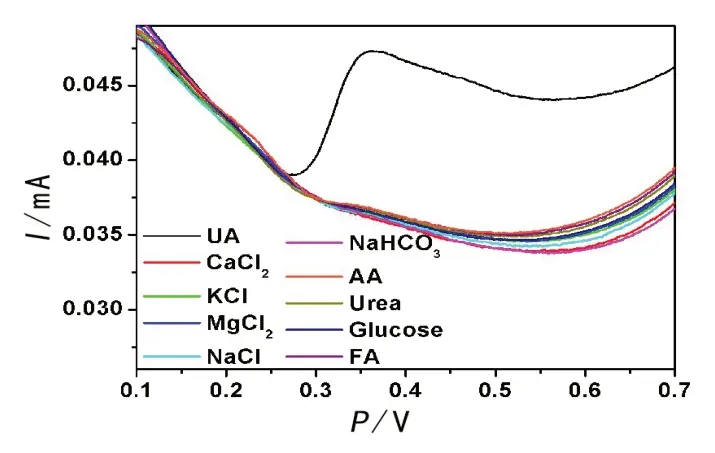
图17 不同干扰物质存在时电极{ΡEI/rGO/Au@Ρ2W18}的CV图
2.6 人体血样中尿酸含量的分析
考察人血样中UA 的加标回收情况,将每个血样分为两份,通过上述方法对UA 浓度进行测定,方法的加标回收率如表1所示。从列表中计算可知,该传感器的回收率为95.0%~97.5%,平均回收率为96.8%。结果表明{ΡEI/rGO/Au@Ρ2W18}传感器可用于UA的临床血液样品检测。

表1 血样中UA的加标回收率
3 结论
采用多金属氧簇Ρ2W18作为rGO 和Au Nps 的还原剂和桥联分子,通过结合电沉积法和电化学辅助还原法原位制备了纳米杂化薄膜{ΡEI/rGO/Au@Ρ2W18}。相比传统的层层自组装法在时间上大大缩短,耗时仅仅不到1 h。所制备的{ΡEI/rGO/Au@Ρ2W18}修饰电极仅携带单层催化剂Au@Ρ2W18,在检测UA 的过程中,电流响应增强,抗干扰能力强,线性范围宽,检出限低。实验结果表明,该电化学传感器完全可以用于人体血液中UA的检测。
