慢性阻塞性肺疾病合并心力衰竭的多因素logistic回归分析
2023-06-28王小龙王琦武宁霞
王小龙 王琦 武宁霞
【摘要】 目的:對影响慢性阻塞性肺疾病(COPD)合并心力衰竭(HF)的相关因素进行logistic回归分析。方法:选择2018年1月1日-2021年12月31日甘肃中医药大学附属天水中西医结合医院呼吸与危重症医学科确诊的COPD合并HF患者76例为观察组,COPD未合并HF患者179例作为对照组。采用多因素logistic回归分析影响COPD合并HF的危险因素(或保护因素)。结果:单因素分析结果显示,观察组呼吸频率、活化部分凝血活酶时间(APTT)、凝血酶原时间(PT)、D-二聚体、低白蛋白血症、高碳酸血症、低氧血症比例、动脉血乳酸(Lac)、左房前后径(LA)、肺动脉内径(PA)和右室舒张末期前后径(RVEDD)均高于对照组,SaO2、FEV1、FEV1%pred和左室内径缩短率(LVFS)均低于对照组,差异均有统计学意义(P<0.05)。将上述单因素分析中P<0.1的15个变量纳入logistic回归分析提示,低氧血症、Lac和RVEDD为COPD合并HF的危险因素[OR=6.852,95%CI(1.278,36.749),P<0.05;OR=11.465,95%CI(1.734,75.810),P<0.05; OR=3.248,95%CI(1.729,6.099),P<0.001];而FEV1%pred、LVFS为COPD合并HF的保护因素[OR=0.463,95%CI(0.288,0.941),P<0.001;OR=0.646,95%CI(0.555,0.753),P<0.001]。结论:低氧血症、Lac和RVEDD为COPD合并HF的危险因素,而FEV1%pred、LVFS为COPD合并HF的保护因素。
【关键词】 慢性阻塞性肺疾病 心力衰竭 危险因素
Multivariate logistic Regression Analysis of Chronic Obstructive Pulmonary Disease with Heart Failure/WANG Xiaolong, WANG Qi, WU Ningxia. //Medical Innovation of China, 2023, 20(11): -151
[Abstract] Objective: logistic regression analysis was carried out to analyze the related factors of chronic obstructive pulmonary disease (COPD) with heart failure (HF). Method: A total of 76 patients with COPD complicated with HF diagnosed in Department of Respiratory and Critical Care Medicine of Tianshui Integrated Traditional Chinese and Western Medicine Hospital Affiliated to Gansu University of Traditional Chinese Medicine from January 1st, 2018 to December 31st, 2021 were selected as observation group, and 179 patients with COPD without HF were selected as control group. Multivariate logistic regression analysis was used to analyze the risk factors (or protective factors) affecting COPD complicated with HF. Result: The results of single factor analysis showed that respiratory rate, APTT, PT, D-dimer, hypoalbuminemia, hypercapnia, hypoxemia ratio, arterial blood lactic acid (Lac), left atrial anterior-posterior diameter (LA), pulmonary artery diameter (PA) and right ventricular end-diastolic diameter (RVEDD) were higher than those in the control group, and SaO2, FEV1, FEV1%pred and left ventricular diameter shortening (LVFS) were lower than those in the control group, the differences were statistically significant (P<0.05). The 15 variables with P<0.1 in the above univariate analysis were included in the multivariate logistic regression analysis, suggesting that hypoxemia, Lac and RVEDD were risk factors for COPD with HF [OR=6.852, 95%CI (1.278, 36.749), P<0.05; OR=11.465, 95%CI (1.734, 75.810), P<0.05; OR=3.248, 95%CI (1.729, 6.099), P<0.001)]; FEV1%pred, LVFS were protective factors affecting COPD with HF [OR=0.463, 95%CI (0.228, 0.941), P<0.001; OR=0.646, 95%CI (0.555, 0.753), P<0.001]. Conclusion: Hypoxemia, Lac and RVEDD are risk factors for COPD with HF, while FEV1%pred and LVFS are protective factors for COPD with HF.
[Key words] Chronic obstructive pulmonary disease Heart failure Risk factors
First-author's address: Tianshui Integrated Traditional Chinese and Western Medicine Hospital Affiliated to Gansu University of Traditional Chinese Medicine, Tianshui 741020, China
doi:10.3969/j.issn.1674-4985.2023.11.035
慢性阻塞性肺疾病(COPD)是以持续存在呼吸系统症状和气流受限为特征的慢性气道性疾病,临床上约30%的COPD患者合并心力衰竭(HF),特别是在老年患者中[1-3]。COPD与HF在症状和体征有明显的重叠,临床表现对两种疾病的早期诊断或鉴别诊断无特异性[4-5],且COPD合并HF时往往相互影响并增加二者的严重程度和病死率[2-3]。此外,在药物治疗方面二者存在一定的矛盾,当二者合并时易因不能早期明确诊断而造成延误治疗。目前国内外仅有针对COPD急性加重期合并HF的研究报道[6],而对COPD稳定期患者早期筛查指标的确定未得到足够重视。本研究纳入COPD不同分期患者为研究对象,旨在分析影响COPD合并HF的危险因素,以期为临床医师及时诊断与合理治疗提供参考。
1 资料与方法
1.1 一般资料 回顾性收集2018年1月1日-2021年
12月31日在甘肃中医药大学附属天水中西医结合医院呼吸与危重症医学科住院COPD合并或者未合并HF的患者。COPD纳入标准:符合2021年修订版COPD诊治指南中的诊断标准,(1)有危险因素暴露史;(2)有慢性咳嗽或咳痰、呼吸困难等症状;(3)均进行肺功能检查,吸入支气管舒张剂后FEV1/FVC<0.7,即明确存在持续的气流受限;(4)并排除可引起类似症状和持续气流受限的其他疾病[1]。HF纳入标准:基于左室射血分数(LVEF),将HF分为射血分数降低性HF、射血分数保留性HF和中间范围射血分数HF。其诊断和评估标准符合文献[7]《中国心力衰竭诊断和治疗指南(2018版)》。排除标准:(1)哮喘、支气管扩张、肺癌、肺结核、弥漫性泛细支气管炎、特发性肺纤维化等疾病;(2)COPD合并其他疾病,如冠心病、先心病、风心病、心脏瓣膜疾病、严重的心律失常、风湿免疫性疾病、气胸、急慢性肾衰竭等。明确诊断且病历资料完整的COPD合并HF患者76例为观察组,COPD未合并HF患者179例作为对照组。本次研究获得甘肃中医药大学附属天水中西医结合医院学术委员会和医学伦理委员会论证批准。
1.2 方法
1.2.1 组间相关因素比较 统计并比较观察组和对照组患者基本情况、血液相关指标、动脉血气分析、肺功能和超声心动图。(1)基本情况:包括性别、年龄、病程和生命体征;(2)血液相关指标:红细胞数(RBC)、血红蛋白浓度(Hb)、白细胞数(WBC)、中性粒细胞数(NEU)、嗜酸性粒细胞数(EOS)、嗜碱性粒细胞数(BAS)、淋巴细胞数(LYM)、血小板数(PLT)、C反应蛋白(CRP)、降钙素原(PCT)、活化部分凝血活酶时间(APTT)、凝血酶原时间(PT)、纤维蛋白原含量(FIB)、凝血酶时间(TT)、D-二聚体、肌酸激酶(CK)、肌酸激酶同工酶(CK-MB)和血清白蛋白(ALB,ALB<35 g/L为低白蛋白血症);(3)动脉血气分析指标:pH值、动脉二氧化碳分压(PaCO2,PaCO2>45 mmHg为高碳酸血症)、动脉氧分压(PaO2,PaO2<60 mmHg为低氧血症)、血氧饱和度(SaO2)和动脉血乳酸(Lac);(4)肺功能:GOLD肺功能分级(轻度、中度、重度和极重度)、肺活量(VC)、用力肺活量(FVC)、第一秒用力呼气容积(FEV1)和FEV1占预计值的百分比(FEV1%pred);(5)超声心动图指标:主动脉瓣内径(AO)、左房前后径(LA)、左室舒张末期前后径(LVEDD)、左室后壁厚度(LVPW)、室间隔厚度(IVS)、左室内径缩短率(LVFS)、肺动脉内径(PA)和右室舒张末期前后径(RVEDD)。
1.2.2 多因素logistic回归分析 将单因素分析后筛选出的指标(P<0.1)纳入模型进行多因素logistic回归分析,确定危险因素(或保护因素)及其OR值。
1.3 统计学处理 采用SPSS 26.0统计软件分析数据。计量资料符合正态分布及方差齊性时以(x±s)表示,组间比较采用独立样本t检验;不符合正态分布及方差齐性时以M(Q1,Q3)表示,组间比较采用Mann-Whitney U检验;计数资料以率(%)表示,组间比较采用字2检验或Fisher确切概率法;等级资料组间比较采用Mann-Whitney U检验。将单因素分析中P<0.1的变量纳入多因素分析,参照文献[8]采用逐步回归向前-条件法进行多因素logistic回归分析。检验水准α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 单因素分析
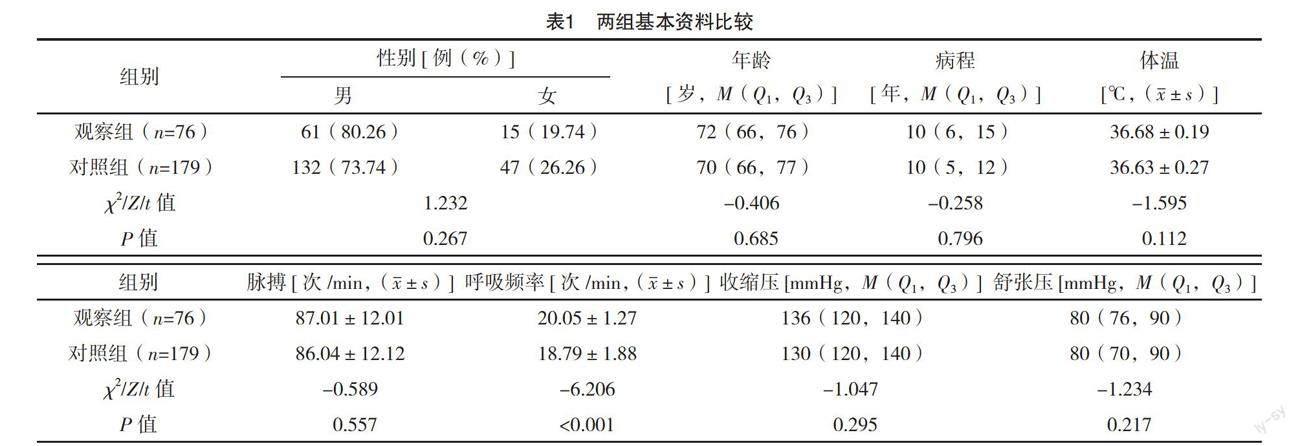
2.1.1 两组基本资料比较 与对照组比较,观察组呼吸频率较快(P<0.001);而两组性别、年龄、病程、体温、脉搏、收缩压和舒张压差异均无统计学意义(P>0.05)。见表1。
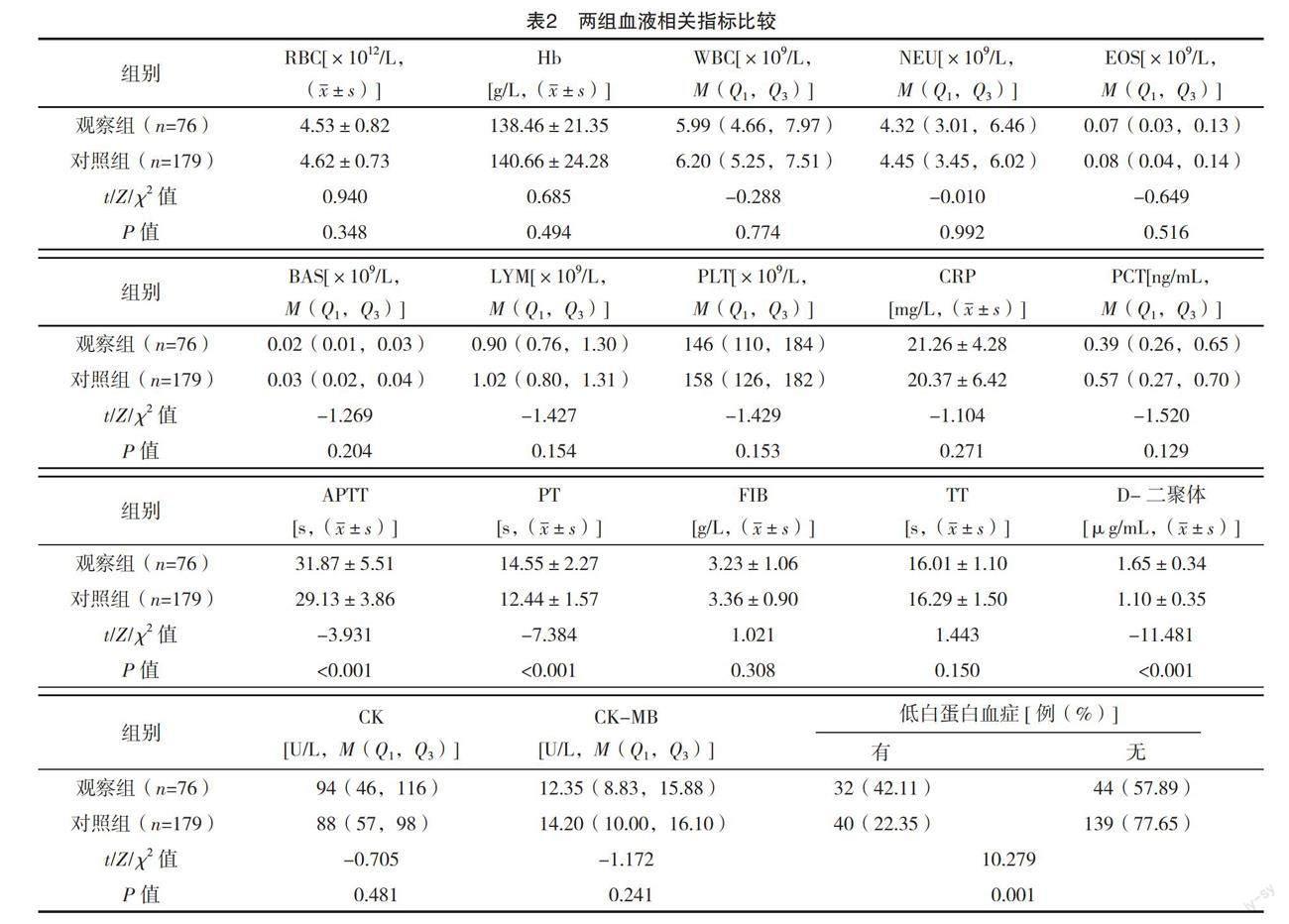
2.1.2 两组血液指标比较 观察组APTT、PT、D-二聚体和低白蛋白血症比例均高于对照组,差异均有统计学意义(P<0.05);两组其他血液指标比较,差异均无统计学意义(P>0.05)。见表2。
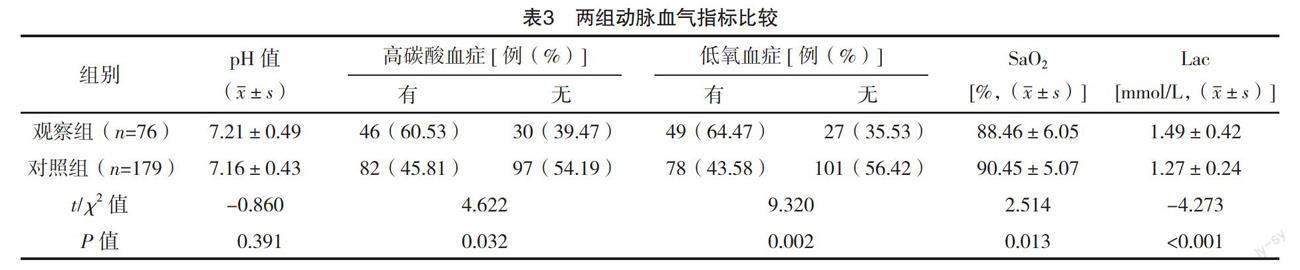
2.1.3 两组动脉血气分析比较 观察组Lac及高碳酸血症、低氧血症比例均高于对照组,SaO2低于对照组,差异均有统计学意义(P<0.05);而两组pH值比较差异无统计学意义(P>0.05)。见表3。
2.1.4 两组肺功能比较 在肺功能检测指标中,观察组FEV1和FEV1%pred均低于对照组,差异均有统计学意义(P<0.001);而两组GOLD分级、VC和FVC比较差异均无统计学意义(P>0.05)。见表4。
2.1.5 两组超声心动图指标比较 与对照组相比,观察组LA、PA和RVEDD均更高,而LVFS低,差异均有统计学意义(P<0.05);其余值差异均无统计学意义(P>0.05)。见表5。
2.2 多因素logistic回归分析
2.2.1 变量赋值 以COPD是否合并HF(否=0,是=1)为应变量,单因素分析中P<0.1的15个变量作为自变量纳入多因素分析,采用逐步回归向前-条件法进行多因素logistic回归分析。所有分类变量均设置哑变量。Hosmer-Lemeshow拟合优度检验表明模型拟合良好(字2=9.799,P=0.279)。见表6。
2.2.2 logistic回归分析 结果显示,低氧血症、Lac和RVEDD为COPD合并HF的危险因素[OR=6.852,95%CI(1.278,36.749),P<0.05;OR=11.465,95%CI(1.734,75.810),P<0.05;OR=3.248,95%CI(1.729,6.099),P<0.001];而FEV1%pred、LVFS为
COPD合并HF的保护因素[OR=0.463,95%CI(0.228,0.941),P<0.001;OR=0.646,95%CI(0.555,0.753),P<0.001]。见表7。
3 讨论
本研究结果发现,合并低氧血症、Lac升高和RVEDD增宽的COPD患者合并HF的风险增加,而LVFS增加可能会减少COPD合并HF的风险,与既往文献[6,9]研究报道结果一致。此外,本研究还发现FEV1%pred与COPD合并HF相关,提示COPD患者气流受限越严重今后合并HF的风险增加。
多个研究表明,临床上由低氧血症引起COPD患者发生严重的右心衰竭,主要是由于低氧性肺血管收缩和慢性肺泡低氧血症介导的右室后负荷增加导致的。前者产生的机制可能是局部肺泡氧分压降低导致肺动脉平滑肌反射性收缩,以維持正常的通气/血流比,但发生广泛的缺氧性血管收缩后,则会出现肺动脉高压和右心室代偿性肥厚;后者可能与以近、远端动脉变窄、僵硬为特征的肺血管重塑有关[10]。国内刘丹琴等[9]研究结果显示,可通过抑制ATP依赖K+通道和诱导产生白三烯等内源性缩血管介质而直接或间接引起肺血管收缩。
血乳酸水平升高(>2 mmol/L)长期以来一直被视作细胞缺氧、组织灌注不足和病情恶化的可靠性标志物,并作为评估脓毒症患者临床预后的重要监测指标[11]。COPD合并高乳酸血症患者病情加重的病理生理变化可能因低氧血症导致外周组织的血液和氧气供应不足导致血氧含量降低、低心排血量和组织灌注受损,进而导致血乳酸产生增多,甚至引起乳酸酸中毒,严重者出现心功能不全[12-13]。因此,动态监测血乳酸及观察血乳酸水平随时间变化的曲线对于检测COPD患者病情变化具有重要的临床价值[13]。也有研究表明,晚期HF患者中血乳酸正常是常见的,这可能表明尽管心功能严重降低,但仍能满足机体的基本代谢需求[11]。
越来越多的证据表明,肺功能可能为COPD合并HF(尤其是有重叠症状者)患者在日常临床诊断和治疗提供有用的信息。本次研究发现,COPD患者FEV1%pred是COPD合并HF的保护因素。Plesner等[14]研究发现,在气流阻塞患者中,FEV1%pred降低10%的多变量Cox风险比为1.42(P<0.001)。另外,Magnussen等[15]推荐肺功能检测应作为HF患者初始诊断程序和随访的一部分,是对临床表现、超声心动图和心脏标志物的补充。此外,肺功能参数可提供HF患者的预后信息,并可能有助于指导治疗决策。
COPD患者由于肺毛细血管床减少、肺动脉收缩和血管重塑等因素导致肺动脉高压,继而右室舒张功能障碍,最终发展为右心衰竭。尽管,目前GOLD指南尚未建议COPD患者进行超声心动图早期筛查,但国内外多个临床研究证实,右心功能相关指标监测对筛查COPD是否合并HF和临床治疗具有重要的价值[16-17],甚至Pellicori等[18]建议病情加重的COPD患者应考虑常规进行超声心动图检查。以上从侧面进一步证实,RVEDD增宽的COPD患者将会增加合并HF的风险。COPD合并HF患者LVFS可反映左室射血功能。本次研究提示,LVFS每增加1%可能会减少COPD合并HF的风险0.646倍,目前国内仅有李霞等[19]报道,LVFS随COPD患者病情严重程度增加而减小,此项结论尚需更严谨的多中心前瞻性随机对照研究中得到证实。
综上所述,低氧血症、Lac和RVEDD为COPD合并HF的危险因素,而FEV1%pred、LVFS为COPD合并HF的保护因素。
参考文献
[1]中华医学会呼吸病学分会慢性阻塞性肺疾病学组,中国医师协会呼吸医师分会慢性阻塞性肺疾病工作委员会.慢性阻塞性肺疾病诊治指南(2021年修订版)[J].中华结核和呼吸杂志,2021,44(3):170-192.
[2]何旭瑜,吴泽佳,黎励文.当心力衰竭遇上慢性阻塞性肺疾病,如何优化β受体阻滞剂治疗?[J].中华心血管病杂志,2020,48(4):344-348.
[3]张开进.慢性阻塞性肺疾病合并心力衰竭诊治进展[J].心血管病学进展,2018,39(3):398-401.
[4] KICHLOO A,MINHAS A M K,JAMAL S,et al.Trends and inpatient outcomes of primary heart failure hospitalizations with a concurrent diagnosis of acute exacerbation of chronic obstructive pulmonary disease (from the national inpatient sample database from 2004 to 2014)[J].Am J Cardiol,2021,150:69-76.
[5] NEDER J A,ROCHA A,ALENCAR M C N,et al. Current challenges in managing comorbid heart failure and COPD[J].Expert Rev Cardiovasc Ther,2018,16(9):653-673.
[6]许文.慢性阻塞性肺疾病急性加重期合并左心衰竭相关危险因素分析[D].恩施:湖北民族大学,2019.
[7]中华医学会心血管病学分会心力衰竭学组,中国医师协会心力衰竭专业委员会,中华心血管病杂志编辑委员会.中国心力衰竭诊断和治疗指南2018[J].中华心血管病杂志,2018,46(10):760-764.
[8]许汝福.Logistic回归变量筛选及回归方法选择实例分析[J].中国循证医学杂志,2016,16(11):1360-1364.
[9]刘丹琴,戴元荣.慢性阻塞性肺疾病对心功能的影响机制[J].中华医学杂志,2015,95(8):628-630.
[10] OGANESYAN A,HOFFNER-HEINIKE A,BARKER A J,et al.Abnormal pulmonary flow is associated with impaired right ventricular coupling in patients with COPD[J].Int J Cardiovasc Imaging,2021,37(10):3039-3048.
[11] NARANG N,DELA CRUZ M,IMAMURA T,et al. Discordance between lactic acidemia and hemodynamics in patients with advanced heart failure[J].Clin Cardiol,2021,44(5):636-645.
[12] BIEGUS J,ZYMLI?SKI R,SOKOLSKI M,et al.Clinical,respiratory,haemodynamic, and metabolic determinants of lactate in heart failure[J].Kardiol Pol,2019,77(1):47-52.
[13] ZHU J J,LIU L J.Analysis of factors influenced by the effectiveness of non-invasive ventilation in the treatment of acute exacerbation of chronic obstructive pulmonary disease with different severities[J].Eur Rev Med Pharmacol Sci,2016,20(22):4775-4781.
[14] PLESNER L L,DALSGAARD M,SCHOU M,et al.The prognostic significance of lung function in stable heart failure outpatients[J].Clin Cardiol,2017,40(11):1145-1151.
[15] MAGNUSSEN H,CANEPA M,ZAMBITO P E,et al.What can we learn from pulmonary function testing in heart failure?[J].Eur J Heart Fail,2017,19(10):1222-1229.
[16] CHERNEVA Z V,DENCHEV S V,CHERNEVA R V.
Echocardiographic predictors of stress induced right ventricular diastolic dysfunction in non-severe chronic obstructive pulmonary disease[J].J Cardiol,2020,76(2):163-170.
[17]畢蓉蓉,郭晓燕,张志华,等.超声心动图对稳定期慢性阻塞性肺疾病患者心脏功能检测价值的分析研究[J].海军医学杂志,2021,42(3):325-328.
[18] PELLICORI P,CLELAND J G F,CLARK A L.Chronic obstructive pulmonary disease and heart failure:a breathless conspiracy[J].Heart Fail Clin,2020,16(1):33-44.
[19]李霞,王健美,朱翔宇.慢性阻塞性肺疾病患者心脏状况的超声心动图研究[J].中国实用医刊,2017,44(8):1-4.
(收稿日期:2023-02-09) (本文编辑:何玉勤)
