不同剂量重组人生长激素对特发性矮小症患儿血清IGF-1和IGFBP-3表达的影响
2023-06-28邓福平陈丹丹李燕燕
邓福平 陈丹丹 李燕燕

【摘要】 目的:探討不同剂量重组人生长激素(rhGH)对特发性矮小症(ISS)患儿血清类胰岛素一号生长因子(IGF-1)和重组人胰岛素样生长因子结合蛋白-3(IGFBP-3)表达的影响。方法:以随机抽签法将2019年11月-2020年12月抚州市第一人民医院收治的90例ISS患儿分为三组(低、中、高剂量组),每组30例。三组均给予常规基础治疗,低、中、高剂量组分别给予皮下注射剂量为0.26、0.35、0.41 mg/kg的rhGH治疗,均连续治疗1年。比较三组治疗前和治疗1年后的生长发育相关指标[身高(Ht)、生长速率(GV)、身高标准差积分(HtSDS)、骨龄]和激素类指标(IGF-1、IGFBP-3)水平,评估三组不良反应发生率。结果:治疗前三组Ht、GV、HtSDS、骨龄比较,差异均无统计学意义(P>0.05);治疗1年后,三组Ht、GV、HtSDS、骨龄比较,差异均有统计学意义(P<0.05);治疗1年后,与低、中剂量组比较,高剂量组Ht、GV、HtSDS、骨龄均明显较优,且中剂量组的GV优于低剂量组(P<0.05)。治疗1年后,高剂量组IGF-1、IGFBP-3水平均高于中、低剂量组(P<0.05)。低、中、高剂量组不良反应发生率分别为6.67%、10.00%、16.67%,三组比较,差异无统计学意义(P>0.05)。结论:与低、中剂量rhGH相比较,给予ISS患儿高剂量rhGH治疗,更能有效促进患儿的生长发育,提高其血清IGF-1、IGFBP-3表达水平,且高剂量rhGH不会增加不良反应发生率,具有较高的安全性。
【关键词】 特发性矮小症 重组人生长激素 类胰岛素一号生长因子 重组人胰岛素样生长因子结合蛋白-3
Effects of Different Doses of Recombinant Human Growth Hormone on the Expression of Serum IGF-1
and IGFBP-3 in Children with Idiopathic Short Stature/DENG Fuping, CHEN Dandan, LI Yanyan. //Medical Innovation of China, 2023, 20(11): 0-039
[Abstract] Objective: To investigate the effects of different doses of Recombinant Human Growth Hormone (rhGH) on the expression of serum insulin-like growth factor-1 (IGF-1) and insulin-like growth factor-binding protein-3 (IGFBP-3) in children with idiopathic short stature (ISS). Method: A total of 90 children with ISS who were admitted to First People's Hospital of Fuzhou from November 2019 to December 2020 were divided into three groups (low, medium and high dose group), according to random drawing of lots, with 30 cases in each group. All the three groups were given routine basic treatment, and the low, medium and high dose group were respectively given rhGH with subcutaneous injection doses of 0.26, 0.35, 0.41 mg/kg, and they were all treated continuously for one year. The levels of growth-related indicators [height (Ht), growth velocity (GV), height standard deviation score (HtSDS) and bone age] and hormone indicators (IGF-1, IGFBP-3) were compared before and after treatment for one year, and the incidence of adverse reactions in the three groups were evaluated. Result: There were no significant differences in Ht, GV, HtSDS and bone age among the three groups before treatment (P>0.05). After treatment for one year, there were significant differences in Ht, GV, HtSDS and bone age among the three groups (P<0.05). After treatment for one year, compared with the low and middle dose group, Ht, GV, HtSDS and bone age in the high dose group were obviously better, and GV in the middle dose group was better than that in the low dose group (P<0.05). After treatment for one year, the levels of IGF-1 and IGFBP-3 in the high dose group were higher than those in the middle and low dose group (P<0.05). The incidence of adverse reactions in low, medium and high dose group respectively were 6.67%, 10.00% and 16.67%, there was no statistical difference among the three groups (P>0.05). Conclusion: Compared with low and medium dose rhGH, high dose rhGH can effectively promote the growth and development of ISS children, improve their serum IGF-1 and IGFBP-3 expression levels, and high dose rhGH will not increase the incidence of adverse reactions, so it has high safety.
[Key words] ISS rhGH IGF-1 IGFBP-3
First-author's address: First People's Hospital of Fuzhou, Jiangxi Province, Fuzhou 344000, China
doi:10.3969/j.issn.1674-4985.2023.11.009
特发性矮小症(ISS)是一种较为常见的内分泌系统疾病。根据流行病学的调查研究结果显示,近年来我国ISS的发病率呈逐渐增长趋势[1]。ISS若不及时给予有效的治疗措施,不仅会导致患儿的生长发育严重滞后,同时也对患儿心理健康和生活质量造成不利影响。目前临床上以重组人生长激素(rhGH)作为ISS的主要治疗手段,通过外源性补充生长激素的方式对患儿的内分泌系统进行调节,从而起到促进患儿骨骼、器官正常发育的作用[2]。但有报道称,有部分ISS患儿在治疗过程中会出现肝肾功能损害等不良反应[3],故合理选择rhGH的使用剂量则显得尤为重要。但目前临床上尚无规范的rhGH用药剂量标准,因此本次研究将对ISS患儿给予不同剂量的rhGH,观察不同剂量的rhGH对ISS患儿血清类胰岛素一号生长因子(IGF-1)和胰岛素样生长因子结合蛋白-3(IGFBP-3)表达水平的影响,现报道如下。
1 资料与方法
1.1 一般资料 选择2019年11月-2020年12月抚州市第一人民医院收治的90例ISS患儿。纳入标准:(1)年龄6~12岁;(2)符合文献[4]《儿科学》中ISS的诊断标准;(3)对本次试验使用的药物无过敏现象。排除标准:(1)近1个月接受过糖皮质激素或内分泌相关治疗;(2)患有染色体病;(3)先天性发育迟缓;(4)合并严重的心理疾病、情感障碍。以随机抽签法将患儿分为三组(低、中、高剂量组),每组30例。本研究已由本院医学伦理委员会获准执行,患儿家属签订相关同意书。
1.2 方法 三组患儿均给予常规的基础治疗:根据患儿实际情况补充维生素、钙制剂,并为其制订科学的饮食和锻炼方案,如多食用新鲜的蔬菜、水果及牛奶、鸡蛋、虾皮、排骨等富含丰富优质蛋白和钙质的食物,定期开展跳高、跳绳等运动锻炼。于患儿每日睡前皮下注射rhGH(生产厂家:Novo Nordisk A/S,批准文号:S20080073,规格:1.5 mL︰5 mg),其中低剂量组注射剂量为0.26 mg/kg,中剂量组注射剂量为0.35 mg/kg,高剂量组注射剂量为0.41 mg/kg,注射部位可选择患儿的大腿内侧或上臂外侧皮下。每周6次,三组患儿均连续治疗1年。
1.3 观察指标及评价标准 (1)生长发育相关指标。分别于三组患儿治疗前和治疗1年后对其左手手腕部位进行X线检查,观察其左手掌指骨、腕骨及桡尺骨下端的骨化中心的发育程度,明确患儿的骨龄,并对其身高(Ht)、生长速率(GV)、身高标准差积分(HtSDS)进行测量和计算,其中GV=两次身高差值/间隔月份×12,HtSDS=(实测身高-同龄身高均值)/同龄身高的标准差。(2)分别采集三组患儿治疗前和治疗1年后的空腹静脉血3 mL,室温放置2 h,3 000 r/min,离心5 min后取上清液,然后应用化学发光法对其IGF-1和IGFBP-3进行检测。(3)评估三组患儿不良反应发生率。
1.4 统计学处理 采用SPSS 21.0软件进行数据处理。正态分布的计量资料以(x±s)表示,多组间比较使用重复测量方差分析,两两比较采用SNK-q检验;不符合正態分布的计量资料用M(P25,P75)表示,比较采用秩和检验;计数资料用率(%)表示,两组间及多组间比较均采用字2检验。P<0.05为差异有统计学意义。
2 结果
2.1 三组一般资料比较 三组在性别、年龄、Tanner分期方面比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
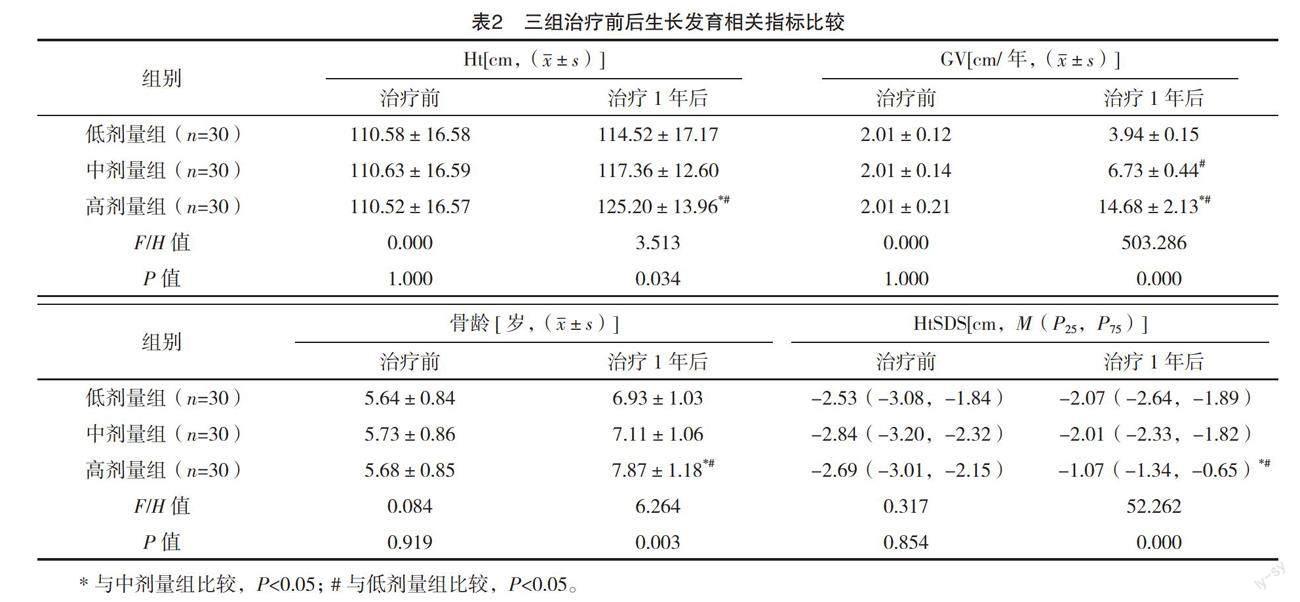
2.2 三组治疗前后生长发育相关指标比较 治疗前三组Ht、GV、HtSDS、骨龄比较,差异均无统计学意义(P>0.05);治疗1年后,三组Ht、GV、HtSDS、骨龄比较,差异均有统计学意义(P<0.05);治疗1年后,与低、中剂量组比较,高剂量组Ht、GV、HtSDS、骨龄均明显较优,且中剂量组的GV优于低剂量组(P<0.05)。见表2。
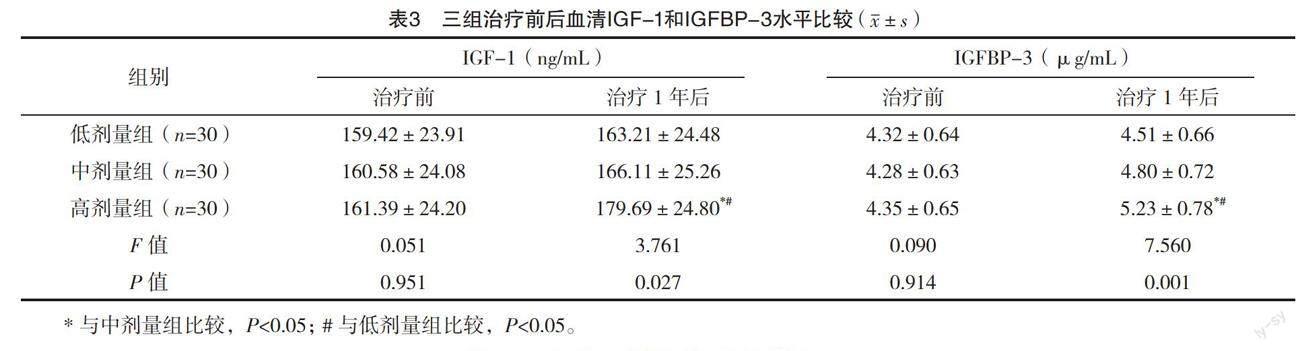
2.3 三组治疗前后血清IGF-1和IGFBP-3水平比较 治疗前三组血清IGF-1和IGFBP-3水平比较,差异均无统计学意义(P>0.05);治疗1年后,三组IGF-1和IGFBP-3水平比较,差异均有统计学意义(P<0.05);治疗1年后,高剂量组IGF-1、IGFBP-3水平均高于中、低剂量组(P<0.05)。见表3。
2.4 三组不良反应发生情况比较 低、中、高剂量组不良反应发生率分别为6.67%、10.00%、16.67%,三组比较,差异无统计学意义(字2=1.575,P=0.455),见表4。
3 讨论
ISS为儿童常见疾病,目前临床上主要采用rhGH治疗,且已有研究报道证实,rhGH能够促进机体代谢,平衡生长激素的分泌功能,补充机体所需的生长激素[5-6],表明采用rhGH对ISS患儿进行治疗具有一定的临床价值。但目前临床上对rhGH剂量的选择尚无统一定论,儿科临床规范建议应用剂量应控制在0.1~0.2 IU/(kg·d)[7-8]。
为进一步分析对ISS患儿给予不同剂量rhGH的临床效果,本次试验分别采用低、中、高剂量rhGH治疗90例ISS患儿,结果显示,治疗1年后,高剂量组Ht、GV、HtSDS、骨龄均优于中、低剂量组,提示给予ISS患儿高剂量rhGH更能有效促进患儿的生长发育,改善未来身高成长结局。考虑原因可能是因为rhGH的氨基酸含量、蛋白质结构与人体垂体分泌生长激素的性质几乎完全相同,通过外源性补充生长激素的方式能促进ISS患儿的器官和骨骼发育,从而促使患儿的身体素质恢复至健康儿童的平均水平[9-11]。故而和低、中剂量的rhGH治疗相比,高剂量的rhGH可发挥更为显著的功效,从而进一步提高治疗效果,促进ISS患儿的生长发育。
IGF-1是一种由肝、肾等内脏细胞合成的与胰岛素类似的多肽蛋白物质,在促进机体内持续性进行合成代谢作用方面具有十分重要的意义,是人体生长发育不可缺少的生理因子[12]。且有报道称,IGF-1能有效促进软骨细胞的增殖,进而促进骨骼的生长[13-14]。而IGFBP-3则对细胞的代谢和增殖具有一定的调节作用,且其表达水平和生长激素有紧密关联,也是检测生长激素水平变化的重要指标[15]。本次研究结果显示,治疗1年后,高剂量组IGF-1、IGFBP-3水平均高于中、低剂量组,提示将高剂量rhGH应用于ISS患儿的治疗当中,更能有效改善患儿的IGF-1、IGFBP-3水平。考虑原因可能是rhGH作为治疗ISS的首选药物,对基因的活化具有一定的促进作用,能诱导新蛋白质的产生,促进细胞的新陈代谢,因此,给予高剂量的rhGH,对ISS患儿生长激素的分泌可起到一定的改善作用,并能有效对自身结构所引起的分泌不足起到调节作用,同时也可对生长激素受体起到刺激作用,进而激活IGF-1、IGFBP-3等生理因子的功能,在改善ISS患儿细胞发育,促进生长方面具有积极意义[16-17]。这与田金富等[18]研究结果基本相符。除此之外,在不良反应发生率方面,三组不良反应发生率比较差异不明显,提示采用高剂量rhGH对ISS患儿进行治疗不会增加不良反应发生风险,具有较高的安全性。究其原因可能是因为0.41 mg/kg剂量的rhGH尚在患儿机体可耐受的范围内,同时在本次试验中,患儿每周用药6 d而并非连续使用,在一定程度上也降低了不良反应发生风险[19]。郭艳艳等[20]在报道中提出,给予ISS患儿大剂量的rhGH治疗不会损害患儿的机体功能,能在保证临床效果的同时具有一定的安全性,这与本次试验结果基本相符。
综上所述,对ISS患儿给予大剂量rhGH治疗,临床效果显著,能有效促进患儿的生长发育,提高其血清IGF-1、IGFBP-3表达水平,且不会增加不良反应发生风险,具有一定的安全性,值得在临床推广和应用。
参考文献
[1]王晶晶,林彬,郑金炉,等.注射用重组人生长激素给药剂量与矮小症患儿临床疗效的相关性分析[J].中国优生与遗传杂志,2020,28(10):1257-1259.
[2]夏雅,潘秋飞,吴安乐,等.重组人生长激素治疗特发性矮身材儿童对骨代谢指标的影响[J].中国妇幼健康研究,2020,31(1):30-34.
[3]袁红虹,韩雯雯,王静静.大剂量重组人生长激素治疗对矮小症患儿生长发育相关指标的影响[J].临床误诊误治,2021,34(12):104-107.
[4]申昆玲.儿科学[M].北京:高等教育出版社,2012.
[5]邓建荣,林小芹,肖小兵,等.基因重组人生长激素治疗不同骨龄的特发性身材矮小儿童对比观察[J].海峡药学,2020,32(11):140-142.
[6]林韬,李莹华,连雅雯,等.重组人生长激素对局灶性脑缺血再灌注小鼠运动功能的改善作用及其机制[J].吉林大学学报(医学版),2022,48(3):568-574.
[7] SOLIMAN A T,ELAWWA A,ITANI M,et al.Responses to growth hormone (GH) therapy in short children with normal GH secretion and no bone age delay: an analysis of potential factors affecting their response to rhGH therapy. A controlled study[J].Acta Biomed,2019,90(8):43-51.
[8]宋祥春,萨初然贵,牛红艳.皮下注射重组人生长激素治疗小儿生长激素缺乏症与特发性矮小症的临床效果[J].中国医药科学,2022,12(14):77-80.
[9]步佳霖,温丙友,姚玲.重组人生长激素联合心理干预治疗特发性矮小症患儿的疗效及机制研究[J].中国现代医学杂志,2021,31(20):91-96.
[10]徐露莲,刘珍珍,徐旭.重组人生长激素对特发性矮小症患儿糖代谢及PINP、β-CTX、IGF-1水平的影响[J].當代医药论丛,2022,20(3):121-124.
[11] PALTOGLOU G,DIMITROPOULOS I,KOURLABA G,et al.The effect of treatment with recombinant human growth hormone (rhGH) on linear growth and adult height in children with idiopathic short stature (ISS): a systematic review and meta-analysis[J].J Pediatr Endocrinol Metab,2020,33(12):1577-1588.
[12]葛青玮,朱志颖.IGF-1、IGFBP3及其比值与生长激素缺乏型矮小症的相关性研究[J].临床和实验医学杂志,2017,16(3):255-257.
[13]肖青凤,吴琰,史晓宁,等.不同剂量重组人生长激素治疗对特发性矮小症患儿骨代谢、甲状腺功能和血清Ghrelin、IGF-1水平的影响[J].现代生物医学进展,2021,21(23):4569-4572,4582.
[14] MATEJEK T,NAVRATILOVA M,ZALOUDKOVA L,et al.
Vitamin D status of very low birth weight infants at birth and the effects of generally recommended supplementation on their vitamin D levels at discharge[J].J Matern Fetal Neonatal Med,2020,33(22):3784-3790.
[15]张明英,钱莹,高龙,等.重组人生长激素对特发性矮小症患者的内分泌轴GHRH/GH/IGF-1的影响[J].哈尔滨医科大学学报,2022,56(1):47-50.
[16]吴雄基.重组人生长激素治疗儿童特发性矮小的效果及对血清IGF-1水平的影响探讨[J].医药前沿,2020,10(33):141-143.
[17]庞兴甫,谭华清,李峥,等.重组人生长激素治疗特发性矮小症对骨代谢的疗效及安全性[J].中国妇幼保健,2021,36(10):2269-2271.
[18]田金富,李芳,赵娜,等.重组人生长激素联合营养支持对特发性矮小症患儿身体构成和血清IGF-1水平的影响[J].罕少疾病杂志,2022,29(7):105-106,112.
[19]符艺影,邢东文,王华,等.特发性矮小儿童血清IGF-1和IGFBP-3水平与生长体格的关系[J].临床和实验医学杂志,2020,19(16):1692-1697.
[20]郭艳艳,蒋成霞,姚兰,等.不同剂量重组人生长激素治疗对特发性矮小症患儿身高、体重以及血清IGF-1和IGFBP-3表达的影响[J].解放军医药杂志,2020,32(3):44-47.
(收稿日期:2022-10-27) (本文编辑:陈韵)
