基于U-net33+的宫颈癌后装治疗中靶区和危及器官位置的预测
2023-06-14杨日赠吴德华
李 霞,杨 磊,杨日赠,吴德华
1南方医科大学南方医院放疗科,广东 广州 510515;2赣州市人民医院(南方医院赣州医院)肿瘤科,江西 赣州341000
宫颈癌是全球发病率第4位的恶性肿瘤,严重威胁女性健康[1]。国际妇产科联盟推荐外照射结合后装治疗作为宫颈癌的重要的治疗手段[2-4]。在精准放疗的大背景下,三维后装治疗计划的应用进一步提高了宫颈癌患者的疗效,而精准的靶区和危及器官的轮廓勾画是三维后装治疗计划的基本要求[5]。但在实际工作中,放疗医生常常使用手工勾画的方式,费时费力,且一致性差[6]。靶区勾画阶段在医生给患者实施施源器植入术后进行,患者需等待较长时间方可进入治疗阶段,并在此期间尽量保持体位不变,缩短患者的等待时间尤为迫切,进一步缩短模型训练及预测时间十分必要。深度学习[7]作为人工智能[8]中非常重要的一种方法,广泛应用于自动勾画及位置预测中,并取得良好的效果。在近距离放射治疗中,已有学者将深度学习应用于前列腺恶性肿瘤的相关研究[9],但在宫颈癌的研究中,大多数应用外照射治疗[10],或聚焦于近距离治疗的剂量学研究[11-13],同时存在病例较少和使用较旧的网络架构等问题。将最新深度学习网络架构应用于后装治疗中靶区和危及器官的位置预测研究未见报道。本研究拟通过构建基于最新的U-net3+架构的端到端自动分割框架,降低模型参数量,提高运行效率,缩短患者等待时间,使用双中心数据进行模型构建和验证,并对人工及自动勾画结果进行对比,探讨U-net3+架构自动位置预测模型在临床中的应用价值。
1 资料与方法
1.1 一般资料
本研究回顾性收集了南方医科大学南方医院放疗科及赣州市人民医院(南方医院赣州医院)肿瘤科2017年4月~2022年8月的共213例宫颈癌患者的CT图像,其中南方医科大学南方医院159例,赣州市人民医院(南方医院赣州医院)54例。纳入标准:均为接受后装治疗插植针植入术的宫颈癌患者。排除标准:只使用单一宫腔管或者穹窿管进行后装治疗的宫颈癌患者。213例患者的年龄为42~77岁,平均56.9岁;均经病理证实,根据国际妇产科联盟分期原则,分别有ⅡA期30例,ⅡB期51例,ⅢB期102例,ⅣA期30例。本研究获得了医院医学伦理委员会的批准,并免除患者知情同意。
1.2 施源器置入、CT图像获取
放疗医生根据患者初步获取的CT图像进行宫腔管的选取,确定适当的插植针数量,并以徒手的方式进行宫腔管置入及插植针的植入。本研究采用飞利浦Brilliance型号大孔径16排CT模拟定位机进行图像采集,扫描电压为140 kV,扫描电流为250 mAs,扫描层厚及层距为3 mm,所有建模及测试的CT图像均统一为DICOM格式,图像分辨率为512×512。所有CT图像均使用直方图均衡化预处理程序将亮度分布进行一致化处理。在获取CT图像时,医生会根据患者膀胱充盈情况,通过提前插好的导尿管注入50~200 mL加有造影剂的生理盐水。为了更好地显示膀胱轮廓,将无菌造影剂与生理盐水以3:100的比例配比,均匀混合后通过留置尿管注入患者膀胱内。最终将获取的CT影像传输至计划系统(瑞典Oncentra)。
1.3 图像勾画
特征轮廓由具有5年以上宫颈癌后装治疗经验的临床医生进行手动勾画,根据欧洲放射治疗与肿瘤学学会临床指南中3D图像引导后装治疗工作组的推荐[14]分别进行高危临床靶区(HRCTV)和危及器官的勾画(图1)。本研究中包含的危及器官主要有膀胱、直肠、小肠。
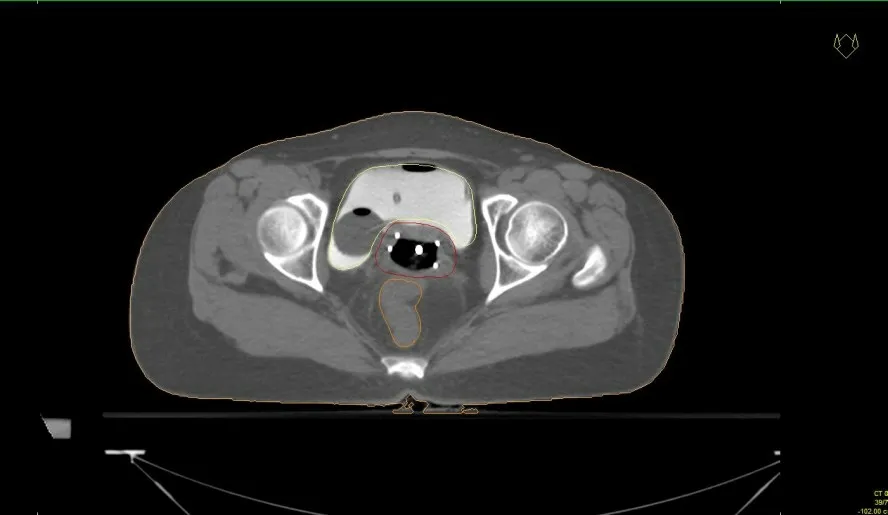
图1 后装放射治疗结构轮廓图Fig.1 Contouring of the structures of after-loading radiation therapy
1.4 自动预测模型构建
U-net[15]广泛应用于图像分割、位置预测等图像处理任务,特别是医学图像处理。U-net3+是U-net的最新改进框架,在多个数据集中均显示出性能上的优势[16]。本研究使用U-net3+深度神经网络作为框架(图2),通过下采样并增加通道使数据量保持一致,最后通过反向的上采样和缩减通道,最终输出和输入矩阵一致的图像。由于U-net3+可将特征图进行融合,增加了图像通道,从而进一步提高了分割精度[17]。
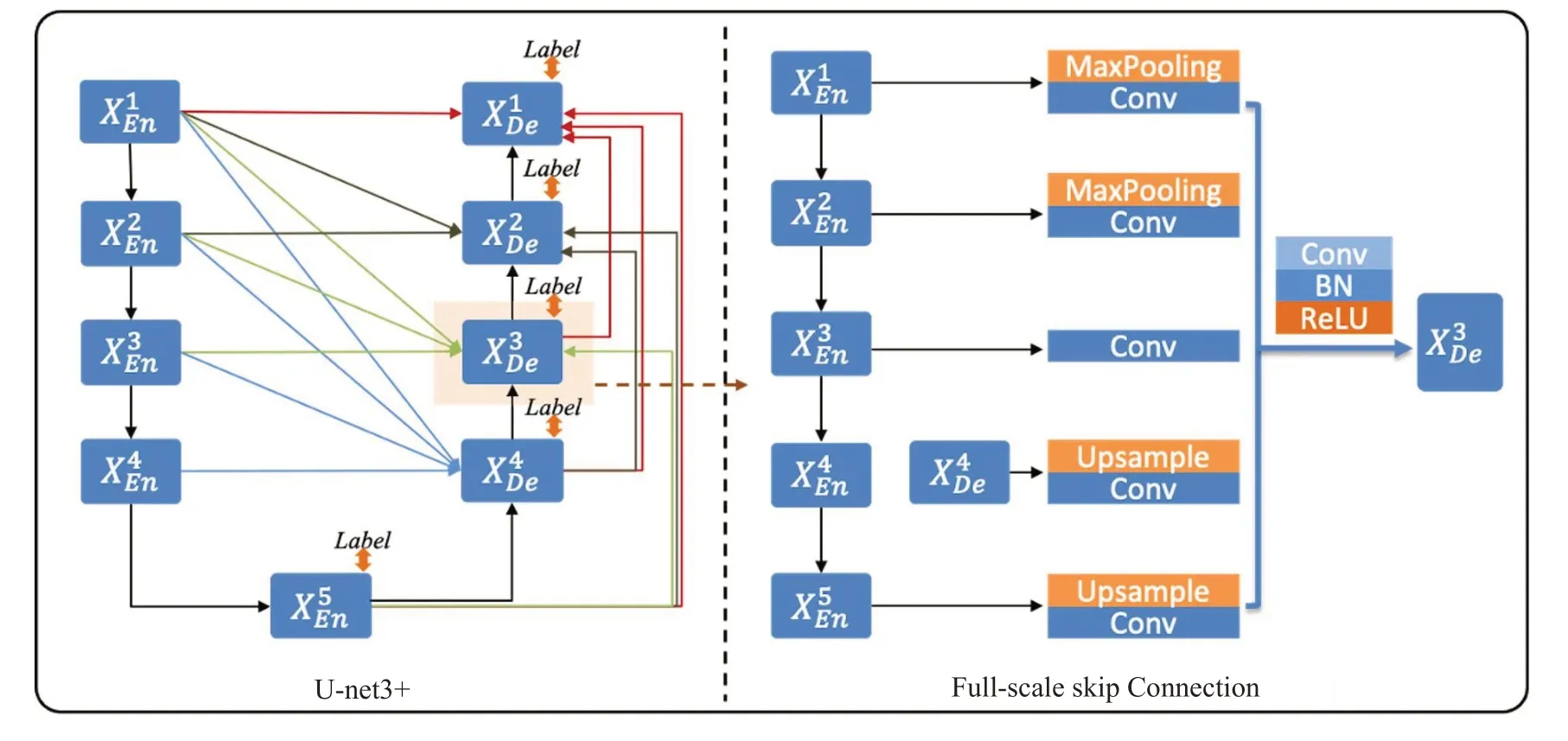
图2 U-net3+网络框架Fig.2 U-net3+network framework.
1.5 模型训练
随机从赣州市人民医院的54例数据中抽取21例作为最终测试集,在其余数据随机抽取训练集149例,验证集43例,以实现训练集、验证集和测试集为7:2:1的比例。训练的内容包括HRCTV、膀胱、直肠、小肠4个部分。实验使用基于Python的Keras框架[18]来进行模型的构建。训练Epoch为200,batch_size为16。使用Adam作为优化器,learning rate[19]为0.0001,使用戴斯相似系数(DSC)作为损失函数。硬件平台采用Intel Xeon E5@3.20GHz处理器,内存为64 GB,2块NVIDIA GeForce RTX™3080 Ti GPU。
1.6 评估方法
使用豪斯多夫距离(HD)[20]和DSC[21]来评估模型。HD的公式如下:
其中h(A,B)表示来自A集合中任意每一个点,到B集合中的最小距离的最大值。HD越小,表示位置预测模型预测效果越好。
DSC的公式如下:
其中A是医生勾画部分,B是模型预测部分,分子是医生勾画部分与模型预测部分的2倍,分母是医生勾画部分与模型预测部分两者的并集。DSC越大,模型效果越好。
2 结果
2.1 训练结果
绘制训练过程曲线可见模型在经历200 个批次Epoch 训练之后,逐渐收敛并趋于稳定(图3)。位置预测模型中验证集损失函数[22-23]分别为:膀胱0.05、直肠0.03、小肠0.06。位置预测模型中HRCTV模型验证集损失函数最终收敛值为0.06。
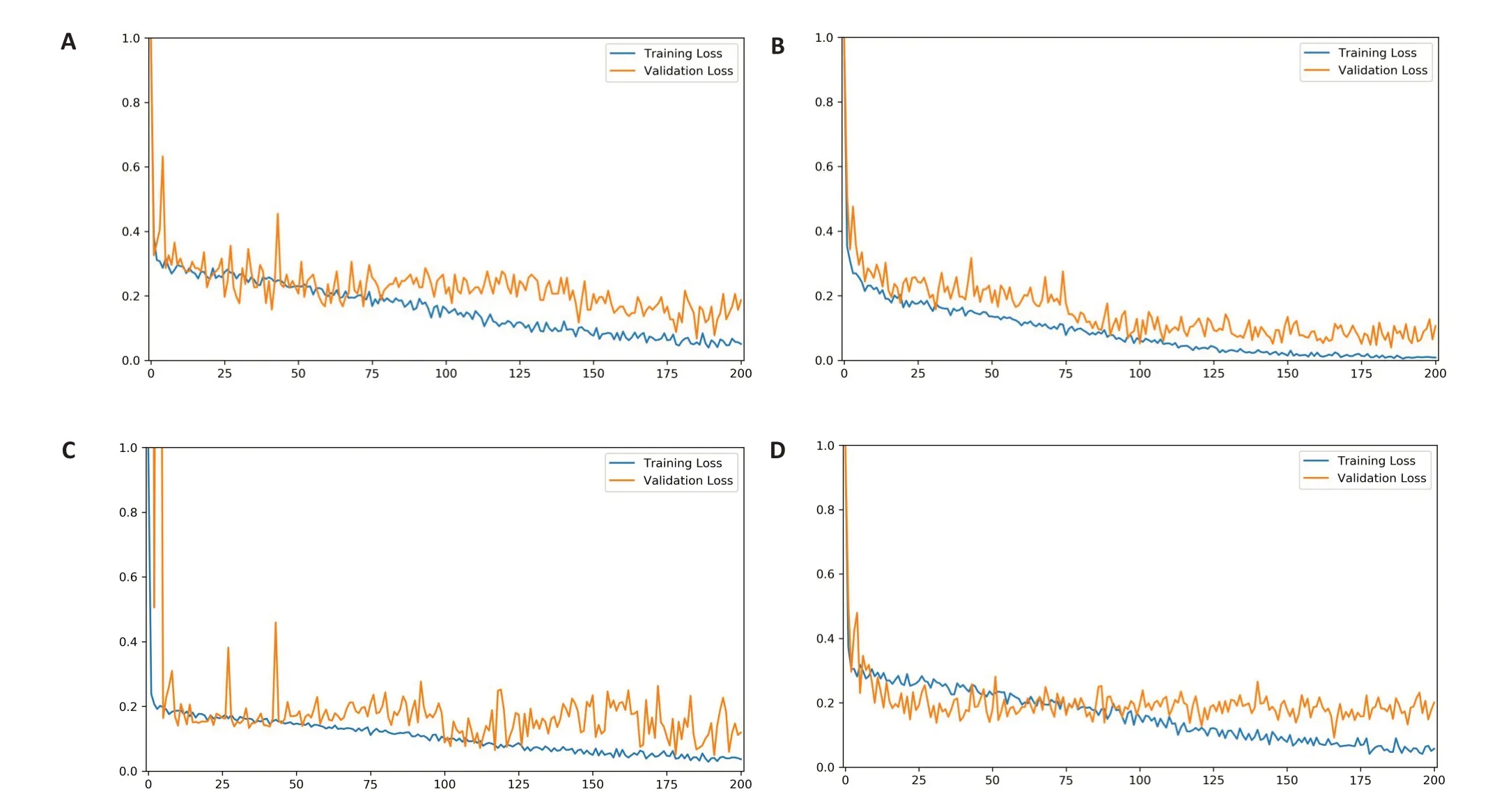
图3 损失值随训练次数变化曲线Fig.3 Loss value changing with the times of training.A:Bladder;B:Rectum;C:Small intestine;D:HRCTV.
2.2 模型自动预测位置结果
在对危及器官的位置预测中,平均DSC 值为0.898,平均HD值为5.4 mm,位置预测模型对危及器官及靶区的预测结果显示(表1),膀胱的DSC值为0.953,直肠和小肠的DSC 值分别为0.885 和0.857。在对HRCTV的训练中,DSC值为0.869,HD值为8.1 mm。自动勾画结果(图4)。

表1 位置预测准确性结果Tab.1 Quantification of the accuracy of automatic segmentation
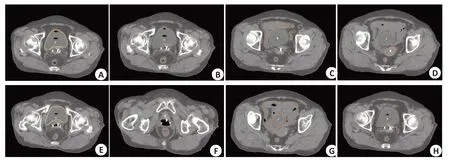
图4 自动勾画结果Fig.4 Automatic segmentation results.A and E,B and F,C and G,D and H indicated the bladder,rectum,small intestine and HRCTV outline results respectively,while A and E indicated the bladder outline results of case 1 and case 2 respectively,B and F indicated the rectum outline results of case 1 and case 2 respectively,C and G indicated the small intestine outline results of case 1 and case 2 respectively,D and H indicated the HRCTV outline results of case 1 and case 2 respectively.The yellow line indicated the manually outlined contour line,and the red line indicated the automatically outlined result.
3 讨论
本课题基于新型的U-net3+神经网络,构建了宫颈恶性肿瘤患者在接受后装放射治疗时HRCTV和周围危及器官膀胱、直肠、小肠的自动位置预测模型并进行验证。针对传统的U-net神经网络训练工作量大、数据集训练耗时较长等问题,U-net3+神经网络对特征信息的提取更加敏感,分割更加精准,加上其先进的网络构架,使得训练时间进一步下降。
本研究采用了双中心数据,使用一个中心的数据进行建模,使用另一个中心的数据进行测试。双中心数据的使用和相应的实验设计提高了模型的泛化能力和鲁棒性[24-26]。实验结果表明,在这个模型下,所研究的各轮廓特征信息提取结果较好,达到了预期效果,其中膀胱的位置预测准确性较高,DSC值达0.953,优于其他研究结果[10],而因患者肠道准备情况不同,加上肠道本身的蠕动,高危临床靶区的位置和大小都有一定差别,直肠、小肠和HRCTV的结果相对较低。肠道中存在的气体以及尿管气囊中的气体在CT图像想表现为低密度区域,这都对实验结果的准确性产生一定影响。
本研究在数据处理时,用于训练集的轮廓信息来源于人工勾画,虽然选择了有经验的临床医生进行勾画,但是仍可能存在一定主观偏差,我们将在未来的工作中继续深入挖掘,进一步改进方法,提高算法的泛化能力、准确率和鲁棒性。
综上所述,本研究所采用的深度学习模型对特征部位的分割结果良好,位置预测准确性较高,且模型训练耗时少,大大缩短了患者治疗前的等待时间,提高患者依从性,为肿瘤患者进一步实现精准放射治疗打下了坚实的理论基础,有望应用于临床,对临床工作有一定的指导作用。但在实际临床工作中,因为肠道蠕动等多种因素使得自动勾画结果会有一定偏差,这就要求临床医生在使用自动勾画初步获得对应解剖结构轮廓以后做出评估和适当修改。