急性前循环大血管闭塞性轻型卒中血管内治疗的疗效分析
2023-05-29王建懿商苏杭韩建峰刘福德
王建懿,商苏杭,陈 晨,于 嘉,韩建峰,刘福德
(西安交通大学第一附属医院神经内科,陕西西安 710061)
短暂性脑缺血发作(transient ischemic attack,TIA)及轻型卒中通常被认为是症状轻、结局良好的一类疾病,但部分TIA 及轻型卒中患者经过影像学评估后发现其合并大血管闭塞(LVO)。TIA 和轻型卒中的急诊治疗对早期复发性脑卒中的影响研究(effect of urgent treatment of transient ischemic attack and minor stroke on early recurrent stroke,EXPRESS study)显示,轻型卒中合并LVO 患者在院卒中复发率高,约1/3患者90 d功能结局不良,不能独立行走或生活,遗留残疾,是早期神经功能恶化和预后结局差的重要影响因素,而积极有效的早期干预可使卒中复发风险降低80%[1]。目前指南推荐,对于发病6 h以内及发病6~24 h经影像学评估存在组织窗错配的前循环大血管闭塞性中重度脑梗死患者行血管内治疗[2],对于TIA 及轻型卒中(NIHSS≤5分)合并LVO的积极再灌注治疗(包括静脉溶栓、血管内治疗)由于获益不明确,临床常被忽略。因此,面对这部分患者时,临床医师面临平衡相对较轻的神经功能缺损与接受血管内治疗的风险-获益比的挑战。为此,本研究纳入单中心急性前循环大血管闭塞性轻型卒中接受血管内治疗患者的临床资料,旨在分析积极再灌注治疗与这部分患者预后改善的关系,以期对临床工作有借鉴意义。
1 对象与方法
1.1 研究对象
回顾性分析2018年1月至2021年8月在西安交通大学第一附属医院连续收治的38例急性前循环大血管闭塞性轻型卒中接受血管内治疗患者的临床资料。轻型卒中定义为NIHSS评分≤5分[3]。纳入标准:①年龄>18岁;②术前经头颅CT 或MRI检查排除颅内出血;③NIHSS评分≤5分;④经MRA 或DSA 证实为前循环大血管(颈内动脉或大脑中动脉M1段)闭塞;⑤经三维动脉自旋标记成像(three dimensioned arterial spin labelling,3D-ASL)评估责任血管侧脑血流低灌注;⑥发病前改良Rankin量表(modified Rankin scale,m RS)评分≤1分;⑦患者或家属签署知情同意书。排除标准:①颅内出血病史或有出血倾向患者;②CT 或MRI提示大面积脑梗死(梗死体积≥70 m L,梗死体积>1/3 MCA 供血区或CT/DWI影像ASPECTS评分<6分);③NIHSS评分≥6分;④术前血小板计数<50×109/L;⑤随机血糖<2.78 mmol/L或>22.20 mmol/L;⑥难以控制的高血压(收缩压>185 mm Hg或舒张压>110 mmHg);⑦有心脏、肺、肾脏等严重器质性疾病;⑧预期寿命可能少于90 d;⑨研究者判断不适合入选的其他情况。
1.2 研究方法
1.2.1临床资料收集 收集患者的临床资料,包括年龄、性别、既往高血压、心房颤动、糖尿病病史、缺血性卒中或TIA 病史、随机血糖、术前血小板计数、基线收缩压水平、闭塞部位、是否桥接治疗(即静脉溶栓联合机械取栓治疗)。对于行桥接治疗患者,收集麻醉方式及穿刺至血管再通的时间。
1.2.2术前评估 根据术前头颅CT平扫或DWI检查进行ASPECTS评分,MRA 或DSA 检查确认急性前循环大血管闭塞,3D-ASL评估脑血流灌注情况。
1.2.3手术过程 局部浸润麻醉或全身麻醉下,采用常规改良Seldinger法穿刺股动脉成功后置入8F动脉鞘(日本泰尔茂公司),DSA 检查明确血管闭塞部位、闭塞长度、侧支循环代偿情况等。对于颈动脉C1段闭塞,采用8F导引导管支撑下顺利释放远端保护装置(Spider,美国ev3公司),球囊亚满意扩张闭塞段后采用导引导管抽吸局部血栓,顺利释放颈动脉支架;对于颈内动脉C4-C7段及大脑中动脉闭塞,采用8F导引导管和125 cm 6F中间导管建立通路,微导丝(Synchro2,美国史塞克公司)引导微导管(Rebar-18,美国美敦力公司)通过闭塞段后撤出微导丝,造影确定血管真腔及血栓长度,术者根据血管闭塞情况综合判断选择合适取栓支架,释放支架后再次造影判断闭塞性质,选择进一步手术策略,包括支架取栓、球囊扩张、支架置入和动脉推注替罗非班等方法再通血管。本中心使用的取栓支架包括Solitaire FR、RECO、Trevo等,球囊包括赛诺、加奇等,置入支架包括Wallstent、Neuroform EZ、Enterprise、Apollo等。术后患者均返回神经内科重症监护病房,密切监测生命体征及神经功能情况,动态复查头颅CT,个体化原则进行抗栓治疗。
1.2.4围手术期抗栓方案 对于在溶栓时间窗内符合溶栓适应证且无溶栓禁忌证的患者予以阿替普酶静脉溶栓,桥接治疗患者术中不进行全身肝素化,直接取栓患者进行全身肝素化。对于考虑机制为动脉粥样硬化性闭塞患者,术中根据体质量动脉给予负荷量替罗非班后静脉持续泵入24 h,复查头颅CT 排除出血后予以负荷量抗血小板药物(阿司匹林300 mg+波立维300 mg)口服并与替罗非班重叠6 h。术后48 h开始阿司匹林100 mg联合波立维75 mg抗血小板聚集,3个月后改为阿司匹林100 mg单药长期口服;对于发病机制为心源性栓塞患者,术后根据中国心源性卒中防治指南(2019)启动抗凝治疗[4]。
1.2.5疗效评估 主要疗效终点事件:90 d良好预后率(m RS评分≤2分)。血管成功再通采用改良脑梗死溶栓分级(modified thrombolysis in cerebral infarction,m TICI)来评价,将m TICI分级≥2b定义为血管成功再通[5]。技术安全性包括术中血栓逃逸发生率和血管穿孔出血,术后24 h症状性颅内出血(symptomatic intracerebral hemorrhage,sICH)及死亡。术后24 h sICH 定义为术后24 h 内复查头颅CT 示颅内新发出血灶并引起神经功能恶化(NIHSS增加≥4分)或死亡[6]。
1.3 统计学分析
采用SPSS 20.0 软件对数据进行统计学分析。计数资料以率(%)表示,符合正态分布的计量资料以±s表示;不符合正态分布的计量资料以中位数(M)[四分位数(P25~P75)]表示,组间比较采用Wilcoxon秩和检验。P<0.05表示差异具有统计学意义。
2 结 果
2.1 一般资料
本研究共纳入38例患者,男性21例(55.3%),女性17例(44.7%),年龄范围34~81岁,平均年龄(62.89±12.41)岁。既往高血压病史12例(31.6%)、心房颤动病史4例(10.5%)、糖尿病病史8例(21.1%),缺血性卒中或TIA 病史2例(5.3%),术前NIHSS评分平均为4 分(4~5 分),ASPECTS 评分平均为9分(8~9 分),桥接治疗4 例(10.5%),外院转入12例(31.6%),全身麻醉21例(55.3%)。38例责任病变血管为颈内动脉C1 段闭塞9 例(23.7%),C4-C7段闭塞10 例(26.3%),大脑中动脉M1 段19例(50%)。血管闭塞性质为动脉粥样硬化性狭窄23例(60.5%),动脉夹层6例(15.8%),心源性栓塞5例(13.2%),串联病变2 例(5.3%),不明原因型2例(5.3%)(表1)。
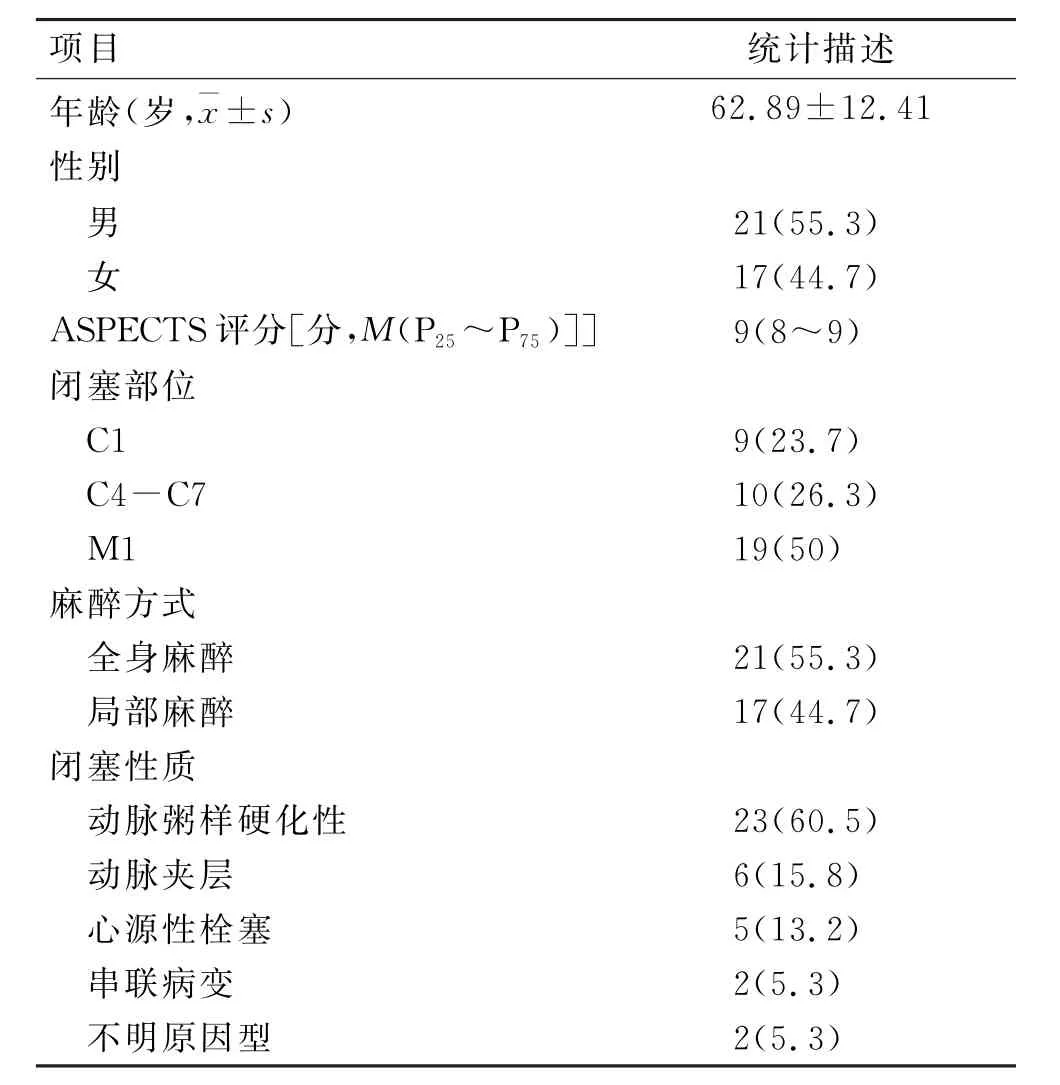
表1 基线数据Tab.1 Baseline characteristics [n(%)]
2.2 治疗及随访情况
38例患者均顺利完成血管内治疗手术,血管成功再通率为100%(m TICI≥2b),其中3 级再通33 例(86.8%),穿刺至手术结束时间平均为(55.76±11.11)min。术中未发生血管穿孔出血事件,血栓逃逸3例(7.9%),1例采用补救性支架取栓实现血管完全再通,2 例采用动脉注射替罗非班后实现再通(m TICI:2b),术后24 h sICH 1例(2.6%),未发生死亡事件。出院时NIHSS评分平均为1分(0~1)分,与术前NIHSS评分平均分4分(4~5分)相比,差异具有统计学意义(P<0.01)。34例患者完成临床及影像学随访,90 d预 后 良 好(mRS 评 分≤2 分)患 者31 例(91.2%),其 中mRS 0 分 患 者21 例(61.8%),mRS 1分患者7例(20.6%),随访期间无TIA 或新发脑梗死事件及死亡发生,影像学随访病变血管通畅性良好,支架置入患者未发生支架内再狭窄。
典型病例:39 岁女性患者,既往高血压病3 级(很高危)、2 型糖尿病病史,因“左侧肢体活动不灵6 h”入院,入院时NIHSS评分4分。急诊完善头颅MRI提示大脑半球多发新鲜梗死灶,右侧半球低灌注合并右侧颈内动脉闭塞。急诊造影提示右侧颈内动脉眼动脉段以远闭塞,急诊予以球囊扩张血管成型后,同期予以支架置入,术后患者血流再通良好,m TICI 3级(图1)。
3 讨 论
对于发病6 h内及6~24 h符合影像学组织“错配”标准的中重型缺血性卒中(NIHSS≥6分)的急性前循环LVO患者,2018年美国AHA指南最高级别推荐机械取栓术为治疗方案[7]。轻型卒中合并急性前循环LVO患者是否应早期行血管内治疗,目前缺乏高级别的临床随机对照研究支持证据,多为回顾性研究分析,且现有指南也无明确推荐。颅内LVO是轻型卒中早期神经功能恶化,导致不良预后的较强预测因子之一。文献报道,临床表现为急性运动或语言功能障碍的轻型卒中或TIA 的患者中,有10%~15%存在颅内外动脉严重狭窄或闭塞[8]。仅给予内科保守治疗,部分患者在入院24 h内会出现早期病情恶化,梗死范围在起始小面积基础上持续增大,90 d内出现中度残疾,造成生活质量严重下降,甚至1%~2%的患者死于卒中相关并发症[9]。因此,临床应高度重视大血管闭塞性轻型卒中的治疗,血管内治疗似乎为轻型卒中患者的良好预后提供了可能。
DA ROS等[10]分析欧洲卒中中心数据库中轻型卒中(NIHSS≤5分)合并LVO 的数据发现,仅接受静脉溶栓治疗的患者血管成功再通率为38%,单纯机械取栓或者桥接治疗的患者血管成功再通率为100%。多因素分析显示,机械取栓是早期(发病<12 h)NIHSS评分向有利方向转变及出院时NIHSS评分降低的唯一预测因素,同时机械取栓治疗与患者90 d良好预后呈正相关。HAUSSEN 等[11]分析两个大型前瞻性轻型卒中合并LVO 的患者行血管内治疗或药物治疗的研究显示,血管内治疗是NIHSS评分向有利方向转变(P=0.02)、出院(P<0.01)和3~6个月随访时(P<0.01)功能独立的唯一预测因素。因此,有学者认为,对于轻型卒中(NIHSS 评分≤5)合并LVO 患者,机械取栓与出院时NIHSS 评分的有利转变及良好预后相关。本研究血管成功再通率为100%,出院时NIHSS评分较手术前NIHSS评分显著改善(P<0.01),90 d良好预后率91.2%,且血管内治疗患者随访过程中显示较高的生活独立性,进一步证明了血管内治疗可能与轻型卒中患者出院时NIHSS评分的改善相关。血管内治疗对于轻型卒中合并LVO 是有效的治疗方式,其安全性也备受重视。本研究中3例血栓逃逸事件均得到补救性再通,术后24 h sICH 事件1例,未出现血管穿孔及死亡事件,我们认为手术是安全的。HILL 等[12]发现血管内治疗的手术并发症(包括血管穿孔、蛛网膜下腔出血、sICH 等)发生率较低(≤2%)。TOTH等[13]进行的血管内治疗轻型卒中合并LVO 患者的前瞻性研究显示,血管内治疗成功率高达95%,未出现sICH,95%患者随访预后良好,出院及随访时NIHSS评分较术前均有显著改善。
前循环轻型卒中伴LVO 患者的血管内治疗存在多重难点,首先为适应证的把握,目前尚不清楚如何鉴别适合血管内治疗或药物保守治疗的患者。多模神经影像学评估可很好地识别出大血管闭塞,国外也有文献报道可通过床旁观察患者坐起后是否因重力因素导致的脑灌注压降低而出现神经功能症状恶化的简单方法识别是否为大血管病变,该方法灵敏度较低,但特异性较高[12]。本研究纳入的病例均采用多模态磁共振显示责任血管的闭塞部位、异常灌注部位、范围及血流灌注状况,帮助识别LVO 导致的血流动力学改变,以帮助制定最佳治疗方式。其次为血管内治疗的时机。目前该类患者应立即行血管内治疗,还是在规范药物治疗基础上出现神经功能恶化(early neurological deterioration,END)后行挽救性治疗依然存在争议。NAGEL 等[14]分析六大国际综合卒中中心低NIHSS评分的LVO 患者研究结果显示,立即治疗组良好预后的可能性较END 挽救性治疗组显著增高(OR=3.1,95%CI:1.4~6.9),立即治疗组90 d 良好预后率也显著增加(84.4%vs.70.1%,P=0.03),但立即治疗组sICH 发生率高于挽救性治疗组患者(5%vs.1.4%,P=0.08)。本研究立即治疗组26 例,END 后挽救性血管内治疗12例,术后24 h sICH 发生率2.6%,略低于文献报道,有效性及安全性均令人满意。最后为血管内治疗的策略。随着材料科学的发展和技术理念的进步,在严格把握适应证和选择合适时机的前提下,经验丰富的卒中中心术者根据血管闭塞原因制订个体化手术策略,手术的安全性和有效性均得到极大的提升。本研究对于心源性栓塞建议在球囊导引导管近端血流阻断基础上采用取栓支架联合中间导管,尽可能完整取出血栓,降低血栓逃逸风险;对于动脉粥样硬化狭窄采取支架取栓后球囊扩张或支架成形术;对于夹层病变选择支架成形术。
综上所述,本研究初步表明,对于急性前循环大血管闭塞性轻型卒中,经多模态影像评估指导的血管内治疗具有较高的有效性和安全性,积极恢复血流再灌注可显著改善患者临床预后。但本研究设计为单中心回顾性观察研究,纳入病例数偏少,更大的样本量可使统计结果更有说服力;其次缺乏与最佳药物组对照,进而可能影响研究结果的可靠性。将来仍需要更多高级别的多中心前瞻性随机对照临床试验提供循证医学证据。
