利格列汀联合贝那鲁肽治疗T2DM 对糖脂代谢及骨代谢的影响
2023-05-27马露余勤郭向阳
马露 余勤 郭向阳
(1.信阳职业技术学院附属医院内分泌科,河南 信阳 464000;2.郑州大学第一附属医院内分泌科,河南 郑州 450000;3.信阳市中心医院内分泌科,河南 信阳 464000)
调查数据表明,我国成人患糖尿病的发生率高达11.2%,其中超过90%为2型糖尿病(T2DM)。患者长期处在高血糖水平,可使机体多个器官发生慢性损害,进而危及患者生命健康[1]。T2DM 的发病机制与胰岛素抵抗有关,胰岛素抵抗性降低时,可直接抑制脂肪酶活性,导致机体糖脂代谢紊乱,进而加快病情发展[2]。临床主要采取药物控制、饮食管理等方式控制病情发展,其中药物多以降糖药为主。二甲双胍是临床治疗T2DM 的首选药物,它通过抑制患者肝脏细胞中葡萄糖释放,加快葡萄糖利用率,以达到降糖作用;但需要配合其他药物联合使用,以控制病情发展[3]。贝那鲁肽是我国自主研发的新型降糖药物,可促进胰岛素分泌,进而达到控制病情发展的目的。利格列汀是一种新型二肽基肽酶-4(Dipeptidyl peptidase-4,DPP-4)抑制剂,其安全性、有效性已在临床上获得认可。有研究发现,利格列汀联合贝那鲁肽可明显改善T2DM 患者糖脂代谢、胰岛素抵抗情况[4],但对T2DM 患者骨代谢的研究未见报道。鉴于此,本研究前瞻性选择我院收治的92 例T2DM 患者作为研究对象,并将其分为两组,主要探究利格列汀联合贝那鲁肽对T2DM 患者糖脂代谢、脂肪因子、骨代谢的影响,为治疗T2DM提供临床参考。现报告如下。
1 资料与方法
1.1 一般资料
前瞻性选取2021 年1 月至2022 年1 月我院收治的92 例T2DM 患者,按随机数字表法分组,分为对照组、联合组,各46 例。对照组:男27例,女19 例;年龄43~70(53.45±5.91)岁;体质量指数25~30(27.61±1.68)kg·m-2;病程1~7(4.76±1.03)y;基础疾病:高血压12 例,冠心病6 例。联合组:男30 例,女16 例;年龄40~71(52.92±6.35)岁;体质量指数23~31(27.31±2.11)kg·m-2;病程1~7(4.94±1.20)y;基础疾病:高血压15 例,冠心病4 例。两组基线资料比较,差异无统计学意义(P>0.05),具有可比性。本研究已经获得本院伦理委员会批准同意,患者或家属均签署知情同意书。纳入标准:参照《中国2 型糖尿病防治指南(2020 年版)》中T2DM 诊断标准[5],空腹血糖(Fasting plasma glucose,FPG)≥7.0 mmol·L-1、糖化血红蛋白(Glycosylated hemoglobin,HbA1c)≥6.5%;近14 d 内未接受其他药物治疗。排除标准:1 型糖尿病;原发性免疫缺陷疾病;甲状腺疾病;糖尿病酮酸中毒;支气管高敏反应;研究药物过敏或过敏体质;肠道疾病史;严重高血脂疾病;合并肾病、酒精性脂肪肝等糖尿病并发症;存在急性心肌梗死、脑卒中等不良心血管事件。剔除、脱落标准:入组后病情加重或需要接受其他药物治疗;中途退出或自愿退出本研究;治疗期间出现严重不良反应或并发症。
1.3 方法
两组均给予口服二甲双胍(北京太洋药业股份有限公司,国药准字20090050,规格0.5 g),0.5 g·次-1,2 次·d-1;根据患者情况均给予对症治疗。对照组给予贝那鲁肽注射液(上海仁会生物制药股份有限公司,国药准字S20160007,规格2.1 mL:4.2 mg)皮下注射,第1~4 d 给予0.6 mg·d-1,第5~7 d 调整一次剂量,2 w 内增加到1.2 mg·d-1(或达到耐受剂量)。联合组在对照组基础上接受口服利格列汀片(Boehringer Ingelheim International GmbH,国药准字HJ20130865,规格5 mg)治疗,5 mg·d-1。两组连续治疗4 m。
1.4 观察指标
1.4.1 血糖指标检测
在两组治疗前、治疗4 m 后,采集受试者空腹静脉血5 mL,离心取上清液,经葡萄糖氧化酶法检测空腹血糖(Fasting plasma glucose,FPG),经低压液相法检测糖化血红蛋白(Glycosylated hemoglobin,HbA1c);并测定餐后2 h 血糖(2 h postprandial glucose,2 h PG)。
1.4.2 血脂指标检测
在两组治疗前、治疗4 m 后,采用MindrayBS-220 型全自动生化分析仪(深圳迈瑞生物医疗电子股份有限公司)检测低密度脂蛋白胆固醇(Low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(High density lipoprotein cholesterol,HDL-C)、总胆固醇(Total cholesterol,TC)、三酰甘油(Three acyl glycerin,TG)。
1.4.3 脂肪因子检测
在两组治疗前、治疗4 m 后,采用酶联免疫吸附法检测促泌素(Secretagogin,SCGN)、白脂素(Asprosin)、趋化素(Chemerin)、网膜素-1(Omentin-1)水平。
1.4.4 骨代谢指标检测
在两组治疗前、治疗4 m 后,采用电化学发光法检测Ⅰ型胶原羧基端肽β 特殊序列(β-crosslinked C-telopeptide of type Ⅰ collagen,β-CTX)、总Ⅰ型胶原氨基酸延长肽(Total procollagen type 1 amino-terminal propeptide,tP1NP)、N 端中段骨钙素(N-MID osteocalcin,N-MID)、25-羟维生素D[25-hydroxyvitamin,25(OH)D]。
1.4.5 不良反应发生率统计
统计两组治疗期间不良反应情况,包括口干、恶心、乏力、腹泻、夜间低血糖。
1.5 统计学分析
采用SPSS 24.0 软件分析处理数据,计数资料n(%)表示,χ2检验,计量资料表示,t检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组血糖指标
治疗前两组FPG、HbA1c、2 h PG 无统计学差异;治疗后,两组FPG、HbA1c、2 h PG 均较治疗前降低(P<0.05),且联合组降低幅度大于对照组(P<0.05)。见表1。
表1 两组治疗前后血糖指标比较(,n=46)

表1 两组治疗前后血糖指标比较(,n=46)
注:与同组治疗前比较,*P<0.05;与对照组相比,#P<0.05。
2.2 两组血脂指标
治疗前两组LDL-C、HDL-C、TC、TG 比较,差异无统计学意义;治疗后两组LDL-C、TC、TG较治疗前降低,联合组降低幅度大于对照组(P<0.05);治疗后两组HDL-C 较治疗前增加,联合组增加幅度大于对照组(P<0.05)。见表2。
表2 两组治疗前后血脂指标比较(,n=46,mmol·L-1)
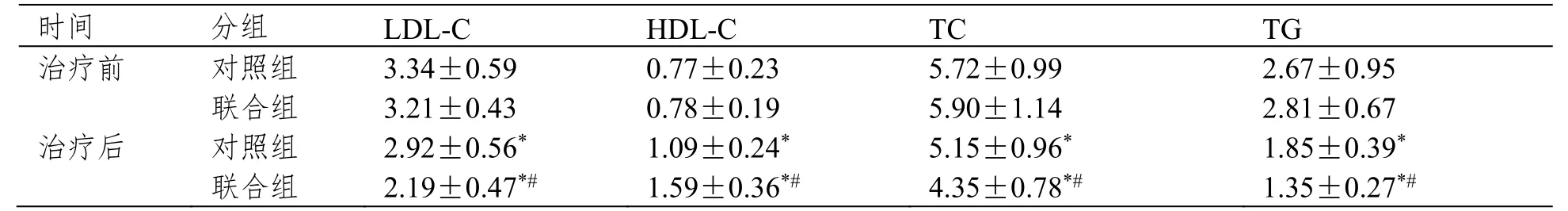
表2 两组治疗前后血脂指标比较(,n=46,mmol·L-1)
注:与同组治疗前比较,*P<0.05;与对照组相比,#P<0.05。
2.3 两组脂肪因子水平
治疗前两组SCGN、Asprosin、Chemerin、Omentin-1 水平比较,差异无统计学意义,治疗后两组SCGN、Omentin-1 较治疗前增加,联合组增加幅度大于对照组(P<0.05);治疗后两组Asprosin、Chemerin 较治疗前降低,联合组降低幅度大于对照组(P<0.05)。见表3。
表3 两组治疗前后脂肪因子水平比较(,n=46)

表3 两组治疗前后脂肪因子水平比较(,n=46)
注:与同组治疗前比较,*P<0.05;与对照组相比,#P<0.05。
2.4 两组治疗前后骨代谢指标
治疗前两组β-CTX、tP1NP、N-MID、25(OH)D 比较,差异无统计学意义。
治疗后两组t-P1NP、N-MID、25(OH)D 较治疗前增加,联合组增加幅度大于对照组(P<0.05);治疗后两组β-CTX 较治疗前降低,联合组降低幅度大于对照组(P<0.05)。
见表4。
表4 比较两组治疗前后骨代谢(,n=46)

表4 比较两组治疗前后骨代谢(,n=46)
注:与同组治疗前比较,*P<0.05;与对照组相比,#P<0.05。
2.5 两组不良反应发生率
联合组治疗后出现口干、恶心各2 例,乏力1 例,腹泻3 例,不良反应发生率为17.39%(8/46);对照组出现恶心、乏力、腹泻、夜间低血糖各1 例,口干各2 例,不良反应发生率为13.04%(6/46),两组不良反应发生率比较,差异无统计学意义。
3 讨论
本研究显示,治疗后联合组血糖指标、血脂指标改善幅度优于对照组,提示利格列汀联合贝那鲁肽可改善T2DM 患者糖脂代谢,这与夏冬等研究一致[4]。贝那鲁肽是为胰高血糖素样肽-1(Glucagon-like peptide-1,GLP-1)类似物,通过皮下在注射体内,可快速促进胰岛素合成和释放,改善胰岛素β 细胞功能,从而降低糖脂指标。利格列汀是一种剂量依赖性的降糖药物,通过抑制DPP-4 活性进而调控GLP-1,促进胰岛素分泌,从而发挥控糖效果。利格列汀与贝那鲁肽联合使用起到协同作用,有利于患者胰岛素合成和释放,从而改善患者糖脂代谢。SCGN 对促进胰岛素分泌、促进胰岛α 细胞向β细胞转化具有重要作用,上调SCGN 可抑制β 细胞凋亡,利于病情的控制[6]。Asprosin 是近年被发现的脂肪因子,由白色脂肪组织释放和合成,在T2DM 血清内其表达增高,可诱导机体发生炎症反应、血管功能障碍[7]。Chemerin 为新发现的脂肪因子,主要通过脂肪组织分泌进而促进脂肪细胞生长分化及肥大,而Chemerin 水平与炎症反应、葡萄糖稳态、胰岛素抵抗具有重要作用[8]。Omentin-1 主要由脂肪组织合成分泌,通过促进脂肪细胞加快葡萄糖转运,达到改善胰岛素抵抗的作用,而Omentin-1 位于染色体1q22-23 区域内,该区域也与T2DM 高发关系密切[9]。本研究显示,治疗后联合组SCGN、Omentin-1 增加幅度大于对照组,而Asprosin、Chemerin 降低幅度大于对照组,可见,利格列汀联合贝那鲁肽可改善患者脂质代谢。研究发现,T2DM 患者发生骨质疏松、骨折的几率极高,因为早期患者胰岛素缺乏,使机体糖脂代谢、蛋白质合成紊乱,从而打破氮平衡,导致骨形成减少和骨吸收增加[10]。β-CTX 主要反应骨吸收能力,当β-CTX 含量增加时,可促进破骨细胞形成[11];tP1NP、N-MID 是骨形成标记物,可促进骨细胞向成骨细胞转化[12];25(OH)D 在骨骼构建中扮演着重要角色,可促进骨组织形成和矿化[13]。本研究显示,治疗后联合组骨代谢指标改善程度优于对照组,表明利格列汀联合贝那鲁肽可改善T2DM 患者骨代谢能力。综上所述,本研究发现利格列汀联合贝那鲁肽治疗T2DM 患者有效,可改善糖脂代谢、脂肪因子、骨代谢。
