度拉糖肽药品不良反应个案文献分析*
2023-05-26蒋伟豪
周 杨,蒋伟豪
(1. 四川省成都市第五人民医院,四川 成都 611130; 2. 西南医科大学,四川 泸州 646000)
度拉糖肽属胰高血糖素样肽-1受体激动剂(GLP-1RA)[1],于2019 年在我国获批上市,常见药品不良反应(ADR)主要为胃肠道反应[2]。目前关于其ADR 的个案报道较少,本研究中以国内外已有个案报道为基础,旨在分析该ADR 发生、发展的特点,为临床安全用药提供参考。
1 资料与方法
1.1 资料来源
检索中国知网、万方、维普数据库、PubMed、Web of Science。中文检索词为“度拉糖肽”“不良反应”“病例报道”;英文检索词为“dulaglutide”“adverse reaction”“case report”。检索时限为2014年9月至2022年3月,剔除表述不清晰、重复病例的文献,得到符合条件的文献共11篇(涉及患者11例),均为国外文献[3-13]。
1.2 方法
统计患者的性别、年龄、合并基础疾病、用药剂量、用药情况,以及ADR 的发生时间、临床表现、处理与转归等信息,并按《药品不良反应报告和监测管理办法》的相关要求判断该ADR与用药的关联性。
2 结果
2.1 患者基本情况
患者的性别与年龄分布情况见表1;基础疾病均有糖尿病,同时合并丙型肝炎、高血压、焦虑症、肥胖、慢性阻塞性肺疾病、冠状动脉疾病、充血性心力衰竭、阻塞性睡眠呼吸暂停、高脂血症等。度拉糖肽给药剂量为每周0.75~1.5 mg;联合用药品种1~4种,主要为降糖药、降压药、调脂药和抗血小板药。其中降糖药为二甲双胍、磺酰脲类降糖药和胰岛素,降压药为氨氯地平、比索洛尔,调脂药为辛伐他汀和瑞舒伐他汀,抗血小板药主要为阿司匹林。参考上述联用药物的药品说明书,其与度拉糖肽未见明显相互作用。但在使用度拉糖肽时,应考虑维持或逐步减少胰岛素剂量,若减量或停药过快,可增加糖尿病酮症酸中毒风险。
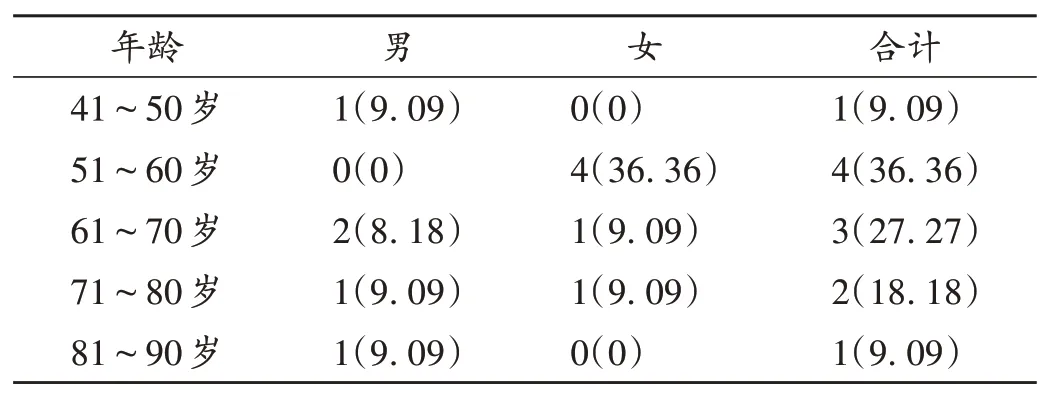
表1 患者性别与年龄分布[例(%),n=11]Tab.1 Distribution of the patients′ gender and age[case(%),n=11]
2.2 ADR 发生特点
ADR 发生时间为用药后0(立即发生且伴随全过程)~16 个月,以用药后2 个月内较多(72.73%),详见表2。ADR 累及器官/系统及临床表现见表3。11例患者中,10 例停药和对症支持治疗后均有好转,1 例严重过敏反应患者预后不良,出现缺血性脑损伤。ADR 的表现、处理及转归详见表4。

表3 ADR累及器官/系统及临床表现(n=11)Tab.3 Organs/systems involved in ADRs and their clinical manifestations(n=11)
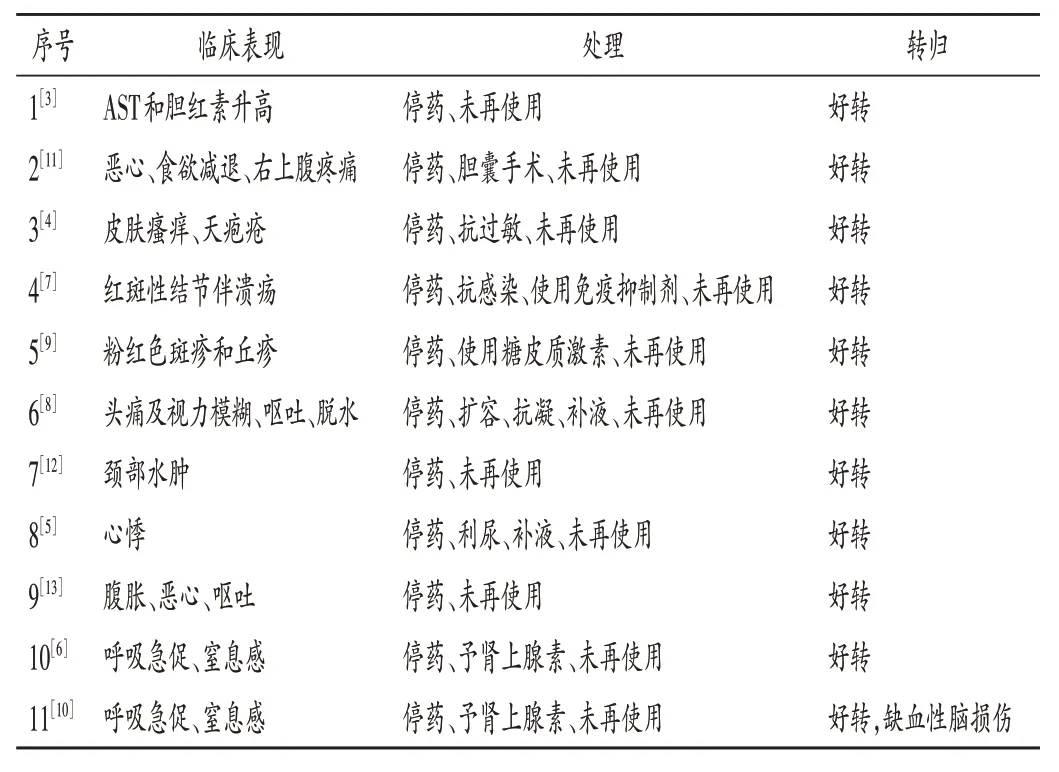
表4 ADR的临床表现、处理及转归Tab.4 Clinical manifestation,treatments and outcomes of ADRs
2.3 关联性评价
按《药品不良反应报告和监测管理办法》评价,11 例ADR与使用度拉糖肽的相关性均为“可能”。
3 讨论
3.1 ADR 类型
度拉糖肽药品说明书中常见ADR 为胃肠道反应,包括恶心、呕吐和腹泻。此外还有低血糖、急性胰腺炎、心率增快、过敏反应等。胆囊炎、房颤加重在其药品说明书中有明确记载,考虑为一般ADR。而涉及皮肤系统的坏疽性脓皮病、麻疹样药疹、大疱性类天疱疮,以及消化系统的药物性肝损伤在其药品说明书中未见收载,应为新的ADR,其中坏疽性脓皮病和大疱性类天疱疮发生程度较严重,延长了患者的住院时间,故考虑为新的严重ADR。
3.2 ADR 与性别、年龄及用药剂量、时间的关系
本研究中纳入ADR 病例的性别差异不明显,年龄以50 岁以上较多(90.91%),与2 型糖尿病的常见发病年龄相符。同时,随着年龄的增加,老年人机体功能减退,肝肾代谢能力下降,这也是ADR增多的因素之一。
本研究中11例患者的用药剂量为每周0.75~1.5 mg,属常规用法用量。虽然近期有研究发现,患者大剂量(每周3.0 mg 和4.5 mg)使用度拉糖肽后的ADR 发生率与使用1.5 mg 时并无显著差异[14],但仍建议按药品说明书规定使用,不应随意增加剂量。
本研究结果发现,度拉糖肽的ADR 发生时间跨度相对较大。故在开始应用度拉糖肽时就要密切监测患者情况,加强用药监护与教育,及时处理ADR。
3.3 ADR 累及系统及临床表现
皮肤及附件:有资料显示,二肽基肽酶4(DPP-4)抑制剂与大疱性类天疱疮有一定相关性[15]。且由于胰高血糖素样肽1(GLP-1)受体在皮肤成纤维细胞和角质形成细胞中表达,GLP-1 RA 也可能会损伤皮肤[16]。因此GLP - 1 RA 与DPP - 4 抑制剂造成皮肤及附件ADR 可能有相似的机制,建议用药前需特别详细询问患者的既往用药史和过敏史。
循环系统:GLP - 1 受体在人类胰腺、肠道和心脏中均有发现[17]。动物实验表明,自主神经系统GLP - 1受体的激活增强了交感神经系统的活性,减弱了副交感神经系统的活性。有学者认为,心肌GLP - 1 受体的过度激活可能会增加阵发性房颤患者的房颤加重风险[18]。另外,关于脑静脉血栓的形成可能和患者恶心呕吐所致脱水有关。度拉糖肽的循环系统ADR 虽发生率较低,但仍需重视,对于既往有心律失常的患者应慎用。
消化系统:胃肠道反应是度拉糖肽最常见的ADR类型。根据国内的一项调查,胃肠道反应在治疗前2 周最显著[19],度拉糖肽药品说明书中也提到分别使用度拉糖肽0.75 mg 和1.5 mg(均为每周)时,累积报告104 周的胃肠道不良事件发生率,包括恶心(12.9% 和21.2%)、腹 泻(10.7% 和13.7%)和 呕 吐(6.9% 和11.5%),多为轻度或中度。本研究中收集到的患者用药后出现的胃轻瘫,考虑目前度拉糖肽尚未在重度胃肠道疾病患者中应用,因此用药前需评估患者胃肠道疾病情况。另外,该药会延缓胃排空和延长胆囊收缩的时间,可能增加胆囊相关并发症的风险。
3.4 药学监护建议
结合本研究收集的案例情况和临床应用实际,建议医务人员从小剂量开始使用度拉糖肽,使用前关注患者既往用药史和过敏史,发现ADR 时及时处理。通常肝功能损害患者无须调整用药剂量,但结合本研究中使用药物后出现药物性肝损伤的案例,使用期间仍需加强肝肾功能的监测。此外,既往有心律失常、急慢性肾功能损伤的患者应慎用该药。若怀疑发生了胰腺炎,应逐步停用。对确诊但未确定由其他原因引起的胰腺炎,不应再次使用度拉糖肽。
综上所述,度拉糖肽作为新型降糖药,为糖尿病的治疗提供了新选择,但其ADR 不容忽视。本研究中纳入度拉糖肽引起的ADR 累及多个系统,部分ADR 在其药品说明书中未收载,随着该药国内上市后的广泛使用,可能会有更多未知ADR 的出现,医务人员需不断加强对度拉糖肽ADR 的认识,尤其加强对合并多种疾病患者的用药监护。同时,关于度拉糖肽ADR 的发生机制还有待进一步研究。
